文章信息
- 刘烨, 邢小罡. 2019.
- LIU Ye, XING Xiao-gang. 2019.
- Argo浮标观测溶解氧数据的原理与质量控制
- Sensor principle and quality control of the dissolved oxygen data observed using Argo floats
- 海洋科学, 43(1): 28-37
- Marine Sciences, 43(1): 28-37.
- http://dx.doi.org/10.11759/hykx20181102001
-
文章历史
- 收稿日期:2018-11-02
- 修回日期:2018-12-05
溶解氧(dissolved oxygen, DO)是溶解于水体中的氧气, 它为海洋生物生存提供必要的生化环境, 是海洋生命活动不可缺少的重要物质。作为海洋学最基本的参数之一, 溶解氧不仅与海-气相互作用联系紧密, 还与海洋中各种生化过程密切相关, 海洋中绝大多数的生命都需要氧气的维持。因此, 海水中的溶解氧含量不仅是衡量海水水质状况、评估海洋生态环境的主要指标、海洋科学实验和资源勘探的重要依据, 也是了解海洋生物地球化学过程、全球气候变化以及海洋碳循环的必要参数, 具有非常重要的观测价值与研究意义[1-7]。特别是近年来, 在全球变暖的大背景下, 海洋中层的最低含氧区(oxygen minimum zone, OMZ)已成为海洋学研究的一大热点, 更凸显出溶解氧观测数据的重要性[8-11]。
然而, 传统的溶解氧观测方式主要通过船载平台获取数据, 先进行水样采集再通过Winkler化学方法[12]进行测定。虽然Winkler方法被认为是最准确的溶解氧观测方式, 但其人力成本与经济成本都很高。此外, 船载平台还存在采样率过低和时空分辨率不足的缺点。以世界海洋地图集World Ocean Atlas 2013(WOA13)[13]为例, 对于绝大部分的开阔大洋水体, 在近60年(1955—2012)中表层溶解氧的观测次数都不超过10次(1°×1°分辨率)。而且, 船载观测平台常常受制于天气与气候条件, 在极端天气(如台风)、恶劣海况(如西风带)的条件下、极地海区以及冰下观测数据都非常缺乏。此外, 船载观测通常是计划性非常强的海洋观测活动, 一次远洋观测通常至少需要提前1个月时间的准备, 因此对于一些偶发事件(如台风、火山喷发、沙尘暴等)的观测能力不足。
Argo计划的出现为海洋现场观测能力带来了革命性的提高, 它通过Argo浮标长期自动化的剖面观测能力以及大量浮标阵列式的投放方法, 可以实现快速、准确、大范围地收集全球海洋上层2000 m的海水温度、盐度和浮标漂移轨迹资料[14]。在全球20余个国家的积极参与共同努力下, 超过3000台Argo浮标组成的全球海洋实时监测系统于2009年正式建成[15]。
随着Argo计划的成功运行, 美、法、德等国科学家开始尝试在传统的温盐剖面浮标上装载各种传感器以进行海洋生物光学与生物地球化学参数的自动化长期剖面观测, 这种新型的剖面浮标, 被称为生物光学剖面浮标(bio-optical profiling float)或生物地球化学剖面浮标(biogeochemical profiling float)[16], 目前在剖面浮标平台上已得到广泛应用的传感器包括溶解氧、硝酸盐、pH传感器、辐射计、叶绿素荧光计、后向散射计、黄色物质荧光计以及透射计。基于多年的实验性研究, 包括溶解氧Argo浮标在内的各种生物地球化学剖面浮标已被证明可以广泛应用于海洋光学、海洋生态学以及生物地球化学的研究[5, 17-19], 其海量的观测数据为上述学科的发展带来了巨大的推动作用。在各国科学家的共同推动下, 国际Argo计划确立了生物地球化学Argo浮标的发展方向[20], 并于2016年10月正式启动了国际生物地球化学Argo计划(Biogeochemical-Argo Program), 作为Argo计划下属的一个官方的国际组织, 这也标志着生物地球化学剖面浮标正式进入了Argo时代[21]。
自2002年起, 溶解氧传感器就成为第一个被装载在Argo浮标上的生物地球化学传感器[5], 其观测数据在海洋学研究中发挥着越来越重要的作用, 研究领域包括海洋通风过程(Ventilation)[5]、净群落生产力[19, 22-23]、海洋碳输出[18]、海气通量[24-25]、以及最低含氧区的变化[10, 26-28]等。伴随着近三十年船载观测数据量的大幅度下降, Argo浮标已成为全球海洋溶解氧观测最主要的数据来源[29], 到2015年时Argo浮标的溶解氧观测量已接近12 000条/年, 这是船载方式所无法比拟的。截至2018年7月全球大洋中总计已投放了926台携带溶解氧传感器的Argo浮标(图 1), 测量的溶解氧剖面超过13万条, 广泛分布于南大洋、印度洋、北大西洋、北太平洋以及地中海, 其中仍在工作的浮标228台。
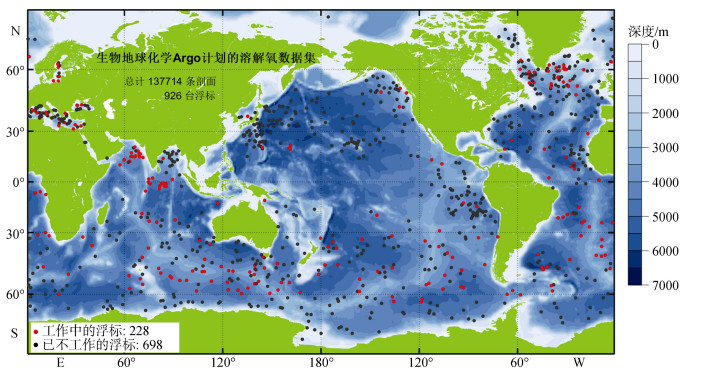 |
| 图 1 截至2018年7月全球大洋中投放的携带有溶解氧传感器的Argo浮标分布图 Fig. 1 The global distribution map of the deployed Argo floats equipped with a dissolved oxygen sensor up to July 2018 (Red points represent the active floats, whereas the black points represent the inactive ones) 注:红色代表 2018年7月仍然工作中的浮标, 黑色代表已不工作的浮标 |
我国对于溶解氧Argo浮标的了解与研究起步较晚, 2014年中国海洋大学首次在西北太平洋投放了17台此类浮标[30]。然而, 目前国内海洋学界对其传感器的测量原理、主要误差来源与质量控制方法等相关内容研究较少。在此背景下, 本文将围绕上述三个内容以及目前在数据质控过程中存在的问题逐一介绍, 以进一步推动我国生物地球化学Argo浮标的技术发展与科学应用。
1 溶解氧传感器的测量原理目前装载在Argo浮标上的溶解氧传感器, 主要分为两型产品:挪威Aanderaa公司生产的4330型和美国Seabird公司生产的SBE63型。两者的差别主要在于: ①SBE63的响应时间(< 6 s)比4330(8~25 s)更短; ②4330目前已应用于APEX、Provor和Arvor型Argo浮标上, SBE63仅装载Navis型浮标上; ③SBE63通过CTD水泵将海水抽进传感器内部进行测量, 优点是最大程度上降低传感器膜受光分解和生物附着等原因产生的数据漂移, 缺点是不能进行空气中的氧气观测; 4330则可通过将传感器加高至天线高度附近, 使其每次浮出水面后进行空气中的氧含量测量, 用于传感器的数据校正[29, 31-32](详见2.3节)。
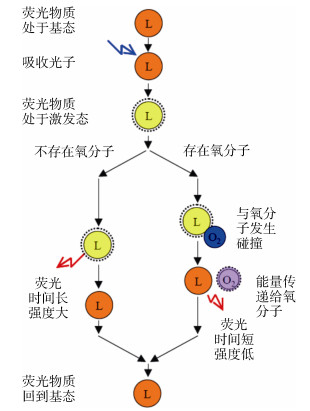
上述两种传感器均属于荧光法传感器(Fluorescent/ fluorescence dissolved oxygen sensor), 也称为“荧光淬灭溶解氧传感器(Fluorescent quenching dissolved oxygen sensor)”、“荧光寿命溶解氧传感器(Fluorescence lifetime oxygen sensor)”以及“相位荧光溶解氧传感器(Phase fluorescent dissolved oxygen sensor)”。此外, Seabird公司称SBE63型传感器为“数字光学溶解氧传感器(Digital optics dissolved oxygen sensor)”, Aanedraa公司称4330型为“光极(Optode)”, 其检测原理是基于荧光淬灭和荧光相位差(寿命)反演溶解氧浓度[33-34]。传感器主要由三个重要的部分组成:传感器膜、激发光系统以及相敏检测系统。由于氧气是许多荧光敏感物质的良性淬灭剂, 所以氧气的浓度和荧光指示剂的一些本征参数(荧光效率、荧光时间等)具有一定的定量关系, 通过测量指示剂的荧光信息就可以计算所测水体中的氧含量。其测量原理如图 2所示:处于传感器膜上的荧光敏感物质(指示剂)开始处于基态(Initial state), 当受到激发光的照射后, 吸收光能跃迁至激发态(Excited state)。当没有氧分子存在的时候, 荧光物质会发射更强、更长时间的荧光, 并最终返回基态; 而当有氧分子存在的时候, 荧光物质会将一部分能量转移到与之碰撞的氧分子上, 从而导致发射荧光量的降低以及时间的缩短, 这种荧光量的减少就称为淬灭(Quenching)[35]。氧分子越多, 则荧光量的强度越低、时间越短。
理论上可以通过两种方法检测溶液中的氧含量, 一是检测荧光强度, 二是测量荧光寿命。检测荧光强度的方法会受到荧光敏感膜的光耦合(optical coupling)或光漂白(optical bleaching)的影响, 所以测量精度不高。因此目前基于荧光淬灭原理的溶解氧传感器都采用测量荧光寿命的方法。荧光寿命(life time), 也称为荧光衰变时间(decay time), 会随溶解氧含量的增大而降低, 两者满足Stern-Volmer方程:
| $ \left[\mathrm{O}_{2}\right]=\left(\tau_{0} / \tau-1\right) / K_{\mathrm{SV}}, $ | (1) |
式中, KSV称为Stern-Volmer常数, τ为荧光寿命, τ0为没有氧分子存在时的荧光寿命。实际测量时, 由于荧光寿命测量也受到诸多因素的影响, 而荧光寿命是荧光相位的函数[36], 因此传感器实际是通过测量荧光相位差反演溶解氧浓度, 但荧光相位同样满足Stern-Volmer方程。
荧光法传感器的基本结构如图 3所示:荧光敏感膜位于光学窗口之外, 并暴露于水体中, 通常设置红蓝两个LED光源。光敏二极管置于中间, 用于测量荧光, 并使用红光滤光片阻挡反射光。蓝光LED光源照射传感器膜上的荧光敏感物质, 使之发射荧光, 光敏二极管接收荧光后, 计算其荧光相位; 考虑到观测数据的准确性以及仪器本身的漂移, 传感器还需要一个红光LED光源, 该光源发射与蓝光激发的荧光相同波长的参考光, 经传感器膜反射后到达光敏二极管, 用于计算其红光相位, 两者差值即为相位差。荧光相位与红光相位即是荧光法传感器的观测值, 依据两者的相位差, 即可反演溶解氧浓度。
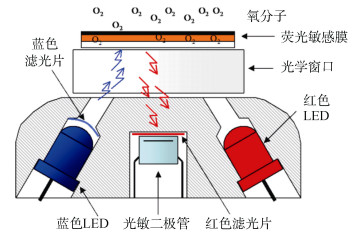 |
| 图 3 荧光法溶解氧传感器的结构示意图(图片来源: www.aanderaa.com) Fig. 3 The structural diagram of the fluorescent dissolved oxygen sensor (www.aanderaa.com) |
荧光法传感器的主要误差来源于“存放漂移(storage drift)”[29], 这一误差在海表层可达30 μmol/kg (海表面溶解氧含量通常在200 μmol/kg左右)[37-38], 这在很大程度上限制了数据的可信性和精度。不过目前还没有研究发现传感器在浮标投放后存在非常明显的数据漂移[29, 31, 38], 说明漂移现象主要发生在“传感器定标后至投放前(一般存放在仓库中)”这一期间, 因而被称为“存放漂移”。这一漂移现象表现为所有观测值的成倍变化, 即观测数据与真实值之间存在一个固定的斜率值m:
| $ \left[\mathrm{O}_{2}\right]=m\left[\mathrm{O}_{2}\right]_{\mathrm{raw}}, $ | (2) |
式中, [O2]raw代表溶解氧传感器观测的原始数据, [O2]cor代表校正后的溶解氧数据。溶解氧的数据质量控制过程需要确定每台传感器的m值, 即传感器的校正系数。
前人提出了三种不同的校正方法:参考剖面校正[31]、气候态校正[38]、空气测量校正[29, 31-32, 36]。参考剖面校正即是在浮标投放时, 在投放位置进行水样采集并利用Winkler法确定其溶解氧剖面, 并与浮标观测的第一个溶解氧剖面进行比对, 获得校正系数m值。但由于大部分Argo浮标投放时并没有同步的船载观测数据, 因此这一方法的普适性不高。
2.2 气候态校正方法气候态校正是Takeshita等[38]提出的使用海洋气候态平均数据集WOA对浮标观测的溶解氧进行校正的方法。WOA是由美国国家大气与海洋局(NOAA)下属的国家海洋数据中心-海洋气候实验室发布的全球海洋年、季节以及月气候态的温度、盐度、溶解氧、磷酸盐、硅酸盐、硝酸盐剖面数据。最早的版本于1994年发布, 由于新的海洋学观测数据不断增加, WOA大约每四年发布新的版本。目前最新的版本为WOA13v2, 水平分辨率包括5°×5°、1°×1°和0.25°× 0.25°三个版本, 垂向102个深度(海表面到5 500 m)。
WOA提供两种溶解氧数据, 溶解氧浓度[O2]和溶解氧饱和度SatO2。荧光法溶解氧传感器实际观测的是氧分压(pO2), 因此通过pO2或SatO2(与pO2基本是等效的)进行校正更符合传感器的测量原理。由于气候态数据仅反映溶解氧月变化的平均态, 并不能真实反映Argo浮标观测的瞬时剖面, 特别是在生物活动丰富的海洋次表层, 两者不可能完全吻合。据此, Takeshita等[38]提出了两种校正方法:深水值校正与表层值校正。前者基于深水中(> 1500 m)溶解氧浓度年际间变化不大的假设, 后者则基于表层溶解氧值一般都接近饱和态(100%)的假设。
在比较了两种方法之后, Takeshita等[38]指出深水值方法虽然从原理上更准确, 但在弱氧/缺氧水体中会出现高估溶解氧浓度的问题, 这主要是由于WOA数据库本身在低氧水体中普遍存在高估溶解氧浓度导致的[39-40], 作者因此认为表层值校正更为准确, 该方法假设WOA观测的表层溶解氧饱和度(SatO2WOA)与浮标观测的表层值(SatO2raw)之间存在线性关系, 其斜率即为待校正的系数m。在实际数据处理过程中, 由于一台浮标观测到的每条剖面均可以得到一个系数, 称为mi(式3), m值的确定则通过将该台浮标观测的所有mi值取平均(式4)。
| $ \mathrm{Sat}_{\mathrm{O}_{2} \mathrm{WOA}}=m_{i} \mathrm{Sat}_{\mathrm{O}_{2} \mathrm{raw}}, $ | (3) |
| $ m=\operatorname{average}\left(m_{i}\right). $ | (4) |
Körtzinger等[41]于2005年首先提出了空气测量校正方法的设想, 认为通过将Argo浮标上的溶解氧传感器加高, 使其可以在浮标到达海表面时露出海面, 从而可以测量空气中的氧气分压, 再通过美国气象环境预报中心(National Centers for Environmental Prediction, NCEP)发布的再分析数据计算浮标所在时间与位置的海表面氧气分压, 从而完成对传感器的同步校正。之后人们对这一方法的实用性和准确性进行了多次研究与证实[31, 42-43], 目前这一方法被认为是Argo观测的溶解氧漂移误差的标准校正方法[36]。
2.3.1 基本原理空气测量法通过溶解氧分压pO2进行校正, 思路与气候态校正方法类似:
| $ p_{\mathrm{O}_{2}}=m p_{\mathrm{O}_{2} \mathrm{raw}}, $ | (5) |
式中, pO2代表校正后的溶解氧分压值或NECP计算的空气中氧分压, pO2raw代表未校正的溶解氧分压值, m代表校正系数。虽然有研究发现如果不进行暗信号校正(截距校正)会导致一定的误差[44], Johnson等[29]和Bittig等[36]分别从实证角度和理论角度说明了空气测量法不进行暗信号校正的原因。从实证角度来说, Johnson等[29]指出现场观测中发现在OMZ的低氧水体中, 仅使用斜率校正的溶解氧浓度观测值与Winkler法测量值基本一致, 反而考虑暗信号漂移的线性回归却经常导致溶解氧高估[38], 说明暗信号校正在低值区可能产生更大的误差。Bittig等[36]则指出, 空气校正方法仅通过海表面溶解氧的观测, 理论上无法进行两个参数(斜率和截距)的反演。由于海表面的溶解氧饱和度基本接近于100%, 因此即便进行不同季节的多次观测, 也仅有一个自由度, 只能反演一个参数; 只有在溶解氧饱和度接近0%的情况下再进行一次观测, 才可能进行两个参数的同时反演。考虑到通常情况下暗信号漂移仅产生不到5 μmol/kg的误差, 而斜率漂移则可造成10%量级的变化, 因此斜率校正更为重要。
空气测量校正方法首先需要通过其他方法估算空气中的氧分压, 进而得到校正斜率m。空气中的氧分压定义为:
| $ p_{\mathrm{O}_{2}}=\left(p_{\mathrm{Air}}-\varphi p_{\mathrm{H}_{2} \mathrm{O}}^{*}\right) x_{\mathrm{O}_{2}}, $ | (6) |
式中, pAir代表大气压强, p*H2O代表饱和水汽分压, φ代表相对湿度, 这里通常假设海表面的相对湿度是100%, 两者相减得到干空气的分压, 再乘以干空气中的氧气比例常数xO2 = 0.209 46, 即为氧气分压。大气压强pAir使用NCEP再分析气象数据集, 并插值到浮标到达海面的时间和位置。
饱和水汽分压p*H2O的估算可以使用简单的经验关系, 直接根据海表面温度计算(空气中盐度为0)。Johnson等[29]使用了4330用户手册中的公式(即式7), 该公式与Weiss和Price[45]的方程基本一致, 仅在回归系数上有微小的差别。
| $ p_{\mathrm{H}_{2} \mathrm{O}}^{*}=\exp \left[52.57-6690.9 / T_{\mathrm{abs}}-4.681 \ln \left(T_{\mathrm{abs}}\right)\right]. $ | (7) |
Tabs表示绝对温标温度(单位: K)。
通过上面的计算得到空气中氧气分压pO2后, 与浮标观测的pO2raw做比值, 得到每次的斜率值mi, 与气候态校正方法相同, 空气测量校正方法也是通过多次测量后的均值计算系数m值(即式4)。
2.3.2 携带效应在实际观测过程中发现, 传感器在海表面的空气观测值包含了空气中氧分压pO2air和水中氧分压pO2water的混合效应, Bittig和Körtzinger[31]将其称为“携带效应(carry-over effect)”, 表示空气测量过程中会携带一部分水中氧分压的信息, 这一效应通过携带斜率(carry-over slope)c表示:
| $ m_{i} p_{\mathrm{O}_{2} \text { surf }}-p_{\mathrm{O}_{2} \text { air }}=c\left(m_{i} p_{\mathrm{O}_{2} \text { water }}-p_{\mathrm{O}_{2} \text { air }}\right). $ | (8) |
pO2surf和pO2water表示实际观测中在海气界面上、下(即空气中和水中)的溶解氧传感器观测值。c的变化范围是0~1(0%~100%), 其物理意义表示观测中有多少比例的水中氧分压的信息。0%代表完全空气中的信号, 上式变为公式(5), 即没有携带效应; 100%代表完全的水中信号, 上式变为pO2surf=pO2water。Bittig和Körtzinger[31]的实验发现, 携带斜率c随时间变化较小, 对于一台浮标来说表现为一个固定的系数[31], 大小一般在0.2~0.3。式(8)也可写为:
| $ p_{\mathrm{O}_{2} \text { surf }}=c p_{\mathrm{O}_{2} \text { water }}-(1-c) / m_{i} \times p_{\mathrm{O}_{2} \text { air }}. $ | (9) |
pO2air仍然通过上述的NCEP再分析数据和经验关系计算, pO2surf变为pO2water的一个线性函数, Bittig和Körtzinger[31]的计算方法是通过多次观测数据进行多元线性回归, 即可得到携带斜率c与校正系数mi。
3 讨论 3.1 两种方法的比较空气测量法目前被认为是最准确的校正方法, 其优势是:它可以看作是一种“实时”校正方法, 浮标每次剖面观测之后都在海表层进行一次校正系数的测量, 虽然每次计算的mi并不单独作为校正系数(所有mi求平均得到m), 但可以进行长期监测传感器是否存在缓慢的漂移或仪器老化。但缺点在于:历史上投放过大量的无法进行空气测量的Argo浮标(目前仍然占总数超过70%), 此外不同Argo浮标对于空气测量法的策略并不统一。目前国际上共投放过四型携带溶解氧传感器的Argo浮标, 分别为法国NKE公司生产的Provor型和Arvor型(一种类似于Provor型的小型浮标)、美国Teledyne Marine公司生产的APEX型以及美国Seabird公司生产的Navis型, 四型浮标目前对于空气测量的方式不一: Navis型浮标设计的SBE63传感器与CTD水泵相连, 不能伸出水面; APEX型浮标采用“水上漂浮测量模式”, 在浮标到达海表面之后进行10~15次空气测量, 但APEX型浮标一般不在近表面进行观测(深度 < 5 m); Provor和Arvor型浮标则采用“水中-空气连续测量模式”, 传感器在上浮过程中直至传感器露出水面连续观测, 这种观测模式是为了去除“携带效应”的影响, 需要获取空气氧分压pO2surf和水中氧分压pO2water两个观测值。简言之: Navis型浮标不能使用空气测量校正方法, 大部分APEX型浮标不能使用携带效应校正方法(式10), 仅Provor和Arvor型浮标可以进行携带效应的去除。由于不同类型的浮标数据无法采用同一种校正方法, 则校正系数之间可能存在系统性误差, 这对于建立一个全球Argo溶解氧数据集会带来一定的困难。
气候态校正方法的优势则在于:它可以应用于目前所有的浮标, 采用统一的气候态数据集进行校正, 不同类型浮标的校正系数之间不会存在系统性误差, 但缺点在于:气候态数据集仅反映了该海区溶解氧的平均态, 而浮标观测的是瞬时状态, 两者不可能完全一致; 此外, 对于一些现场观测数据较少的海区, 其WOA气候态数据集是基于插值得到的, 可信度不高, 在一定程度上增加了气候态校正方法的难度。
需要说明的是, Johnson等[29]对气候态方法与空气测量方法进行了比对, 结果表明两种方法得到的m值非常接近, 相对误差仅为1.6%。说明对于大部分浮标, 两种方法的校正结果具有很高的一致性。
3.2 空气测量法存在的问题空气测量法是目前被认为最准确的溶解氧传感器校正方法, 但我们在实际操作过程中发现大量浮标其“水中-空气连续测量模式”可能没有观测到空气中的氧含量。这种模式虽然可以连续获得表层海水中的氧分压和空气中的氧分压, 但也增加了测量的不准确性, 传感器很有可能还未完全露出水面, 就已经提前结束了“空气测量”。此外, Provor和Arvor型浮标没有气囊设计, 增加了传感器探出水面的难度。气囊的作用是使浮标在到达海表面时为浮标提供足够的浮力将其顶出水面, 没有气囊的Provor和Arvor型浮标则很有可能在到达海表面时, 溶解氧传感器还浸渍在水中。图 4显示了一台Provor型浮标(WMO编号6900953)观测的空气氧分压pO2surf和水中氧分压pO2water以及NCEP数据计算的空气氧分压。可以看到, 该浮标测量到的空气和水中氧分压几乎是相同的, 且与NCEP空气氧分压的季节变化形态相差较大, 说明该浮标测量到的空气氧分压几乎都是水中氧分压的信号, 无法得到准确的m值。图 5展示了所有可计算携带效应的浮标计算得到的携带系数c值, 大部分Provor和Arvor型浮标计算后携带系数c异常偏大(c > 0.8), 而采用“水上漂浮测量模式”的APEX型浮标出现这种问题的情况非常少(注意:另有大量APEX型浮标没有观测到近表层溶解氧因而无法计算携带系数)。正常情况下, 浮标的携带系数c值应小于0.5(表示更多的信号来自于空气中), 如果携带系数过高, 则说明测量到的空气氧分压携带较多的水汽信号, 最可能的原因就是传感器并没有充分伸出水面。此外值得注意的是, 这些异常高的携带系数主要出现在2016年之前投放的浮标, 这是由于早期溶解氧传感器一般只加高10 cm, 最近则开始使用加高20 cm的设计方式, 由此也可以看出更高的传感器位置可以大大提高空气测量的准确性。
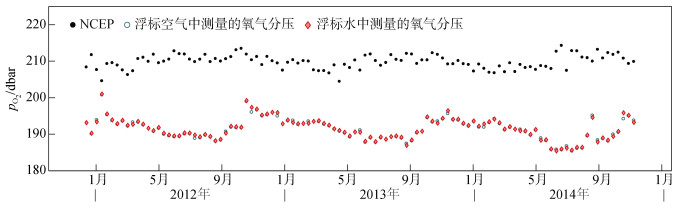 |
| 图 4 浮标6900953(WMO编号)观测的空气氧分压pO2surf(绿色)水中氧分压pO2water(红色)以及NCEP数据计算的空气氧分压(黑色) Fig. 4 The partial oxygen pressure in air, pO2surf (green), and in water, pO2water (red), observed by Float 6900953 (WMO number) as well as pO2 in air calculated using the NCEP dataset (black) |
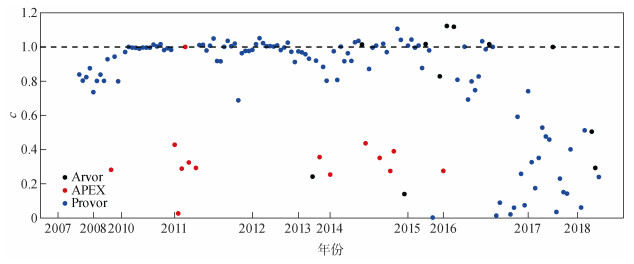 |
| 图 5 携带系数c值与浮标投放时间 Fig. 5 The carry-over coefficient (c) values vs. the deployment dates of float |
Argo浮标观测的溶解氧剖面大部分都拥有较高的准确性, 但是仍然存在一些异常剖面。异常剖面指某个剖面因仪器老化或不明原因而大幅度偏离正常值的剖面。图 6a显示了一台浮标(WMO编号5902303)基于气候态校正方法得到的系数mi的时间序列及其平均值m。可以看出, 除7个点计算的mi值明显偏低外, 剩余大部分mi值非常接近, 平均值m值则明显低于这些mi值, 说明7个异常值的存在影响了m值的计算。图 6b-d展示了其中一个异常剖面(剖面10)及其相邻的两个剖面(剖面09和11)观测的溶解氧饱和度SatO2, 可以看出, 前后两个剖面与气候态溶解氧剖面非常接近, 但剖面10则出现明显的高估, 从表层至2000 m所有的溶解氧饱和度均超过100%。
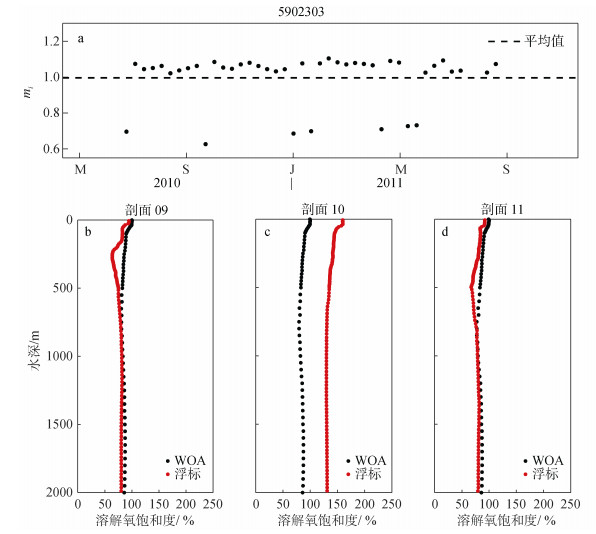 |
| 图 6 浮标5902303(WMO编号)基于气候态校正方法计算的mi值时间序列及其平均值(黑色虚线)(a)以及它的三个相邻剖面(剖面09、10、11)的溶解氧饱和度(黑色代表WOA13气候态剖面, 红色代表浮标观测剖面)(b—d) Fig. 6 The time series of the climatology-based obtained mi for Float 5902303 (WMO number) and average value m (black dashed line) (a) as well as the three adjacent profiles (Profiles 09, 10, and 11) of SatO2 (%) (WOA13 in black and float-observed profile in red) (b–d) |
异常剖面的存在不仅影响m值的计算, 还会干扰数据分析的结果, 因而需要在使用数据之前将其识别并剔除, 这应该是溶解氧数据质量控制中的关键步骤。然而到目前为止, 国际上还没有此类的质控研究, 这在一定程度上大大限制了Argo溶解氧数据的可靠性。
目前两种溶解氧校正方法都使用mi的平均值作为最终该传感器的校正系数(式(4))。当传感器测量到的都是正常剖面时, 选择平均值作为校正系数可以较为准确获得这一系数; 但由于平均值对于异常值较为敏感的特性, 一旦浮标测量到多个异常剖面, 校正系数就会受到比较大的影响, 图 5a显示出7个异常剖面对于整体平均值的影响, 使其显著低于大部分mi值, 用这种方法得到的m值将导致该浮标观测的大部分剖面低于WOA气候态平均值。虽然剔除异常剖面也是一种有效的解决办法, 但这也表明在计算m值时使用mi的平均值可能存在问题。
此外, 对于某些浮标还存在传感器老化或海洋生物附着的问题。图 7显示了一台浮标(WMO编号3900347)基于气候态校正方法得到的mi的时间序列, 可以看到, 该浮标从2005年投放开始至2008年夏季的mi值一直保持较高的稳定性, 但自2008年夏季开始, mi值突然持续增大, 从1.1一直增大至接近11.0, 在不到一年的时间内增大了接近10倍。虽然气候态数据集并不能真实反映浮标现场观测的溶解氧剖面, 但如此巨大的mi值变化则是由于该传感器的老化或海洋生物附着导致的。对于这种情况, 如果使用平均值得到的m值(m=1.6)则会显著高于之前正常观测时的mi值, 进而导致校正后的溶解氧含量显著高于气候态平均值。值得注意的是, mi的中值没有受到后期传感器老化的影响, 这时使用中值则更加准确。
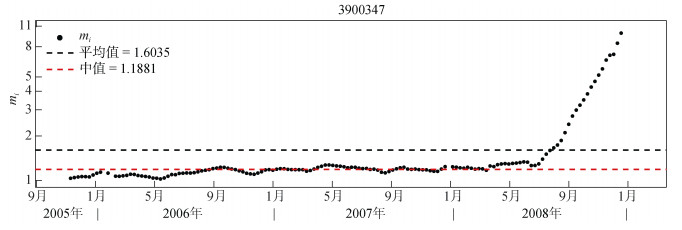 |
| 图 7 浮标3900347(WMO编号)基于气候态校正方法计算的mi值时间序列、及其平均值(黑色虚线)与中值(红色虚线) Fig. 7 The time series of the climatology-based obtained mi for Float 3900347 (WMO number) as well as the average (black dashed line) and median (red dashed line) values |
目前国际上对于Argo浮标观测溶解氧的数据校正主要分为空气测量法和气候态校正法。随着空气测量校正方法的出现, 气候态方法已不是校正斜率漂移的最优方法。然而, 对于没有加高处理的溶解氧传感器观测的历史数据以及所有Seabird公司生产的Navis型浮标观测数据(不能进行空气测量), 气候态校正方法仍然是一种可以有效降低溶解氧测量误差以及有效减小不同传感器之间差异的重要方法。
本文首先介绍了溶解氧传感器的测量原理与两种数据校正方法, 并总结了目前溶解氧数据质控过程中存在的一些问题:
1) 表现为各型Argo浮标空气测量的策略不统一, 这可能导致不同浮标之间(由于使用不同的校正方法)存在系统性误差;
2) 虽然采用了空气测量法, 但大部分早期的溶解氧传感器并没有伸出水面观测到空气氧分压, 致使计算得到的携带系数c偏大, m值估计不准确。浮标本身的浮力问题和测量模式对空气测量法存在比较大的影响, 建议至少将传感器加高到浮标卫星天线的高度。
3) 浮标的异常剖面会影响观测数据的准确性和校正系数的计算, 有一些异常剖面原因不明, 而有些则是因为传感器老化或者海洋生物附着引起的。使用mi的平均值作为校正系数容易受到异常剖面的干扰, 这时使用中值更加准确。
| [1] |
Boyer B T, Conkright M E, Levitus S. Seasonal variability of dissolved oxygen, percent oxygen saturation, and apparent oxygen utilization in the Atlantic and Pacific Oceans[J]. Deep-Sea Research I, 1999, 46: 1593-1613. DOI:10.1016/S0967-0637(99)00021-7 |
| [2] |
Matear R J, Hirst A C, McNeil B I. Changes in dissolved oxygen in the Southern Ocean with climate change[J]. Geochem Geophys Geosyst, 2000, 1: 2000GC000086. DOI:10.1029/2000GC000086 |
| [3] |
Keeling R, Garcia H. The change in oceanic O2 inventory associated with recent global warming[J]. Proc. U S Natl Acad Sci, 2002, 99: 7848-7853. DOI:10.1073/pnas.122154899 |
| [4] |
Matear R J, Hirst A C. Long-term changes in dissolved oxygen concentrations in the ocean caused by protracted global warming[J]. Global Biogeochem Cycles, 2003, 17: 1125. DOI:10.1029/2002GB001997 |
| [5] |
Körtzinger A, Schimanski J, Send U, et al. The ocean takes a deep breath[J]. Science, 2004, 306: 1337. DOI:10.1126/science.1102557 |
| [6] |
Garcia H E, Boyer T P, Levitus S, et al. On the variability of dissolved oxygen and apparent oxygen utilizationcontent for the upper world ocean:1955 to 1998[J]. Geophys Res Lett, 2005, 32: L09604. DOI:10.1029/2004GL022286 |
| [7] |
Schmidtko S, Stramma L, Visbeck M. Decline in global oceanic oxygen content during the past five decades[J]. Nature, 2017, 542: 335-339. DOI:10.1038/nature21399 |
| [8] |
Stramma L, Johnson G C, Sprintall J, et al. Expanding oxygen-minimum zones in the tropical oceans[J]. Science, 2008, 320: 655-658. DOI:10.1126/science.1153847 |
| [9] |
Keeling R F, Körtzinger A, Gruber N. Ocean deoxygenation in a warming world[J]. Annual Rev Mar Sci, 2010, 2: 199-229. DOI:10.1146/annurev.marine.010908.163855 |
| [10] |
Ulloa O, Canfield D E, Delong E F, et al. Microbial oceanography of anoxic oxygen minimum zones[J]. Proc Natl Acad Sci USA, 2012, 109: 15996-16003. DOI:10.1073/pnas.1205009109 |
| [11] |
Cavan E L, Trimmer M, Shelley F, et al. Remineralization of particulate organic carbon in an ocean oxygen minimum zone[J]. Nature Communication, 2017, 8: 14847. DOI:10.1038/ncomms14847 |
| [12] |
Winkler L. Die bestimmung des in wasser gelösten sauerstoffes[J]. Berichte der Deutschen Chemischen Gesellschaft, 1888, 21: 2843-2855. DOI:10.1002/(ISSN)1099-0682 |
| [13] |
Garcia H E, Locarnini R A, Boyer T P, et al. World Ocean Atlas 2013, Volume 3: Dissolved Oxygen, Apparent Oxygen Utilization, and Oxygen Saturation (Levitus S, Mishonov A eds)[DB]//Silver spring, Maryland, US: NOAA Atlas NESDIS 75, 2014: 27.
|
| [14] |
许建平. 阿尔戈全球海洋观测大探秘[M]. 北京: 海洋出版社, 2002. Xu Jianping. Studies of Global Argo Ocean Observation[M]. Beijng: Ocean Press, 2002. |
| [15] |
Roemmich D, Johnson G C, Riser S, et al. The Argo Program:Observing the global ocean with profiling floats[J]. Oceanography, 2009, 22: 34-43. |
| [16] |
Claustre H, Bishop J, Boss E, et al. Bio-optical profiling floats as new observational tools for biogeochemical and ecosystem studies[C]//Hall J, Harrison D E, Stammer D. Proceedings of the " OceanObs'09: Sustained Ocean Observations and Information for Society" Conference (Vol. 2), Venice, Italy, 21-25 September 2009. Paris: ESA Publication, 2010, WPP-306, doi: 105270/OceanObs09.cwp.17.
|
| [17] |
Bishop J K B, Davis R E, Sherman J T. Robotic observations of dust storm enhancement of carbon biomass in the North Pacific[J]. Science, 2002, 298: 817-821. DOI:10.1126/science.1074961 |
| [18] |
Martz T R, Johnson K S, Riser S C. Ocean metabolism observed with oxygen sensors on profiling floats in the Pacific[J]. Limnol Oceanogr, 2008, 53: 2094-2111. DOI:10.4319/lo.2008.53.5_part_2.2094 |
| [19] |
Johnson K S, Riser S C, Karl D M. Nitrate supply from deep to near-surface waters of the North Pacific subtropical gyre[J]. Nature, 2010, 465: 1062-1065. DOI:10.1038/nature09170 |
| [20] |
Jayne S R, Roemmich D, Zilberman N, et al. The Argo Program:Present and Future[J]. Oceanography, 2017, 30: 18-28. |
| [21] |
Johnson K S, Claustre H. Bringing Biogeochemistry into the Argo Age[J]. Eos, 2016, 97: 11-15. |
| [22] |
Riser S C, Johnson K S. Net production of oxygen in the subtropical ocean[J]. Nature, 2008, 451: 323-325. DOI:10.1038/nature06441 |
| [23] |
Huang Y, Yang B, Chen B, et al. Net community production in the South China Sea Basin estimated from in situ O2 measurements on an Argo profiling float[J]. Deep-Sea Res I, 2018, 131: 54-61. DOI:10.1016/j.dsr.2017.11.002 |
| [24] |
Kihm C, Körtzinger A. Air-sea gas transfer velocity for oxygen derived from float data[J]. J Geophys Res, 2010, 115: C12003. DOI:10.1029/2009JC006077 |
| [25] |
Bushinsky S M, Gray A R, Johnson K S, et al. Oxygen in the Southern Ocean from Argo Floats:Determination of Processes Driving Air-Sea Fluxes[J]. J Geophys Res, 2017, 122: 8661-8682. DOI:10.1002/2017JC012923 |
| [26] |
Czeschel R, Stramma L, Johnson G C. Oxygen decreases and variability in the eastern equatorial Pacific[J]. J Geophys Res, 2012, 117: C11019. DOI:10.1029/2012JC008043 |
| [27] |
Prakash S, Nair T M B, Bhaskar T V S U, et al. Oxycline variability in the central Arabian Sea:An Argo-oxygen study[J]. J Sea Res, 2012, 71: 1-8. DOI:10.1016/j.seares.2012.03.003 |
| [28] |
Stanev E, Poulain P-M, Grayek S, et al. Understanding the dynamics of the worlds' largest oxic-anoxic interface[J]. Geophys Res Lett, 2018, 45: 864-871. DOI:10.1002/grl.v45.2 |
| [29] |
Johnson K S, Plant J N, Riser S C, et al. Air oxygen calibration of oxygen optodes on a profiling float array[J]. J Atmos Oceanic Technol, 2015, 32: 2160-2172. DOI:10.1175/JTECH-D-15-0101.1 |
| [30] |
Gao W, Li P, Xie S P, et al. Multicore structure of the North Pacific subtropical mode water from enhanced Argo observations[J]. Geophys Res Lett, 2016, 43: 1249-1255. DOI:10.1002/2015GL067495 |
| [31] |
Bittig H C, Körtzinger A. Tackling oxygen optode drift:Near-surface and in-air oxygen optode measurements on a float provide an accurate in situ reference[J]. J Atmos Oceanic Technol, 2015, 32: 1536-1543. DOI:10.1175/JTECH-D-14-00162.1 |
| [32] |
Bushinsky S M, Emerson S R, Riser S C, et al. Accurate oxygen measurements on modified Argo floats using in situ air calibrations[J]. Limnol Oceanogr Methods, 2016, 14: 491-505. DOI:10.1002/lom3.10107 |
| [33] |
Tengberg A, Hovdenes J, Barranger D, et al. Optode to measure oxygen in the aquatic environment[J]. Sea Technol, 2003, 44: 10-20. |
| [34] |
Tengberg A, Hovdenes J, Andersson H J, et al. Evaluation of a life time based optode to measure oxygen in aquatic systems[J]. Limnol Oceanogr Methods, 2006, 4: 7-17. DOI:10.4319/lom.2006.4.7 |
| [35] |
Kautsky H. Quenching of luminescence by oxygen[J]. Trans Faraday Soc, 1939, 35: 216-219. DOI:10.1039/tf9393500216 |
| [36] |
Bittig H C, Körtzinger A, Neill C, et al. Oxygen Optode Sensors:Principle, Characterization, Calibration, and Application in the Ocean[J]. Front Mar Sci., 2018, 4: 429. DOI:10.3389/fmars.2017.00429 |
| [37] |
D'Asaro E A, McNeil C. Calibration and stability of oxygen sensors on autonomous floats. J. Atmos[J]. Oceanic Technol, 2013, 30: 1896-1906. DOI:10.1175/JTECH-D-12-00222.1 |
| [38] |
Takeshita Y, Martz T R, Johnson K S, et al. A climatology-based quality control procedure for profiling float oxygen data[J]. J Geophys Res Oceans, 2013, 118: 5640-5650. DOI:10.1002/jgrc.20399 |
| [39] |
Fuenzalida R, Schneider W, Garcés-Vargas J, et al. Vertical and horizontal extension of the oxygen minimum zone in the eastern South Pacific Ocean[J]. Deep Sea Res, Part Ⅱ, 2009, 56: 992-1003. DOI:10.1016/j.dsr2.2008.11.001 |
| [40] |
Bianchi D, Dunne J P, Sarmiento J L, et al. Databased estimates of suboxia, denitrification, and N2O production in the ocean and their sensitivities to dissolved O2[J]. Global Biogeochem Cycles, 2012, 26: GB2009. DOI:10.1029/2011GB004209 |
| [41] |
Körtzinger A, Schimanski J, Send U. High-quality oxygen measurements from profiling floats:A promising new technique[J]. J Atmos Oceanic Technol, 2005, 22: 302-308. DOI:10.1175/JTECH1701.1 |
| [42] |
Fiedler B, Fietzek P, Vieira N, et al. In situ CO2 and O2 measurements on a profiling float[J]. J Atmos Oceanic Technol, 2013, 30: 112-126. DOI:10.1175/JTECH-D-12-00043.1 |
| [43] |
Emerson S, Bushinsky S. Oxygen concentrations and biological fluxes in the open ocean[J]. Oceanography, 2014, 27: 168-171. DOI:10.5670/oceanog |
| [44] |
Nicholson D P, Feen M L. Air calibration of an oxygen optode on an underwater glider[J]. Limnol Oceanogr Methods, 2017, 15: 495-502. DOI:10.1002/lom3.v15.5 |
| [45] |
Weiss R F, Price B A. Nitrous-oxide solubility in water and seawater[J]. Mar Chem, 1980, 8: 347-359. DOI:10.1016/0304-4203(80)90024-9 |
 2019, Vol. 43
2019, Vol. 43