文章信息
- 皮永蕊, 唐永政, 王爱敏, 吕永红, 刘红梅, 高丽. 2019.
- PI Yong-rui, TANG Yong-zheng, WANG Ai-min, LV Yong-hong, LIU Hong-mei, GAO Li. 2019.
- 化学消油剂对原油乳化及微生物降解的影响
- Effect of Chemical Dispersant on the Emulsification and Microbial Degradation of Crude Oil
- 海洋科学, 43(3): 19-26
- Marine Sciences, 43(3): 19-26.
- http://dx.doi.org/10.11759/hykx20181107003
-
文章历史
- 收稿日期:2018-11-07
- 修回日期:2019-01-12
各类海洋污染中, 溢油污染发生频率高、分布面积广、危害程度大, 严重威胁着海洋生态系统。自20世纪初, 有超过700万t的石油通过140余次的大型溢油事故进入到海洋环境系统[1], 其中2010年美国墨西哥湾“深水地平线”溢油事故, 致使70多万t原油泄漏, 约692 km的湿地海岸线受到了污染[2]。近年来, 中国沿海发生多起重大溢油事故: 2010年, 大连新港输油管道爆炸漏油事故, 造成约430 km2海面污染[3]; 2011年6月, 蓬莱19-3油田海底地层裂缝导致原油泄漏, 污染面积达840 km2[4]。2018年1月6日, 载有13.6万吨凝析油的“桑吉”轮与“长峰水晶”轮相撞, 导致“桑吉”轮起火并最终沉入海底, 对事发海区的生态环境造成了巨大破坏。2018年11月4日, 福建泉州东港石化公司裂解碳九实际泄漏量达到69.1 t, 给当地渔民生产生活及身体健康造成了危害, 同时也对当地的环境带来严重的污染。
海上溢油发生后, 海面溢油在海洋环境中会经历一系列风化过程, 主要包括蒸发、分散、溶解、乳化、光氧化等过程, 最终会被微生物降解为二氧化碳和水。具有降解石油烃化合物能力的细菌和真菌, 广泛存在于海洋及陆地环境中。据今所知, 约有80多种微生物已被确认为能够高效降解石油烃化合物[5]。在海洋溢油污染物的修复治理中, 微生物降解石油烃化合物的潜力巨大, 特别是通过该技术有效地处理了几次溢油事故, 如Exxon Valdez溢油事故[6]。微生物修复海洋溢油的方式主要有两种:生物添加和生物刺激。生物添加是通过添加纯的石油烃降解菌株、微生物群落等, 从而补充现有污染环境中的微生物群落, 但是现实情况下, 引入的微生物的数量短时间内会急剧下降。生物刺激是通过向污染物现场添加营养盐、氧气或者改变电子受体, 从而刺激土著微生物加速降解石油烃化合物, 然而高浓度的N、P营养盐会造成富营养化。
向海洋溢油污染水域喷洒化学分散剂已成为溢油事故应急处理的重要措施[7], 特别是风浪大、回收效率低的开阔海域和深海海域。化学分散剂将浮油分散成小油滴, 使其稀释在水体中, 其基本原理是利用化学表面活性剂的“亲水-亲油”性, 在油/水界面形成具有一定强度的界面膜, 当水体的洋流运动和波浪作用的混合能足以克服油/水交界处的表面张力时, 使悬浮溢油分散成大小不等的水包油型乳化油滴(甚至小于100 µm), 增大油的表面积, 继而增大了其可生物降解的面积[8]。使用化学分散剂后, 海面油膜迅速扩散, 溢油会在海面形成乳状液, 大片的油膜转化成几微米到几毫米大小不等的油滴, 从而避免油膜到达海岸, 降低了溢油对海鸟和海洋生物的毒害[7]。
表面活性剂在海洋溢油应急处理中得到了广泛的应用, 如墨西哥湾溢油事故中, 共有约3700 m3的化学消油剂(主要为9500A和9527A)被喷洒在墨西哥湾海面及溢油井口处[9]。消油剂广泛应用于海洋溢油的应急处理, 为了刺激溢油的微生物降解。但是, 许多文献报道了化学消油剂与原油混合后, 对细菌、浮油植物、浮游动物及珊瑚幼虫的毒性更强。化学消油剂并不能增强墨西哥湾深水或表面水中异养微生物的活性或者碳氢化合物的氧化速率[10]。化学消油剂能够有效去除海面的浮油, 可以促使石油烃组分溶解在水中, 同时, 也留下一个问题, 究竟化学消油剂的使用能否促进溢油的微生物降解。实际上, 对于这个问题, 并没有确切的答案。
针对上述问题, 基于国产光明化学消油剂GM-8, 探索其对正十四烷及原油的乳化效果, 并考察了GM-8对原油的微生物降解的影响。通过本文的探索, 进一步明确化学消油剂GM-8对原油的乳化及生物降解的影响, 为GM-8在我国海洋溢油应急处理中的应用提供技术支撑。
1 材料与方法 1.1 化学试剂和样品本文所使用的试验试剂皆为分析纯, 购于不同的厂家, 原油来自胜利油田。化学消油剂GM-8购于青岛光明环保有限公司。天然海水取自烟台大学附近海域, 使用前经0.45 μm滤膜过滤处理。
1.2 石油烃降解菌群实验中用到的石油烃降解菌群, 筛选自烟台港附近石油烃污染的海水及表层沉积物样品。
1.3 乳液的制备及表征将一定量的GM-8和一定体积的正十四烷或正十四烷稀释的原油加入到10 mL的试管中, 然后加入一定量的海水。手动晃30 s, 然后斡旋30 s, 静置10 min, 重复上述过程, 然后静置24 h。测定乳化层的高度, 从而确定正十四烷以及原油的乳化指数EI24。乳化指数的公式(1)所示。
| $ {\rm{EI}}_{24}=乳化层高度/混合物总高度. $ | (1) |
天然海水经0.45 μm滤膜过滤后, 加入一定量的原油, 高压蒸汽灭菌(121℃, 20 min)后, 接入5%(V/V)混合菌种子培养液, 加入一定比例的GM-8, 25℃, 120 r/min的条件下降解一周, 通过吸光光度法测定实验组和空白组中的原油浓度, 进而计算原油的降解率。
1.4.2 油标准曲线的绘制利用分光光度法来测定生物降解前后样品中石油烃的总浓度。原油标准曲线的绘制方法如下:称取0.500 0 g原油溶于100 mL的正己烷中, 将不溶物用快速滤纸过滤, 转移至100 mL容量瓶定容, 配置成5.00 g/L的基准油储备液。准确移取5.00 mL上述油基准储备液, 稀释至25.00 mL, 得到1.00 g/L的原油使用液。移取0.00, 2.00, 4.00, 6.00, 8.00, 10.00 mL的原油使用液至50 mL的比色管中, 用正己烷稀释到刻度, 此标准系列浓度分别为0, 0.04, 0.08, 0.12, 0.16, 0.20 g/L, 在分光光度计上测定其225 nm处的吸光度, 然后绘制原油浓度与吸光度之间的标准曲线。
1.4.3 样品油含量的测定微生物在摇瓶中降解原油一周后, 将50 mL正己烷, 分两次加入到150 mL的培养液中, 摇晃2 min, 静置30 min, 充分萃取上层有机相, 在λmax = 225 nm处, 通过紫外分光光度法对培养基中残余的油组分进行测定。利用下述公式(2)计算混合菌群对原油的降解率:
| $\eta {\rm{ = }}\frac{{{C_{\rm{0}}} - {C_{\rm{s}}}}}{{{C_{\rm{0}}}}} \times 100\% ,$ | (2) |
其中, C0为空白瓶中正己烷萃取后的原油正己烷溶液的吸光度, Cs为实验瓶中正己烷萃取后的原油正己烷溶液的吸光度。
2 结果与讨论 2.1 不同条件下GM-8对正十四烷及原油乳化 2.1.1 不同GM-8用量对正十四烷及原油的乳化GM-8用量对正十四烷及原油的乳化效果如图 1所示。图 1的柱状图图结果显示, 随着GM-8的增加, 正十四烷及原油的乳化指数先增加后略有降低。当GM-8的用量为正十四烷的3%时, 正十四烷的乳化指数达到最大值, 约为0.58。当GM-8为原油正十四烷(5 g/L)的5%时, 原油的乳化指数为0.55。右图直观地展现了GM-8对正十四烷(a)及原油溶液(b)乳化的情况。可以看出, GM-8对正十四烷及原油都有很好的乳化效果, 正十四烷及原油几乎完全被乳化, 油水明显分层。正十四烷被GM-8乳化后, 上层为乳白色的油包水乳液, 乳液质地均匀, 相对比较稳定。原油被GM-8乳化后, 上层为咖啡色油包水的乳液, 乳液的颜色主要来自于原油中的芳烃及多环芳烃等物质的颜色。下层略显黄色, 是由于部分石油烃溶于海水而呈现的颜色。
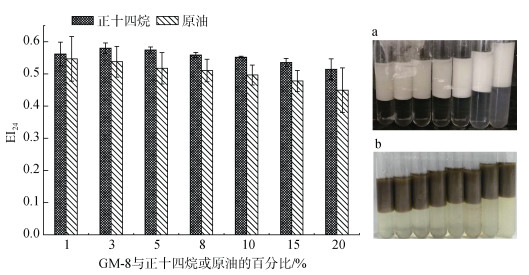 |
| 图 1 GM-8用量对正十四烷及原油的乳化效果 Fig. 1 Emulsifying effect of GM-8 on n-tetradecane and crude oil |
GM-8对正十四烷乳化粒径的影响如图 2所示。乳化粒径是通过光学显微镜(OLYMPUS BX51+DP72)拍照成像, 并通过自身所带软件OLYMPUS-BSW计算得到的。从图中可以看出, 随着GM-8用量的增加, 正十四烷的乳化粒径逐渐减小。乳液的粒径对乳液的稳定性有重要作用。对于相同质量的同种原油, 化学消油剂的相对用量越大, 增加了原油与消油剂的作用机会, 原油乳化分散的效果越好, 乳化粒径越小[11]。
 |
| 图 2 GM-8用量对正十四烷乳化粒径的影响 Fig. 2 Effect of GM-8 dosage on the particle size of n-tetradecane emulsion |
GM-8乳化原油后, 形成咖啡色的油包水乳液, 在光学显微镜下的视野比正十四烷乳化后乳液的视野要暗, 且形成的乳液液滴相对不太稳定, 在显微镜下会发生碰撞、融合、破裂等显现, 使观测到的乳液粒径未呈现一定的规律性, 粒径大小结果在此未做展示。
美国墨西哥湾“深水地平线”钻井平台发生溢油事故后, 130万加仑的消油剂被用来应急处理这次溢油事故[12]。虽然消油剂可以降低油水界面的表面张力, 减少油聚集在一起的倾向, 但是进入海洋环境的溢油总量并没有减少。相反, 消油剂的添加, 会改变溢油固有的理化性质, 从而改变溢油的迁移甚至归趋。同时, 化学消油剂属于化学药剂, 会对海洋环境造成二次污染, 加重海洋环境的生态破坏。近年来, 低毒化学分散剂的研究有了一定的进展, 但是化学消油剂的使用仍需谨慎。因此, 现今国内外化学消油剂的用量一般不超过原油的20%, 本实验结果可以看出, 光明化学消油剂的用量为原油的5%~ 20%时, 原油均可以被有效地乳化。若将GM-8用于海洋溢油事故的应急处理, 能够很好地发挥其对原油的乳化, 从对GM-8在实际应用中的用量提供数据支撑。
2.1.2 油水比对GM-8乳化正十四烷和原油的影响在GM-8的用量为正十四烷及原油用量的5%时, 油水比对原油乳化效果的影响如图 3所示。结果显示, 随着油水比的增加, 正十四烷及原油的乳化指数逐渐降低, 然而乳化层的高度并没有发生变化。在一定的化学消油剂及相同质量的原油的情况下, 也就是说消油剂与原油的用量比值为一定值时, 原油的乳化效果是一样的, 与海水的量几乎没有关系。
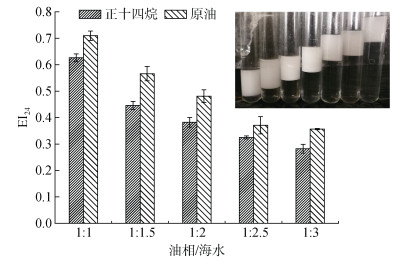 |
| 图 3 油水比对GM-8乳化正十四烷及原油的的影响 Fig. 3 Effect of oil–water ratio on the emulsification of n-tetradecane and crude oil by GM-8 |
由图 4可知, 正十四烷及原油的乳化指数受pH值变化的影响较小。pH从5增加到8, 其中正十四烷及原油的乳化指数几乎没有任何变化, 说明该GM-8能够在海水环境中稳定地发挥乳化原油的作用。pH值影响乳化效果的途径主要有: 1)影响化学分散剂酸碱特性; 2)影响海水中Ca2+、Mg2+等离子的存在状态, 从而改变化学分散剂的化学性质和电荷特性[13]。实验中所用的GM-8的pH值在7~7.5之间, 呈弱碱性, 在中性及弱碱性条件下, 乳化效果较好。在整个乳化实验过程中, 海水用量不超过10 mL, 体系中Ca2+、Mg2+等离子含量较小, 对GM-8几乎没有影响, 因此, 对正十四烷及原油的乳化效果影响较小。
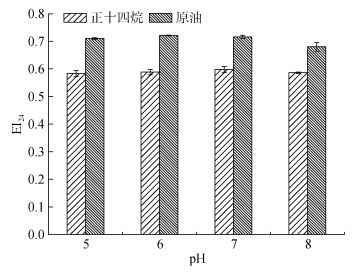 |
| 图 4 pH对GM-8乳化正十四烷及原油的影响 Fig. 4 Effect of pH on the emulsification of n-tetradecane and crude oil by GM-8 |
在GM-8的用量为正十四烷或者原油5%, 油水比为1︰1, pH为7的条件下, 考察了正十四烷及原油乳化的稳定性。结果如图 5所示, 在乳液形成的7 d内, 正十四烷及原油的的乳化指数几乎没有发生改变。原油乳化后, 能够形成稳定的乳液, 在海洋环境中稳定存在7 d以上。原油乳化后, 增大了原油与海洋中的石油烃降解微生物之间的接触面积, 对原油的进一步的微生物降解有一定的助益。海面上的乳化原油, 增大了原油的光照面积, 能够促进原油的光降解。同时, 增大了风、浪等与原油的接触面积, 增加了原油的风化速率。
 |
| 图 5 GM-8乳化正十四烷及原油的稳定性 Fig. 5 Stability of the emulsion of n-tetradecane and crude oil by GM-8 |
原油的标准曲线测定结果如图 6所示。由结果可知, 原油的标准曲线可以表示为y=6.123 6x–0.005 9, 其中R2=0.996 3。通过外标法, 基于上述原油的标准曲线, 从而测定微生物降解后样品中残留的原油的浓度, 进而计算原油的降解率。
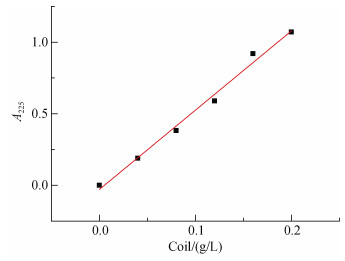 |
| 图 6 原油-吸光度标准曲线 Fig. 6 Standard curve of the concentration and absorbance of crude oil |
在原油的浓度为2.00 g/L的浓度下, 考察了化学消油剂添加量对乳化后原油微生物降解的影响, 结果如图 7所示。从图中可以看出, 随着化学消油剂用量的增加, 乳化原油的微生物降解率逐渐增加。当化学消油剂的用量为1.5 mL时, 乳化原油的微生物降解率达到最大值, 为46.7%, 没有添加化学消油剂时, 微生物对原油的降解率仅为29.9%, 化学消油剂对乳化后原油微生物降解率的贡献为16.8%。随着化学消油剂用量的继续增加, 乳化原油的微生物降解率略有降低。化学消油剂的主要组成成分为有机碳化合物, 这些化合物也可以作为石油烃降解菌的碳源。当化学消油剂的用量持续增加时, 增加了体系中的碳负荷。此时, 化学消油剂与原油形成了碳源的竞争, 当持续增加化学消油剂的用量时, 并不会使原油的生物降解率增加, 反而由于碳源的竞争, 降低了原油的生物降解率。
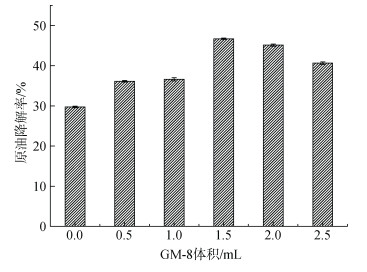 |
| 图 7 GM-8对原油的降解的影响 Fig. 7 Effect of GM-8 on the microbial degradation of crude oil |
化学消油剂具有亲疏水基团, 可以通过溶解或乳化作用增加疏水性有机化合物在海水中的溶解度。化学消油剂的使原油在水中的溶解度有所增加, 增大了原油与石油烃降解菌的接触面积, 从而增加了原油的生物可利用性[14]。另外, 化学消油剂是由大量的碳氢化合物组成的, 而这些碳氢化合物可以作为微生物生长的碳源。Prince[15]等证实了消油剂能够有效地缩短生物降解石油烃化合物的半衰期(13.8 d缩短到11 d)。Brakstad等[16]探究了微生物对分散后原油的降解, 结果表明相对于物理分散, 化学消油剂Corexit 9500分散原油后, 得到的乳液粒径更小, 因而油滴的表面积更大, 有利于石油烷烃的生物降解。Zahed等[17]对Corexit 9500作用后的原油的生物降解进行了研究, 证实了分散剂的使用促进了模拟溢油污染系统中的石油的生物降解。当原油浓度为100 mg/L时, 加入分散剂的原油的生物降解率最高达到了67.3%。特别是当原油浓度为100、500、1 000和2 000 mg/L时, 添加分散剂的原油的生物降解的半衰期相对于没有添加分散剂的情况, 分别降低了3、8、12和17 d。然而, Kleindienst等[10]采用放射性示踪技术定量测定了正十六烷和萘的生物氧化速率, 虽然添加了消油剂, 结果原油的生物降解既没有增强也没有被抑制。
2.2.3 N/P对乳化后原油的微生物降解的影响图 8显示了在原油的浓度为2.00 g/L, GM-8的用量为1.5 mL时, 营养元素N/P对乳化后原油微生物降解的影响。结果表明, 不同营养盐配比对分散剂乳化后原油的生物降解的影响不同。N/P为1︰1的情况下, 乳化原油的微生物降解率达到最大65.9%, 然后依次为N/P为7︰1、3︰1、10︰1和5︰1。其中, N/P为1︰1的乳化原油的微生物降解率比5︰1时高出7.6%。另外, 乳化原油的生物降解收到微生物生长繁殖的影响, 而微生物体内的N/P约为5.67︰1[18], 与本文中N/P为7时较为接近, 有助于微生物本身的生长繁殖, 从而可以促进原油的微生物降解。
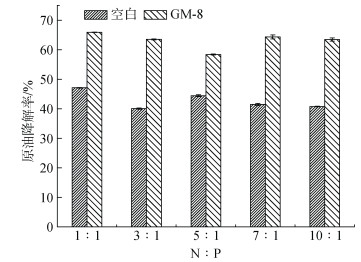 |
| 图 8 氮磷比对乳化后原油微生物降解的影响 Fig. 8 Influence of N/P on the microbial degradation of emulsified crude oil |
pH对乳化原油的微生物降解有较大的影响, 随着pH的增加, 乳化原油的微生物降解率呈现显著增加后减小的趋势。在中性的条件下, 降解效果较好, 降解率高达67.5%。而在碱性的环境下, 乳化原油的生物降解率逐渐减小, 特别是在酸性环境下, 乳化原油的降解率仅为37.8%, 证实了pH值是影响乳环原油微生物降解的一个重要的环境因素。而在现实海水环境中, pH值约为8.3, 微生物对乳化原油的降解率约为57.6%, 仍然保持在一个相对较高的水平。因而, GM-8可用于处理海洋溢油事故, 并能在一定程度上促进原油的微生物降解。
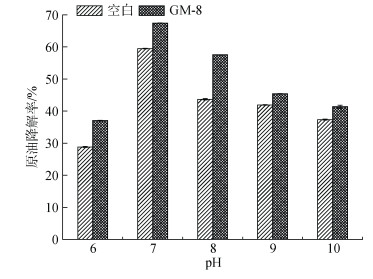 |
| 图 9 pH对乳化后原油的微生物降解的影响 Fig. 9 Influence of pH on the microbial degradation of emulsified crude oil |
微生物的接种量影响生物降解开始时环境微生物群落密度, 在化学消油剂用量1.5 mL, N/P为7, pH为7的情况下, 考察了降解开始时微生物接种量对乳化原油降解的影响, 结果如图 10所示。微生物的接种量对乳化原油的降解有较大的影响, 当接种量为液体培养基的1%时, 乳化原油的降解率约为42.0%。逐渐增加微生物的接种量时, 乳化原油的微生物降解率也逐渐增加。当微生物的接种量增加到10%时, 乳化原油的降解率增加了一倍, 达到91.6%。
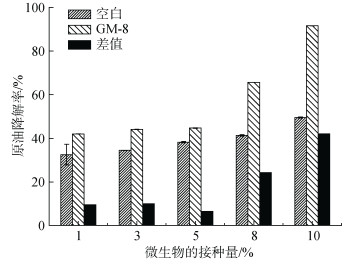 |
| 图 10 微生物接种量对乳化原油微生物降解的影响 Fig. 10 Influence of microbial inoculation on the microbial degradation of emulsified crude oil |
化学消油剂的使用可以促进海洋溢油的乳化分散, 增加原油在水中的溶解度, 从而进一步促进溢油的微生物降解, 然而化学消油剂的投加量仍需要谨慎控制。通过本文实验可知, GM-8对正十四烷及原油均有较好的乳化效果。GM-8的用量对乳化指数有一定的影响, GM-8用量增加时, 正十四烷乳化液滴的粒径逐渐减小。当GM-8与正十四烷及原油的量为一定值时, 乳化指数几乎不受海水量的影响。乳化后的原油能够稳定7d以上, 且乳液几乎不受环境中pH值的影响。
GM-8能促进乳化原油的微生物降解, 但是偏酸偏碱条件均不利于乳化原油的微生物降解。在中性条件下, 微生物对乳化原油的降解率达到67.5%。当N/P比为7︰1, 微生物对乳化原油的降解率较高, 为65.9%。微生物的接种量对乳化原油的生物降解有较大的影响, 当微生物的接种量从液体培养基体积的1%增加到10%时, 乳化原油的生物降解率增加了一倍。基于以上结果, 本文对GM-8在海洋溢油应急处理中的应用有一定的指导意义。
| [1] |
Li Pu, Cai Qinhong, Lin Weiyun, et al. Offshore oil spill response practices and emerging challenges[J]. Marine Pollution Bulletin, 2016, 110(1): 6-27. DOI:10.1016/j.marpolbul.2016.06.020 |
| [2] |
King G M, Kostka J E, Hazen T C, et al. Microbial responses to the Deepwater Horizon oil spill:from coastal wetlands to the deep sea[J]. Annual Review of Marine Science, 2015, 7: 377-401. DOI:10.1146/annurev-marine-010814-015543 |
| [3] |
Zhang Dayi, Ding Aizhong, Cui Shuangchao, et al. Whole cell bioreporter application for rapid detection and evaluation of crude oil spill in seawater caused by Dalian oil tank explosion[J]. Water Research, 2013, 47: 1191-1200. DOI:10.1016/j.watres.2012.11.038 |
| [4] |
Liu Xin, Guo Jie, Guo Mingxian, et al. Modelling of oil spill trajectory for 2011 Penglai 19-3 coastal drilling field, China[J]. Applied Mathematical Modelling, 2015, 39: 5331-5340. DOI:10.1016/j.apm.2014.10.063 |
| [5] |
Head I M, Jones D M, Roling W F. Marine microorganisms make a meal of oil[J]. Nature Reviews Microbiology, 2006, 4: 173-182. DOI:10.1038/nrmicro1348 |
| [6] |
Atlas R M, Hazon T C. Oil biodegradation and bioremediation:a tale of the two worst spills in US history[J]. Environmental Science and Technology, 2011, 45(16): 6709-6715. DOI:10.1021/es2013227 |
| [7] |
Grote M, Van Bernerm C, Bohme B, et al. The potential for dispersant use as a maritime oil spill response measure in German waters[J]. Marine Pollution Bulletin, 2018, 129(2): 623-632. DOI:10.1016/j.marpolbul.2017.10.050 |
| [8] |
Kleindienst S, Paul J H, Joye S B. Using dispersants after oil spills:impacts on the composition and activity of microbial communities[J]. Nature Reviews Microbiology, 2015, 13: 388-396. DOI:10.1038/nrmicro3452 |
| [9] |
Hamdan L J, Fulmr P A. Effects of COREXIT® EC9500A on bacteria from a beach oiled by the Deepwater Horizon spill[J]. Aquatic Microbial Ecology, 2011, 63(2): 101-109. |
| [10] |
Kleindienst S, Seidel M, Ziervogel K, et al. Chemical dispersants can suppress the activity of natural oil-degrading microorganisms[J]. Proceedings of the National Academy of Sciences, 2015, 112(48): 14900-14905. DOI:10.1073/pnas.1507380112 |
| [11] |
钱国栋. 消油剂对原油乳化效果评估波浪槽实验[J]. 海洋环境科学, 2016, 35(2): 274-278. Qian Guodong. Evaluating chemical dispersant efficacy on crude oils in awave tank[J]. Marine Environmental Science, 2016, 35(2): 274-278. |
| [12] |
包木太, 皮永蕊, 孙培艳, 等. 墨西哥湾"深水地平线"溢油事故处理研究进展[J]. 中国海洋大学学报(自然科学版), 2015, 45(1): 55-62. Bao Mutai, Pi Yongrui, Sun Peiyan, et al. Research Progress on "Deepwater Horizon" Oil Spill of Gulf of Mexico[J]. Periodical of Ocean University of China, 2015, 45(1): 55-62. |
| [13] |
刘迪.分散剂作用下溢油乳化和生物降解效果研究[D].青岛理工大学2013 http://cdmd.cnki.com.cn/Article/CDMD-10429-1014184281.htm
|
| [14] |
叶志波, 杨乐, 邓瑞杰, 等. 消油剂对海洋溢油中多环芳烃环境行为的影响[J]. 青岛理工大学学报, 2017, 38(6): 89-94. Ye Zhibo, Yang Le, Deng Ruijie, et al. Influence of dispersants on the environmental behavior of polycyclic aromatic hydrocarbons derived from marine spilled oil[J]. Journal of Qingdao Technological University, 2017, 38(6): 89-94. DOI:10.3969/j.issn.1673-4602.2017.06.015 |
| [15] |
Prince R C, Mcfarlin K M, Butler J D, et al. The primary biodegradation of dispersed crude oil in the sea[J]. Chemosphere, 2013, 90(2): 521-526. DOI:10.1016/j.chemosphere.2012.08.020 |
| [16] |
Brakstad O G, Daling P S, Faksness L G, et al. Depletion and biodegradation of hydrocarbons in dispersions and emulsions of the Macondo 252 oil generated in an oil-on-seawater mesocosm flume basin[J]. Marine Pollution Bulletin, 2014, 84(1-2): 125-134. DOI:10.1016/j.marpolbul.2014.05.027 |
| [17] |
Zahed M A, Aziz H A, Isa M H, et al. Kinetic modeling and half life study on bioremediation of crude oil dispersed by Corexit 9500[J]. Journal of Hazardous Materials, 2011, 185(2-3): 1027-1031. DOI:10.1016/j.jhazmat.2010.10.009 |
| [18] |
Pritchard P H, Costaia C F. EPA's Alaska oil spill bioremediation project. Part 5[J]. Environmental Science & Technology, 1991, 25(3): 372-379. |
 2019, Vol. 43
2019, Vol. 43

