文章信息
- 陈梦, 韩振莲, 付晓丹, 朱常亮, 牟海津. 2019.
- CHEN Meng, HAN Zhen-lian, FU Xiao-dan, ZHU Chang-liang, MOU Hai-jin. 2019.
- 低分子质量κ-卡拉胶钾的酶法制备及其对原发性高血压大鼠降血压作用的研究
- Preparation of low-molecular-weight potassium κ-carrageenan by enzymatic hydrolysis and its antihypertensive effect on SHR
- 海洋科学, 43(8): 36-42
- Marine Sciences, 43(8): 36-42.
- http://dx.doi.org/10.11759/hykx20190320003
-
文章历史
- 收稿日期:2019-03-20
- 修回日期:2019-04-25
高血压是导致脑溢血、动脉粥状硬化和肾功能衰竭最重要的一个危险因素, 且具有一定的家族遗传趋势[1]。有研究表明, 非西班牙裔白人长期服用某些光敏性降压药物(氢氯噻嗪、硝苯地平等)可增加患唇癌的风险[2], 服用10年或以上钙离子通道阻滞剂的女性患乳腺癌的机率成倍增加[3]。因此, 从天然产物中获取降血压功效成分成为新药研发和功能食品开发的突破口。
近年来, 海洋生物活性物质引起了人们极大的关注, 尤其在中国科学院上海药物研究所等机构联合研发的治疗阿尔茨海默症的新药“甘露寡糖二酸(GV-971)”顺利完成临床3期试验后, 海洋寡糖的功效活性更受关注。卡拉胶是从红藻中提取的硫酸酯化多糖, 其中κ-卡拉胶由硫酸基化的或非硫酸基化的半乳糖和3, 6-脱水半乳糖, 通过α-1, 3糖苷键和β-1, 4键交替连接而成。由于分子质量较大的卡拉胶粘性大、扩散困难, 难以被机体所吸收, 对于其生物活性的报道较少。有报道称卡拉胶寡糖具有多种生物活性, 如抗肿瘤[4]、抗病毒[5]、调节免疫[6]等。然而, 因受限于学术界关于卡拉胶促炎的观点, 关于卡拉胶寡糖的研究多数停留在体外试验, 其降血压活性也鲜有报道。
有研究指出[7], κ-卡拉胶寡糖具有抗凝血作用; 而改善高血压病人的凝血和血液流变学功能异常与紊乱不仅有助于控制原发性高血压病人的病情, 还可降低其发生血栓栓塞性心脑血管事件的风险[8], 这预示着κ-卡拉胶寡糖可能具有潜在降压作用。补钾排钠是临床上控制高血压的常用手段, Iimura等[9]发现高钾饮食可显著降低实验组的平均动脉压, 且增加尿钠的排泄量; Suzuki等[10]用氯化钾作用于两肾一夹型高血压模型鼠, 发现钾负荷后减缓了高血压的发展, 并且减轻了肾血管性高血压的临床症状。本研究首次将LC与钾离子结合, 旨在研究LCP对SHR血压的影响以填补LCP在心脑血管疾病领域数据的空白。
1 材料与方法 1.1 材料 1.1.1 动物选取SPF级的雄性SHR 18只, 9周龄, 220~260 g, 收缩压 > 165 mmHg, 供货商北京维通利华实验动物技术有限公司, 生产许可证号为SCXK(京)2016-0011。
1.1.2 原料及试剂κ-卡拉胶80目精粉购自青岛德慧海洋生物科技有限公司; 所用酶为实验室前期构建的能够高效酶解κ-卡拉胶的重组cgkZΔPst菌株所产; 卡托普利购自深圳海王药业有限公司; 体积分数95%的乙醇为工业乙醇; 其他试剂皆为国产分析纯。
1.2 仪器与设备大小鼠智能无创血压计BP-2010A, 租自北京软隆科技有限公司; 火焰原子吸收分光光度仪, 购自岛津企业管理有限公司; AKTA蛋白质层析系统, 购自通用电气医疗集团生命科学部; OLYMPUS BX41显微镜, 购自南京贝登医疗股份有限公司; 傅立叶变换红外光谱仪, 购自赛默飞世尔科技有限公司; 高效液相色谱仪等购自安捷伦科技有限公司。
1.3 方法 1.3.1 低分子质量κ-卡拉胶寡糖(LC)制备平板上挑取单菌落至YPD种子液中, 转速200 r/min、28℃发酵24 h, 按1%发酵液体积的量接种至BMGY发酵液中, 转速200 r/min、22℃发酵36 h, 加入1%发酵液体积的甲醇, 此后每隔24 h加1次甲醇, 共加4次, 发酵结束后, 离心得上清发酵液。按1%加酶量、1%底物(κ-卡拉胶)浓度, 40℃不停搅拌酶解8 h, 酶解液浓缩1倍后加入1倍体积预冷乙醇, 4℃静置醇沉1 h, 离心, 弃去沉淀, 上清浓缩到初始酶解液体积的1/5, 加入3倍浓缩液体积的预冷乙醇, 4℃静置醇沉1 h, 离心, 沉淀用水复溶, 旋转蒸发冻干, 得LC。
1.3.2 分子质量的测定色谱柱: TSK G4000PWXL(7.5 mm×600 mm×17 μm); 流动相: 10 mmol/L NaH2PO4和200 mmol/L NaNO3; 柱温: 25℃; 流速: 0.3 mL/min; 进样量: 10 μL; 检测器:示差折光检测器RID。
1.3.3 低分子质量κ-卡拉胶钾(LCP)制备60 g/L的LC与1 g/L的KCl等体积混合, 转速130 r/min、25℃反应4 h以上, 浓缩1倍后加入3倍浓缩液体积的预冷乙醇, 4℃静置醇沉1 h, 离心, 沉淀用水复溶, 蒸发至原浓缩液体积, 加入3倍体积预冷乙醇, 4℃静置醇沉1 h, 离心, 沉淀用水复溶, 旋转蒸发, 冻干, 得LCP。
1.3.4 Sephadex G-10葡聚糖凝胶柱脱盐选取内径1 cm, 柱长80 cm的层析柱, 垂直固定并检漏, 手动灌制Sephadex G-10葡聚糖凝胶填料, 以超纯水为流动相, 连接AKTA蛋白纯化系统, 开启紫外和电导率检测。将1次、2次、3次醇沉后得到的LCP以超纯水为溶剂配制成5 g/L的浓度, 进样5 mL, 以电导率为观测对象, 辅助评价不同醇沉次数后残留的游离钾离子的含量。
1.3.5 火焰原子吸收分光光度法测定钾元素整个实验过程所需溶剂皆为超纯水。将实验所需玻璃制品浸泡在3%~5%的硝酸中超声过夜, 超纯水冲洗2~3次, 低温烘干。称取10 mg样品, 加混酸(V(硝酸)︰V(高氯酸)= 4︰1)高温消解4~7 h, 用超纯水转移至10 mL容量瓶中, 充分混匀, 稀释到合适浓度进行上样测定吸光值, 对应标准曲线计算钾元素的质量分数。
1.3.6 SHR饲喂及尾动脉收缩压测定方法18只SHR于SPF级屏障环境动物房适应性喂养1周, 温度: 20~25℃; 湿度: 50%~70%;饲养密度: 3只/笼; 照明时间: 12 h。根据体质量和血压随机分为3组, 每组6只。空白对照组灌胃蒸馏水, 实验组灌胃LCP(600 mg/kg), 阳性对照组灌胃卡托普利(10 mg/kg)。实验周期4周, 每周固定时间测量收缩压(SBP)和心率1次, 称重2次。SBP测量部位为尾动脉, 将老鼠固定入套, 保持体温在37~39℃之间且安静的情况下将传感器固定在尾动脉处, 连续测定5次SBP和心率, 取平均值。
1.3.7 肾素、血管紧张素Ⅱ、脂多糖的测定双抗体酶联免疫吸附试验(ELISA), 具体步骤及细节问题见试剂盒说明书。
1.3.8 结肠组织病理切片制作及观察小鼠处死后, 取远端结肠1 cm, 固定、脱水、透明、浸蜡、包埋、切片(厚度5 μm), 进行HE染色, 组织病理切片的HE染色由武汉塞维尔生物科技有限公司制作。通过OLYMPUS BX41显微镜进行观察拍片。
1.4 统计学分析试验结果表示方式为“平均数±标准偏差”, 采用SPSS 22.0软件进行统计分析, 组间数据采用单因素方差分析(one-way ANOVA)的方法, P < 0.05为差异有统计学意义。
2 结果与分析 2.1 LC制备及其分子质量测定借助于高效液相色谱仪和TSK G4000PWXL, 以1、5、12、21、80 kDa标准品的保留时间为横坐标, 分子质量的对数形式为纵坐标绘制标准曲线(图 1)。用流动相配制5 g/L的LC溶液, 上样10 μL, 保留时间为35.820 min(图 2)。代入标准曲线得出: LC分子质量约为3.5 kDa。
 |
| 图 1 TSK G4000PWXL标准曲线 Fig. 1 Standard curve of TSK G4000PWXL |
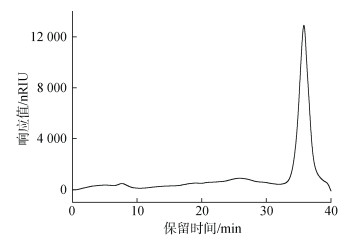 |
| 图 2 LC的保留时间(色谱柱: TSK G4000PWXL) Fig. 2 Retention time of LC (Column: TSK G4000PWXL) |
根据κ-卡拉胶的结构计算可得, 若结构中的硫酸基全部与钾结合, 则钾元素的饱和质量分数接近9.18%。考虑到LC的溶解状态, 以60 g/L的LC与不同质量分数的KCl结合, 一次醇沉后测定钾元素含量(表 1)。由表 1可知, 由于饱和结合率的限制, 不同质量分数的KCl与60 g/L的LC结合后其钾元素含量基本趋近于饱和值。由于KCl浓度越高, 后续醇沉除去游离钾离子的难度越大, 故选择60 g/L的LC与1 g/L的KCl进行反应。
| KCl质量浓度(g/L) | 1 | 5 | 10 | 20 | 30 |
| 钾元素含量/% | 9.262 | 9.472 | 10.072 | 9.767 | 10.176 |
| 9.236 | 9.336 | 9.969 | 10.618 | 10.498 | |
| 8.761 | 9.073 | 9.371 | 9.746 | 10.112 | |
| 平均含量/% | 9.086 | 9.294 | 9.804 | 10.044 | 10.262 |
为了尽可能地排除游离钾离子对后续降血压实验的干扰, 方便评价结合型的LCP对SHR血压的影响, 在低浓度KCl环境下对反应混合液进行醇沉以脱除游离钾离子。以10 mL 60 g/L LC与10 mL 1 g/L KCl反应为例, 分别对反应后的LCP进行1次、2次、3次的3倍体积乙醇醇沉操作。以超纯水为流动相, 用Sephadex G-10葡聚糖凝胶柱检测游离的钾离子, 评价不同醇沉次数对游离钾离子的脱除情况(图 3); 计算不同醇沉次数的得率, 3次实验取平均值(表 2); 同时火焰原子吸收法测定不同醇沉次数后钾元素的含量, 3次实验取平均值(表 3)。
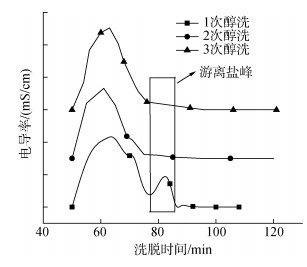 |
| 图 3 不同醇沉次数后LCP电导率的变化 Fig. 3 Change in conductivity of LCP after different times of alcohol precipitation |
| 醇沉次数 | 1 | 2 | 3 |
| 冻干后质量/g | 0.362 | 0.255 | 0.170 |
| 0.350 | 0.252 | 0.155 | |
| 0.358 | 0.256 | 0.161 | |
| 平均质量/g | 0.357 | 0.254 | 0.162 |
| 得率/% | 59.5% | 42.4% | 27.0% |
对应图 3中1次醇沉的图谱, 根据体积排阻色谱的原理可知, LCP与游离盐离子(基本为钾离子)两种组分分离效果良好。比较2次和3次醇沉的图谱可知, 2次醇沉后游离盐峰显著减小, 游离钾离子基本脱除殆尽; 而3次醇沉后基本无游离盐峰。结合2次醇沉后的LCP得率为42.4%, 3次醇沉后的LCP得率为27.0%, 综合考虑确定LCP的制备工艺为二次醇沉。此外, 根据火焰原子吸收的结果, LCP中钠元素的含量基本稳定在0.5%, 可以忽略不计。因此, LC经过与KCl溶液结合以及2次3倍体积乙醇醇沉操作后, 其中结合的钾元素的质量分数为8.7%, 基本接近理论饱和结合率9.18%, 与LC中6.5%左右的钾含量相比, 钾元素含量增加了2.2%。
2.3 LCP对SHR收缩压的影响由表 4可知, 实验期间, 空白组(B组)SHR的血压值随着周龄增大而上升, 第3周稳定在210 mmHg左右。实验组(LCP组)在灌胃第1周基本无降压作用, 从第2周开始便控制血压不再上升, 第3周开始与空白组有了显著差异(P < 0.05), 这种显著的降压效果持续到了第4周, 且与B组相比, 有18 mmHg左右的血压差, 说明LCP具有一定的降压作用且能够保持稳定持续的降压效果。卡托普利组(P组)控制血压的效果较为明显, 灌胃1周后就出现了显著的降压效果并持续到实验结束。
| 组别 | 第0周 | 第1周 | 第2周 | 第3周 | 第4周 |
| B | 166±15 | 185±9 | 197±10 | 210±18 | 211±8 |
| P | 167±9 | 165±14* | 161±18** | 176±9** | 166±14** |
| LCP | 172±12 | 196±11 | 198±11 | 192±5* | 193±9* |
| 注: *表示与空白组比较差异显著(P < 0.05), **表示与空白组比较差异极显著(P < 0.01).下同 | |||||
王金玲等[11]研究发现, 用分子质量低于3 kDa的降血压肽灌胃SHR, 实验周期为6周, 降压幅度最高达20 mmHg。林峰等[12]研究发现, 以玉米低聚肽灌胃SHR, 实验周期为8周, 在第4周时, 显著降压20 mmHg, 第8周显著降压38 mmHg。比较可以看出, LCP的降压效果与一些降血压肽的效果旗鼓相当, 关于其更长实验周期的降压效果以及停药后对血压的控制效果都有待进一步研究。
2.4 LCP对SHR肾素-血管紧张素(RAS)系统的影响RSA系统主要包括肾素、血管紧张素原(Ang)、血管紧张素转换酶(ACE)和血管紧张素Ⅱ(Ang Ⅱ), 过度激活的RAS系统是导致高血压形成的重要原因之一。来源于肾脏球旁细胞的肾素可将血液中的Ang转变为无生理活性的Ang Ⅰ, 紧接着在ACE的作用下生成具有强烈升压作用的物质Ang Ⅱ。肾素被视为RAS系统活跃的初始和限速因素, 而Ang Ⅱ则被认为是导致血压升高的直接因素。分析各组血液中的肾素和Ang Ⅱ水平(图 4)可知, 与B组相比, LCP显著降低了肾素(P < 0.05)和Ang Ⅱ(P < 0.01)的水平, 而P组对于两项重要指标的降低程度不如LCP组。虽然宏观上P组的血压降低程度优于LCP组, 但更深层次的体液调节方面却略逊于LCP组, 这也突出显示了天然产物的活性作用以及在降压机理上的优势。因此推测: LCP可能是通过调节RAS系统, 抑制这一通路的表达和活性进而降低SHR的血压。
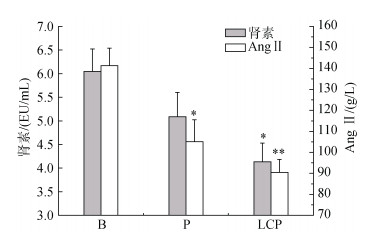 |
| 图 4 各组血浆中肾素以及Ang Ⅱ的含量 Fig. 4 The content of renin and Ang Ⅱ in plasma of each group |
脂多糖(LPS)来源于革兰氏阴性菌, 是其外膜的主要组成成分, 当肠道环境受到外界刺激损伤或者自身系统紊乱等威胁时, 会导致革兰氏阴性菌增多甚至裂解释放出过量的LPS, 进而引起肿瘤坏死因子-α(TNF-α)、白细胞介素(IL)等促炎因子的过量表达、中性粒细胞的过量堆积等一系列炎症症状, 宏观表现为肠黏膜水肿、肠绒毛细胞坏死, 致使肠道通透性增加, 无法拦截细菌和LPS进入血液引发一系列损伤问题。严玉霖[13]在研究LPS对大鼠小肠黏膜免疫指标的影响中发现, LPS可显著降低肠黏膜杯状细胞的量以及分泌性免疫球蛋白A的含量。杯状细胞在增加肠黏膜表面黏液分泌量上贡献巨大, 分泌的黏液物质对黏膜上皮有润滑和保护作用, 可以阻止病原微生物等各类有害物质的入侵; 而免疫球蛋白A可增强肠黏膜中和病毒、毒素等异物的能力。总之, LPS的降低可以在一定程度上表征肠道内环境的改善。
血液中LPS测定结果如图 5所示, LCP与B相比出现显著性差异, P与B相比差异极显著, LCP和P都显著降低了LPS的效价, 但两者之间无显著性差异, 即两者降低血浆中LPS效价的能力差别不大。数据形式上显示, LCP和卡托普利对SHR的肠道通透性均有一定的改善。
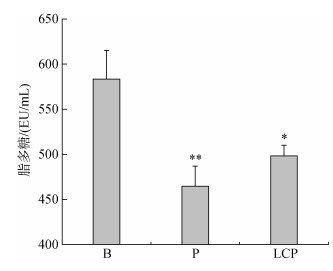 |
| 图 5 各组血浆中LPS的含量 Fig. 5 The content of LPS in plasma of each group |
学术界一直都有关于卡拉胶是否会导致炎症的争论, Watt等[14]研究指出, 将酸解的卡拉胶制备成2%的饮用液可在短时间内引起豚鼠的结肠性溃疡, 而不久后的Norris等[15]利用三种类型的卡拉胶(κ-、ι-、λ-)及同样的酸解方法获得的降解产物均未引起豚鼠肠胃溃疡的结果反驳了Watt等的研究。值得注意的是上述研究所用到的卡拉胶分子质量基本都在10 kDa以上。李苗苗[16]的研究表明, 分子质量为4.5kDa的LC通过与定殖在无菌小鼠肠道中的一种木糖降解拟杆菌的共同作用引起小鼠肠道炎症, 但该木糖降解拟杆菌在结肠癌病人肠道粘膜中呈增长趋势[17], 所以存在该菌通过其他途径引起肠道炎症的可能性。郭娟娟[6]研究表明四种κ-卡拉胶寡糖从生理水平及转录水平上分别剂量依赖性地抑制了多种炎症介质的分泌, 降低了细胞炎症反应。
此外, Jaworska等[18]的研究表明, 大鼠的高血压与结肠对三甲胺(肠道细菌代谢物)的通透性增加有关, 这一结果伴随着结肠形态学的改变, 如杯状细胞减少、黏膜以及上皮细胞浸润等, 暗示结肠形态学的改变导致肠道对某些代谢物的通透性增加, 而这一结果与大鼠的高血压相关。Santisteban等[19]的研究表明, 肠道交感神经活动增加, 改变肠道病理, 导致肠道通透性增加, 出现炎症状态以及肠道菌群微生态失调现象, 而有研究表明交感神经系统活动增加是动物和人类高血压的标志[20]。因此LCP对于结肠环境的改善或许与其降低SHR血压有一定的关系。
本研究对SHR的结肠部位进行切片染色, 发现B组多个个体出现了较明显面积的淋巴细胞及伴中性粒细胞等的浸润现象, 绒毛损伤严重, 腺体隐窝结构被破坏, 杯状细胞丢失。P组同样也有一定程度的炎症, 但与B组相比略有缓解。而LCP组与B组相比, 并未表现出更严重的炎症表象, 甚至有一定程度的改善, 大部分肠上皮结构完整, 存在完整的隐窝结构, 保留了大量的杯状细胞, 炎症细胞浸润也得到了缓解(图 6)。
 |
| 图 6 SHR结肠组织病理切片 Fig. 6 Colon histopathological section of spontaneously hypertensive rat 注: 40x显微镜下圈中部分为炎症浸润 |
利用酶解法和醇沉法, 以κ-卡拉胶粉为原料制备出分子质量在3.5 kDa左右的LC, 将LC与KCl溶液混合, 经过两次醇沉后得到LCP, 将其作用于SHR, 发现其对SHR有稳定且持续的降压作用, 降压幅度为18 mmHg。进一步研究发现, LCP显著降低了RAS系统中肾素(P < 0.05)和血管紧张素Ⅱ(Ang Ⅱ) (P < 0.01)的水平, 推测LCP可能是通过降低RAS系统的活化程度发挥降压作用; 此外LCP显著降低了血液中脂多糖(LPS)的水平(P < 0.05), 减轻了肠道通透性程度, 进一步改善了肠道上皮结构的完整性, 众多研究表明肠道结构的完整与高血压密切相关, 所以LCP也可能通过改善肠道内环境进而降低了SHR的血压。
| [1] |
Boda H, Uchida H, Takaiso N, et al. A PDE3A mutation in familial hypertension and brachydactyly syndrome[J]. Journal of Human Genetics, 2016, 61(8): 701-703. DOI:10.1038/jhg.2016.32 |
| [2] |
Friedman G D, Asgari M M, Warton E M, et al. Antihypertensive drugs and lip cancer in non-Hispanic whites[J]. Archives of Internal Medicine, 2012, 172(16): 1246-1251. DOI:10.1001/archinternmed.2012.2754 |
| [3] |
闫睿. 长期应用钙离子拮抗剂或与乳腺癌风险增加相关[J]. 中国循证心血管医学杂志, 2013, 5(5): 544-544. Yan Rui. Long-term use of calcium antagonists or associated with increased risk of breast cancer[J]. Chinese Journal of Evidence-Based Cardiovascular Medicine, 2013, 5(5): 544-544. DOI:10.3969/j.issn.1674-4055.2013.05.057 |
| [4] |
Zhou G, Sun Y P, Xin H, et al. In vivo antitumor and immunomodulation activities of different molecular weight lambda-carrageenans from chondrus ocellatus[J]. Pharmacological Research, 2004, 50(1): 47-53. |
| [5] |
Wang W, Zhang P, Yu G L, et al. Preparation and anti- influenza a virus activity of κ-carrageenan oligosaccharide and its sulphated derivatives[J]. Food Chemistry, 2012, 133(3): 880-888. |
| [6] |
郭娟娟. κ-卡拉胶寡糖酶法制备及其免疫防御调节机制的研究[D].福州: 福建农林大学, 2018. Guo Juanjuan. Enzymatic hydrolysis preparation of κ-carrageenan oligosaccharides and its mechanism in immunologic defense[D]. Fuzhou: Fujian Agriculture and Forestry University, 2018. http://cdmd.cnki.com.cn/Article/CDMD-10389-1018185679.htm |
| [7] |
吴海歌, 姚子昂. κ-卡拉胶寡糖抗凝血作用的研究[J]. 中国食品添加剂, 2014, 5: 84-88. Wu Haige, Yao Ziang. Anti-coagulation effects of κ- carrageenan oligosaccharides[J]. China Food Additives, 2014, 5: 84-88. |
| [8] |
黄海云, 蔡召忠. 氯沙坦对高血压患者凝血和纤溶活性指标的影响[J]. 血栓与止血学, 2017, 23(1): 108-109, 112. Huang Haiyun, Cai Zhaozhong. Effect of losartan on blood coagulation and fibrinolysis in hypertensive patients[J]. Chinese Journal of Thrombosis and Hemostasis, 2017, 23(1): 108-109, 112. DOI:10.3969/j.issn.1009-6213.2017.01.033 |
| [9] |
Iimura O, Kijima T, Kikuchi K, et al. Studies on the hypotensive effect of high potassium intake in patients with essential hypertension[J]. Clinical Science, 1981, 61(Suppl): 77-80. |
| [10] |
Suzuki H, Kondo K, Saruta T. Effect of potassium chloride on the blood pressure in two-kidney, one clip Goldblatt hypertensive rats[J]. Hypertension, 1981, 3(5): 566-573. DOI:10.1161/01.HYP.3.5.566 |
| [11] |
王金玲, 何国庆. 酶解法制备带鱼脊骨降血压肽及其降血压效果[J]. 食品与发酵工业, 2010, 36(4): 54-58. Wang Jinling, He Guoqing. Study on ACEIP production by enzyme hydrolysis from ribbonfish (trichiurus haumela) backbone and its anti-hypertensive activity[J]. Food and Fermentation Industries, 2010, 36(4): 54-58. |
| [12] |
林峰, 梁锐, 王军波, 等. 玉米低聚肽降血压作用的实验研究[J]. 食品与发酵工业, 2009, 35(8): 1-4. Lin Feng, Liang Rui, Wang Junbo, et al. The experimental study on the antihypertensive effect of corn oligopeptides[J]. Food and Fermentation Industries, 2009, 35(8): 1-4. |
| [13] |
严玉霖, 高洪, 杨进成, 等. 内毒素血症大鼠小肠黏膜免疫相关指标的变化及CA的保护作用[J]. 中国兽医学报, 2015, 35(7): 1164-1167. Yan Yulin, Gao Hong, Yang Jincheng, et al. Changes of small intestine mucosa immunity and protection of cation A in endotoxemia rats[J]. Chinese Journal of Veterinary Science, 2015, 35(7): 1164-1167. |
| [14] |
Watt J, Mclean C, Marcus R. Degradation of carrageenan for the experimental production of ulcers in the colon[J]. Journal of Pharmacy & Pharmacology, 1979, 31(1): 645-646. |
| [15] |
Norris A A, Lewis A J, Zeitlin I J. Inability of degraded carrageenan fractions to induce inflammatory bowel ulceration in the guinea-pig[J]. Journal of Pharmacy & Pharmacology, 1981, 33(1): 612-613. |
| [16] |
李苗苗.人体肠道微生物对琼胶与κ-卡拉胶及其寡糖的降解和利用研究[D].青岛: 中国海洋大学, 2014. Li Miaomiao. The degradation and utilization study of agarose, κ-carrageenan and their oligosaccharides by human gut microbiota[D]. Qingdao: Ocean University of China, 2014. http://cdmd.cnki.com.cn/Article/CDMD-10423-1014203965.htm |
| [17] |
Chen W, Liu F, Ling Z, et al. Human intestinal lumen and mucosa-associated microbiota in patients with colorectal cancer[J]. PloS One, 2012, 7(6): e39743. DOI:10.1371/journal.pone.0039743 |
| [18] |
Jaworska K, Huc T, Samborowska E, et al. Hypertension in rats is associated with an increased permeability of the colon to TMA, a gut bacteria metabolite[J]. PloS One, 2017, 12(12): e0189310. DOI:10.1371/journal.pone.0189310 |
| [19] |
Santisteban M M, Qi Y, Zubcevic J, et al. Hypertension-linked pathophysiological alterations in the gut[J]. Circulation Research, 2017, 120(2): 312-323. DOI:10.1161/CIRCRESAHA.116.309006 |
| [20] |
Grassi G, Mark A, Esler M. The sympathetic nervous system alterations in human hypertension[J]. Circulation Research, 2015, 116(6): 976-990. DOI:10.1161/CIRCRESAHA.116.303604 |
 2019, Vol. 43
2019, Vol. 43


