文章信息
- 王威, 李莉, 黎奥, 王冲, 孙同秋, 张国范. 2020.
- WANG Wei, LI Li, LI Ao, WANG Chong, SUN Tong-qiu, ZHANG Guo-fan. 2020.
- 近江牡蛎(Crassostrea ariakensis)规模化人工育苗及养成
- Large-scale artificial reproduction and cultivation of the Jinjiang Oyster (Crassostrea ariakensis
- 海洋科学, 44(2): 108-112
- Marine Sciences, 44(2): 108-112.
- http://dx.doi.org/10.11759/hykx20190711003
-
文章历史
- 收稿日期:2019-07-11
- 修回日期:2019-10-21
2. 青岛海洋科学与技术试点国家实验室海洋渔业可续与食物产出过程功能实验室, 山东 青岛 266237;
3. 青岛海洋科学与技术试点国家实验室海洋海洋生物学与生物技术功能实验室, 山东 青岛 266237;
4. 海洋生态养殖技术国家地方联合工程实验室, 山东 青岛 266071;
5. 滨州市海洋与渔业研究所, 山东 滨州 256600
2. Laboratory for Marine Fisheries Science and Food Production Processes, Pilot National Laboratory for Marine Science and Technology(Qingdao), Qingdao 266237, China;
3. Laboratory for Marine Biology and Biotechnology, Pilot National Laboratory for Marine Science and Technology(Qingdao), Qingdao 266237, China;
4. National and Local Joint Engineering Laboratory of Ecological Mariculture, Qingdao 266071, China;
5. Binzhou Ocean and Fisheries Research Institute, Binzhou 256600, China
近江牡蛎(Crassostrea ariakensis)隶属于双壳纲(Bivalvia), 珍珠贝目(Pterioida), 牡蛎科(Ostreidae), 巨蛎属(Crassostrea), 是广盐适应种, 最适盐度范围10~25, 对低盐耐受更强, 栖息在河口区淡咸水交汇处, 是我国南、北方主要河口区特有牡蛎种。近江牡蛎分布曾非常广泛, 北至中朝边境, 南至中越边境的北海都有分布[1]。巨蛎属牡蛎因形态特征与生态习性比较接近, 曾分类较混乱, 当地渔民常根据肉色差异区分为“赤蚝”与“白蚝”, “赤蚝”因受壳型、肉色、肉质等因素影响, 多被认为营养及口感不及其他牡蛎品种。根据线粒体基因(16S rRNA, COI)和核基因(28S rRNA)的序列比对, 澄清了“赤蚝”近江牡蛎(C. ariakensis)与“白蚝”香港巨牡蛎(C. hongkongensis)分类问题[2]。近江牡蛎具有强大的污染物滤除功能, 在历史上是我国河口区牡蛎礁形成的核心种[3]。牡蛎礁在净化水体、提供栖息生境、保护生物多样性、以及固碳固氮等方面具有重要的生态功能[4-6]。近年来, 受地表径流下降、港口建设等影响, 我国北方近江牡蛎呈功能性灭绝状态, 仅能见零星样品报道[7]。2017年3月, 在黄河三角洲流域滨州、东营河口区发现近江牡蛎成片的自然种群, 面临着港口建设、滥采乱捕的局面, 亟待需要尽快开展相关资源补充和保护修复工作。
鉴于近江牡蛎在北方资源量锐减甚至在多个地区河口濒危的局面, 种苗规模繁育和原位增殖是其资源保护及礁体恢复的关键。结合前期近江牡蛎不同盐度繁育实验结果[8]及成贝的耐高盐特性(尚未发表数据), 研究开展的北方近江牡蛎种群的规模化人工育苗, 采用南方低盐海区育苗, 北方原位养殖以及牡蛎主养区越冬育肥的策略, 并取得一定成效。人工养殖近江牡蛎生长快, 肉味鲜美, 有望成为我国北方高端牡蛎品种, 减小对近江牡蛎野生资源的采捕需求。规模繁育的近江牡蛎种苗, 也有助于牡蛎礁修复与重建工作的开展, 从而实现河口区生态修复与绿色治理。
1 材料和方法 1.1 材料来源近江牡蛎采集自黄河三角洲流域滨州、东营主要河口区, 采集到的近江牡蛎样品具有较大的形态差异。
1.2 实验方法 1.2.1 种质鉴定线粒体细胞色素C氧化酶Ⅰ(COI)是一个通用性强, 进化快的基因。COI基因在长牡蛎和近江牡蛎中会有碱基的差异(图 2), 不同碱基的Tm值不同, 利用HRM的方法通过SNP分型对采集牡蛎亲本进行物种鉴定[9]。
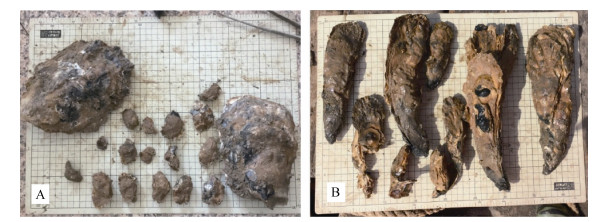 |
| 图 1 不同河口区近江牡蛎形态表现出较大差异 Fig. 1 The appearance of C. ariakensis in different estuaries revealed significant differences 注: A:马颊河河口近江牡蛎样品; B:套尔河河口近江牡蛎样品 |
将采自山东滨州的近江牡蛎, 2017年4月29日送往福建省宁德市三都澳育苗企业开展亲贝促熟管理。室内促熟条件为:盐度16~18;温度24~25℃; 饵料为混合藻类(虾塘水以及人工培养的角毛藻、扁藻和硅藻), 每天2次, 投喂量以投喂前水清为准; 培育密度35只/m3, 每2天换水一次。
1.2.3 人工授精解剖选择性腺发育较好、镜检无精子污染的的母贝, 将30只个体的卵子混合并重新分成30份, 分别与30只雄性个体的精子一对一授精, 镜检确定每份中大部分卵子出现第一极体后, 混匀30份受精卵并转入大池进行培育。
1.2.4 幼虫管理受精卵发育24h后, 大部分达到D型幼虫阶段, 孵化的种苗选取健康无畸形的上浮幼虫至培育池。每天取幼虫, 奥林巴斯数显显微镜下用数显软件测量幼虫的生长参数(壳高)。在实验期间, 每天换水1/2量, 期间投喂金藻和小球藻, 每天4次, 投喂量以投喂前水变清做调整。当幼虫平均壳高超过320μm以上, 培育水层表层取样获得幼虫超过2/3眼点幼虫时, 投放附着基使用4.3×15 cm规格塑料片、牡蛎壳串进行采苗。
1.2.5 稚贝中间培育福建宁德近江牡蛎种苗经冷藏(4℃)转运至滨州无棣县海旺育苗场, 在车间盐度20的海水中暂养2天后, 转移至盐度26~28的虾池中开展中间培育。待种苗适应滨州海区盐度后, 分苗至每串10片附着基, 每片附着基间隔15cm, 转移至养殖区筏架养殖。
1.2.6 养成以及育肥在滨州无棣县埕口镇大口河口盐场取水河道(38°14′01″N, 117°51′19″E)中开展近江牡蛎浮筏养殖, 养殖密度为每串间隔25cm。受盐场上水影响, 运河水体盐度范围17~30。将养殖1年的近江牡蛎运到山东乳山传统长牡蛎养殖区(盐度27~30), 开展常规海区的近江牡蛎笼养育肥试验。育肥期间密度为每层10只, 每笼100只。
1.2.7 氨基酸含量测定将近江牡蛎取样后, 软体部冷冻干燥后研磨成粉末, 每个样品取固体粉末100mg, 利用高效液相色谱法检测近江牡蛎中水解氨基酸的含量。
2 结果 2.1 种类鉴定图 2中可以看出待测牡蛎样品的COI基因片段溶解曲线(矫正温度后的荧光值: d(荧光值)/d(温度))和近江牡蛎标准品溶解曲线聚集在一起, 与长牡蛎标准品溶解曲线分离, 可以判断待测牡蛎样品为近江牡蛎。
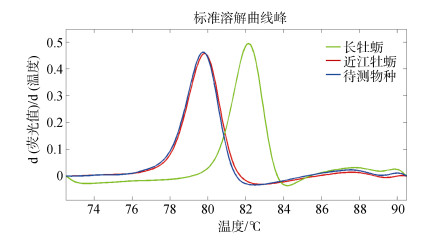 |
| 图 2 牡蛎样品的HRM鉴定结果 Fig. 2 HRM identification results of oyster samples |
2017年6月, 在福建省宁德市三都澳育苗企业投放聚丙烯塑料片附着基1 400片, 每片附苗量1 458粒, 共计培育种苗204万粒; 投放牡蛎壳附着基8万片, 平均每壳附苗量111粒, 共计培育种苗888万粒, 累计获得平均壳高 > 500μm的牡蛎稚贝苗1 092万粒, 实现了近江牡蛎规模化人工育苗。
2.3 中间培育出池后在宁德垦区及滨州无棣虾池进行中间培育标粗, 至2017年8月, 平均壳高达2.63cm, 分苗后每串有10个牡蛎壳, 共计7 820串, 平均每壳附着近江牡蛎10.6个。
2.4 养成及育肥2017年8月将附壳苗移养至运河浮筏, 至2017年10月, 成活种苗72万粒, 平均壳高6.55cm, 成活率86.84%。至2018年10月, 15月龄近江牡蛎平均壳高达98.23mm, 平均个体重90.50g。在山东乳山传统长牡蛎养殖区开展了近江牡蛎的育肥试验, 至2019年4月份, 育肥试验的近江牡蛎存活率达88%, 平均壳高达108.89mm, 平均个体重160.13g。比同期海区养殖商品规格长牡蛎个体重高37.9%。
2.5 氨基酸组成检测与长牡蛎相比, 近江牡蛎水解氨基酸含量占到干重的33.18%, 所检测到的氨基酸种类组成及含量与长牡蛎相比并无明显差异。
3 讨论早期已有近江牡蛎的人工育苗工作的报告[10-11], 但由于当时近江牡蛎的分类不明, 该类工作多为香港巨牡蛎育苗, 无法确定为近江牡蛎。盐度是近江牡蛎幼虫生长发育和附着变态的重要影响因素[12], 充分利用中国南方丰富的淡水资源, 克服了北方育苗场淡水资源匮乏的难题, 通过在人工规模繁育期间盐度、水温的调控, 在高温、低盐度的条件下对近江牡蛎进行规模化人工育苗, 并在近江牡蛎的原产区养殖以及在牡蛎主养区育肥, 构建了一条近江牡蛎“育苗-养殖”南北接力, 原产地与主养转场养殖链条。
| 化合物名称 | 水解氨基酸含量/% | |
| 近江牡蛎 | 长牡蛎 | |
| Glu | 5.32 | 5.73 |
| Asp | 3.36 | 3.92 |
| Gly | 2.81 | 2.66 |
| Lys | 2.68 | 3.11 |
| Leu | 2.53 | 2.80 |
| Arg | 2.33 | 2.73 |
| Ala | 2.10 | 2.33 |
| Pro | 2.01 | 2.08 |
| Val | 1.69 | 2.05 |
| Ser | 1.62 | 1.71 |
| Ile | 1.51 | 1.87 |
| Thr | 1.42 | 1.68 |
| Phe | 1.3 | 1.69 |
| His | 1.21 | 1.45 |
| Tyr | 1.09 | 1.01 |
| Met | 0.13 | 0.21 |
| Cys | 0.07 | 0.52 |
已有的研究表明, 牡蛎等贝类不同地理群体存在显著的遗传分化[13-14]。鉴于近江牡蛎自然分布在河口区, 不同地理群体存在基因隔离且环境差异, 近江牡蛎不同群体间也存在显著的适应性分化[15]。为了提高养殖存活率以及最大可能的保护近江牡蛎不同群体的多样性, 我们对近江牡蛎滨州群体进行了基于原产地的养殖与资源的原位修复。本次近江牡蛎中间培育获得的稚贝量仅占培育种苗量的6.65%, 较长牡蛎生产保苗率偏低, 可能受到夏季高温期长途转运幼苗的影响, 后期可以进一步优化运输与中间培育、养殖条件以提升各个环节的存活率。
近江牡蛎氨基酸含量分析表明滨州生长的近江牡蛎在氨基酸成分组成及呈味氨基酸含量上与滨州本地长牡蛎及南方的香港巨牡蛎并无显著差异[16-17], 该品种在南方养殖较少且不受市场认可的主要还是因为肉色、出肉率等原因[18]。而在中国北方, 近年来因采捕到的野生近江牡蛎个体较长牡蛎大, 受到了市场的追捧, 引发的渔民无序的采捕导致其资源的枯竭, 牡蛎礁的生态功能也遭受到严重破坏。近江牡蛎的规模化人工育苗与海区养殖的全链条的打通, 可增加近江牡蛎的养殖产量, 缓解市场对野生近江牡蛎的采捕需求, 对北方河口区近江牡蛎资源补充及牡蛎礁生态修复有着重要的现实意义。此外, 基于近江牡蛎规模化人工育苗工作开展, 近江牡蛎高盐适应、高肥满度群体的遗传改良工作以及适应性分化等基础性研究也在进行之中。
| [1] |
Zhou M F, Allen S K. A review of published work on Crassostrea ariakensis[J]. Journal of Shellfish Research, 2003, 22(1): 1-20. |
| [2] |
王海艳, 郭希明, 刘晓, 等. 中国近海"近江牡蛎"的分类和订名[J]. 海洋科学, 2007, 3(1): 85-86. Wang Haiyan, Guo Ximing, Liu Xiao, et al. Classification of "Jinjiang" oysters in China[J]. Marine Sciences, 2007, 3(1): 85-86. DOI:10.3969/j.issn.1671-6647.2007.01.012 |
| [3] |
许飞.小庙洪牡蛎礁巨蛎属牡蛎间生殖隔离研究[D].山东青岛: 中国科学院海洋研究所, 2009. Xu Fei. Reproductive isolations between oysters of genus Crassostrea on the Xiaomiaohong oyster reef[D]. Qingdao, Shandong Province: Institute of Oceanology, Chinese Academy of Sciences, 2009. |
| [4] |
Quan W M, Humphries A T, Shen X Q, et al. Oyster and associated benthic macrofaunal development on a created intertidal oyster (Crassostrea Ariakensis) reef in the Yangtze river estuary, China[J]. Journal of Shellfish Research, 2012, 31(3): 599-610. DOI:10.2983/035.031.0302 |
| [5] |
Rodney W S, Paynter K T. Comparisons of macrofaunal assemblages on restored and non-restored oyster reefs in mesohaline regions of Chesapeake Bay in Maryland[J]. Journal of Experimental Marine Biology and Ecology, 2006, 335(1): 39-51. DOI:10.1016/j.jembe.2006.02.017 |
| [6] |
Volety A K, Savarese M., Tolley S G. Eastern oysters (Crassostrea virginica) as an indicator for restoration of Everglades Ecosystems[J]. Ecological Indicators, 2009, 9: S120-S136. DOI:10.1016/j.ecolind.2008.06.005 |
| [7] |
张娜, 刘晓, 许飞, 等. 辽宁沿海巨蛎属牡蛎的分布[J]. 海洋科学, 2007, 31(9): 91-95. Zhang Na, Liu Xiao, Xu Fei, et al. Distribution of Crassostrea oysters in Liaoning coast[J]. Marine Sciences, 2007, 31(9): 91-95. DOI:10.3969/j.issn.1000-3096.2007.09.018 |
| [8] |
Xu F, Guo X M, Li L, et al. Effects of salinity on larvae of the oysters Crassostrea ariakensis, C. sikamea and the hybrid cross[J]. Marine Biology Research, 2011, 7(8): 796-803. DOI:10.1080/17451000.2011.569555 |
| [9] |
Wang J F, Xu F, Li L, et al. A new identification method for five species of oysters in genus Crassostrea from China based on high-resolution melting analysis[J]. Chinese Journal of Oceanology and Limnology, 2014, 32(2): 419-425. DOI:10.1007/s00343-014-3124-4 |
| [10] |
蔡英亚, 刘志刚, 何水养. 近江牡蛎的人工育苗[J]. 海洋科学, 1989, 13(1): 53-56. Cai Yingya, Liu Zhigang, He Shuiyang. Artificial breeding of Jinjiang oyster[J]. Marine Sciences, 1989, 13(1): 53-56. |
| [11] |
梁广耀, 陈生泰, 许国领. 近江牡蛎人工育苗试验报告[J]. 海洋科学, 1983, 7(5): 41-44. Liang Guangyao, Chen Shengtai, Xu Guoling. Experimental report on artificial breeding of Jinjiang oyster[J]. Marine Sciences, 1983, 7(5): 41-44. |
| [12] |
薛凌展, 阙华勇, 张国范, 等. 盐度对近江牡蛎幼虫生长及存活的影响[J]. 海洋科学, 2007, 31(9): 73-77. Xue Lingzhan, Que Huayong, Zhang Guofan, et al. The effect of salinity on growth and survival of Crassostrea rivularis larvae[J]. Marine Sciences, 2007, 31(9): 73-77. DOI:10.3969/j.issn.1000-3096.2007.09.014 |
| [13] |
Li L, Li A, Song K, et al. Divergence and plasticity shape adaptive potential of the Pacific oyster[J]. Nature Ecology & Evolution, 2018, 2(11): 1751-1760. |
| [14] |
Zhan A B, Hu J J, Hu X L, et al. Fine-scale population genetic structure of zhikong scallop (Chlamys farreri):do local marine currents drive geographical differentiation?[J]. Marine Biotechnology, 2009, 11(2): 223-235. DOI:10.1007/s10126-008-9138-1 |
| [15] |
Liu X Y, Li L, Li A, et al. Transcriptome and gene coexpression network analysis of two wild populations provides insight into the high-salinity adaptation mechanisms of Crassostrea ariakensis[J]. Marine Biotechnology, 2019. DOI:10.1007/s10126-019-09896-9 |
| [16] |
迟淑艳, 周歧存, 周健斌, 等. 华南沿海5种养殖贝类营养成分的比较分析[J]. 水产科学, 2007, 26(2): 79-83. Chi Shuyan, Zhou Qicun, Zhou Jianbin, et al. Comparative nutrition components in five cultured molluscs in coastal south China[J]. Fisheries Science, 2007, 26(2): 79-83. DOI:10.3969/j.issn.1003-1111.2007.02.005 |
| [17] |
刘云, 宫向红, 徐英江, 等. 烟台近海3种贝类中呈味核苷酸和氨基酸的测定及比较分析[J]. 中国水产科学, 2014, 21(2): 351-360. Liu Yun, Gong Xianghong, Xu Yingjiang, et al. Determination and comparative analysis of flavor-enhancing nucleotides and amino acids in three common shellfish from offshore Yantai[J]. Journal of Fishery Sciences of China, 2014, 21(2): 351-360. |
| [18] |
张亚锋, 雷俊, 郑晓坤, 等. 珠海牡蛎养殖业现状初步调查分析和思考[J]. 水产科技, 2010(Z1): 21-23. Zhang Yafeng, Lei Jun, Zheng Xiaokun, et al. Preliminary investigation, analysis and reflection on the status quo of oyster aquaculture in Zhuhai[J]. Fisheries Science & Technology, 2010(Z1): 21-23. |
 2020, Vol. 44
2020, Vol. 44


