文章信息
- 方士鑫, 李宪璀. 2020.
- FANG Shi-xin, LI Xian-cui. 2020.
- 壳聚糖基高吸水性树脂的制备与应用进展
- Research progress in the preparation and application of chitosan-based superabsorbent polymer
- 海洋科学, 44(3): 138-145
- Marine Sciences, 44(3): 138-145.
- http://dx.doi.org/10.11759/hykx20190614002
-
文章历史
- 收稿日期:2019-06-14
- 修回日期:2019-07-18
2. 中国科学院 海洋研究所, 山东 青岛 266071
2. Institute of Oceanology, Chinese Academy of Science, Shandong, Qingdao 266071, China
高吸水性树脂(Superabsorbent polymers, SAPs)是一类具有3维网状结构的功能高分子材料, 具有良好的吸水能力和保水能力, 吸水能力可以达到自身重量的几百至上千倍。高吸水性树脂因其优良的特性, 被广泛应用于尿布、卫生用品、干旱地区的农业和林业保水剂、污水处理以及各种各样的生物材料等领域[1-4]。尤其是干旱日益严重的今天[5], 发展高吸水性树脂材料更加具有重要的意义。目前, 商业化生产的高吸水性树脂产品大多数为石油工业的产物, 例如丙烯酸、丙烯酰胺等, 该类高吸水性树脂虽然吸水倍率高、成本低, 但也存在生物相容性差、不易降解、对环境危害等缺点[6]。近年来, 以天然多糖为原料制备高吸水性树脂成为了研究的热点, 其中, 以废弃物虾蟹壳为原料制备的壳聚糖[7], 由于原料丰富、安全无毒、良好生物相容性、可降解性以及特殊的抗菌性能等优点, 在高吸水性树脂的制备中得到了广泛的关注[8]。壳聚糖通过引入亲水基团可以制备高吸水性树脂, 壳聚糖基高吸水性树脂在保证吸水、保水能力的同时, 还具有良好的生物相容性、生物降解性以及特殊的抗菌性能等[9], 从而拓宽了高吸水性树脂的应用领域。
本文综述了壳聚糖基高吸水性树脂不同的制备方法, 及其在农业、污水处理以及生物材料中的应用, 最后对壳聚糖基高吸水性树脂的研究及应用前景进行了展望。
1 壳聚糖基高吸水性树脂 1.1 壳聚糖简介壳聚糖(Chitosan, CS)是甲壳素经过脱乙酰化处理(一般认为, 当脱乙酰度达到50%以上时)后, 得到的能溶于稀酸溶液中的产物, 壳聚糖的结构化学名称是聚(1-4)-2-氨基-β-D葡萄糖[10], 化学结构如图 1所示。与甲壳素分子相比, 壳聚糖分子结构中的C-2位主要以氨基为主, 在酸性介质中, 壳聚糖分子结构上氨基会发生质子化, 从而将壳聚糖转化为一种聚电解质, 提高了壳聚糖的溶解性[11]。
 |
| 图 1 壳聚糖化学结构图 Fig. 1 Chemical structure of chitosan |
壳聚糖是目前自然界中发现的唯一的天然碱性多糖, 具有许多优良特性, 例如生物形容性、生物降解性、成膜性、安全性、抗菌性能等[12-13]。壳聚糖的应用范围广阔, 在农业、食品、化工、医药、环保、化妆品等领域均得到了广泛的研究和应用[14-16]。数据显示, 在地球上平均每年有超过10亿吨的壳聚糖被合成, 壳聚糖是一种取之不尽用之不竭的天然生物高分子化合物, 我国海洋渔业发达, 具有丰富的壳聚糖来源。从图 1中可以看出, 壳聚糖的分子结构中含有大量的活性较高的氨基和羟基, 利于其在比较温和的条件下进行化学修饰, 得到壳聚糖基高吸水性树脂[17]。
1.2 壳聚糖高吸水性树脂的制备壳聚糖基高吸水性树脂主要采用溶液聚合法制备, 通过接枝共聚的方法将具有亲水基团的单体接枝共聚到壳聚糖骨架上, 常用的亲水性单体包括丙烯酸(AA)和丙烯酰胺(AM)等。Mahdavinia等[18]以过硫酸铵为引发剂, N, N-亚甲基双丙烯酰胺为交联剂, 采用自由基引发基质共聚反应将丙烯酸和丙烯酰胺的混合物接枝共聚到壳聚糖骨架上来制备高吸水性树脂, 反应机理如图 2所示。研究结果表明, 该高吸水性树脂具有良好的吸水能力和pH敏感性, 最大吸水倍率可达300g/g。
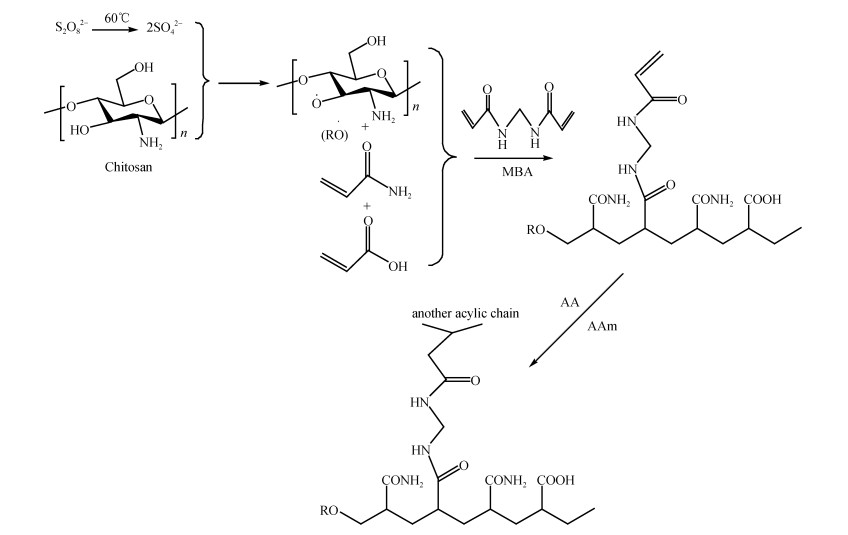 |
| 图 2 壳聚糖接枝丙烯酸-co-丙烯酰胺反应机理 Fig. 2 General mechanism for radical graft polymerization of acrylamide and acrylic acid onto chitosan |
高吸水性树脂制备过程中, 引发剂和交联剂的使用提高了生产成本, 同时增加了高吸水性树脂产品潜在的危害性和毒性, 限制了其在医学以及组织工程材料中的应用[19]。随着研究的进展, 一些更加安全、高效的方法被用来制备新型高吸水性树脂。Ge等[20]通过无引发剂和交联剂的热反应制备了壳聚糖接枝丙烯酸高吸水性树脂。通过红外光谱、固态核磁等方法表征了高吸水性树脂的结构, 确定了其成功合成。热制备方法的反应机理如图 3所示。该高吸水性树脂的最大吸水能力可达644 g/g, 这与自由基聚合制备的高吸水性树脂吸水能力相当。制备过程中没有引发剂和交联剂的加入, 减少了高吸水性树脂的毒性, 拓宽了壳聚糖基高吸水性树脂的应用范围。该研究提供了一种环境友好的壳聚糖基高吸水性树脂合成方法。
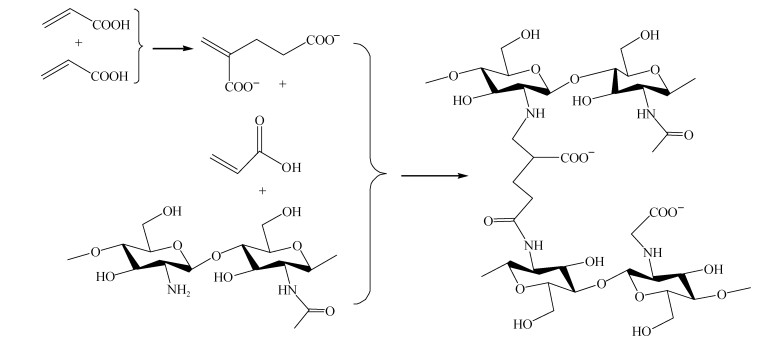 |
| 图 3 热反应法制备壳聚糖接枝丙烯酸高吸水性树脂反应机理 Fig. 3 Possible mechanism for the thermal preparation of chitosan–acrylic acid superabsorbent |
辐射诱导方法也是制备壳聚糖基高吸水性树脂的常用方法之一, 具有高效、安全等优点, 同时还可以减少制备过程中引发剂的用量。Ismail等[21]使用60Co γ射线作为引发和交联源制备基于壳聚糖和丙烯酸的高吸水性树脂, 通过表征确定了高吸水性树脂的成功制备, 该高吸水性树脂在去离子水中具有300 g/g的高溶胀能力。Samandari等[22]以紫外线诱导辐射, 在无引发剂的条件下制备了壳聚糖接枝聚丙烯酰胺高吸水性树脂, 采用红外等技术对高吸水性树脂的结构进行了表征, 研究了不同实验变量对树脂性能的影响, 确定了高吸水性树脂的最佳制备条件。在最佳制备条件下, 高吸水性树脂的吸水能力可达106 g/g。该高吸水性树脂还表现出了对Zn2+良好的吸附能力, 最大吸附量可达20.8 mg/g。
1.3 壳聚糖衍生物高吸水性树脂的制备如前所述, 壳聚糖的分子结构中含有大量活性较高的羟基和氨基基团, 可以在比较温和的条件下进行修饰, 从而得到多种壳聚糖衍生物。通过特定功能基团的引入, 可以提高壳聚糖的溶解性、生物活性、抗菌性能等。壳聚糖的衍生物也可以被用来制备高吸水性树脂。
陈煜等[23]使用羧甲基壳聚糖作为骨架, 通过接枝共聚制备了新型高吸水性树脂, 该高吸水性树脂具有良好的吸水能力。其中, 在去离子水中可以吸收自身重量550倍左右的水分, 与此同时, 该高吸水性树脂还表现出了良好pH敏感性, 在中性及弱碱性条件下, 吸水能力大; 在酸性和碱性较强的溶液中, 吸水能力下降明显。
He等[24]以壳聚糖季铵盐为原料, 通过接枝共聚制备了壳聚糖季铵盐-g-聚(丙烯酸-丙烯酰胺)高吸水性树脂, 通过傅立叶变换红外光谱和扫描电子显微镜表征了高吸水性树脂的结构和形态, 研究了新型高吸水性树脂对大肠杆菌(Escherichia coli, E. coli)和金黄色葡萄球菌(Staphylococcus aureus, S. aureus)的抑菌性能。结果表明, 以壳聚糖季铵盐为骨架制备的高吸水性树脂对两种细菌具有良好的抑菌性能, 且随着壳聚糖季铵盐用量的增大, 树脂的抑菌性能增强。季铵基团的引入是壳聚糖基高吸水性树脂具有良好抑菌性能的主要原因。
1.4 壳聚糖有机无机复合高吸水性树脂的制备壳聚糖基高吸水性树脂的制备过程中加入无机材料, 可以提高壳聚糖基高吸水性性树脂的性能, 尤其是其在溶胀状态下的机械强度。目前研究中, 应用比较多的无机材料包括黏土、金属氧化物等[25-26]。
王爱勤等[27]在以壳聚糖、凹凸棒土、丙烯酸为原料制备了有机无机复合高吸水性树脂。制备的高吸水性树脂在蒸馏水和生理盐水中分别具有159.6 g/g和42.3 g/g的吸水能力。凹凸棒土的引入, 改变了高吸水性树脂的表观形貌, 使得高吸水性树脂表面形成了更多的孔状结构。同时, 凹凸棒土还提高了高吸水性树脂的热稳定性。Tu等[28]制备了壳聚糖基高吸水性树脂, 通过引入强度较大的天然多糖纤维素及无机材料累托石提高了高吸水性树脂的机械强度, 饱和溶胀状态下, 其最大压缩模量可达到5.6 MPa。
近年来, 越来越多的无机环保材料作为添加剂被用于高吸水性树脂制备过程中。Marcelo等[29]在制备壳聚糖接枝丙烯酸高吸水性树脂过程中, 添加了稻壳灰作为无机材料, 制备了有机无机复合高吸水性树脂。实验结果表明, 该高吸水性树脂具备良好的溶胀性能。该高吸水性树脂被用于处理含有亚甲基蓝的废水, 最大除去效率可达91%。无机材料稻壳灰的加入, 增强了高吸水性树脂对亚甲基蓝染料的吸附能力。
2 壳聚糖基高吸水性树脂的应用 2.1 壳聚糖基高吸水性树脂在农业中的应用高吸水性树脂在农业中主要用作土壤保水剂, 具有保持土壤水分、降低灌溉频率、提高灌溉用水的有效利用率、促进土壤中微生物活动等作用, 同时, 天然多糖基高吸水性树脂还具有促进作物生长、提高作物抗逆性等作用[30]。
2.1.1 土壤保水剂壳聚糖为原料制备的高吸水性树脂除了具备提高土壤保水能力外, 还具有调节作物生长、提高作物产量的作用。M. Elbarbary等[31]以低分子质量的壳聚糖、海藻酸钠为原料, 采用诱导辐射方法进行聚合, 得到了多种高吸水性树脂产品。其中, 以低分子质量壳聚糖为原料制备的高吸水性树脂具有578 g/g的吸水能力。低分子质量壳聚糖和海藻酸钠的存在还提高了其保水能力。采用玉米作为模型作物, 对高吸水性树脂调节作物生长的作用进行了研究, 相同条件下, 壳聚糖/聚丙烯酸高吸水性树脂可以将玉米产量提高50%, 具有作为土壤调节剂的良好前景。该树脂产品对玉米生长的促进作用主要包括两个原因:一是低分子质量的壳聚糖具有调节植物生长的作用[32]; 二是天然多糖基具有良好的生物降解性, 被微生物分解后, 提高了土壤中的C、N元素含量, 从而增强作物的光合作用。
我国是一个干旱缺水的国家, 水资源的人均占有量不足世界人均水平的1/4, 同时水资源分布不均匀、水体污染等加重了水资源短缺的现象。水资源短缺成为制约经济社会发展的重要原因之一, 尤其是在农业生产中[33]。开发高吸水性树脂在农业保水剂上的应用对于我国农业的发展与稳定具有重要的现实意义。
2.1.2 缓控释肥料高吸水性树脂具有良好的保水能力, 进入其网络结构中的水分或者其他液体即使在一定压力下也不容易被释放, 从而起到缓释材料的作用, 高吸水性树脂用作肥料缓释材料也得到了广泛地研究[34]。
Sabadini等[35]通过在采用壳聚糖和瓜尔胶为原料通过交联作用制备了高吸水性树脂。通过红外光谱证实了瓜尔胶(HAGG)和壳聚糖(CS)之间的形成了聚合物网络结构。热重结果表明该高吸水性树脂具有良好的热稳定性。交联剂的用量对高吸水性树脂的组成与性能具有明显的影响, 随着交联剂用量的增加, 高吸水性树脂结构中瓜尔胶的含量降低, 同时高吸水性树脂的吸水能力和平均分子量也出现降低的趋势。当瓜尔胶与壳聚糖摩尔比为4︰1时, 制备的高吸水性树脂样品具有最高的吸水倍率, 可以达到218 g/g, 最长保水时间可达500 min。对高吸水性树脂中的单磷酸钾肥料释放行为进行测试, 测试结果表明, 高吸水性树脂内的养分释放时间可以达到8 h, 其释放量主要受所用肥料浓度以及高吸水性树脂性能的影响, 该高吸水性树脂表现出了良好的缓释能力。
Wang等[36]以磷酸锌铵和尿素为肥料内核, 以醋酸丁烯纤维素为内涂层, 以羧甲基壳聚糖接枝丙烯酸/坡缕石复合高吸水性树脂为外涂层, 制备了一种新型多功能控释肥, 并且评估了外涂层在土壤溶液中的降解能力和养分的释放行为。实验结果表明, 高吸水性树脂包膜的缓释肥料, 可以有效降低磷元素的淋失, 提高土壤保水能力, 改善土壤酸碱度。León等[37]采用壳聚糖接枝衣康酸的方法, 制备了新型高吸水性树脂, 并在高吸水性树脂中负载尿素颗粒, 研究了尿素的缓释行为。
2.2 壳聚糖基高吸水性树脂在污水处理中的应用高吸水性树脂还可以用于污水处理。工业和生活污水直接排入天然水资源, 造成水体污染, 加重了水资源短缺。特别是含有染料和重金属离子的废水, 即使浓度很低, 也会对人体健康产生不利影响[38]。研究者采用多种方法处理废水, 在这些方法中, 吸附被认为是一种有效且经济的废水处理方法。高吸水性树脂具有良好的吸附能力, 因此常被用来处理含有染料、重金属离子、磷酸盐、硝酸盐、药物等有害物质的污水[39, 40]。
Puspitasari等[41]在室温下使用辐射诱导制备了壳聚糖接枝共聚丙烯酰胺高吸水性树脂, 其对废水中的重金属离子(包括Zn2+, Cr6+, Pb2+, Cu2+, Co2+和Ni2+)展现出了比较高的吸附能力。研究者还发现可以通过壳聚糖和丙烯酰胺之间不同的重量比来调节高吸水性树脂对重金属离子的吸附能力。Wang等[42]制备了壳聚糖接枝丙烯酸/明胶复合高吸水性树脂, 用于吸附污水中的Cu2+, 最大吸附量可达153.9 mg/g。
除了吸附重金属离子之外, 壳聚糖基高吸水性树脂还被用来去除污水中含有的染料。Zhou等[43]采用两步聚合法成了纳米TiO2/壳聚糖/聚(N-异丙基丙烯酰胺)复合高吸水性树脂用于去除水溶液中的酸性品红(AF)染料。通过红外光谱和扫描电子显微镜研究了该吸水性树脂的结构和表面形态。结果表明, 复合高吸水性树脂具有发达的微孔结构。通过对含有AF染料的废水进行处理发现, 温度和pH是影响AF染料去除效率的主要因素。随着温度的升高, 染料去除率略有下降, AF染料在40℃时可以很容易地去除。实验结果表明染料与高吸水性树脂之间存在静电吸引力。Bhattacharyya等[44]将微米和纳米尺寸的膨润土添加到壳聚糖接枝丙烯酸高吸水性树脂的制备过程中, 制得了有机无机复合高吸水性树脂材料。该高吸水性树脂对孔雀石绿和甲基紫染料均具有良好的吸附能力。Ngwabebhoh等[45]以壳聚糖和淀粉为原料制备了复合高吸水性树脂, 研究了其对染料Direct Red 80(DR80)的吸附能力, 最大吸附能力可以达到312.77 mg/g。
壳聚糖基高吸水性树脂具有吸收速率快、吸附容量高以及良好的可重复使用性等优点, 且具有良好的降解性, 在废水处理过程中不会造成二次污染。因此, 壳聚糖的基高吸水性树脂在污水处理的研究与应用前景广阔。
2.3 高吸水性树脂在生物材料中的应用高吸水性树脂可以在其网络结构内吸收和保留大量的液体, 并呈现出类似软组织的机械性能。高吸水性树脂被认为是一种理想的组织工程材料, 可以应用于伤口敷料, 药物递送, 组织工程等[46]。
2.3.1 伤口敷料高吸水性树脂是一种非常理想的伤口敷料材料, 可以吸收伤口渗出物并提供潮湿的环境, 以促进伤口的愈合。特别是壳聚糖基高吸水性树脂, 具有其他材料无可比拟的优点, 例如无毒性、生物相容性、特殊的抗菌性能以及促进伤口愈合等[47]。
Fan等[48]开发了一种基于壳聚糖的高吸水性树脂作为伤口敷料。在该研究中, 壳聚糖(CS), 明胶(Gel)和聚乙烯醇(PVA)作为原料, 在γ射线辐射诱导下制备了新型复合高吸水性树脂, 并对其性能进行了一系列测试。结果表明CS / Gel / PVA高吸水性树脂具有优异的性能, 如pH敏感性、良好的溶胀能力、适宜的水蒸发速率以及一定的机械性能。该产品可以快速吸收伤口的血液并粘附在伤口表面, 刺激血小板释放凝血因子, 促进和加速血液凝固。这种高吸水性树脂在伤口敷料的应用中具有很大的临床潜力。
Chen等[49]通过乙醇沉淀法制备了一种具有多孔结构的羧甲基壳聚糖接枝丙烯酸高吸水性树脂, 研究了其在伤口敷料中的应用。研究结果表明该高吸水性树脂表现出了良好的生物相容性和无毒性。与其他临床伤口敷料相比, 该产品对新西兰白兔耳动脉、股动脉、脾脏出血模型均具有更加良好的止血性能。Yang等[50]制备了一种基于聚(乙烯醇)、水溶性壳聚糖的高吸水性树脂作为伤口敷料。细胞毒性试验表明高吸水性树脂对小鼠成纤维细胞无毒。与纱布敷料相比, 高吸水性树脂可以加速大鼠模型中伤口的愈合过程。用高吸水性树脂伤口敷料处理伤口, 14天后, 观察到伤口处成熟的表皮结构形成。实验结果表明, 该高吸水性树脂是一种良好的伤口敷料。
2.3.2 组织工程材料高吸水性树脂还可以作为组织替代的生物医学支架。主要原因是高含水量使高吸水性树脂与大多数活的组织具有良好的生物相容性。同时, 高吸水性树脂的机械性能适合于修复组织的形态和功能特征[51]。
Hao等[52]制备了一种具有温度敏感性壳聚糖基高吸水性树脂, 采用壳聚糖、甘油磷酸钠(GP)和羟乙基纤维素(HEC)为原料, 制备的高吸水性树脂用于重建组织工程软骨, 并修复绵羊模型中的关节软骨缺损。通过将羊软骨细胞与壳聚糖基高吸水性树脂混合, 在体外环境下, 对受损的组织系统软骨进行重建实验。实验结果表明, 受损的软骨组织在24周内完全被修复。壳聚糖基高吸水性树脂具有支持软骨细胞的基质积累、修复绵羊软骨缺损的作用。
2.3.3 药物控释材料壳聚糖基高吸水性树脂还可以用作药物控释材料。Sohail等[53]以低分子质量壳聚糖为原料, 通过化学交联制备了壳聚糖共聚甲基丙磺酸高吸水性树脂, 研究了其溶胀行为和pH敏感性, 采用模型药物对该树脂的控释能力进行了测试, 该树脂具有控释药物系统所需的合适特征。Samanta等[54]制备了多种壳聚糖基高吸水性树脂。通过红外、核磁X射线衍射表征高吸水性树脂的结构和性质。研究茶碱和替硝唑模型药物在高吸水性树脂中的负载和体外释放行为。两种药物均表现出了良好的控释行为。壳聚糖基高吸水性树脂在药物控释系统中具有良好的应用前景。
3 结论与展望本文旨在综述和讨论壳聚糖基高吸水性树脂的合成方法和应用现状。壳聚糖可以与丙烯酸、丙烯酰胺等通过自由基聚合方法制备高吸水性树脂。本文还综述热制备法、诱导辐射等更加环境友好的制备方法, 并讨论了其制备机理。壳聚糖基高吸水性树脂除了优异的吸水性和保水能力外, 还具有良好的生物相容性、可降解性、安全无毒, 环境友好和原料来源丰富的优点。由于其优异的性能, 壳聚糖基高吸水性树脂在伤口止血材料、个人护理产品、农田保水剂以及污水处理等方面均得到了研究与应用。
然而, 制备性能更加优异的壳聚糖基高吸水性树脂仍然具有一定的挑战, 未来的研究工作应考虑以下几个方面:
开发更加环境友好的壳聚糖基高吸水性树脂制备方法, 减少引发剂、交联剂等在制备过程中的使用。
研究壳聚糖基高吸水性树脂结构与功能之间的关系, 根据功能需求, 设计高吸水性树脂的结构。
加强壳聚糖基高吸水性树脂生物学功能的研究, 特别是利用壳聚糖在抑菌能力方面的突出优点, 制备具有抑菌性能的新型壳聚糖基高吸水性树脂, 拓宽壳聚糖基高吸水性树脂在生物材料领域的应用。
| [1] |
王爱勤, 张俊平. 有机-无机复合高吸水性树脂[M]. 北京: 科学出版社, 2006: 9-12. Wang Aiqin, Zhang Junping. Organic-inorganic superabsorbent composite[M]. Beijing: Sicence Press, 2006: 9-12. |
| [2] |
Zohuriaan-Mehr M J, Omidian H, Doroudiani S, et al. Advances in non-hygienic applications of superabsorbent hydrogel materials[J]. Journal of Materials Science, 2010, 45(21): 5711-5735. DOI:10.1007/s10853-010-4780-1 |
| [3] |
Zhan F, Liu M, Guo M, et al. Preparation of superabsorbent polymer with slow-release phosphate fertilizer[J]. Journal of Applied Polymer Science, 2004, 92(5): 3417-3421. DOI:10.1002/app.20361 |
| [4] |
Csada R D, Brigham R M. Application of Superabsorbent Polymers for Improving the Ecological Chemistry of Degraded or Polluted Lands[J]. CLEAN-Soil, Air, Water, 2010, 37(8): 517-526. |
| [5] |
Marvel K, Cook B I, Bonfils C J W, et al. Twentieth-century hydroclimate changes consistent with human influence[J]. Nature, 2019, 569(7754): 59-65. DOI:10.1038/s41586-019-1149-8 |
| [6] |
贾振宇, 崔英德, 黎新明, 等. 聚丙烯酸钠高吸水性树脂的改性研究进展[J]. 化工进展, 2004, 23(5): 468-471. Jia Zhenyu, Cui Yingde, Li Xinming, et al. Progress in modification of poly -AA -Na super absorbent polymer[J]. Chemical Industry and Engineering Progress, 2004, 23(5): 468-471. DOI:10.3321/j.issn:1000-6613.2004.05.003 |
| [7] |
Anitha A, Sowmya S, Kumar P T S, et al. Chitin and chitosan in selected biomedical applications[J]. Progress in Polymer Science, 2014, 39(9): 1644-1667. DOI:10.1016/j.progpolymsci.2014.02.008 |
| [8] |
Dash M, Chiellini F, Ottenbrite R M, et al. Chitosan-A versatile semi-synthetic polymer in biomedical applications[J]. Progress in Polymer Science, 2011, 36(8): 981-1014. DOI:10.1016/j.progpolymsci.2011.02.001 |
| [9] |
El-Mekawy A, Hudson S, El-Baz A, et al. Preparation of Chitosan Films Mixed with Superabsorbent Polymer and Evaluation of Its Haemostatic and Antibacterial Activities[J]. Journal of Applied Polymer Science, 2010, 116(6): 3489-3496. |
| [10] |
Hayes M. Chitin, Chitosan and their derivatives from marine rest raw materials: potential food and pharmaceutical applications[M]. 2012, Springer, Boston, MA.
|
| [11] |
Choi C, Nam J P, Nah J W. Application of chitosan and chitosan derivatives as biomaterials[J]. Journal of Industrial and Engineering Chemistry, 2016, 33: 1-10. DOI:10.1016/j.jiec.2015.10.028 |
| [12] |
Dutkiewicz J K. Superabsorbent materials from shellfish waste-A review[J]. Journal of Biomedical Materials Research, 2002, 63(3): 373-381. |
| [13] |
Kong M, Chen X G, Xing K, et al. Antimicrobial properties of chitosan and mode of action:A state of the art review[J]. International Journal of Food Microbiology, 2010, 144(1): 51-63. |
| [14] |
Pillai C K S, Paul W, Sharma C P. Chitin and chitosan polymers:Chemistry, solubility and fiber formation[J]. Progress in Polymer Science, 2009, 34(7): 641-678. DOI:10.1016/j.progpolymsci.2009.04.001 |
| [15] |
Rabelo V M, Magalhaes P C, Bressanin L A, et al. The foliar application of a mixture of semisynthetic chitosan derivatives induces tolerance to water deficit in maize, improving the antioxidant system and increasing photosynthesis and grain yield[J]. Scientific reports, 2019, 9(1): 8164-8164. DOI:10.1038/s41598-019-44649-7 |
| [16] |
Hassan M A, Omer A M, Abbas E, et al. Preparation, physicochemical characterization and antimicrobial activities of novel two phenolic chitosan Schiff base derivatives[J]. Scientific Reports, 2018, 8(1): 1-14. DOI:10.1038/s41598-017-17765-5 |
| [17] |
Alves N M, Mano J F. Chitosan derivatives obtained by chemical modifications for biomedical and environmental applications[J]. International Journal of Biological Macromolecules, 2008, 43(5): 401-414. DOI:10.1016/j.ijbiomac.2008.09.007 |
| [18] |
Mahdavinia G R, Pourjavadi A, Hosseinzadeh H, et al. Modified chitosan 4. Superabsorbent hydrogels from poly(acrylic acid-co-acrylamide) grafted chitosan with salt- and pH-responsiveness properties[J]. European Polymer Journal, 2004, 40(7): 1399-1407. DOI:10.1016/j.eurpolymj.2004.01.039 |
| [19] |
Rai P, Lee B M, Liu T Y, et al. Safety evaluation of disposable baby diapers using principles of quantitative risk assessment[J]. Journal of Toxicology and Environmental Health-Part a-Current Issues, 2009, 72(21-22): 1262-1271. DOI:10.1080/15287390903212246 |
| [20] |
Ge H, Wang S. Thermal preparation of chitosan-acrylic acid superabsorbent:Optimization, characteristic and water absorbency[J]. Carbohydrate Polymers, 2014, 113: 296-303. DOI:10.1016/j.carbpol.2014.06.078 |
| [21] |
Ismail S A, Hegazy E S A, Shaker N O, et al. Radiation synthesis of superabsorbent hydrogels based on chitosan and acrylic acid for controlled drug release[J]. Journal of Macromolecular Science Part a-Pure and Applied Chemistry, 2009, 46(10): 967-974. DOI:10.1080/10601320903158560 |
| [22] |
Saber-Samandari S, Gazi M, Yilmaz E. UV-induced synthesis of chitosan-g-polyacrylamide semi-IPN superabsorbent hydrogels[J]. Polymer Bulletin, 2012, 68(6): 1623-1639. DOI:10.1007/s00289-011-0643-4 |
| [23] |
Chen Y, Liu Y F, Tang H L, et al. Study of carboxymethyl chitosan based polyampholyte superabsorbent polymer Ⅰ Optimization of synthesis conditions and pH sensitive property study of carboxymethyl chitosan-g-poly(acrylic acid-co-dimethyldiallylammonium chloride) superabsorbent polymer[J]. Carbohydrate Polymers, 2010, 81(2): 365-371. DOI:10.1016/j.carbpol.2010.02.007 |
| [24] |
He G H, Ke W W, Chen X, et al. Preparation and properties of quaternary ammonium chitosan-g-poly (acrylic acid-co-acrylamide) superabsorbent hydrogels[J]. Reactive & Functional Polymers, 2017, 111: 14-21. |
| [25] |
Ferfera-Harrar H, Aiouaz N, Dairi N, et al. Preparation of chitosan-g-poly (acrylamide)/montmorillonite superabsorbent polymer composites:Studies on swelling, thermal, and antibacterial properties[J]. Journal of Applied Polymer Science, 2014, 131(1): 1-14. |
| [26] |
Dehaghi S M, Rahmanifar B, Moradi A M, et al. Removal of permethrin pesticide from water by chitosan-zinc oxide nanoparticles composite as an adsorbent[J]. Journal of Saudi Chemical Society, 2014, 18(4): 348-355. DOI:10.1016/j.jscs.2014.01.004 |
| [27] |
Zhang J P, Wang Q, Wang A Q. Synthesis and characterization of chitosan-g-poly (acrylic acid)/attapulgite superabsorbent composites[J]. Carbohydrate Polymers, 2007, 68(2): 367-374. DOI:10.1016/j.carbpol.2006.11.018 |
| [28] |
Tu H, Yu Y, Chen J, et al. Highly cost-effective and high-strength hydrogels as dye adsorbents from natural polymers:chitosan and cellulose[J]. Polymer Chemistry, 2017, 8(19): 2913-2921. DOI:10.1039/C7PY00223H |
| [29] |
Vaz M G, Pereira A G B, Fajardo A R, et al. Methylene blue adsorption on chitosan-g-poly(acrylic acid)/rice husk ash superabsorbent composite:Kinetics, equilibrium, and thermodynamics[J]. Water Air & Soil Pollution, 2017, 228(1): 1-14. |
| [30] |
王勇, 小岛纪德. 改良荒漠化土壤的多功能高分子复合材料的制备及其应用[J]. 中国水土保持, 2008(8): 44-47. Wang Yong, Kojim Toshinor. Preparation and application of multi-functional polymer composite material to improving desertification soil[J]. Solid and water conservation in China, 2008(8): 44-47. DOI:10.3969/j.issn.1000-0941.2008.08.017 |
| [31] |
Elbarbary A M, Abd El-Rehim H A, El-Sawy N M, et al. Radiation induced crosslinking of polyacrylamide incorporated low molecular weights natural polymers for possible use in the agricultural applications[J]. Carbohydrate Polymers, 2017, 176: 19-28. DOI:10.1016/j.carbpol.2017.08.050 |
| [32] |
Abd El-Rehim H A, El-Sawy N M, Farag I A, et al. Synergistic effect of combining ionizing radiation and oxidizing agents on controlling degradation of Na-alginate for enhancing growth performance and increasing productivity of zea maize plants[J]. Carbohydrate Polymers, 2011, 86(4): 1439-1444. DOI:10.1016/j.carbpol.2011.05.066 |
| [33] |
Piao S L, Ciais P, Huang Y, et al. The impacts of climate change on water resources and agriculture in China[J]. Nature, 2010, 467(7311): 43-51. DOI:10.1038/nature09364 |
| [34] |
Essawy H A, Ghazy M B M, Abd El-Hai F, et al. Superabsorbent hydrogels via graft polymerization of acrylic acid from chitosan-cellulose hybrid and their potential in controlled release of soil nutrients[J]. International Journal of Biological Macromolecules, 2016, 89: 144-151. DOI:10.1016/j.ijbiomac.2016.04.071 |
| [35] |
Sabadini R C, Martins V C A, Pawlicka A. Synthesis and characterization of gellan gum:chitosan biohydrogels for soil humidity control and fertilizer release[J]. Cellulose, 2015, 22(3): 2045-2054. DOI:10.1007/s10570-015-0590-6 |
| [36] |
Wang X, Lu S, Gao C, et al. Biomass-based multifunctional fertilizer system featuring controlled-release nutrient, waterretention and amelioration of soil[J]. Rsc Advances, 2014, 4(35): 18382-18390. DOI:10.1039/c4ra00207e |
| [37] |
Leon O, Munoz-Bonilla A, Soto D, et al. Preparation of oxidized and grafted chitosan superabsorbents for urea delivery[J]. Journal of Polymers and the Environment, 2018, 26(2): 728-739. DOI:10.1007/s10924-017-0981-x |
| [38] |
Pakdel P M, Peighambardoust S J. Review on recent progress in chitosan-based hydrogels for wastewater treatment application[J]. Carbohydrate Polymers, 2018, 201: 264-279. DOI:10.1016/j.carbpol.2018.08.070 |
| [39] |
Ma Y L, Lv L, Guo Y R, et al. Porous lignin based poly (acrylic acid)/organo-montmorillonite nanocomposites:Swelling behaviors and rapid removal of Pb (Ⅱ) ions[J]. Polymer, 2017, 128: 12-23. DOI:10.1016/j.polymer.2017.09.009 |
| [40] |
Cruz H, Luckman P, Seviour T, et al. Rapid removal of ammonium from domestic wastewater using polymer hydrogels[J]. Scientific Reports, 2018, 8. |
| [41] |
Puspitasari T, Oktaviani, Pangerteni D S, et al. Study of metal ions removal from aqueous solution by using radiation crosslinked chitosan-co-poly (acrylamide)-based adsorbent[J]. Macromolecular Symposia, 2015, 353(1): 168-177. DOI:10.1002/masy.201550323 |
| [42] |
Wang W B, Huang D J, Kang Y R, et al. One-step in situ fabrication of a granular semi-IPN hydrogel based on chitosan and gelatin for fast and efficient adsorption of Cu2+ ion[J]. Colloids and Surfaces B-Biointerfaces, 2013, 106: 51-59. DOI:10.1016/j.colsurfb.2013.01.030 |
| [43] |
Zhou J H, Hao B Z, Wang L B, et al. Preparation and characterization of nano-TiO2/chitosan/poly(N-isopropylacrylamide) composite hydrogel and its application for removal of ionic dyes[J]. Separation and Purification Technology, 2017, 176: 193-199. DOI:10.1016/j.seppur.2016.11.069 |
| [44] |
Bhattacharyya R, Ray S K. Micro- and nano-sized bentonite filled composite superabsorbents of chitosan and acrylic copolymer for removal of synthetic dyes from water[J]. Applied Clay Science, 2014, 101: 510-520. DOI:10.1016/j.clay.2014.09.015 |
| [45] |
Ngwabebhoh F A, Gazi M, Oladipo A A. Adsorptive removal of multi-azo dye from aqueous phase using a semi-IPN superabsorbent chitosan-starch hydrogel[J]. Chemical Engineering Research & Design, 2016, 112: 274-288. |
| [46] |
Ismail S, Hegazy E S, Shaker N, et al. Radiation synthesis of superabsorbent hydrogels based on chitosan and acrylic acid for controlled drug release[J]. Journal of Macromolecular Science:Part A-Chemistry, 2009, 46(10): 967-974. |
| [47] |
Muzzarelli R a A. Chitins and chitosans for the repair of wounded skin, nerve, cartilage and bone[J]. Carbohydrate Polymers, 2009, 76(2): 167-182. DOI:10.1016/j.carbpol.2008.11.002 |
| [48] |
Fan L H, Yang H, Yang J, et al. Preparation and characterization of chitosan/gelatin/PVA hydrogel for wound dressings[J]. Carbohydrate Polymers, 2016, 146: 427-434. DOI:10.1016/j.carbpol.2016.03.002 |
| [49] |
Chen Y, Zhang Y, Wang F, et al. Preparation of porous carboxymethyl chitosan grafted poly (acrylic acid) superabsorbent by solvent precipitation and its application as a hemostatic wound dressing[J]. Materials Science & Engineering C-Materials for Biological Applications, 2016, 63: 18-29. |
| [50] |
Yang X, Yang K, Wu S, et al. Cytotoxicity and wound healing properties of PVA/ws-chitosan/glycerol hydrogels made by irradiation followed by freeze-thawing[J]. Radiation Physics and Chemistry, 2010, 79(5): 606-611. DOI:10.1016/j.radphyschem.2009.12.017 |
| [51] |
Croisier F, Jerome C. Chitosan-based biomaterials for tissue engineering[J]. European Polymer Journal, 2013, 49(4): 780-792. DOI:10.1016/j.eurpolymj.2012.12.009 |
| [52] |
Hao T, Wen N, Cao J K, et al. The support of matrix accumulation and the promotion of sheep articular cartilage defects repair in vivo by chitosan hydrogels[J]. Osteoarthritis and Cartilage, 2010, 18(2): 257-265. DOI:10.1016/j.joca.2009.08.007 |
| [53] |
Sohail M, Ahmad M, Minhas M U, et al. Controlled delivery of valsartan by cross-linked polymeric matrices:Synthesis, in vitro and in vivo evaluation[J]. International Journal of Pharmaceutics, 2015, 487(1-2): 110-119. DOI:10.1016/j.ijpharm.2015.04.013 |
| [54] |
Samanta H S, Ray S K. Controlled release of tinidazole and theophylline from chitosan based composite hydrogels[J]. Carbohydrate Polymers, 2014, 106: 109-120. DOI:10.1016/j.carbpol.2014.01.097 |
 2020, Vol. 44
2020, Vol. 44


