文章信息
- 周玉婷, 李佳霖, 赵振军, 秦松. 2022.
- ZHOU Yu-ting, LI Jia-lin, ZHAO Zhen-jun, QIN Song. 2022.
- 海洋微微型蓝藻与异养细菌相互作用的研究进展
- Advances in the interactions between marine picocyanobacteria and heterotrophic bacteria
- 海洋科学, 46(4): 123-132
- Marine Sciences, 46(4): 123-132.
- http://dx.doi.org/10.11759/hykx20210805002
-
文章历史
- 收稿日期:2021-08-05
- 修回日期:2021-09-15
2. 烟台大学 生命科学学院, 山东 烟台 264005;
3. 中国科学院海洋大科学研究中心, 山东 青岛 266071
2. College of Life Sciences, Yantai University, Yantai 264005, China;
3. Center for Ocean Mega-Science, Chinese Academy of Sciences, Qingdao 266071, China
海洋微生物处于复杂的微食物网络中, 光合自养微生物和异养微生物之间的相互作用是海洋食物网的基础, 驱动了海洋物质循环[1]。原绿球藻和聚球藻是海洋微微型蓝藻最重要的两个属, 在全球碳循环中发挥关键作用[2]; 尤其是在寡营养开阔海域, 它们贡献浮游植物总碳生物量的20%~58%[3]。在加利福尼亚近岸及临近开阔海域使用原子力显微镜观察, 发现超过40%的聚球藻细胞表面附着有细菌[4], 这说明两者有着非常密切的关系, 且可能存在一定的相互作用机制; 实验室培养中, 原绿球藻和聚球藻的单克隆培养物通常附着有异养细菌, 主要原因是它们之间有密切的相互作用关系[5-6]。浮游细菌和真核藻类在菌藻圈中的相互作用已经被证实[7], 而关于海洋微微型蓝藻与共栖异养细菌的相互作用研究刚起步且不全面[6, 8-9], 本综述旨在论述海洋微微型蓝藻与共栖异养细菌的相互作用方式及互惠关系, 为促进两者相互作用机制及海洋代谢流过程的研究提供参考。
1 相互作用的研究意义与研究方法自然界中处于同一生境的不同物种之间存在复杂的相互作用关系, 这些相互作用关系主要包括: 种间共处、互生、共生、拮抗、竞争、寄生和捕食, 一个典型的例子就是植物根际环境中植物与细菌之间的相互作用。作为连接土壤与植物的媒介, 根际所含生物种类众多, 被认为是地球上最复杂的生态系统之一[10], 自1904年德国生物学家Lorenz Hiltner首次提出根际环境以来, 根际中植物与细菌之间的相互作用受到了研究者的广泛关注。植物根际微生物中同时存在对植物生长起促进作用和抑制作用的微生物, 并且这些微生物的群落组成随着植物种类以及发育时期等因素的改变而发生变化[11]。
蓝藻是最小的原核光合生物。原绿球藻属与聚球藻属是其中最重要的2个属, 是海洋生态系统中丰度最高的微微型浮游植物。根据生态模型估计原绿球藻和聚球藻的全球年平均丰度分别为2.9±0.1× 1027个/mL和7.0±0.3×1026个/mL, 两者的全球净初级生产力分别为4 Gt C·y–1和8 Gt C·y–1, 相当于海洋净初级生产力的8.5%和16.7%, 是全球丰度最高的初级生产者[12]。两者处于邻近的遗传分支, 但在生理生态特征上存在差别。在细胞大小上, 原绿球藻的粒径为0.4~1.2 μm, 是目前发现的最小的单细胞海洋蓝藻[13], 聚球藻比原绿球藻稍大, 其直径介于0.6~1.7 μm[14]。从生态分布来看, 它们在海洋中占据互补但重叠的生态位, 原绿球藻地理分布较窄, 在寡营养海域的数量丰富[12], 而聚球藻广泛存在于从高纬度至热带的所有海洋环境中, 在富营养的海域中丰度更高[15]。从系统发育来看, 原绿球藻根据光适应特性和二乙烯基叶绿素b/a的比值分为高光适应型和低光适应型, 每一种适应型含有多种基因型; 聚球藻根据其DNA的G+C含量和光合色素特点主要被分为3个亚簇即5.1, 5.2和5.3, 每一个亚簇都包含几十种基因型。
随着根际微生态中植物与微生物相互作用研究的深入, 发现根际微生物对植物的生长、营养供应、疾病抑制等方面具有重要作用[16], 海洋环境中的菌-藻关系包括协同作用、拮抗作用以及群体感应的研究也逐渐开展[17]。协同作用表现为菌-藻的相互选择和相互协调[1], 是维持菌-藻复杂的群落结构的基础, 藻类释放的溶解有机碳、维生素、氨基酸等营养物质会被细菌吸收[18-19], 细菌代谢产物中的营养盐和生长因子对藻类生长起着促进作用[20]。拮抗作用是菌-藻间的竞争性排斥、干扰、抑制的过程[21]。细菌对藻类有毒害作用, 例如, 溶藻细菌可以直接吸附到藻类细胞表面或在藻类细胞表面滑动, 释放溶藻酶来溶解、杀死藻细胞[22-23]; 藻类能够产生抗菌化合物对细菌表现出拮抗[24]。群体感应是菌-藻相互感应的调控机制, 当种群到达一定密度时对基因表达产生影响, 进而对生理、生化产生影响[25-26]。藻类与细菌的共栖体系中, 藻类分泌的代谢产物以及细菌达到一定浓度后都会产生群体感应现象[27-28]。相对于传统成熟的土壤根际微生物研究, 处于海洋环境中的微微型蓝藻与异养细菌的相互作用研究存在特殊性。首先, 海洋的水体环境使相互作用处于流通变化中, 而根际环境位于相对稳定的土体; 其次, 海洋微微型蓝藻是最简单的原核初级生产者, 呈浮游状态广泛分布于全球海洋中; 最后, 海洋微微型蓝藻与共栖异养细菌的大小相似, 相互作用方式相对于大型植物与其根际异养细菌的作用会有所不同。无论是原位还是实验室培养, 都发现海洋微微型蓝藻周围存在共栖异养细菌, 且长期培养过程中添加了异养细菌的原绿球藻和聚球藻培养体系相对于无菌体系都能保持更长时间的生长[9, 29]; 对长期培养体系中的代谢产物进行研究, 发现微微型蓝藻产生的溶解性有机物可以被异养细菌利用, 异养细菌分解产生的无机营养盐进一步被微微型蓝藻利用[30-31]。原绿球藻和聚球藻还能产生不同类型被称为细菌素的次级代谢产物, 这是一种合成核糖体的肽, 可能在海洋微微型蓝藻的信号传导或化感作用中发挥潜力[32-33], 对异养细菌群落产生一定的促进或抑制作用。因此, 相对于海洋环境中其他藻类与异养细菌的几种相互作用方式, 海洋微微型蓝藻与异养细菌的相互作用方式主要是互惠共生, 两者之间促进作用大于抑制作用[34]。本综述研究海洋微微型蓝藻与共栖异养细菌的相互作用, 可以揭示海洋复杂环境中微微型蓝藻与共栖异养细菌的功能互补关系及代谢物流过程, 为全球海洋物质循环的深入研究, 以及共存微生物之间的相互作用方式和对种群结构的影响提供新的见解。
目前海洋微微型蓝藻与异养细菌的相互作用研究主要通过共培养实验进行, 通过基因组学、蛋白质组学以及基因敲除技术揭示探讨相互作用的方式和机制。相互作用的物质基础一般需要对共培养体系中的代谢产物进行分析, 代谢产物的分析主要采用质谱方法[35]。非靶向稳定同位素辅助的液相色谱-质谱联用(LCMS)方法适用于海洋微微型蓝藻的代谢产物分析, 对聚球藻PCC7002的代谢产物进行分析发现, 主要的代谢产物包括氨基酸及氨基酸衍生物、糖衍生物、碱基和核苷、有机酸和二氢鞘氨醇[36], 这些产物可以作为异养细菌的营养来源被吸收[18]。
2 相互作用的异养细菌类群在海洋水体中, 高通量测序结果显示主要的微生物类群通常是蓝藻(Cyanobacteria)、α-变形杆菌(α-Proteobacteria)、γ-变形杆菌(γ-Proterbacteria)和拟杆菌(Bacteroidetes)[37]。而浮游植物藻华过程中水体的微生物优势类群主要包括拟杆菌中的黄杆菌(Flavobacteria)、α-变形杆菌中的玫瑰杆菌(Roseobacter)和根瘤菌(Rhizobiales)、γ-变形杆菌中的交替单胞菌(Alteromonas)、浮霉菌(Planctomycetacia)、厚壁菌(Firmicute)和放线菌(Actinobacteria)等[31, 38-40]。两者相比, 拟杆菌比例明显增高, α-变形菌和γ-变形菌同样占有较大比例, 因此, 拟杆菌、α-变形菌和γ-变形菌被认为是与浮游微藻共存的主要异养细菌。在共培养实验中也证实, 与原绿球藻和聚球藻共栖的异养细菌主要集中在以上3种细菌纲中, 黄杆菌、玫瑰杆菌和交替单胞菌是其中的主要类群(表 1)。
| 属 | 菌株 | 共存异养细菌 | 参考文献 |
| 聚球藻 | XM-5, XM-11, XM-24, XM-13, Cy04, YX-A3-2, YX04-3, YX02-3, ZS01-1, ZS02-2 |
Fluviicola taffensis DSM 16823, Algoriphagus ornithinivorans IMSNU 14014, Phaeocystidibacter marisrubri G18, Polaribacter marinivivus GYSW-15, Balneola vulgaris DSM 17893, Ichthyenterobacterium magnum Th6, Lewinella marina MKG-38, Owenweeksia hongkongensis DSM 17368, Marinoscillum luteum SJP7, Balneola alkaliphila CM41_14b, Lewinella nigricans NBRC 102662, Fabibacter pacificus DY53, Thalassobius gelatinovorus IAM 12617, Thalassobius mediterraneus XSM19, Celeribacter halophilus ZXM137, Maricaulis maris ATCC 15268, Marivita geojedonensis DPG-138, Roseicyclus mahoneyensis ML6, Loktanella koreensis GA2-M3, Pelagibius litoralis CL-UU02, Alteromonas maeleodii ATCC 27126, Pseudomonas songnenensis' NEAU-ST5-5, Candidatus Limnoluna rubra MWH-EgelM2-3 | [6] |
| WH8102 | V. parahaemolyticus | [61] | |
| XM-24 | Flavobacterales, Rhodobacterales, Cytophagales, Sphingomonadales | [44] | |
| CC9311 | Tropicibacter sp., Stappia sp. | [30] | |
| BL107 | Paracoccus sp., Marinobacter sp., Muricauda sp. | [30] | |
| WH7803 | R. pomeroyi DSS-3, Ruegeria lacuscaerulensis ITI1157, Dinoroseobacter shibae DFL12, Roseobacter denitrificans OCh114 | [30] | |
| 原绿球藻 | MED4 | Alteromonas sp. strain EZ32, Rhodospirillaceae strain EZ35 | [62] |
| MIT9313 | Alteromonas sp. strain EZ33, Halomonas sp. strain EZ34, Alteromonas macleodii HOT1A3 | [34, 62] | |
| MIT9312 | Flavobacteriaceae strain EZ40, Sphingomonas sp. strain EZ41, Alteromonas sp. strain EZ42 | [62] | |
| MIT9211 | Marinobacter sp. strain EZ43, Marinobacter sp. strain EZ44 | [62] | |
| NATL2A | Alteromonas sp. strain EZ45, Alcanivorax sp. strain EZ46, Alteromonas macleodii MIT1002 | [62, 68] | |
| SS120 | Pseudoalteromonas sp. strain EZ48, Rhodospirillaceae strain EZ49 | [62] | |
| MIT9215 | Alteromonas sp. strain EZ55, Rhodospirillaceae strain EZ54 | [62] | |
| MED4, MIT9313 |
Rhodobacterales, Alcanivoracaceae, Marinobacter, Alteromonadales, OM60, Oceanospirillales | [34] |
黄杆菌是海洋环境中重要的拟杆菌, 含有编码α-甘露糖苷酶基因, 是能水解糖苷的优势菌, 在浮游植物赤潮过程中是微生物“第一响应者”, 偏好利用复杂的高分子量有机物或生物聚合物, 如藻类多糖、纤维素、甲壳素和果胶等[38-39]。玫瑰杆菌在全球海洋中分布广泛, 被认为是重要的生态学“通才(generalist)”[41-42], 可以利用生物聚合物和不稳定的低分子量有机物, 包括浮游植物生长和黄杆菌生长的副产物, 如二甲基硫丙酸盐(DMSP)和香草酸盐(vanillate)等[31, 39, 41]。通过对黄杆菌和玫瑰杆菌胞内(胞外)的蛋白质进行组学分析, 发现其含有附着/聚集的外膜黏附蛋白[38, 43], 能够实现在细胞表面的黏附, 进而实现有机物的降解功能[44]。
在海洋微微型蓝藻的生长过程中, 由于释放的有机物组分存在差异, 共存微生物利用有机碳的模式不同形成对释放有机物存在响应和动态变化[40]。对聚球藻XM-24在培养过程中的有机碳浓度和优势异养细菌种群动态变化及在聚球藻表面聚集/附着细胞比例的评估分析发现, 异养细菌与微微型蓝藻的共栖方式主要有附着、游离以及在附着与游离两种状态中交替进行的3种方式, 同时异养细菌能利用培养体系中不同的有机物, 且按丰度从高至低存在一定的连续关系(图 1)[6]: 黄杆菌是最丰富的类群, 附着在聚球藻表面, 专门降解复杂的高分子量有机物。玫瑰杆菌是培养体系中的第二大群体, 主要以游离生长的方式存在, 不仅利用由水解酶降解的生物聚合物, 而且吸收不稳定的低分子量有机物, 以及来自聚球藻和黄杆菌生长的副产物。交替单胞菌是第三大共栖类群, 共栖方式在附着和游离状态之间交替发生, 其表现出广泛的底物偏好, 主要吸收黄杆菌和玫瑰杆菌的遗留产物, 与二者互补。
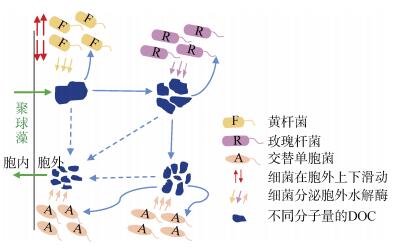 |
| 图 1 聚球藻与共栖异养细菌代谢物流动模式图 Fig. 1 Model diagram of metabolic flow between Synechococcus sp. and symbiotic heterotrophic bacteria |
海洋生物固定的碳在海洋生态系统中沿食物链不断循环利用, 碳的初级和次级生产过程主要由浮游植物和异养细菌完成[45]。仅在透光层(光照层)内, 初级生产力(约为40 Gt C·y–1)和异养呼吸(约为37 Gt C·y–1)占全球海洋碳循环通量的一半以上[46]。海洋微微型蓝藻贡献了海洋净初级生产的相当大比例, 并在亚微米级尺度上与异养细菌有着密切的联系[8], 微微型蓝藻能够外渗支持异养细菌生长的细胞质多肽[47], 异养细菌能吸收海洋微微型蓝藻渗出或溶解产生的溶解性有机碳(DOC)[48]。在海洋微微型蓝藻和异养细菌共培养体系中, 不提供任何外源性有机碳源, 共培养第15 d左右两者都能达到高细胞丰度(> 108 cells·mL–1)[30]。海洋微微型蓝藻是兼性异养光合细菌, 它们一方面具有氨基酸、糖、寡肽和磷酸盐同化基因, 能摄取简单的有机化合物, 如氨基酸和葡萄糖[49], 另一方面能通过光合作用产生DOC和POC, 为自身生长以及异养细菌提供营养; 由于海洋微微型蓝藻缺乏必要的胞外水解酶[47], 不能摄取复杂的高分子量有机物[31], 因此可能依赖异养细菌胞外酶的水解, 从而以互惠的方式实现营养物质的流动及交换。
无机氮也是相互作用中的一种重要物质。虽然不同生态位的原绿球藻和聚球藻在利用氮源上存在一定差别, 但都能在含有NH4+的培养基上生长良好, 并且能够利用尿素[50]。氮缺乏的情况下, 聚球藻可以降解细胞内氮源丰富的捕光色素蛋白藻红蛋白, 向环境中释放氮源[51]。在对厦门近岸微生物分解聚球藻衍生代谢产物的研究中发现[52], 微生物在整个培养期间介导了C和N代谢过程之间的耦合, 异养细菌快速消耗聚球藻代谢产物并伴随大量NH4+产生, 微生物种群丰度也随之增加。这说明在两者之间进行碳循环的同时氮元素也可能处于循环状态。但是在海洋微微型蓝藻与异养细菌相互作用过程中对氮元素的研究较少, 氮元素的流向与循环可以作为以后的研究重点。
3.2 相互作用的作用机制 3.2.1 相互作用中异养细菌的有机碳来源方式浮游植物通过光合作用合成的有机物除供给自身生长能量需要外, 最终以溶解有机物(DOM)和颗粒有机物(POM)的形式释放到周围环境中, 释放的途径主要包括主动/被动分泌、浮游动物摄食、病毒裂解和细胞衰老腐烂等[53]。释放的有机物绝大部分可以通过异养细菌的“二次生产”进入微食物网[54]。异养细菌对来自海洋微微型蓝藻的代谢物表现出快速趋向性, 这种聚集现象称为趋化性[55]。趋化性是海洋异养细菌中常见的行为[56-57], 其结果是造成异养细菌与浮游植物之间的距离缩减[6, 30]。趋化性在细菌-海洋微微型蓝藻的相互作用中普遍存在, 影响了海洋真光层的碳和营养物质循环。浮游植物释放的化学物质是海洋细菌产生趋化性的有效诱导剂[58-59]。海洋微微型蓝藻向水体中分泌的DOC也能使异养细菌产生趋化性, 通过微流控化学趋化实验研究, 发现所有异养细菌菌株对聚球藻产物都产生强烈而快速趋化行为[60]。
通过测定总有机碳(TOC)及溶解有机碳通量可以评估海洋微微型蓝藻与异养细菌之间的营养物质流动[48, 52]。基于显微放射自显影结合荧光原位杂交技术(MAR-FISH)的阳性细胞百分比分析表明, 拟杆菌对海洋微微型蓝藻产生的DOC具有极高的亲和力, 在原绿球藻和聚球藻的阳性异养细菌群落中拟杆菌所占比例最高, 分别为65%和23%[45]。聚球藻WH8102与弧菌(Vibrio)的共培养体系, 在不添加外源有机碳的条件下可以实现指数生长, 此共培养的成功也反映了弧菌具有利用聚球藻产生的有机碳生存的能力[61]。培养实验发现, 聚球藻PCC7002和CCMP1334在生长过程中能向培养体系释放丰富的DOC; 与异养细菌共培养20 d后, PCC7002的DOC浓度从85.7 μmol/L降至68.6 μmol/L, 减少了20%, CCMP1334的DOC浓度从75.7 μmol/L降至50.0 μmol/L, 减少了35%, 两者均显著降低; 且随着DOC浓度的降低, 与聚球藻PCC7002和CCMP1334共培养的异养细菌数量分别增加了550%(从0.18×107至1.17×107个·mL–1)和850% (从0.33×107至3.16×107个·mL–1)[8]。结合以上实验, 说明海洋微微型蓝藻释放至胞外的有机碳作为异养细菌的趋化动力, 使异养细菌靠近, 最终被异养细菌利用并转化为自身的有机碳。
3.2.2 海洋微微型蓝藻的生存优势依赖异养细菌的协助大部分稀释的原绿球藻菌株不能在平板上生长, 而与异养细菌共存的情况下生长效果明显变好, 能在液体培养基中以稀释培养物的形式生长, 也能在半固体琼脂糖平板上形成菌落[62]。此外, 原绿球藻的全基因组序列中缺乏过氧化氢酶的编码基因, 异养细菌产生的过氧化氢酶通过催化HOOH转化为H2O和O2, 降解体系中的过氧化氢, 进而避免原绿球藻受到氧化损伤。例如Alteromonas sp. EZ55与原绿球藻的共培养体系可以有效迅速地将HOOH降至零, 使原绿球藻免受氧化损伤并促进生长[63]。海洋中HOOH的主要来源是降雨和溶解有机碳的光化学降解[64-65], 在太平洋和马尾藻海透光层中, HOOH的浓度范围约为0~0.2 μmol/L, 在此浓度范围内原绿球藻可以生长, 但若没有辅助异养细菌去除海水中的HOOH, HOOH将达到原绿球藻无法生存的浓度水平(0.8 μmol/L)[63]。
在长期营养缺乏或能量胁迫情况下, 海洋蓝藻能够通过形成代谢活性非常低的休眠细胞而存活。实验室培养的聚球藻PCC7942在氮饥饿即N浓度低于1 mmol/L, 或重金属胁迫即Cd浓度达到2.5 μmol/L的情况下, 培养超过28 d左右进入休眠期来保持存活的状态[66-67]; 在这一过程中, 聚球藻会发生黄化现象, 光合作用关闭、光系统及蛋白质合成活性降低、细胞叶绿素自发荧光丧失, 同时培养物漂白, 而发生黄化的聚球藻细胞在转移到新的培养基后很难继续存活。对原绿球藻菌株在长期黑暗胁迫实验表明, 原绿球藻只能在35 h内忍受光饥饿, 向共培养中添加交替单胞菌MIT002能使它们在黑暗中存活的时间延长了11 d[68]。原位极端营养限制条件下, 原绿球藻细胞较小, 能正常成长, 通过增加生物量的特异性扩散和特定的代谢策略最小化细胞营养需求能够实现正常生长, 但这些生存机制在无菌培养中作用不显著[69]。在氮或磷饥饿的多重压力条件下, 通过纳米二次离子质谱仪(NanoSIMS)测定碳和氮吸收效率, 原绿球藻菌株MIT9313代谢活性降低, 会发生黄化过程, 转移到新的无菌培养基后, 黄化的原绿球藻不能存活且无法再生; 同样条件下与异养细菌(交替单胞菌HOT1A3)共培养不仅能存活数月且原绿球藻菌株转入培养基后可以实现生长[9]。
3.2.3 海洋微微型蓝藻生长吸收异养细菌“释放”的营养物质海洋微食物网碳流循环的一个重要途径是海洋浮游植物与异养细菌的相互作用。浮游植物初级生产释放的碳水化合物、氨基酸、有机磷酸盐等营养物质, 可以被异养细菌吸收利用[19]; 异养细菌吸收利用这些有机物后大部分通过呼吸作用返回大气, 部分转化为自身的生物质碳, 还有部分被异养细菌代谢后转化为无机营养盐甚至小分子有机物再重新被初级生产者利用[30, 48]。
在经过不提供外源有机碳和N、P充分饥饿处理后, 用NaHCO3-13C和NH4Cl-15N同位素标记的培养基来培养原绿球藻菌株与异养细菌, 结果发现原绿球藻能吸收这两种无机养分[9]。原绿球藻除了能摄取无机养分, 还能摄取小分子有机物, 北太平洋环流中的原绿球藻能大量吸收亮氨酸[70]; 在阿拉伯海域, 以35S标记的蛋氨酸示踪剂作为不稳定含氮化合物的标志物, 通过测定示踪剂浓度, Zubkov等[71]发现, 原绿球藻在寡营养海域消耗有机含氮化合物, 并且负责蛋氨酸周转(~1 nmol/L)和高达30%的蛋氨酸吸收(20 nmol/L)。同时, 原绿球藻全基因组分析也表明, 其存在氨基酸转运系统[72]。在不添加外源有机碳的培养体系中, 聚球藻WH8102与弧菌共培养后, 通过基因组微阵列分析发现, 聚球藻的转运蛋白及光合作用相关基因明显上调; 另外, 培养体系中不改变磷酸盐浓度, 参与磷酸盐获取和磷酸盐胁迫反应的基因显著上调, 说明种间相互作用对聚球藻的生理存在多重影响, 聚球藻可以利用弧菌代谢产生的磷酸盐[61]; 聚球藻也可能同化DOM, 聚球藻WH8102的基因组分析发现, 其存在与运输氨基酸、寡肽和氰酸盐基因的同源基因[73]: 聚球藻能吸收甘氨酸和二甲基硫丙酸盐(DMSP)[74-75], 且作为DMSP的主要消费者, 其同化的DMSP量占原核生物总同化量的20%; 聚球藻还可以利用尿素[76]和氨基酸[77]等其他简单有机物。
虽然海洋蓝藻能通过光合作用进行碳固定产生有机物, 但是不能吸收复杂的有机物, 需要辅助酶水解后才能吸收[78], 异养细菌产生的胞外水解酶可以将大分子的生物聚合物水解成小分子物质[31]。大多数海洋有机物是以生物聚合物的形式存在于海水中, 生物聚合物是由共价键结合形成的较大分子量的结构单元, 但是微生物的运输系统以小于0.6 kDa分子大小输送, 因此在微生物获取它们之前, 必须在细胞外水解[79]。胞外酶是指附着在细菌细胞膜上的酶, 在生物聚合物水解和初始加工中起着重要作用。通过外蛋白质组学研究发现, 异养细菌中高达35%的编码基因能水解细胞分泌的蛋白质, 包括膜连接蛋白(例如膜转运蛋白、胞外酶或运动蛋白), 这些蛋白很容易被转运到细胞外并在胞外蛋白质组部分发现[31, 80]。对2种不同的玫瑰杆菌菌株的细胞组分进行蛋白质组学分析, 发现其胞外蛋白质组的很大一部分参与了可利用的碳和能量来源的主动膜转运[81-82]。
3.2.4 海洋微微型蓝藻与共栖异养细菌相互作用对碳循环的帮助颗粒有机碳(POC)以下沉颗粒的形式存在, 主要由浮游植物、细菌和无机物的絮凝物组成, 是海洋碳循环的主要组成部分。由于微微型蓝藻的体积小, 缺乏天然沉降矿物(如高岭黏土), 下沉速度慢, 因此它们在POC通量中的贡献仍然不确定。在百慕大的寡营养海域, 沿水柱向下, 聚球藻在下沉颗粒中占有较高比例, 而原绿球藻则相反[83]。与原绿球藻相比, 聚球藻具有较高的聚集和POC输出潜力, 且更容易形成快速沉降的颗粒。聚球藻的聚集体形成取决于粒子碰撞的次数, 并随着介质中粒子的丰度(即细胞数)和黏性系数(即碰撞后细胞保持附着的概率)的增加凝聚作用增强。Cruz和Neuer[2]的研究表明, 与直链菌的共培养体系中, 异养细菌的存在使培养基中含有更多颗粒, 其与微微型蓝藻大小相似, 增加了培养基中颗粒碰撞的频率, 使微微型蓝藻的聚集增强。TEP是透明的胞外聚合物颗粒, 主要由酸性多糖组成的有机颗粒[84], 被认为是海洋中生物碳泵的关键成分[85-86]。异养细菌对聚球藻与原绿球藻聚集的影响是通过TEP介导的两种不同方式: 聚球藻的聚集增强是由于异养细菌对聚球藻产生的TEP的修饰; 原绿球藻的聚集增强是由于异养细菌产生的TEP使颗粒黏性增强而增加聚集(图 2)。而异养细菌在TEP的产生和原绿球藻和聚球藻的聚集中的特殊作用目前还没有相关结论, 需要通过将每种微微型蓝藻与代表性的异养分离株共同培养来阐明。
 |
| 图 2 异养细菌产生的TEP对海洋微微型蓝藻的修饰作用 Fig. 2 Modification of picocyanobacteria by TEP produced by heterotrophic bacteria |
海洋微微型蓝藻是遍布全球海洋的重要初级生产者, 与共栖异养细菌构成了海洋微食物网的重要组成部分, 两者相互依存, 其相互作用关系的研究具有重要意义。相互作用的异养细菌谱系主要集中在黄杆菌、玫瑰杆菌及交替单胞菌, 它们不仅共栖方式不同, 而且通过不同的碳利用模式将蓝藻产生的有机碳转化为生物质碳, 从而对蓝藻产生的有机碳做出快速响应。同时, 异养细菌能为蓝藻提供必要的有机营养物及再矿化释放的无机质; 与原绿球藻共栖的异养细菌, 不仅能使原绿球藻免受过氧化氢的毒害, 还能维持其在长期营养胁迫下的生存, 共栖异养细菌产生的TEP能协助微微型蓝藻加速下沉, 有助于形成POC絮凝, 是海洋生态系统中碳循环的重要途径。
由于海洋微微型蓝藻与共栖异养细菌之间的相互作用方式复杂多样, 基于目前的研究结果仍无法准确说明两者之间的相互作用关系及机制, 未来的研究内容主要包括: (1) 聚球藻和原绿球藻已经证实存在转运蛋白编码基因, 能够利用共培养体系中的有机营养物质, 可以采用分子生物学中基因操作的方法验证相关蛋白的功能, 研究海洋微微型蓝藻与共栖异养细菌的功能互补及代谢物流过程; (2) 海洋微微型蓝藻释放不同组成特征的初级产物, 这些产物能够影响异养细菌群落的种群结构, 从而产生生态位和生物地化循环特征, 通过宏基因组学及代谢组学的方法对不同环境条件微微型蓝藻和异养细菌的共培养实验研究海洋微微型蓝藻代谢产物对原始海洋微生物类群的影响, 论证其对微生物群落变化的生物影响作用及其对生态环境可能产生的反馈; (3) 海洋微微型蓝藻与异养细菌相互作用中的的物质交换是微食物网的基础, 揭示微微型蓝藻初级生产产物经共栖异养细菌降解过程对微食物网的影响也是后期研究的重点。通过对以上内容的研究可以深入阐明海洋微微型蓝藻与共栖异养细菌相互作用的方式、机制及影响要素, 为系统研究海洋生态系统的物质循环和能量输送提供科学依据和理论支撑。
| [1] |
AZAM F, FENCHEL T, FIELD J G, et al. The ecological role of water-column microbes in the sea[J]. Marine Ecology, 1983, 10: 257-263. DOI:10.3354/meps010257 |
| [2] |
CRUZ B N, NEUER S. Heterotrophic bacteria enhance the aggregation of the marine picocyanobacteria Prochlorococcus and Synechococcus[J]. Front in Microbiology, 2019, 10(1864): 1-11. |
| [3] |
DURAND M D, OLSON R J, CHISHOLM S W. Phytoplankton population dynamics at the Bermuda Atlantic Time-series station in the Sargasso Sea[J]. Deep Sea Research PartⅡ, 2001, 48(8/9): 1983-2003. |
| [4] |
MALFATTI F, AZAM F. Atomic force microscopy reveals microscale networks and possible symbioses among pelagic marine bacteria[J]. Aquatic Microbial Ecology, 2009, 58(1): 1-14. DOI:10.1007/s00248-008-9442-3 |
| [5] |
MOORE L R, COE A, ZINSER E R, et al. Culturing the marine cyanobacterium Prochlorococcus[J]. Limnology and Oceanography, 2007, 5(10): 353-362. |
| [6] |
ZHENG Q, WANG Y, XIE R, et al. Dynamics of heterotrophic bacterial assemblages within Synechococcus cultures[J]. Applied Environmental Microbiology, 2018, 84(3): AEM. 01517-17.
|
| [7] |
THOMPSON H F, SUMMERS S, YUECEL R, et al. Hydrocarbon-degrading bacteria found tightly associated with the 50−70 μm cell-size population of eukaryotic phytoplankton in surface waters of a Northeast Atlantic region[J]. Microorganisms, 2020, 8(1955): 1-16. |
| [8] |
ZHANG Z, TANG L, LIANG Y, et al. The relationship between two Synechococcus strains and heterotrophic bacterial communities and its associated carbon flow[J]. Journal of Applied Phycology, 2021, 33(2): 953-966. DOI:10.1007/s10811-020-02343-6 |
| [9] |
ROTH-ROSENBERG D, AHARONOVICH D, LUZZATTO- KNAAN T, et al. Prochlorococcus cells rely on microbial interactions rather than on chlorotic resting stages to survive long-term nutrient starvation[J]. mBio, 2020, 11(4): e01846-20. DOI:10.1128/mBio.01846-20 |
| [10] |
RAAIJMAKERS J M, PAULITZ T C, STEINBERG C, et al. The rhizosphere: a playground and battlefield for soilborne pathogens and beneficial microorganisms[J]. Plant and Soil, 2008, 321(1/2): 341-361. |
| [11] |
周文杰, 吕德国, 秦嗣军. 植物与根际微生物相互作用关系研究进展[J]. 吉林农业大学学报, 2016, 38(3): 253-260. ZHOU Wenjie, LV Deguo, QIN Sijun. Research progress in interaction between plant and rhizosphere microorganism[J]. Journal of Jilin Agricultural University, 2016, 38(3): 253-260. |
| [12] |
FLOMBAUM P, GALLEGOS J L, GORDILLO R A, et al. Present and future global distributions of the marine Cyanobacteria Prochlorococcus and Synechococcus[J]. Proceedings of the National Academy of Sciences, 2013, 110(24): 9824-9829. DOI:10.1073/pnas.1307701110 |
| [13] |
JOHNSON P W, SIEBURTH J M J L, OCEANOGRAPHY. Chroococcoid cyanobacteria in the sea: A ubiquitous and diverse phototrophic biomass[J]. Limnology and Oceanography, 1979, 24(5): 928-935. DOI:10.4319/lo.1979.24.5.0928 |
| [14] |
WATERBURY J B, WATSON S W, VALOIS F W, et al. Biological and ecological characterization of the marine unicellular cyanobacterium Synechococcus[J]. Canadian Journal of Fisheries and Aquatic Sciences, 1986, 214: 71-120. |
| [15] |
PARTENSKY F, BLANCHOT J, VAULOT D. Differential distribution and ecology of Prochlorococcus and Synechococcus in oceanic waters: a review[M]//Charpy L and Larkum A W D. Marine Cyanobacteria. Bulletin de l'Institut océanographique, Monaco Numéro spécial 19, 1999: 457-475.
|
| [16] |
KHAN A, DING Z T, ISHAQ M, et al. Applications of beneficial plant growth promoting rhizobacteria and mycorrhizae in rhizosphere and plant growth: A review[J]. International Journal of Agricultural and Biological Engineering, 2020, 13(5): 199-208. DOI:10.25165/j.ijabe.20201305.5762 |
| [17] |
李芸, 刘发龙, 王巧晗, 等. 藻际微环境中藻体与微生物相互作用[J]. 河北渔业, 2019(3): 43-48. LI Yun, LIU Falong, WANG Qiaohan, et al. The Interaction between algae and microorganisms in the phycosphere[J]. Hebei Fisheries, 2019(3): 43-48. |
| [18] |
白洁, 易齐涛, 李佳霖. 海洋异养细菌对小球藻生长和无机营养盐吸收的影响研究[J]. 海洋科学, 2009, 33(11): 6-10. BAI Jie, YI Qitao, LI Jialin. The effect of Chlorella growth and inorganic nutrients absorption by marine heterotrophic bateria[J]. Marine Sciences, 2009, 33(11): 6-10. |
| [19] |
周文礼, 肖慧, 王悠, 等. 小球藻与2株藻际异养细菌相互作用的研究[J]. 北京理工大学学报, 2008, 28(7): 643-647. ZHOU Wenli, XIAO Hui, WANG You, et al. A Study on the Interaction Between Chlorella Vulgaris and Heterotrophic Bacteria in Phycosphere[J]. Transactions of Beijing Institute of Technology, 2008, 28(7): 643-647. |
| [20] |
JIAO N Z, HERNDL G J, HANSELL D A, et al. Microbial production of recalcitrant dissolved organic matter: long-term carbon storage in the global ocean[J]. Nature Reviews Microbiology, 2010, 8(8): 593-599. DOI:10.1038/nrmicro2386 |
| [21] |
BIDLE K D, FALKOWSKI P G. Cell death in planktonic, photosynthetic microorganisms[J]. Nature Reviews Microbiology, 2004, 2(8): 643-655. DOI:10.1038/nrmicro956 |
| [22] |
MAYALI X, AZAM F. Algicidal bacteria in the sea and their impact on algal blooms[J]. Journal of Eukaryotic Microbiology, 2004, 51(2): 139-144. DOI:10.1111/j.1550-7408.2004.tb00538.x |
| [23] |
SHILO M. Lysis of blue-green algae by myxobacter[J]. Journal of Bacteriology, 1970, 104(1): 453-461. DOI:10.1128/jb.104.1.453-461.1970 |
| [24] |
RIZZO L, FRASCHETTI S, ALIFANO P, et al. Association of Vibrio community with the Atlantic Mediterranean invasive alga Caulerpa cylindracea[J]. Journal of Experimental Marine Biology and Ecology, 2016, 475: 129-136. DOI:10.1016/j.jembe.2015.11.013 |
| [25] |
FUQUA W C, WINANS S C, GREENBERG E P. Quorum sensing in Bacteria: the LuxR-LuxI family of cell density-responsive transcriptional regulatorst[J]. Journal of Bacteriology, 1994, 176(2): 269-275. DOI:10.1128/jb.176.2.269-275.1994 |
| [26] |
SCHAUDER S, BASSLER B L. The languages of bacteria[J]. Genes & Development, 2001, 15(12): 1468-1480. |
| [27] |
NATRAH F M I, KENMEGNE M M, WIYOTO W, et al. Effects of micro-algae commonly used in aquaculture on acyl-homoserine lactone quorum sensing[J]. Aquaculture, 2011, 317(1/4): 53-57. |
| [28] |
WILLIAMS P. Quorum sensing, communication and cross-kingdom signalling in the bacterial world[J]. Microbiology, 2007, 153(12): 3923-3838. DOI:10.1099/mic.0.2007/012856-0 |
| [29] |
KAUR A, HERNANDEZ-FERNAUD J R, AGUILO- FERRETJANS M D M, et al. 100 Days of marine Synechococcus-Ruegeria pomeroyi interaction: A detailed analysis of the exoproteome[J]. Environmental Microbiology, 2018, 20(2): 785-799. DOI:10.1111/1462-2920.14012 |
| [30] |
CHRISTIE-OLEZA J A, SOUSONI D, LLOYD M, et al. Nutrient recycling facilitates long-term stability of marine microbial phototroph-heterotroph interactions[J]. Nature Microbiology, 2017, 2: 17100. DOI:10.1038/nmicrobiol.2017.100 |
| [31] |
CHRISTIE-OLEZA J A, SCANLAN D J, ARMENGAUD J. "You produce while I clean up", a strategy revealed by exoproteomics during Synechococcus-Roseobacter interactions[J]. Proteomics, 2015, 15(20): 3454-3462. DOI:10.1002/pmic.201400562 |
| [32] |
LI B, SHER D, KELLY L, et al. Catalytic promiscuity in the biosynthesis of cyclic peptide secondary metabolites in planktonic marine cyanobacteria[J]. Proceedings of the National Academy of Sciences, 2010, 107(23): 10430-10435. DOI:10.1073/pnas.0913677107 |
| [33] |
AHARONOVICH D, SHER D. Transcriptional response of Prochlorococcus to co-culture with a marine Alteromonas: differences between strains and the involvement of putative infochemicals[J]. The ISME Journal, 2016, 10: 2892-2906. DOI:10.1038/ismej.2016.70 |
| [34] |
SHER D, THOMPSON J W, KASHTAN N, et al. Response of Prochlorococcus ecotypes to co-culture with diverse marine bacteria[J]. The ISME Journal, 2011, 5: 1125-1132. DOI:10.1038/ismej.2011.1 |
| [35] |
GARCIA D E, BAIDOO E E, BENKE P I, et al. Separation and mass spectrometry in microbial metabolomics[J]. Current Opinion in Microbiology, 2008, 11(3): 233-239. DOI:10.1016/j.mib.2008.04.002 |
| [36] |
GOMEZ-BAENA G, LOPEZ-LOZANO A, GIL-MARTINEZ J, et al. Glucose uptake and its effect on gene expression in Prochlorococcus[J]. PLoS One, 2008, 3(10): e3416. DOI:10.1371/journal.pone.0003416 |
| [37] |
WILLIAMS T J, WILKINS D, LONG E, et al. The role of planktonic Flavobacteria in processing algal organic matter in coastal East Antarctica revealed using metagenomics and metaproteomics[J]. Environmental Microbiology, 2013, 15(5): 1302-1317. DOI:10.1111/1462-2920.12017 |
| [38] |
KIRCHMAN D L. The ecology of Cytophaga-Flavobacteria in aquatic environments[J]. FEMS Microbiology Ecology 2002, 39(2): 91-100.
|
| [39] |
TEELING H, FUCHS B M, BECHER D, et al. Substrate- controlled succession of marine bacterioplankton populations induced by a phytoplankton bloom[J]. Science, 2012, 336(6081): 608-611. DOI:10.1126/science.1218344 |
| [40] |
BUCHAN A, LECLEIR G R, GULVIK C A, et al. Master recyclers: features and functions of bacteria associated with phytoplankton blooms[J]. Nature Reviews Microbiology, 2014, 12(10): 686-698. DOI:10.1038/nrmicro3326 |
| [41] |
MOU X Z, SUN S L, EDWARDS R A, et al. Bacterial carbon processing by generalist species in the coastal ocean[J]. Nature, 2008, 451(7179): 708-711. DOI:10.1038/nature06513 |
| [42] |
NEWTON R J, GRIFFIN L E, BOWLES K M, et al. Genome characteristics of a generalist marine bacterial lineage[J]. The ISME Journal, 2010, 4: 784-798. DOI:10.1038/ismej.2009.150 |
| [43] |
BUCHAN A, GONZALEZ J M, MORAN M A. Overview of the marine roseobacter lineage[J]. Applied Environmental Microbiology, 2005, 71(10): 5665-5677. DOI:10.1128/AEM.71.10.5665-5677.2005 |
| [44] |
ZHENG Q, LU J Y, WANG Y, et al. Genomic reconstructions and potential metabolic strategies of generalist and specialist heterotrophic bacteria associated with an estuary Synechococcus culture[J]. FEMS Microbiology Ecology, 2019, 95(3): 1-13. |
| [45] |
SARMENTO H, GASOL J M. Use of phytoplankton- derived dissolved organic carbon by different types of bacterioplankton[J]. Environmental Microbiology, 2012, 14(9): 2348-2360. DOI:10.1111/j.1462-2920.2012.02787.x |
| [46] |
GIORGIO P A D, DUARTE C M. Respiration in the open ocean[J]. Nature, 2002, 420: 379-384. DOI:10.1038/nature01165 |
| [47] |
CHRISTIE-OLEZA J A, ARMENGAUD J, GUERIN P, et al. Functional distinctness in the exoproteomes of marine Synechococcus[J]. Environmental Microbiology, 2015, 17(10): 3781-3794. DOI:10.1111/1462-2920.12822 |
| [48] |
GASOL J M, PINHASSI J, ALONSO-SÁEZ L, et al. Towards a better understanding of microbial carbon flux in the sea[J]. Aquatic Microbial Ecology, 2008, 53: 21-38. DOI:10.3354/ame01230 |
| [49] |
YELTON A P, ACINAS S G, SUNAGAWA S, et al. Global genetic capacity for mixotrophy in marine picocyanobacteria[J]. The ISME Journal, 2016, 10: 2946-2957. DOI:10.1038/ismej.2016.64 |
| [50] |
LISA R. MOORE, ANTON F. POST, GABRIELLE ROCAP, et al. Utilization of different nitrogen sources by the marine cyanobacteria Prochlorococcus and Synechococcus[J]. Limnology and Oceanography, 2002, 47(4): 989-996. DOI:10.4319/lo.2002.47.4.0989 |
| [51] |
WYMAN M, GREGORY R, CARR N J S. Novel role for phycoerythrin in a marine cyanobacterium, Synechococcus strain DC2[J]. Science, 1985, 230(4727): 818-820. DOI:10.1126/science.230.4727.818 |
| [52] |
XIE R, WANG Y, CHEN Q, et al. Coupling between carbon and nitrogen metabolic processes mediated by coastal microbes in Synechococcus-derived organic matter addition incubations[J]. Frontiers in Microbiology, 2020, 11(1041): 1-15. |
| [53] |
MUHLENBRUCH M, GROSSART H P, EIGEMANN F, et al. Mini-review: Phytoplankton-derived polysaccharides in the marine environment and their interactions with heterotrophic bacteria[J]. Environmental Microbiology, 2018, 20(8): 2671-2685. DOI:10.1111/1462-2920.14302 |
| [54] |
ANTHONY F. MICHAELS, SILVER M W. Primary production, sinking fluxes and the microbial food web[J]. Deep-Sea Research, 1988, 35(4): 473-490. DOI:10.1016/0198-0149(88)90126-4 |
| [55] |
SEYMOUR J R, AHMED T, DURHAM W M, et al. Chemotactic response of marine bacteria to the extracellular products of Synechococcus and Prochlorococcus[J]. Aquatic Microbial Ecology, 2010, 59: 161-168. DOI:10.3354/ame01400 |
| [56] |
PAULSEN M L, DORÉ H, GARCZAREK L, et al. Synechococcus in the Atlantic gateway to the Arctic Ocean[J]. Frontiers in Maine Science, 2016, 3(191): 1-14. |
| [57] |
PITTERA J, HUMILY F, THOREL M, et al. Connecting thermal physiology and latitudinal niche partitioning in marine Synechococcus[J]. The ISME Journal, 2014, 8: 1221-1236. DOI:10.1038/ismej.2013.228 |
| [58] |
SOHM J A, AHLGREN N A, THOMSON Z J, et al. Co- occurring Synechococcus ecotypes occupy four major oceanic regimes defined by temperature, macronutrients and iron[J]. The ISME Journal, 2016, 10: 333-345. DOI:10.1038/ismej.2015.115 |
| [59] |
MILLER T R, HNILICKA K, DZIEDZIC A, et al. Chemotaxis of Silicibacter sp. strain TM1040 toward dinoflagellate products[J]. Applied and Environmental Microbiology, 2004, 70(8): 4692-4701. DOI:10.1128/AEM.70.8.4692-4701.2004 |
| [60] |
BERTLISSON S, BERGLUND O, PULLIN M J, et al. Release of dissolved organic matter by Prochlorococcus[J]. Vie et Milieu, 2005, 55(3/4): 225-232. |
| [61] |
TAI V, PAULSEN I T, PHILLIPPY K, et al. Whole-genome microarray analyses of Synechococcus-Vibrio interactions[J]. Environmental Microbiology, 2009, 11(10): 2698-2709. DOI:10.1111/j.1462-2920.2009.01997.x |
| [62] |
MORRIS J J, KIRKEGAARD R, SZUL M J, et al. Facilitation of robust growth of Prochlorococcus colonies and dilute liquid cultures by "helper" heterotrophic bacteria[J]. Applied Environmental Microbiology, 2008, 74(14): 4530-4534. DOI:10.1128/AEM.02479-07 |
| [63] |
MORRIS J J, JOHNSON Z I, SZUL M J, et al. Dependence of the cyanobacterium Prochlorococcus on hydrogen peroxide scavenging microbes for growth at the ocean's surface[J]. PLoS One, 2011, 6(2): e16805. DOI:10.1371/journal.pone.0016805 |
| [64] |
LOES J. A. GERRINGA, MICHA J. A. RIJKENBERG, KLAAS R. TIMMERMANS, et al. The influence of solar ultraviolet radiation on the photochemical production of H2O2 in the equatorial Atlantic Ocean[J]. Journal of Sea Research, 2004, 51: 3-10. DOI:10.1016/j.seares.2003.03.002 |
| [65] |
HANSON A K, TINDALE N W, ABDEL-MOATI M A R. An Equatorial Pacific rain event: influence on the distribution of iron and hydrogen peroxide in surface waters[J]. Marine Chemistry, 2001, 75: 69-88. DOI:10.1016/S0304-4203(01)00027-5 |
| [66] |
SAUER J, SCHREIBER U, SCHMID R, et al. Nitrogen starvation-induced chlorosis in Synechococcus PCC 7942. low-level photosynthesis as a mechanism of long-term survival[J]. Plant Physiology, 2001, 126: 233-243. DOI:10.1104/pp.126.1.233 |
| [67] |
SELIM K A, HAFFNER M. Heavy metal stress alters the response of the unicellular cyanobacterium Synechococcus elongatus PCC 7942 to nitrogen starvation[J]. Life, 2020, 10(275): 1-8. |
| [68] |
COE A, GHIZZONI J, LEGAULT K, et al. Survival of Prochlorococcus in extended darkness[J]. Limnology and Oceanography, 2016, 61(4): 1375-1388. DOI:10.1002/lno.10302 |
| [69] |
READ R W, BERUBE P M, BILLER S J, et al. Nitrogen cost minimization is promoted by structural changes in the transcriptome of N-deprived Prochlorococcus cells[J]. The ISME Journal, 2017, 11: 2267-2278. DOI:10.1038/ismej.2017.88 |
| [70] |
CHURCH M J, DUCKLOW H W, KARL D M J A, et al. Light dependence of [3H] leucine incorporation in the oligotrophic North Pacific Ocean[J]. Applied Enivernmental Microbiology, 2004, 70(7): 4079-4087. DOI:10.1128/AEM.70.7.4079-4087.2004 |
| [71] |
ZUBKOV M V, FUCHS B M, TARRAN G A, et al. High rate of uptake of organic nitrogen compounds by Prochlorococcus cyanobacteria as a key to their dominance in oligotrophic oceanic waters[J]. Applied Environmen tal Microbiology, 2003, 69(2): 1299-1304. DOI:10.1128/AEM.69.2.1299-1304.2003 |
| [72] |
ROCAP G, LARIMER F W, LAMERDIN J, et al. Genome divergence in two Prochlorococcus ecotypes reflects oceanic niche differentiation[J]. Nature, 2003, 424: 1042-1047. DOI:10.1038/nature01947 |
| [73] |
PALENIK B, BRAHAMSHA B, LARIMER F, et al. The genome of a motile marine Synechococcus[J]. Nature, 2003, 424: 1037-1042. DOI:10.1038/nature01943 |
| [74] |
MALMSTROM R R, KIENE R P, VILA M, et al. Dimethylsulfoniopropionate (DMSP) assimilation by Synechococcus in the Gulf of Mexico and northwest Atlantic Ocean[J]. Limnology and Oceanography, 2005, 50(6): 1924-1931. DOI:10.4319/lo.2005.50.6.1924 |
| [75] |
VILA-COSTA M, SIMÓR, HARADA H, et al. Dimethylsulfoniopropionate uptake by marine phytoplankton[J]. Science, 2006, 314(5799): 652-654. DOI:10.1126/science.1131043 |
| [76] |
COLLIER J L, BRAHAMSHA B, PALENIK B J M. The marine cyanobacterium Synechococcus sp. WH7805 requires urease (urea amiohydrolase, EC 3.5. 1.5) to utilize urea as a nitrogen source: molecular-genetic and biochemical analysis of the enzyme[J]. Microbiology, 1999, 145: 447-459. DOI:10.1099/13500872-145-2-447 |
| [77] |
CHEN T H, CHEN T L, HUNG L M, et al. Circadian rhythm in amino acid uptake by Synechococcus RF-1[J]. Plant Physiol, 1991, 97: 55-59. DOI:10.1104/pp.97.1.55 |
| [78] |
EILER A. Evidence for the ubiquity of mixotrophic bacteria in the upper ocean: implications and consequences[J]. Applied Environmental Microbiology, 2006, 72(12): 7431-7437. DOI:10.1128/AEM.01559-06 |
| [79] |
WEISS M, ABELE U, WECKESSER J, et al. Molecular architecture and electrostatic properties of a bacterial porin[J]. Science, 1991, 254(5038): 1627-1630. DOI:10.1126/science.1721242 |
| [80] |
ARMENGAUD J, CHRISTIE-OLEZA J A, CLAIR G, et al. Exoproteomics: exploring the world around biological systems[J]. Expert Review of Proteomics, 2012, 9(5): 561-575. DOI:10.1586/epr.12.52 |
| [81] |
CHRISTIE-OLEZA J A, PINA-VILLALONGA J M, BOSCH R, et al. Comparative proteogenomics of twelve Roseobacter exoproteomes reveals different adaptive strategies among these marine bacteria[J]. Molecular & Cellular Proteomics, 2012, 11(2): M111.013110. |
| [82] |
CHRISTIE-OLEZA J A, ARMENGAUD J. In-depth analysis of exoproteomes from marine bacteria by shotgun liquid chromatography-tandem mass spectrometry: the Ruegeria pomeroyi DSS-3 case-study[J]. Marine Drugs, 2010, 8: 2223-2239. DOI:10.3390/md8082223 |
| [83] |
AMACHER J, NEUER S, LOMAS M. DNA-based molecular fingerprinting of eukaryotic protists and cyanobacteria contributing to sinking particle flux at the Bermuda Atlantic time-series study[J]. Deep Sea Research Part Ⅱ, 2013, 93: 71-83. DOI:10.1016/j.dsr2.2013.01.001 |
| [84] |
PASSOW U, ALLDREDGE A L. Distribution, size and bacterial colonization of transparent exopolymer particles (TEP) in the ocean[J]. Marine Ecology Progress Series, 1994, 113: 185-198. DOI:10.3354/meps113185 |
| [85] |
RIEBESELL U, SCHULZ K G, BELLERBY R, et al. Enhanced biological carbon consumption in a high CO2 ocean[J]. Nature, 2007, 450: 545-548. DOI:10.1038/nature06267 |
| [86] |
CORREGE T, GAGAN M K, BECK J W, et al. Interdecadal variation in the extent of South Pacific tropical waters during the Younger Dryas event[J]. Nature, 2004, 428: 927-929. DOI:10.1038/nature02506 |
 2022, Vol. 46
2022, Vol. 46


