文章信息
- 李建华, 王楠, 段继周, 侯保荣. 2023.
- LI Jian-hua, WANG Nan, DUAN Ji-zhou, HOU Bao-rong. 2023.
- 氧掺杂碳气体扩散电极用于电催化产活性氧抗菌防污研究
- Electrocatalytic production of reactive oxygen species with oxygen-doped carbon-based gas diffusion electrode for antibacterial antifouling
- 海洋科学, 47(10): 1-9
- Marine Sciences, 47(10): 1-9.
- http://dx.doi.org/10.11759/hykx20230320001
-
文章历史
- 收稿日期:2023-03-20
- 修回日期:2023-04-21
2. 中国科学院大学, 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
随着我国海洋强国的建设和海洋经济的发展, 海洋中各类工程设施(海洋平台、海水管路、海洋浮标等)不断增加, 当这些设施处在高生物活性的海洋环境时, 海水中的微生物在短时间内就会在其表面附着形成微生物膜, 随之多细胞藻类及污损生物幼虫附着, 形成肉眼可见的生物污损。生物污损一旦形成, 不仅会导致船舶航行阻力增大, 增加能耗和运行成本, 而且会引起海水管路堵塞、平台载荷增加以及设施的腐蚀问题, 减少工程服役寿命, 造成巨大经济损失。过去人们基于物理、化学和生物原理开发了一系列的海洋生物污损控制技术[1]。但是, 现有防污技术仍不能完全满足对海洋环境保护的要求, 研究绿色无毒的海洋污损防控技术具有重要意义。传统电解防污方法如电解铜-铝和电解产氯, 因具备有效防污效果而广泛应用于海上平台、船舶及滨海电厂等场景[2-3]。但释放的有毒的铜离子或三氯甲烷等消毒副产物可能对海洋生物及生态环境产生直接或间接的影响[4-5]。
电催化生成活性氧杀菌, 因低能耗、高效环保, 无消毒副产物等特点, 成为一种非常具有应用前景的电化学防污技术[6]。在持续通电或者周期性通电的情况下, 电极材料通过电催化氧还原产生H2O2等活性氧物质[7-8], 该活性氧能阻止细菌在设施表面寄生定植形成生物膜, 在污损形成过程早期杀灭细菌, 以进而达到防止海洋生物附着的效果, 且活性氧作用后产物为氧气和水, 绿色环保, 对水体无危害。
电催化剂的设计对电极的活性和选择性而言至关重要。已报道高性能的铂-汞、钯-金等贵金属基催化剂由于贵金属稀缺, 使用成本高等特点限制了他们的应用场景[9-11]。与之相比, 氧掺杂碳材料(oxygen-doped carbon materials)被证明在电催化氧还原反应合成H2O2中表现出良好的催化性能[12-14]。与其他类型的催化剂相比, 炭黑具有经济高效、成本低、易于获取等优点, 更加利于实际应用。
过去人们更多地关注于高活性催化剂材料的制备, 然而, 电极结构设计方面的研究也同样重要[15-17]。相较于传统的平面电极(如金属箔, 玻碳等), 气体扩散电极(GDE)可以使催化剂层周围保持较高的气体浓度, 从而改善传质过程[18-19]。本文利用商用炭黑作为催化原料, 并经过简单的氧化处理方法进行改性制备氧化炭黑材料, 并进一步通过两步“喷涂-热解”工艺将改性炭黑粉末和聚四氟乙烯粉末结合到碳毡基体上制备O−CB/PTFE气体扩散电极, 考察了该电极在0.5 mol·L-1氯化钠溶液中H2O2的产率, 初步探索了其对典型的海洋中好氧菌Pseudomonas sp.的实际抗菌效果。
1 实验方法 1.1 实验材料与试剂炭黑粉末(XC-72R)购买自Fuel Cell Store。碳毡购自于台湾碳能科技。质子交换膜(Nafion N117), Nafion分散液(D520, 5 wt %)采购自美国杜邦公司。聚四氟乙烯微粉(PTFE, 5 μm), 无水硫酸铈(99.95%)采购自上海麦克林公司。氯化钠(AR)、氯化钾(AR)、无水乙醇(AR)、浓硝酸(AR)、琼脂粉、酵母提取物、磷酸氢二钠(AR)、磷酸二氢钾(AR)均采购自国药集团, 所有试剂均使用前未经进一步纯化。
1.2 O-CB及O-CB/PTFE电极制备 1.2.1 炭黑的氧化处理将600 mg商用炭黑添加到600 mL, 12.0 mol·L–1硝酸中。然后, 将上述溶液在85 ℃温度下水浴冷凝回流3 h。反应结束后, 自然冷却后进行离心, 用水和乙醇反复清洗, 直到pH值为中性。最后, 将氧化炭黑(O−CB)样品在真空干燥箱中于70 ℃下干燥12 h, 得到氧化处理后的样品。
1.2.2 “喷涂-热解”制备O−CB/PTFE电极将碳毡裁剪成尺寸1.0 cm×1.5 cm, 并在去离子水和乙醇中依次超声清洗15 min后, 将其在2.5 wt %的PTFE悬浮液中浸泡10 min, 进行疏水化处理。将处理过的碳毡用镊子取出, 放入真空干燥箱中60 ℃下进行干燥, 干燥后置于管式炉中, 空气条件下, 360 ℃煅烧30 min。
取2.0 mg的O−CB催化剂, 1 mL的无水乙醇制成催化剂墨水, 超声30 min后, 使用5 mL微型喷枪均匀喷涂在预处理后的碳毡上。待溶液干燥后, 使用喷枪分别喷涂不同比重(2.5 wt %、5 wt %、10 wt %、20 wt %)PTFE乳液, 其中, PTFE乳液的体积与催化剂墨水的体积相同为1 mL。置于60 ℃真空箱中干燥, 干燥后, 在360 ℃下煅烧30 min, 最终制备成不同PTFE修饰量的O−CB/PTFE电极(图 1)。
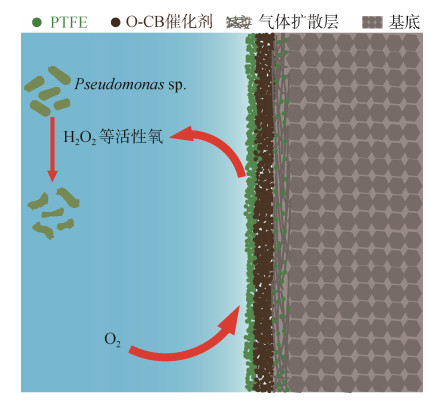 |
| 图 1 氧化炭黑(O−CB)/多孔碳毡电极示意图 Fig. 1 Schematic of O−CB/PTFE electrode |
材料的成分和晶体结构通过在日本理学的Rigaku D/max-Ultima IV上使用Cu Kα辐射(λ= 0.154 06 nm)进行广角X射线衍射(XRD)分析来获得。X射线光电子能谱(XPS)使用美国赛默飞世尔科技公司的Thermo Scientific K-Alpha进行测试, 以Al Kα辐射源并通过C 1s峰能量为284.8 eV进行校准。样品的形貌组成及结构信息使用美国FEI公司的FEI Quanta 250型号的扫描电子显微镜(SEM)和FEI Tecnai F20型号的透射电子显微镜(TEM)获得。使用全自动比表面及孔隙度分析仪(Micromeritics ASAP 2460, 美国)进行N2吸脱附曲线测试, 以获取材料的比表面积和孔结构信息, 测试温度为77.300 K。紫外光谱使用日本日立公司的HitachiU-3900H型号紫外可见分光光度计进行测定。接触角的测量是通过德国Dataphysics公司的OCA20型号接触角测量仪完成。
1.4 电化学性能测试 1.4.1 旋转环盘电极(RRDE)测试室温下, 在0.5 mol·L–1 NaCl溶液中, 分别以石墨电极和饱和甘汞电极作为对电极和参比电极, 配制O−CB催化剂墨水, 并吸取适量的催化剂滴涂到环盘电极上, 等待自然干燥, 作为工作电极。分别在氧气饱和与氮气饱和条件下, 进行循环伏安(CV)测试, 并在1 600 r/min转速下进行线性扫描伏安(LSV)测试。H2O2的选择性和转移电子数按照如下公式进行计算[20]:
其中, jD为盘电流密度(mA·cm–2), jR为环电流密度(mA·cm–2), N为收集系数(0.37)。
1.4.2 电催化生成H2O2含量测试室温下, 采用恒电位仪提供恒电位进行电化学测试, 电解池由阴极室、阳极室和Nafion膜组成, 阴极室和阳极室由Nafion膜隔开, 制备的不同PTFE修饰量的O−CB/PTFE电极、石墨和饱和甘汞电极分别为工作电极、对电极和参比电极, 以0.5 mol·L–1 NaCl溶液为电解液。电解30 min后, 取出阴极室内的电解液, 将其与1 mmol·L–1硫酸铈溶液混合后, 利用紫外可见分光光度计对H2O2的浓度进行测定。改变给定电位值0.1 V、0.2 V、0.3 V vs RHE, 重复相应实验过程。其中H2O2标准曲线的测定如下: 采用硫酸铈比色法对电催化产生的H2O2定量分析[21-22]。所依据的原理: H2O2可以使黄色的Ce4+被还原为无色的Ce3+离子(2Ce4+ + H2O2 → 2Ce3+ + 2H+ + O2), 且Ce4+与H2O2的浓度之间存在化学计量关系:
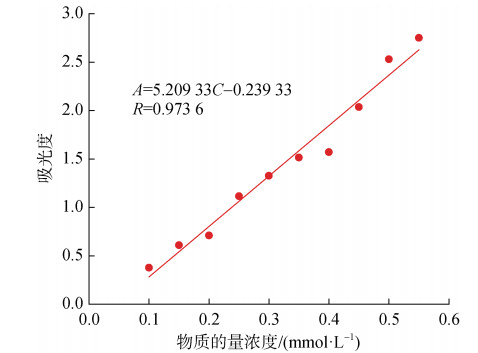 |
| 图 2 吸光度与Ce(SO4)2物质的量浓度的线性关系曲线图 Fig. 2 Linear relation between the Ce(SO4)2 concentration and absorbance |
实验使用本课题组分离获得的菌株Pseudomonas sp., 并由海洋微生物菌种保藏管理中心完成菌种鉴定。实验前进行活化, 接种到无菌Luria-Bertani (LB)液体培养基中, 培养基成分为: 酵母提取物5 g, 氯化钠5 g和胰蛋白胨10 g溶于1 000 mL二次水中, 在121 ℃下高压蒸汽灭菌20 min。在摇床中180 r/min进行过夜培养, 培养温度为37 ℃。利用涂板计数法结合测量光密度值(OD值)确定细菌浓度: 首先, 将培养后的菌液进行逐级浓度梯度稀释, 然后, 取100 µL稀释的菌液涂板, 每一个稀释浓度涂3个平板, 培养12 h。同时对初始的菌液进行OD值的测定。最后, 根据每种细菌形成的平均菌落单元(cfu)和稀释倍数, 确定菌株的浓度。在进行电解实验前, 再次测定菌液OD值, 对菌液浓度进行校正。将细菌培养液, 4 000 r/min离心5 min, 从培养液中分离出菌株。然后, 使用磷酸盐缓冲溶液(PBS)稀释菌株, 得到浓度约为107 cfu·mL–1的菌液。本实验以~107 cfu·mL–1的Pseudomonas sp.的PBS溶液进行抗菌实验。PBS溶液的成分为: 8 g氯化钠, 0.2 g氯化钾, 1.44 g磷酸氢二钠, 0.44 g磷酸二氢钾溶于1 000 mL二次水中, 调节pH到7.4, 在121 ℃下高压蒸汽灭菌20 min。
1.5.2 杀菌测试取30 mL约107 cfu·mL–1的Pseudomonas sp.的PBS缓冲溶液作为电解质溶液。并根据1.4.2实验的结果, 进一步选取最高H2O2产量的O−CB/PTFE电极为工作电极, 抗菌实验在0.1 V vs RHE电位下进行恒电位(i-t)测试, 测试时间为210 min。在0 min、15 min、30 min、60 min、120 min、150 min、200 min时间点间隔取样, 取出电解质溶液通过逐级浓度梯度稀释并进行涂板计数。培养一定时间后对平板观察拍照, 进而计算得出杀菌率, 评价杀菌效果。
2 结果与讨论 2.1 氧化炭黑的结构表征氧化前后炭黑的形貌通过SEM和TEM表征, 通过结果可以看出样品整体呈现典型的不规则的球形颗粒形貌。对比观察氧化处理前后的炭黑样品, 发现氧化处理后, 催化材料原有形貌没有改变(图 3)。
 |
| 图 3 氧化前后炭黑材料的形貌图 Fig. 3 Morphology of carbon black material before and after oxidation |
XRD结果表明O−CB与CB均在25°和40°有明显的衍射峰, 分别对应石墨碳的(002)和(100)晶面。通过XRD谱上(002)峰的强度可以反映碳材料的石墨化程度, 一般而言石墨化程度越高, 碳材料的导电性和化学稳定性越好[23]。因此, 氧化处理不会破坏炭黑的结构, 同时, 保留了炭黑的高石墨化度的特点(图 4)。
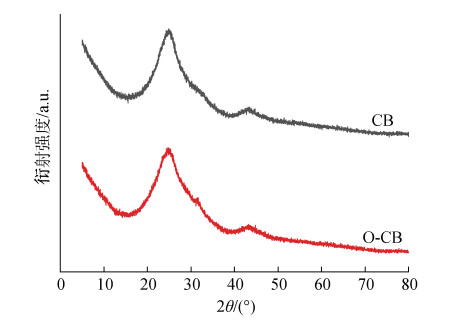 |
| 图 4 CB和O−CB的X射线衍射图 Fig. 4 X-ray diffraction patterns of CB and O−CB |
此外, 我们通过氮气吸脱附实验表征材料内部的孔结构和材料的比表面积。一般而言, 催化剂的比表面积越高, 可以承载更多的催化活性位点, 因而具有更高的电催化活性[24]。结果表明O−CB样品的平均孔径为95.611 Å, 为介孔结构, 且样品在0.8~ 1.0范围内出现回滞环(图 5), 且与CB的比表面积(115.500 4 m2/g)相比, 处理后的O−CB(342.876 8 m2/g)具有更高的比表面积, 这表明通过化学氧化处理不仅保持材料原有结构和形貌不变, 而且能够增加O−CB的比表面积, 使其具有更高的催化活性。
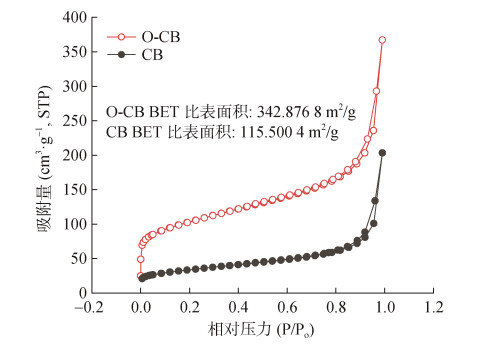 |
| 图 5 O−CB催化剂的氮气吸脱附曲线 Fig. 5 N2 absorption and desorption isotherms plots of O−CB catalyst |
羧基, 羰基, 醚键等含氧官能团, 被认为是氧掺杂碳材料的氧还原反应产生H2O2催化活性来源[15, 25-26]。通过XPS表征可以获得表面元素的种类和价态信息。XPS结果表明, C 1s可以分为C=C键(284.8 eV), C−C键(285.5 eV), C−O键(286.8 eV), O=C−O键(289.0 eV) (图 6a)。O 1s可以拟合为531.8 eV、532.9 eV、534 eV、536 eV 4个峰, 分别对应C=O键, C−O−C或COOH键, C−OH键, 化学吸附氧(图 6b)[27]。以上结果证明, 通过硝酸氧化处理后, 获得的O−CB表面引入了多种氧官能团, 其中的C−O−C键或−COOH含量最高。
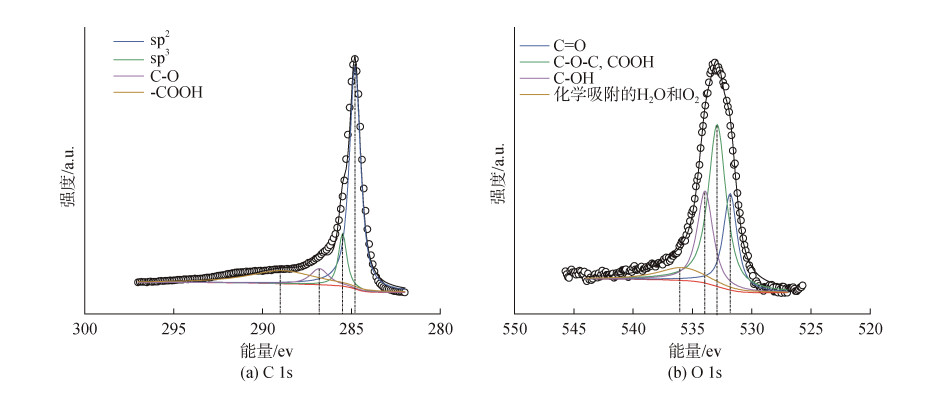 |
| 图 6 O−CB催化剂的XPS精细谱图 Fig. 6 High-resolution XPS spectra of O−CB catalyst |
为了评价O−CB的电催化性能, RRDE技术被用于测定O−CB在中性的氯化钠溶液(pH≈7)中的电催化性能。首先, 通过对比氮气饱和溶液条件和氧气饱和溶液条件下的CV曲线, 结果发现O−CB对氧还原反应(ORR)具有明显的电催化活性(图 7)。
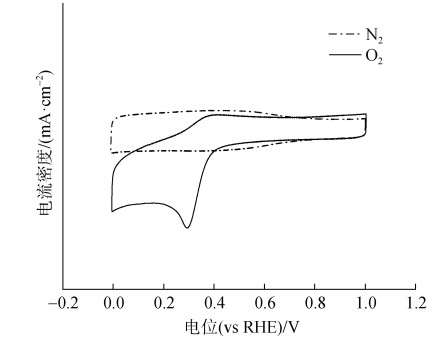 |
| 图 7 O−CB催化剂在0.5 mol·L–1的氯化钠溶液中的CV曲线图 Fig. 7 CV curve of O−CB catalyst in 0.5 mol·L−1 NaCl solution |
利用旋转环盘电极技术测得O−CB在1 600 r/min转速下的极化曲线, 通过计算公式得出该催化材料的转移电子数为2.7, H2O2选择性约为60%(图 8)。上述电化学实验结果证明所制备的O−CB催化剂具有较高的催化活性和H2O2选择性, 在中性氯化钠溶液中能够电催化氧还原反应产生H2O2。
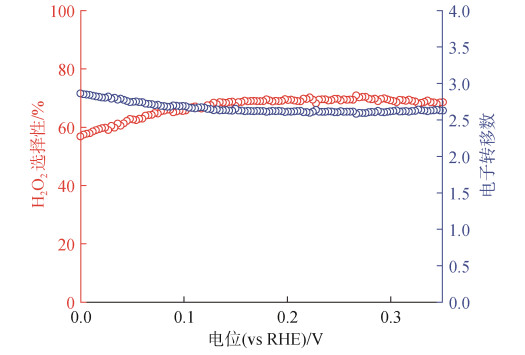 |
| 图 8 基于RRDE获取的极化曲线所计算的H2O2选择性和转移电子数结果 Fig. 8 Calculated H2O2 selectivity and number of transferred electrons based on the polarization curve obtained using RRDE |
通过SEM观察, 碳毡基底呈现光滑的碳纤维交织组成的多孔网状结构, 通过喷涂-热解过程, 将O−CB催化剂包覆到碳纤维的表面而使其表面呈现疏松多孔的形貌, 对单根纤维表面进行放大观察尤为明显(图 9)。此外, 当喷涂PTFE比重为20 wt %时, 在碳纤维表面出现团聚现象, 这是由于过多的PTFE会导致结块(图 9d), 这种团聚的催化剂可能会影响实际的电催化性能。
 |
| 图 9 不同PTFE修饰量的O–CB/PTFE电极的扫描电镜图 Fig. 9 SEM images of O–CB/PTFE electrodes modified using different PTFE contents 注: (a) PTFE-2.5 wt %; (b) PTFE-5 wt %; (c) PTFE-10 wt %; (d) PTFE-20 wt % |
此外, 为了评估PTFE对电极表面浸润性及气体界面调控的影响, 我们测试电极表面的固-液接触角, 结果表明不同PTFE修饰量的电极表面的接触角均大于130°, 呈现为疏水化表面。这证明了PTFE有助于电极表面疏水界面层的形成, 然而改变用量对电极表面的疏水性的影响差别并不明显(图 10)。
 |
| 图 10 不同PTFE修饰量的O−CB/PTFE电极表面的接触角 Fig. 10 Contact angle of O−CB/PTFE electrodes modified using different PTFE contents 注: (a) PTFE-2.5 wt %; (b) PTFE-5 wt %; (c) PTFE-10 wt %; (d) PTFE-20 wt % |
基于硫酸铈比色法原理, 结合紫外可见吸收光谱, 经过进一步计算得到H2O2的电催化产生速率(图 11)。对比不同含量PTFE修饰的电极在0.1 V、0.2 V、0.3 V vs RHE电位下的H2O2产生速率, 可以发现在不同电位下, 喷涂PTFE比重为20 wt %的均明显低于其他用量。且5 wt %对应的电极产率最高, 在0.1 V vs RHE电位下可以达到27.19 mg·L−1(mg catalyst) −1·cm−1·h−1, 10 wt %的电极次之。证明PTFE的用量确实会影响电极实际电催化产生的H2O2的量, 与SEM观察到的结果相符。这可能是由于PTFE用量过多导致产量明显降低。另外, PTFE本身不导电且没有电催化活性, 过多的添加会阻碍电子传递, 降低催化位点的暴露, 从而降低实际的电催化产生H2O2的效果; 其次, 使用过少的PTFE修饰, 导致电极表面的疏水界面层不稳定, 从而不利于形成氧气扩散传质的固-液-气三相界面层, 进而限制了整个电催化过程的发生[28-29]。因此, 适量的PTFE修饰不仅有利于电子传递, 而且利于氧气扩散, 通过优化PTFE的用量, 可以提高电催化产生H2O2的实际产量。当PTFE添加量为5 wt %时, 对氧气扩散和电子阻碍作用达到一个相对平衡的状态, 此时实现相对更大的H2O2产量。
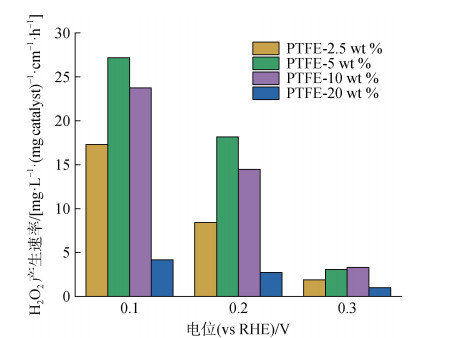 |
| 图 11 不同PTFE修饰量的O−CB/PTFE电极在相应电位下的H2O2产生速率 Fig. 11 H2O2 production rate with O−CB/PTFE electrodes modified using different PTFE contents at corresponding potentials |
为了测试O−CB/PTFE-5 wt %电极实际的电催化杀菌消毒效果, 我们选择Pseudomonas sp.作为模式菌进行相关实验[30]。为防止电解液成分对细菌存活状态的影响, 我们选择在中性pH的PBS电解液中进行测试。根据平板计数结果, 计算得到相应电催化过程的杀菌率曲线, 误差棒代表3个平行培养平板间误差(图 12)。从结果来看, O−CB/PTFE-5 wt %电极在电催化30 min内可以杀灭48.5%的细菌, 60 min内即可灭杀97.69%的细菌, 对Pseudomonas sp.实现较强的抗菌作用, 120 min内可杀灭99.99%以上的细菌。
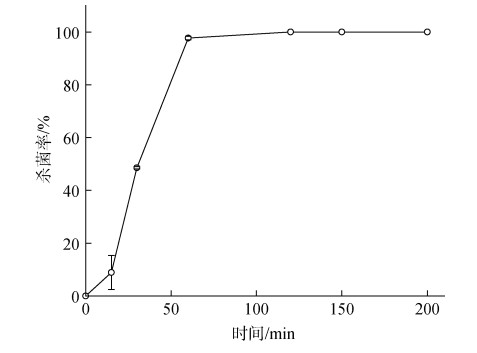 |
| 图 12 杀菌率随处理时间的关系曲线 Fig. 12 Disinfection efficiency as a function of treatment time |
相同稀释倍数涂布的平板, 经过过夜培养后, 通过对比平板上细菌的菌落结果, 可以直观地看出由于活性氧逐渐积累, 细菌随着处理时间增加而被彻底杀灭。当处理时间为60 min时, 细菌几乎不生长。持续作用120 min, 平板上没有细菌菌落生长。因此, O−CB/PTFE-5 wt %电极用于电催化产生的H2O2等活性氧物质作用于Pseudomonas sp., 在短时间内就呈现出很好的杀菌效果(图 13)。
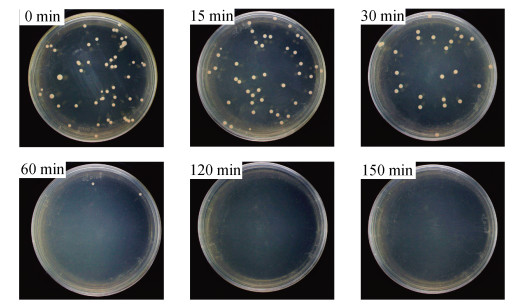 |
| 图 13 假单胞菌在不同电解时间取样涂布的平板上生长情况 Fig. 13 Pseudomonas sp. on plates sampled at different electrolysis time |
本文利用炭黑为原料, 通过化学氧化的方法在炭黑表面引入丰富含氧官能团并利用喷涂-热解工艺成功制备O−CB/PTFE电极。该电极在中性氯化钠介质中高效电催化产H2O2。研究结果表明, 适量的PTFE修饰可以有利于电极表面氧气扩散, 进而提高H2O2产生速率; O-CB/PTFE-5 wt %电极最高可以达到27.19 mg·L–1·(mg catalyst)–1·cm–1·h–1产生速率。以Pseudomonas sp.为海洋污损微生物的模式菌, 进一步评价O−CB/PTFE-5 wt %电极电催化产生活性氧的杀菌效果。杀菌实验证明利用该电极可以电催化持续不断产生活性氧, 在60 min内即可灭杀97.69%的细菌, 对Pseudomonas sp.实现较强的抗菌作用, 在120 min内, 对假单胞菌可达到99.99%的杀菌率。O−CB/PTFE电极制备方法简单, 成本低, 为探索电催化活性氧杀菌防污装置提供了可能。利用电催化产活性氧为海洋污损防治的开展提供一种新的思路。
| [1] |
段继周, 刘超, 刘会莲, 等. 海洋水下设施生物污损及其控制技术研究进展[J]. 海洋科学, 2020, 44(8): 162-177. DUAN Jizhou, LIU Chao, LIU Huilian, et al. Research progress of biofouling and its control technology in marine underwater facilities[J]. Marine Sciences, 2020, 44(8): 162-177. |
| [2] |
李长彦, 张桂芳, 付洪田. 电解海水防污技术的发展及应用[J]. 材料开发与应用, 1996, 11(1): 38-43. LI Changyan, ZHANG Guifang, FU Hongtian. Development and application of electrolyzing seawater antifouling technique[J]. Development and Application of Materials, 1996, 11(1): 38-43. |
| [3] |
逯艳英, 吴建华, 孙明先, 等. 海洋生物污损的防治——电解防污技术的新进展[J]. 腐蚀与防护, 2001, 22(12): 530-534. LU Yanying, WU Jianhua, SUN Mingxian et al. Prevention of ocean halobios fouling—development of electrolystic antifouling technology[J]. Corrosion & Protection, 2001, 22(12): 530-534. |
| [4] |
YTREBERG E, KARLSSON J, EKLUND B. Comparison of toxicity and release rates of Cu and Zn from anti-fouling paints leached in natural and artificial brackish seawater[J]. Science of The Total Environment, 2010, 408(12): 2459-2466. DOI:10.1016/j.scitotenv.2010.02.036 |
| [5] |
SEDLAK D L, VON GUNTEN U. The chlorine dilemma[J]. Science, 2011, 331(6013): 42-43. DOI:10.1126/science.1196397 |
| [6] |
ZHANG J K, SU P D, CHEN H H, et al. Impact of reactive oxygen species on cell activity and structural integrity of Gram-positive and Gram-negative bacteria in electrochemical disinfection system[J]. Chemical Engineering Journal, 2023, 451: 138879. DOI:10.1016/j.cej.2022.138879 |
| [7] |
CHANG Q W, ZHANG P, MOSTAGHIMI A H B, et al. Promoting H2O2 production via 2-electron oxygen reduction by coordinating partially oxidized Pd with defect carbon[J]. Nature Communications, 2020, 11(1): 2178. DOI:10.1038/s41467-020-15843-3 |
| [8] |
XIAO F, WANG Z N, FAN J Q, et al. Selective electrocatalytic reduction of oxygen to hydroxyl radicals via 3-electron pathway with FeCo alloy encapsulated carbon aerogel for fast and complete removing pollutants[J]. Angewandte Chemie International Edition, 2021, 60(18): 10375-10383. DOI:10.1002/anie.202101804 |
| [9] |
JIRKOVSKÝ J S, PANAS I, AHLBERG E, et al. Single atom hot-spots at Au–Pd nanoalloys for electrocatalytic H2O2 production[J]. Journal of the American Chemical Society, 2011, 133(48): 19432-19441. DOI:10.1021/ja206477z |
| [10] |
SIAHROSTAMI S, VERDAGUER-CASADEVALL A, KARAMAD M, et al. Enabling direct H2O2 production through rational electrocatalyst design[J]. Nature Materials, 2013, 12(12): 1137-1143. DOI:10.1038/nmat3795 |
| [11] |
WANG C, CHEN K, ZHANG X, et al. Optimizing the Pd sites in pure metallic aerogels for efficient electrocatalytic H2O2 production[J]. Advanced Materials, 2023, 35(14): 2211512. DOI:10.1002/adma.202211512 |
| [12] |
KIM H W, ROSS M B, KORNIENKO N, et al. Efficient hydrogen peroxide generation using reduced graphene oxide-based oxygen reduction electrocatalysts[J]. Nature Catallysis, 2018, 1(4): 282-290. DOI:10.1038/s41929-018-0044-2 |
| [13] |
CHEN S Y, LUO T, CHEN K J, et al. Chemical identification of catalytically active sites on oxygen-doped carbon nanosheet to decipher the high activity for electro- synthesis hydrogen peroxide[J]. Angewandte Chemie International Edition, 2021, 60(30): 16607-16614. DOI:10.1002/anie.202104480 |
| [14] |
GUO Y, ZHANG R, ZHANG S C, et al. Ultrahigh oxygen-doped carbon quantum dots for highly efficient H2O2 production via two-electron electrochemical oxygen reduction[J]. Energy & Environmental Science, 2022, 15(10): 4167-4174. |
| [15] |
ZHENG Y S, HE J G, QIU S, et al. Boosting hydrogen peroxide accumulation by a novel air-breathing gas diffusion electrode in electro-Fenton system[J]. Applied Catalysis B: Environmental, 2022, 316: 121617. DOI:10.1016/j.apcatb.2022.121617 |
| [16] |
LI C, HU C Q, SONG Y, et al. Active oxygen functional group modification and the combined interface engineering strategy for efficient hydrogen peroxide electrosynthesis[J]. ACS Applied Materials & Interfaces, 2022, 14(41): 46695-46707. |
| [17] |
XU W W, LIANG Z, GONG S, et al. Fast and stable electrochemical production of H2O2 by electrode architecture engineering[J]. ACS Sustainable Chemistry & Engineering, 2021, 9(20): 7120-7129. |
| [18] |
RABIEE H, GE L, ZHANG X Q, et al. Gas diffusion electrodes (GDEs) for electrochemical reduction of carbon dioxide, carbon monoxide, and dinitrogen to value-added products: a review[J]. Energy & Environmental Science, 2021, 14(4): 1959-2008. |
| [19] |
WU Y M, CHARLESWORTH L, MAGLAYA I, et al. Mitigating electrolyte flooding for electrochemical CO2 reduction via infiltration of hydrophobic particles in a gas diffusion layer[J]. ACS Energy Letters, 2022, 7(9): 2884-2892. DOI:10.1021/acsenergylett.2c01555 |
| [20] |
WEN Y, ZHANG T, WANG J, et al. Electrochemical reactors for continuous decentralized H2O2 production[J]. Angewandte Chemie International Edition, 2022, 61(35): e202205972. DOI:10.1002/anie.202205972 |
| [21] |
LU Z Y, CHEN G X, SIAHROSTAMI S, et al. High-efficiency oxygen reduction to hydrogen peroxide catalysed by oxidized carbon materials[J]. Nature Catalysis, 2018, 1(2): 156-162. DOI:10.1038/s41929-017-0017-x |
| [22] |
WANG M J, DONG X, MENG Z D, et al. An efficient interfacial synthesis of two-dimensional metal-organic framework nanosheets for electrochemical hydrogen peroxide production[J]. Angewandte Chemie International Edition, 2021, 60(20): 11190-11195. DOI:10.1002/anie.202100897 |
| [23] |
LI Z S, LI B L, YU C L, et al. Recent progress of hollow carbon nanocages: general design fundamentals and diversified electrochemical applications[J]. Advanced Science, 2023, 10(7): 2206605. DOI:10.1002/advs.202206605 |
| [24] |
XU H, LV X H, WANG HY, et al. Impact of pore structure on two-electron oxygen reduction reaction in nitrogen-doped carbon materials: rotating ring-disk electrode vs. Flow cell[J]. ChemSusChem, 2022, 15(5): e202102587. DOI:10.1002/cssc.202102587 |
| [25] |
HAN G F, LI F, ZOU W, et al. Building and identifying highly active oxygenated groups in carbon materials for oxygen reduction to H2O2[J]. Nature Communications, 2020, 11(1): 2209. DOI:10.1038/s41467-020-15782-z |
| [26] |
ZHANG C Y, LIU G Z, LONG Q F, et al. Tailoring surface carboxyl groups of mesoporous carbon boosts electrochemical H2O2 production[J]. Journal of Colloid and Interface Science, 2022, 622: 849-859. DOI:10.1016/j.jcis.2022.04.140 |
| [27] |
XIA C, XIA Y, ZHU P, et al. Direct electrosynthesis of pure aqueous H2O2 solutions up to 20% by weight using a solid electrolyte[J]. Science, 2019, 366(6462): 226-231. DOI:10.1126/science.aay1844 |
| [28] |
YANG C W, SUN F, QU Z B, et al. Interfacial O2 accumulation affects microenvironment in carbon- based electrocatalysts for H2O2 production[J]. ACS Energy Letters, 2022, 7(12): 4398-4407. DOI:10.1021/acsenergylett.2c02021 |
| [29] |
ZHANG Q Z, ZHOU M H, REN G, B et al. Highly efficient electrosynthesis of hydrogen peroxide on a superhydrophobic three-phase interface by natural air diffusion[J]. Nature Communications, 2020, 11(1): 1731. DOI:10.1038/s41467-020-15597-y |
| [30] |
JIANG K, BACK S, AKEY A J, et al. Highly selective oxygen reduction to hydrogen peroxide on transition metal single atom coordination[J]. Nature Communications, 2019, 10(1): 3997. DOI:10.1038/s41467-019-11992-2 |
 2023, Vol. 47
2023, Vol. 47


