中国海洋湖沼学会主办。
文章信息
- 杨智景, 李长红, 张浩, 苗亮, 陈炯. 2015.
- YANG Zhi-Jing, LI Chang-Hong, ZHANG Hao, MIAO Liang, CHEN Jiong. 2015.
- 香鱼(Plecoglossus altivelis)肿瘤坏死因子-α (TNF-α) 基因的分子克隆、鉴定及免疫相关性表达
- MOLECULAR CLONING, CHARACTERISATION AND IMMUNE-RELATED EXPRESSION OF TUMOR NECROSIS FACTOR α (TNF-α) GENE IN AYU PLECOGLOSSUS ALTIVELIS
- 海洋与湖沼, 46(6): 1380-1389
- Oceanologia et Limnologia Sinica, 46(6): 1380-1389.
- http://dx.doi.org/10.11693/hyhz20150600166
-
文章历史
- 收稿日期:2015-06-15
- 改回日期:2015-07-09
肿瘤坏死因子-α(tumor necrosis factor-alpha,TNF-α)是机体在病原体入侵时,由激活的巨噬细胞、淋巴细胞以及其它免疫细胞产生的促炎细胞因子(Horiuchi et al,2010)。在哺乳动物中,TNF-α 可以抑制肿瘤细胞增殖,诱导肿瘤细胞凋亡,并且参与机体的免疫调节,诱导相关的细胞因子及其受体基因的表达(Horiuchi et al,2010; Rajmani et al,2015); 在抵抗细菌、病毒和寄生虫感染的过程中,TNF-α 还起着重要介质的作用,与白介素-1(interleukin-1,IL-1)和白介素-6(interleukin-1,IL-6)等细胞因子被归为正急性期蛋白(Gruys et al,2005; Horiuchi et al,2010)。目前,已有应用TNF-α 治疗肿瘤、牛皮癣、白塞病、风湿性关节炎、炎性肠病等的研究报道(Van Horssen et al,2006; Horiuchi et al,2010; Willrich et al,2015)。
目前,已经有数十种硬骨鱼类的TNF-α 基因得到了克隆,比如虹鳟(Oncorhynchus mykiss)(Laing et al,2001; Hong et al,2013)、鲤鱼(Cyprinus carpio)(Savan et al,2004)、大菱鲆(Psetta maxima)(Ordás et al,2007)、鳜鱼(Siniperca chuatsi)(Xiao et al,2007)和草鱼(Ctenopharyngodon idella)(Zhang et al,2012)等。在克隆TNF-α 基因的同时,部分研究对其转录水平及免疫功能进行了测定。例如,在海弧菌(Vibrio pelagius)和病毒性出血败血症病毒(Viral haemorrhagic septicemia virus,VHSV)感染后,大菱鲆肝和肾组织中TNF-α mRNA 表达量明显增加,且不同个体表达量差异明显(Ordás et al,2007); 在传染性脾肾坏死病毒(infectious spleen and kidney necrosis virus,ISKNV)感染后,鳜鱼血液和脾组织中TNF-α mRNA 表达量明显增加(Xiao et al,2007); 经草鱼呼肠孤病毒(grass carp reovirus,GCRV)感染后,草鱼脾中TNF-α mRNA表达量显著升高,而且GCRV 感染的草鱼肾细胞TNF-α mRNA 表达量也增加显著(Wang et al,2013);在体外实验中,重组的虹鳟TNF-α 能促进虹鳟头肾来源巨噬细胞的趋化和吞噬活性(Zou et al,2003),并且重组的金鱼(Carassius auratus)TNF-α 不仅能促进金鱼头肾来源的巨噬细胞的趋化和吞噬活性,还能促进其呼吸爆发功能等(Grayfer et al,2008)。上述研究结果表明,鱼类TNF-α 在细菌和病毒感染引起的炎症免疫防御反应发挥着重要作用。
香鱼(Plecoglossus altivelis),又名年鱼、仙胎鱼,隶属胡瓜鱼目、香鱼科,是一种一年生小型洄游性经济鱼类,为东亚地区中国、朝鲜和日本等国所特有。由于其体形优美、肉质鲜美,人工养殖规模逐年增加。然而,集约化、高密度养殖以及不当的病害防治技术导致香鱼病害频发,主要为细菌性病害,其中鳗弧菌是危害最严重的病原之一(李长红等,2009)。因此,香鱼以绿色健康养殖为要,应限制使用抗生素等药物,有必要从免疫学角度入手加强对香鱼免疫机制的研究,为香鱼病害防治及抗病品种选育提供指导。鉴于TNF-α 在动物免疫反应中的作用,本实验拟对香鱼TNF-α(PaTNF-α)进行初步研究。测定基因cDNA 序列,明确其序列结构特征、系统进化关系及表达特征,解明鳗弧菌感染后香鱼免疫组织及细胞中PaTNF-α mRNA 的表达变化以及鳗弧菌、脂多糖(lipopolysaccharide,LPS)和聚肌胞苷酸胞嘧啶核苷酸poly(I: C)分别处理后香鱼单核/巨噬细胞中PaTNF-αmRNA 的表达变化; 原核表达PaTNF-α 重组蛋白并制备抗血清,分析鳗弧菌感染的香鱼血清及单核/巨噬细胞上清中PaTNF-α 的表达变化。研究结果将为进一步探讨PaTNF-α 在香鱼炎症免疫反应中的作用机制及机理提供基础。
1 材料与方法1.1 实验材料与试剂健康香鱼(20—30g)购自浙江省宁波市宁海县凫溪香鱼养殖基地,规格均一、健康无伤。运回实验室后暂养于充分曝气的自来水中,水温(20±1)°C。暂养期间连续充气,每天换水2 次,早晚各一次。
ICR 小鼠购自浙江医学科学院实验动物中心。大肠杆菌BL21 pLys E 菌株、TG1 菌株、鳗弧菌ayu-H080701(李长红等,2009)、pGEX-4T-3 载体等由实验室保存。LPS(Escherichia coli 055: B5)和poly(I:C)购自Sigma 公司(美国)。pMD19-T Simple Vector、RNAiso 试剂、T4 DNA 连接酶、AMV 逆转录酶、Ex Taq DNA 聚合酶、BamH I、EcoR I,和SYBR Premix Ex Taq 试剂盒等购自TaKaRa 公司(日本)。压片暗盒、显影定影试剂盒、ECL 化学发光试剂盒,和柯达X-OMAT BT 胶片等购自碧云天生物技术研究所(北京)。SDS-PAGE 低分子量标准蛋白试剂盒购自中国科学院上海生物化学研究所(上海),预染蛋白分子量蛋白标准购自Fermentas 公司(加拿大)。琼脂糖凝胶回收试剂盒购自Omega 公司(美国)。二抗(辣根酶标记山羊抗小鼠IgG)购自北京中杉金桥生物技术有限公司(北京)。序列测序和引物合成工作由英维捷基贸易有限公司(上海)完成。
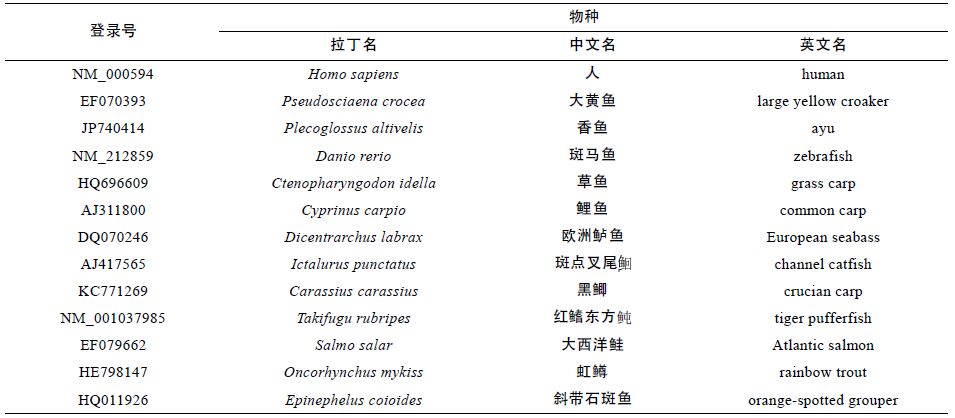
1.2 PaTNF-α cDNA 序列获得及序列分析采用Illumina HiSeq 2000 测序平台对健康香鱼单核/ 巨噬细胞进行转录组测序,从中获得PaTNF-αcDNA 序列,并采用常规PCR 方法进行扩增和测序验证。采用SignalP 4.1 在线程序(http: //www.cbs.dtu.dk/services/SignalP/)预测信号肽序列; 采用TMHMMServer v. 2.0(http: //www.cbs.dtu.dk/services/TMHMM/)预测跨膜结构域; 采用ClustalW 在线程序(http: //clustalw.ddbj.nig.ac.jp/)进行多重序列比对; 采用MEGA 6.0 软件构建系统进化树(Tamura et al,2013)。多重序列比对及进化树构建所用序列详见表 1。
 |
用0.03%(V/V)的乙二醇苯醚麻醉香鱼,无菌条件下迅速取出头肾,剪刀剪碎头肾置140 目筛网中,加入适量RPMI1640 培养基,无菌注射器活塞轻轻研磨,获得分散单细胞; 采用Ficoll 密度梯度离心法分离细胞(2000 r/min,25 min),取含单核/巨噬细胞的白膜层细胞,用含2%胎牛血清的RPMI1640 培养基洗涤2 次,最后重悬于含2%胎牛血清的RPMI1640 培养基中。血球计数板计数,将细胞浓度调整为107cells/mL,每皿铺2 mL 细胞。将细胞置于24°C、5%CO2 培养箱培养过夜,PBS 洗去非贴壁细胞,贴壁细胞在含10%胎牛血清的RPMI1640 培养基中培养。吉姆萨染色后显微镜观察,确定超过95%的贴壁细胞是单核/巨噬细胞(Lu et al,2013)。
1.4 香鱼外周血白细胞的分离参考Lam等(2011)的方法分离香鱼外周血白细胞,具体步骤如下: 75%酒精消毒香鱼尾部,用肝素钠溶液润洗后的1.0 mL 注射器于香鱼尾静脉采血,加等量PBS 稀释。将稀释后的血液沿管壁加到70%的Ficoll/磷酸缓冲液(PBS)液面上,500 g 离心30 min,吸取中间白膜层细胞于15.0 mL 离心管中,加入等量PBS,500 g 离心20 min 收集白细胞,重复2 次,加适量PBS 重悬,瑞士染色鉴定,确定超过95%的细胞是外周血白细胞。
1.5 鳗弧菌感染的香鱼组织样品制备鳗弧菌感染香鱼的实验过程及感染剂量参考杨旦阳等(2013)的方法,具体步骤如下: 感染组香鱼用1.0×104 CFU/尾的浓度腹腔注射鳗弧菌菌悬液,对照组香鱼注射相同体积的灭菌生理盐水,分别在感染后4、8、12和24 h(hours post infection)时采集脾、肝和头肾等组织并立即投入液氮中; 从香鱼尾静脉抽取血液,4°C 静置过夜后低速离心收集血清,随后转于-70°C 超低温冰箱保存。
1.6 LPS、poly(I: C)和鳗弧菌感染的香鱼单核/巨噬细胞样品制备将LPS和poly(I: C)分别以10 ng/mL和40 μg/mL的作用浓度加入香鱼单核/巨噬细胞中,于作用4、8、12和24 h 时收集培养基上清,无菌滤膜过滤后分装;细胞用PBS 洗涤3 次,加入RNAiso 试剂裂解细胞,5 min 后收集裂解液作为香鱼单核/巨噬细胞样品,同上清样品置于-70°C 保存。
过夜培养的鳗弧菌用PBS 稀释后,按照感染复数(multiplicity of infection,MOI)为10: 1 的比例接种至香鱼单核/巨噬细胞中,于4、8、12和24 h 时收集培养基上清和单核/巨噬细胞样品,收集和保存方法同上。
1.7 qRT-PCR 检测参考黄左安等(2011)的方法进行总RNA 的抽提、第一链cDNA 的合成及qRT-PCR 检测。根据已获得的香鱼TNF-α cDNA序列设计检测引物,PaTNF-α test(+):5′-ACATGGGAGCT GTGTTCCTC-3′和PaTNF-α test(-):5′-GCAAACACACCGAAAAAGGT-3′,预期扩增大小115 bp; 根据香鱼管家基因β-actin cDNA 序列(AB020884)设计内参检测引物PaActin2(+):5′-TCGTGCGTGACATCAAGGAG-3′和PaActin2(-):5′-CGCACTTCATGATGCTGTTG-3′,预期扩增片段长度为231 bp。qRT-PCR 扩增体系25 μL,包括灭菌水10 μL、SYBR Premix Ex Taq(2×)缓冲液12.5 μL、cDNA 模板0.5 μL、上下游引物各(10 μmol/L)1 μL。扩增反应在ABI StepOne 荧光定量PCR 仪(美国ABI公司)上进行,反应条件为: 94°C 180 s(预变性,1 个循环); 94°C 30 s,58°C 30 s,72°C 30 s(扩增段,共40个循环); 94°C 30 s,72°C 60 s,95°C 30 s(熔解段,1 个循环)。每个样品重复3 次。荧光定量的结果由仪器自带程序读取。根据2-ΔΔCt 相对标准曲线法计算PaTNF-α mRNA 的相对表达量(Livak et al,2001)。
1.8 PaTNF-α 的原核表达、抗血清制备根据获得的PaTNF-α 开放阅读框(ORF)设计原核表达引物,引物序列如下: pGEX-4T3-PaTNF-α(+):5′-CGGATCCATGGATACTAATTGCAAAGTAC-3′和pGEX-4T3-PaTNF-α(-): 5′-GGAATTCTCACAGCAA ACACACC-3′,其中下划线碱基为的限制性内切酶BamH I和EcoR I 识别序列,斜体字母为保护碱基。PCR 扩增体系25 μL,包括10×Ex Taq buffer 2.5 μL,dNTP(2.5 mmol/L)4.0 μL,cDNA 模板0.5 μL,上下游引物(10 μmol/L)各1 μL,Ex Taq DNA 聚合酶0.25 μL,ddH2O 15.75 μL。扩增反应在Mastercycler pro 梯度PCR 仪(德国Eppendorf 公司)上进行,反应程序为:94°C 预变性120 s; 再30 个循环: 94°C 变性 30 s,58°C 退火30 s,72°C 延伸60 s; 最后72°C 延伸10 min。与预期相符的扩增片段经EcoR I和BamH I 双酶切,插入到经相同内切酶酶切的原核表达载体pGEX-4T-3 中,获得重组质粒pGEX-4T-3-PaTNF-α。该重组质粒经测序验证无误后转化大肠杆菌BL21 pLys E 菌株,经IPTG 诱导表达,表达产物经SDS-PAGE 检测,考马斯亮蓝G-250 染色观察目的蛋白是否表达。
pGEX-4T-3-PaTNF-α/BL21 经IPTG 大量诱导后,经5%—20%梯度胶分离,用预冷的0.25 mol/L KCl溶液染色10 min,切下目的蛋白用于免疫ICR 小鼠。每周免疫1 次,共免疫3 次。最后1 次免疫后第3 天从小鼠眼动脉取血,4°C 静置过夜后冷冻离心收集血清,于-70°C 保存备用。
1.9 Western blot 检测将收集的香鱼血清和单核/巨噬细胞上清样品用Bradford 法定量(Bradford,1976),参考黄左安等(2011)的方法进行Western blot 检测。香鱼单核/巨噬细胞培养上清和重组蛋白样本经SDS-PAGE 电泳分离后湿转法转移至聚偏二氟乙烯(polyvinylidene fluoride,PVDF)膜上,转膜结束后将PVDF 膜转移至封闭液(含5%脱脂奶粉的PBS-T)中于4°C 封闭过夜,按1:500 的比例加入PaTNF-α 抗血清(一抗),37°C 摇床孵育2 h,PBS-T 洗涤后按1: 1000 的比例加入HRPIgG(二抗),37°C 摇床孵育1 h,PBS-T 洗涤采用ECL化学发光法显影,胶片扫描后采用Quantity One 软件对电泳条带计算灰度值。
2 结果2.1 PaTNF-α cDNA 序列分析PaTNF-α cDNA 全长1932 bp(GenBank 登录号:JP740414),包括一个完整 ORF,起始于第347—350位的一个ATG 起始密码子,终止于第1051—1054 位的一个TGA 终止密码子,预测编码一个由235 个氨基酸组成、分子量大小约为26.4 kDa 的前体蛋白,等电点为6.35。
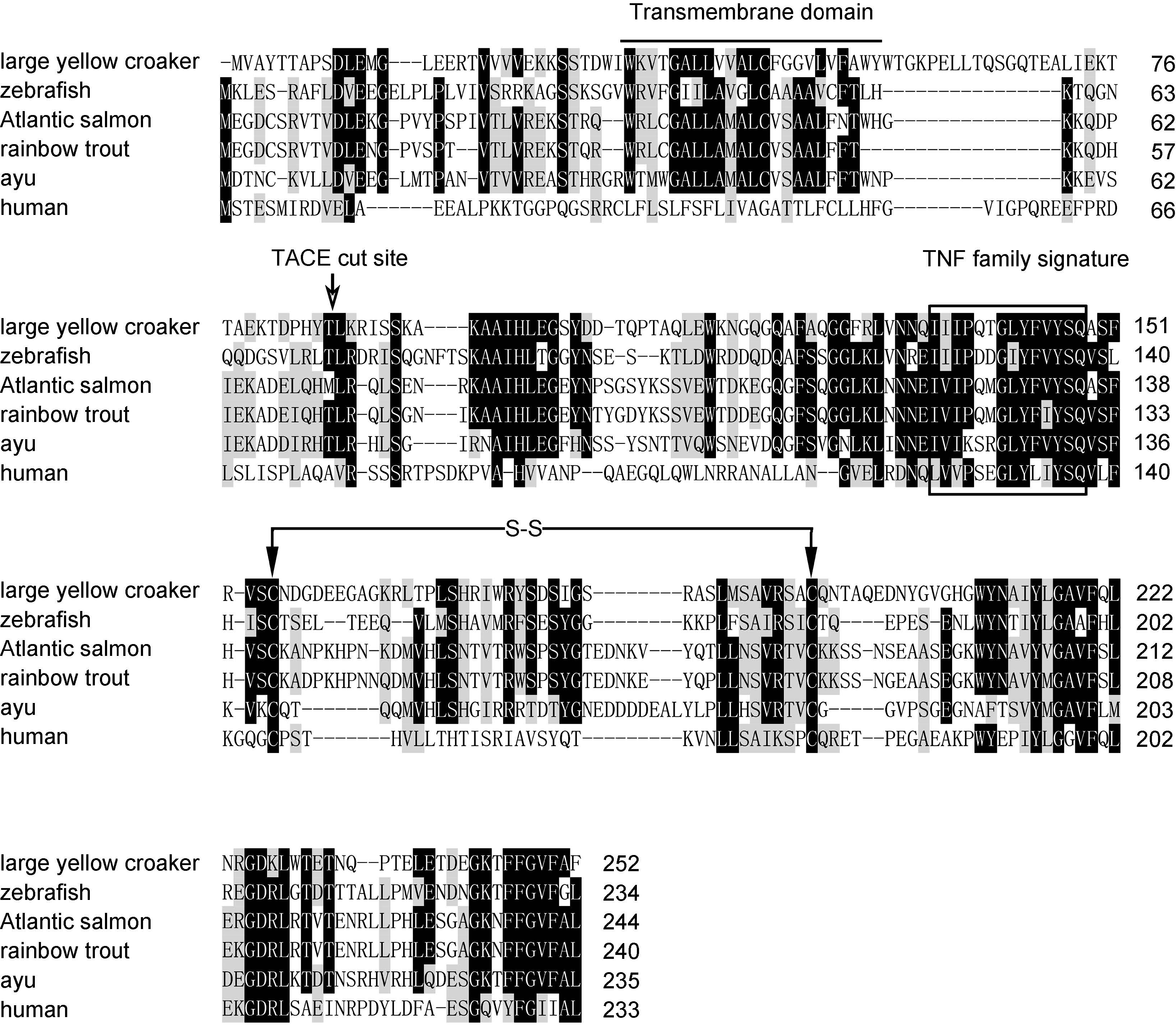
软件分析结果表明,推测的PaTNF-α 不具有信号肽序列,具有TNF 家族典型的特征序列“IIIPDDG IYFVYSQ”,分子内包含一个保守的二硫键Cys140-Cys181和位于72 位Thr和73 位Leu 之间TNF-α 转化酶(TNF-α converting enzyme,TACE)酶切位点,并且在第34—56 位氨基酸处有一个单一的跨膜结构域“WTMWGALLAMALCVSAALFFTWN”(图 1)。
|
|
图 1 香鱼与其它动物TNF-α 氨基酸序列的多重比对
Fig. 1 Multiple alignment of TNF-α amino acid sequences of ayu and other animals “—”代表TNF-α 跨膜结构域,“□”代表TNF 家族特征序列,“↓”代表潜在的TACE 酶切位点,“—S-S—”代表保守的半胱氨酸残基形成的二硫键,阴影阈值>60%,黑色阴影代表相同氨基酸,灰色阴影代表相似氨基酸 |
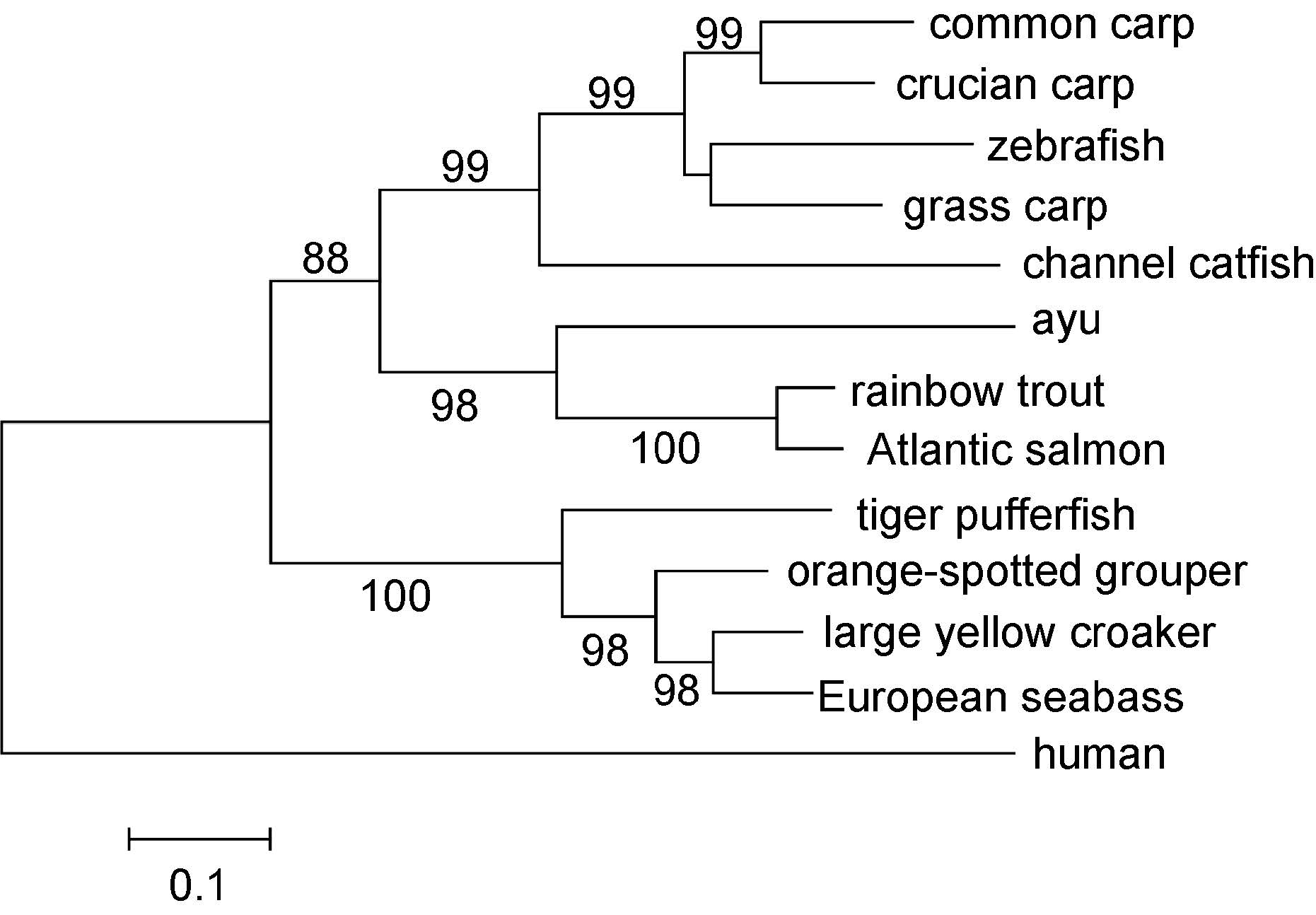
序列分析表明,PaTNF-α 与其它鱼类TNF-α 具有较高的氨基酸序列同源性(31.2%—53.4%),其中与虹鳟TNF-α 同源性最高,为53.4%。根据哺乳动物和鱼类的TNF-α 氨基酸全长序列构建的系统进化树揭示,鱼类TNF-α 单独形成一个大簇,香鱼与虹鳟、大西洋鲑的TNF-α 独立成簇,且与虹鳟TNF-α 的进化相关性最高(图 2)。
|
|
图 2 基于NJ 法构建的香鱼和其它物种TNF-α 全长氨基酸序列的系统进化树
Fig. 2 Phylogenetic tree of the full-length amino acid sequences of ayu and other animals TNF-α using neighbor-joining method 分叉处数值表示重复抽样1000 次所得到的置信度百分比,只显示置信度60%以上的数值; 标尺长度表明每个位点发生0.1 次置换 |
取健康香鱼的肝、脾、体肾、头肾、脑、肠、肌、外周血白细胞和单核/巨噬细胞进行qRT-PCR 检测,结果表明,健康香鱼TNF-α mRNA 在头肾中表达量最高,其次是脾、体肾、肝、肌、单核/巨噬细胞和外周血白细胞(图 3)。腹腔注射鳗,感染组香鱼表现典型的弧菌病症状,并能从肝、脾和肾等组织中分离出病原菌(结果未显示),对照组香鱼无明显症状。与对照组相比,鳗弧菌感染4 h 时,肝、脾和头肾中PaTNF-α mRNA 的表达量显著增加,分别为对照组的2.62、19.52和3.09 倍(P<0.05); 在8 h 时,肝和头肾中PaTNF-α mRNA 表达量继续增加,12 h 时达到峰值,分别为对照组30.08和11.69 倍(P<0.05),而在8 h 后,脾中PaTNF-α mRNA与对照组无明显差异;外周白血细胞中PaTNF-α mRNA 表达量在12 h 时显著高于对照组,为对照组的2.20 倍(P<0.05),在24 h时,与对照组无明显差异(图 3)。

|
|
图 3 qRT-PCR 分析PaTNF-α mRNA 的表达
Fig. 3 qRT-PCR analysis of PaTNF-α transcripts a. PaTNF-α mRNA 在健康香鱼中的表达,1: 脑; 2: 肠; 3: 肌; 4: 肝; 5: 脾; 6: 体肾; 7: 头肾; 8: 外周血白细胞; 9: 单核/巨噬细胞。b—e:PaTNF-α mRNA 在鳗弧菌感染香鱼中的表达,b: 肝; c: 脾; d: 头肾; e: 外周血白细胞。以香鱼TNF-α 与β-actin mRNA 的比值作为PaTNF-α mRNA 的相对表达量,*: 与对照组比较差异显著(P<0.05)(n=4) |
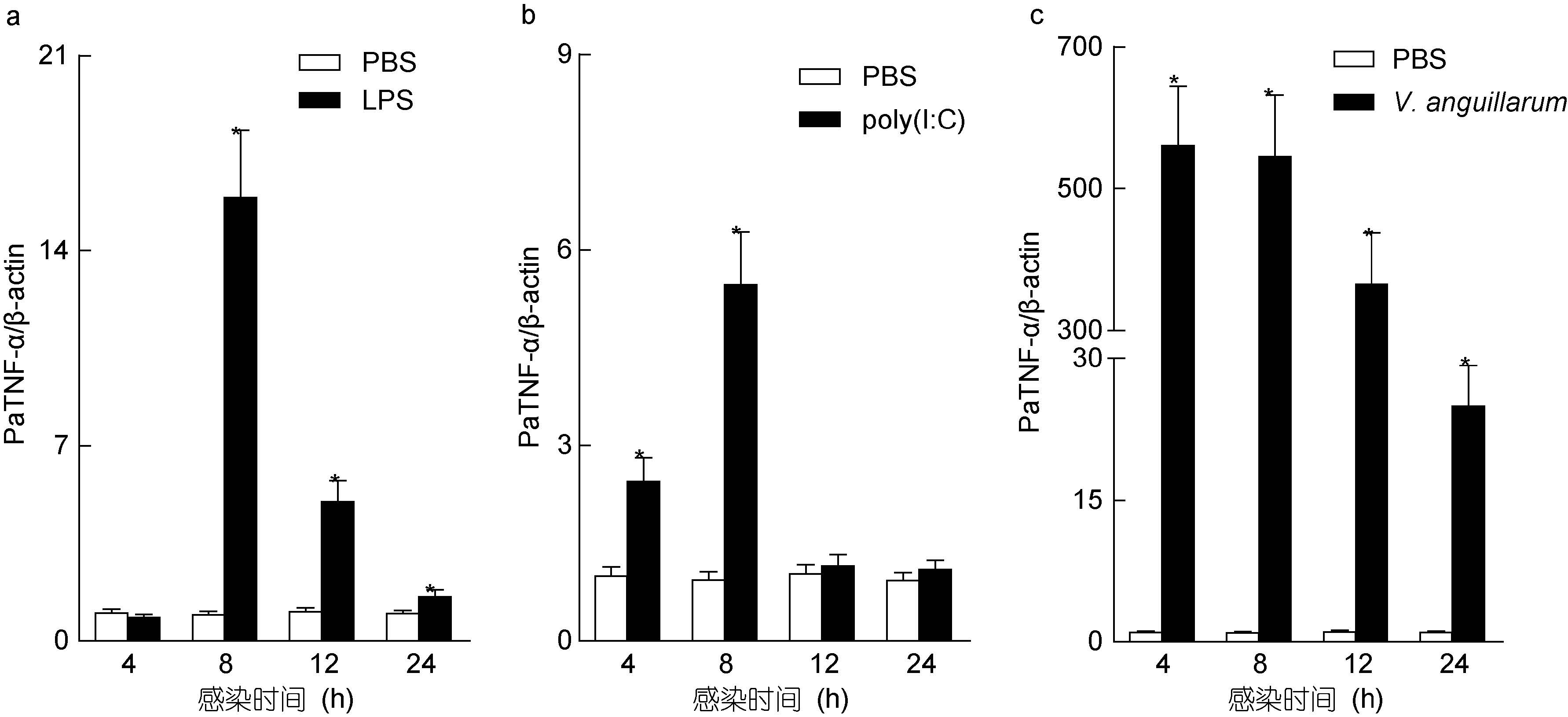
LPS、poly(I: C)和鳗弧菌处理香鱼单核/巨噬细胞后PaTNF-α mRNA 的表达量显著增加,其中poly(I: C)和鳗弧菌处理组PaTNF-α mRNA的表达量在4 h 时显著增加,分别为对照组的2.45和560.28 倍,LPS 处理组PaTNF-α mRNA 与对照组无明显差异(P<0.05); 在8 h时,LPS、poly(I: C)和鳗弧菌处理组PaTNF-α mRNA 表达量分别为对照组的15.89、5.46和544.96 倍(P<0.05);12 h 时,LPS和鳗弧菌处理组PaTNF-α mRNA 表达量仍然高于对照组,分别为对照组的4.99和365.03 倍,而poly(I: C)处理组与对照组无明显差异(P<0.05); 24 h时,LPS和poly(I: C)处理组PaTNF-α mRNA表达量均与对照组无明显差异,而鳗弧菌处理组PaTNF-α mRNA表达量仍高于对照组,为对照组的24.95 倍(图 4)。
|
|
图 4 qRT-PCR 分析LPS、poly(I: C)和鳗弧菌处理前后香鱼单核/巨噬细胞PaTNF-α mRNA 表达变化
Fig. 4 qRT-PCR analysis of PaTNF-α transcripts in ayu moncytes/macrophages upon LPS,poly(I: C) and V. anguillarum infection 以香鱼TNF-α 与β-actin mRNA 的比值作为PaTNF-α mRNA 的相对表达量,*: 与对照组比较差异显著(P<0.05)(n=4) |
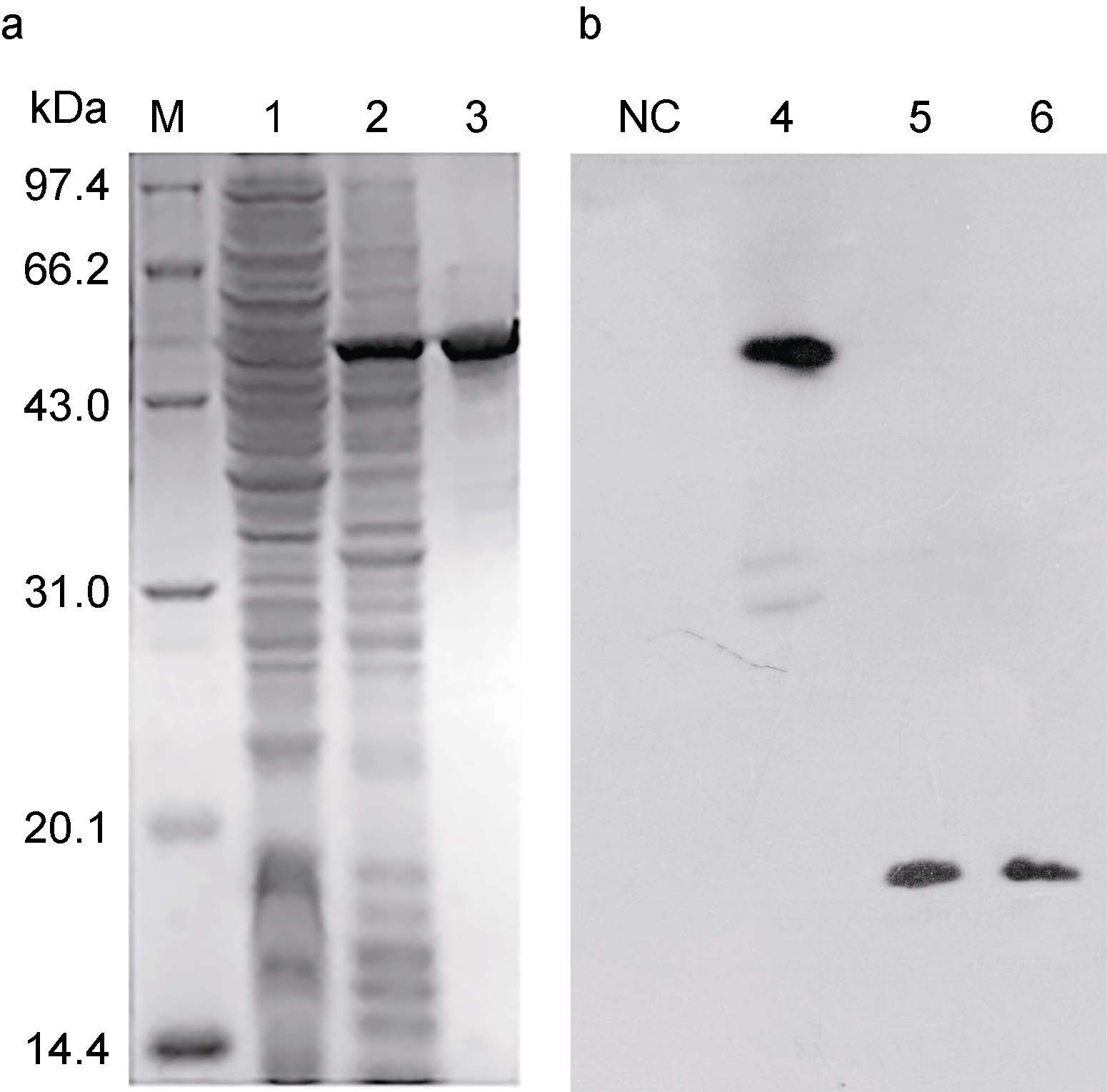
重组质粒pGEX-4T-3-PaTNF-α 经测序验证无误后转至BL21 pLys E,加入IPTG 诱导后高效表达,菌体总蛋白经SDS-PAGE 分离后出现一条高表达蛋白带,分子量为53.0 kDa 左右,与预测的重组蛋白分子量(52.7 kDa)相符(图 5a)。将目的条带切胶验证后,用于抗血清制备。
|
|
图 5 PaTNF-α 的原核表达和抗血清检测
Fig. 5 Prokaryotic expression of PaTNF-α and the detection of its antiserum a: SDS-PAGE 检测PaTNF-α 的原核表达,考马斯亮蓝G-250 染色。M: 低相对分子质量标准蛋白质(kDa); 1: BL21 plys E,IPTG 诱导;2: pGEX-4T-3-PaTNF-α/BL21 plys E,IPTG 诱导; 3: PaTNF-α 重组蛋白的切胶纯化产物; b: Western blot 检测PaTNF-α 抗血清特异性,ECL 显影。NC: 空白对照; 4: 原核表达产物; 5: 香鱼血清; 6: 香鱼单核/巨噬细胞上清 |
以PaTNF-α 抗血清进行Western blot,结果能观察到单一的反应条带,说明PaTNF-α 抗血清制备成功,且特异性较好(图 6b),而香鱼血清中PaTNF-α 成熟肽蛋白分子量约为18 kDa,比重组蛋白大约小34.7 kDa,比前体蛋白大约小8.4 kDa(图 5b)。

|
|
图 6 Western blot 检测鳗弧菌感染前后香鱼血清和单核/巨噬细胞上清中PaTNF-α 的表达变化
Fig. 6 Western blot analysis of PaTNF-α in ayu serum and monocytes/macrophage supernatant after V. anguillarum infection a: 不同感染时间香鱼血清中PaTNF-α Western blot 条带及灰度值分析; b: 不同感染时间香鱼单核/巨噬细胞上清中PaTNF-α Western blot条带及灰度值分析。*: 与对照组相比差异显著(P<0.05)(n=3) |
采用Western blot 检测鳗弧菌感染前后香鱼血清和单核/巨噬细胞上清中PaTNF-α 的表达。结果显示,鳗弧菌感染后,香鱼血清中PaTNF-α 的表达显著增加,4 h 时鳗弧菌感染香鱼血清中PaTNF-α 的表达量为对照组的5.20 倍,8 h 后含量达到峰值,为对照组的13.22 倍,随感染时间延长,12和24 h 血清中的含量略微下降,但仍为对照组的12.55 倍和11.55 倍(图 6a)。香鱼单核/巨噬细胞感染鳗,培养基上清中PaTNF-α 的表达也显著增加,在12 h 达到峰值,为对照组的2.92 倍,在24 h 时略有降低,但仍为对照组的1.92 倍(图 6b)。
3 讨论TNF-α 是一种具有多效性的促炎性细胞因子,在哺乳动物以及某些鱼类中被广泛克隆和报道。本研究从香鱼单核/巨噬细胞转录组数据库中获得了PaTNF-α 全长cDNA 序列。序列分析结果揭示,PaTNF-α 氨基酸序列与其它鱼类都拥有TNF 家族的特征序列"IIIPDDGIYFVYSQ",它与虹鳟的TNF-α 氨基酸序列同源性最高,为53.4%。系统进化树分析表明,鱼类TNF-α 独立成簇,香鱼与虹鳟TNF-α 进化相关性最高。Western blot 分析结果表明,香鱼血清和单核/巨噬细胞上清中PaTNF-α 的分子量均为18 kDa 左右,与预测的PaTNF-α 经TACE 加工裂解之后产生的成熟肽分子量大小一致。Lu et al 研究表明,香鱼TACE能影响头肾来源单核/巨噬细胞中PaTNF-α 的表达(Lu et al,2015)。因此,可以推测鱼类TACE 能影响TNF-α 的释放(Horiuchi et al,2010; Lu et al,2015)。
表达特征分析表明,PaTNF-α mRNA 在健康香鱼被检组织与细胞中有不同程度的表达,且在头肾的表达量最高,与已报道的鲤鱼(Savan et al,2004)和条纹婢(Latris lineata)(Covello et al,2009)等鱼类研究结果较为一致。目前,已有较多文献揭示,鱼类TNF-α 的表达与病原体感染密切相关,主要体现为,病原体感染后鱼类TNF-α 的表达显著上调(Hirono et al,2000; Zhang et al,2012; Wang et al,2013)。例如,草鱼感染嗜水气单胞菌(Aeromonas hydrophila)后,肝TNF-α mRNA 的表达在12 h和24 h 时分别上调2.2倍和2.1 倍,48 h 时达到最高(2.24 倍),脾TNF-αmRNA 的表达在3 h 时达到峰值,上调6.64 倍,头肾TNF-α mRNA 表达量在3 h 时达到峰值,上调17.16倍,6 h 时上调约11 倍,随后降至对照组水平(Wang et al,2014); 草鱼感染杀鲑气单胞菌(Aeromonas salmonicida)3 h和24 h 时,脾TNF-α mRNA 的表达量分别增加约100 倍和4 倍(Zanuzzo et al,2015)。本研究中,香鱼感染鳗,肝、头肾和外周血白细胞中PaTNF-α mRNA 表达变化趋势与上述研究结果相似,但达到峰值的时间点和峰值不同,肝、头肾和外周血白细胞PaTNF-α mRNA 在感染12 h 时达到最高,分别为对照组的30.08、11.69和2.20 倍,而脾PaTNF-α mRNA 表达量在4 h 时即达到峰值,为对照组的19.52 倍。本研究还发现,鳗弧菌感染后,香鱼血清中PaTNF-α 的表达逐渐增加,8 h 时达到峰值,为对照组的13.22 倍,12 h和24 h 时略微下降,但仍显著高于对照组。
头肾是硬骨鱼类重要的造血组织和免疫器官,含有丰富的单核/巨噬细胞,已知单核/巨噬细胞是鱼类TNF-α 的主要产生部位(Stafford et al,2001; Hong et al,2013)。因此,我们从香鱼头肾中分离了单核/巨噬细胞,分别研究了LPS、poly(I: C)和鳗弧菌刺激对其PaTNF-α mRNA 表达的影响,结果表明,LPS、poly(I: C)和鳗弧菌都能诱导香鱼单核/巨噬细胞PaTNF-α mRNA 表达量显著增加,与已报道的虹鳟(Zou et al,2003; Hong et al,2013)、鲤鱼(Saeij et al,2003)和草鱼(Zhang et al,2012; Wang et al,2013)等鱼类较为一致。在草鱼中,poly(I: C)免疫刺激肾细胞8 h时,TNF-α mRNA 表达量上调了61 倍,而GCRV 免疫刺激肾细胞24 h,TNF-α mRNA 表达量上调了51 倍(Wang et al,2013); 在虹鳟中,LPS和poly(I: C)诱导头肾巨噬细胞TNF-α mRNA 表达的变化趋势相同,均在4 h 时达到峰值,但LPS 的诱导明显强于poly(I:C),LPS 诱导4 h 时头肾巨噬细胞TNF-α mRNA 表达上调约1000 倍,而此时poly(I: C)诱导TNF-α mRNA表达上调约80 倍(Hong et al,2013)。上述研究中,各免疫刺激对鱼类TNF-α mRNA 表达的诱导程度均高于本研究结果,可能由于LPS和poly(I: C)的处理浓度不同所致。同时,鳗弧菌对PaTNF-α mRNA 表达的诱导程度高于LPS和poly(I: C)的诱导,且较早达到峰值。Zhang等(2012)研究还揭示,LPS 诱导草鱼头肾白细胞培养基上清中TNF-α 浓度显著增加,12 h 时达到最高,与本研究中鳗弧菌诱导香鱼单核/巨噬细胞上清PaTNF-α 的表达较为一致。上述研究结果揭示,头肾来源的单核/巨噬细胞是鱼类TNF-α 的重要产生部位,在免疫刺激下短期内大量合成并释放TNF-α(Hirono et al,2000; Xie et al,2008; Zhang et al,2012)。
4 结论本研究测定了香鱼TNF-α cDNA 序列,序列分析揭示其与虹鳟TNF-α 序列最相似。健康香鱼中,PaTNF-α mRNA 在头肾中表达量最高; 腹腔注射鳗,香鱼肝、脾、头肾和外周白血细胞中PaTNF-αmRNA 表达量显著上调; 头肾来源的单核/巨噬细胞经鳗弧菌、LPS和poly(I: C)体外处理后PaTNF-αmRNA 表达量增加; 鳗弧菌感染后香鱼血清和单核/巨噬细胞上清中的PaTNF-α 表达量含量也显著增加,揭示香鱼TNF-α 表达与鳗弧菌感染紧密相关,可能参与病原体感染诱导的炎症免疫反应。研究结果为进一步研究鱼类TNF-α 的生物学功能及其在鱼类病原体感染的炎症反应中的作用机制提供基础资料。
| 李长红, 陈炯, 史雨红等. 2009. 宁海地区香鱼弧菌病病原菌鉴定. 微生物学报, 49(7): 931-937 |
| 杨旦阳, 陈炯, 陆新江等. 2013. 香鱼CCL4-like 基因的克隆、序列分析及免疫相关性表达变化分析. 中国细胞生物学学报, 35(5): 676-683 |
| 黄左安, 陈炯, 陆新江等. 2011. 香鱼凝血因子X 基因表达与鳗利斯顿氏菌感染的相关性. 动物学研究, 32(5):492-498 |
| Bradford M M. 1976. A rapid and sensitive method for thequantitation of microgram quantities of protein utilizing theprinciple of protein-dye binding. Anal Biochem, 72(1-2):248-254 |
| Covello J M, Bird S, Morrison R N et al. 2009. Cloning andexpression analysis of three striped trumpeter (Latris lineata)pro-inflammatory cytokines, TNF-α, IL-1β and IL-8, inresponse to infection by the ectoparasitic, Chondracanthusgoldsmidi. Fish Shellfish Immunol, 26(5): 773-786 |
| Grayfer L, Walsh J G, Belosevic M. 2008. Characterization andfunctional analysis of goldfish (Carassius auratus L.) tumornecrosis factor-alpha. Dev Comp Immunol, 32(5): 532-543 |
| Gruys E, Toussaint M J M, Niewold T A et al. 2005. Acute phasereaction and acute phase proteins. J Zhejiang Univ Sci,6B(11): 1045-1056 |
| Hirono I, Nam B-H, Kurobe T et al. 2000. Molecular cloning,characterization, and expression of TNF cDNA and genefrom Japanese flounder Paralychthys olivaceus. J Immunol,165(8): 4423-4427 |
| Hong S, Li R G, Xu Q Q et al. 2013. Two types of TNF-α exist inteleost fish: phylogeny, expression, and bioactivity analysisof type-II TNF-α3 in rainbow trout Oncorhynchus mykiss. JImmunol, 191(12): 5959-5972 |
| Horiuchi T, Mitoma H, Harashima S et al. 2010. Transmembrane TNF-α: structure, function and interaction with anti-TNFagents. Rheumatology, 49(7): 1215-1228 |
| Laing K J, Wang T H, Zou J et al. 2001. Cloning and expressionanalysis of rainbow trout Oncorhynchus mykiss tumournecrosis factor-α. Eur J Biochem, 268(5): 1315-1322 |
| Lam F W-S, Wu S-Y, Lin S-J et al. 2011. The expression of twonovel orange-spotted grouper (Epinephelus coioides) TNFgenes in peripheral blood leukocytes, various organs, andfish larvae. Fish Shellfish Immunol, 30(2): 618-629 |
| Livak K J, Schmittgen T D. 2001. Analysis of relative geneexpression data using real-time quantitative PCR and the2-ΔΔCT method. Methods, 25(4): 402-408 |
| Lu X J, Chen J, He Y Q et al. 2013. Molecular characterization ofan IL-1β gene from ayu, Plecoglossus altivelis. FishShellfish Immunol, 34(5): 1253-1259 |
| Lu X J, Chen Q, Yang G J et al. 2015. The TNFα convertingenzyme (TACE) from ayu (Plecoglossus altivelis) exhibitsTNFα shedding activity. Mol Immunol, 63(2): 497-504 |
| Ordás M C, Costa M M, Roca F J et al. 2007. Turbot TNFα gene:molecular characterization and biological activity of therecombinant protein. Mol Immunol, 44(4): 389-400 |
| Rajmani R S, Singh P K, Kumar G R et al. 2015. In-vitrocharacterization and evaluation of apoptotic potential ofbicistronic plasmid encoding HN gene of Newcastle diseasevirus and human TNF-α. Anim Biotechnol, 26(2): 112-119 |
| Saeij J P J, Stet R J M, de Vries B J et al. 2003. Molecular andfunctional characterization of carp TNF: a link between TNFpolymorphism and trypanotolerance?. Dev Comp Immunol,27(1): 29-41 |
| Savan R, Sakai M. 2004. Presence of multiple isoforms of TNFalpha in carp (Cyprinus carpio L.): genomic and expressionanalysis. Fish Shellfish Immunol, 17(1): 87-94 |
| Stafford J L, McLauchlan P E, Secombes C J et al. 2001.Generation of primary monocyte-like cultures from rainbowtrout head kidney leukocytes. Dev Comp Immunol, 25(5-6):447-459 |
| Tamura K, Stecher G, Peterson D et al. 2013. MEGA6: Molecularevolutionary genetics analysis version 6.0. Mol Biol Evol,30(12): 2725-2729 |
| Van Horssen R, ten Hagen T L M, Eggermont A M M. 2006.TNF-α in cancer treatment: molecular insights, antitumoreffects, and clinical utility. Oncologist, 11(4): 397-408 |
| Wang H, Shen X B, Xu D et al. 2013. LipopolysaccharideinducedTNF-α factor in grass carp (Ctenopharyngodonidella): evidence for its involvement in antiviral innateimmunity. Fish Shellfish Immunol, 34(2): 538-545 |
| Wang L, Liu L C, Zhou Y et al. 2014. Molecular cloning andexpression analysis of mannose receptor C type 1 in grasscarp (Ctenopharyngodon idella). Dev Comp Immunol, 43(1):54-58 |
| Willrich M A V, Murray D L, Snyder M R. 2015. Tumor necrosisfactor inhibitors: clinical utility in autoimmune diseases.Transl Res, 165(2): 270-282 |
| Xiao J, Zhou Z C, Chen C et al. 2007. Tumor necrosisfactor-alpha gene from mandarin fish, Siniperca chuatsi:Molecular cloning, cytotoxicity analysis and expressionprofile. Mol Immunol, 44(14): 3615-3622 |
| Xie F J, Zhang Z P, Lin P et al. 2008. Cloning and infectionresponse of tumour-necrosis factor alpha in large yellowcroaker Pseudosciaena crocea (Richardson). J Fish Biol,73(5): 1149-1160 |
| Zanuzzo F S, Urbinatia E C, Rise M L et al. 2015. Aeromonassalmonicida induced immune gene expression in Aloe verafed steelhead trout, Oncorhynchus mykiss (Walbaum).Aquaculture, 435: 1-9 |
| Zhang A Y, Chen D Y, Wei H et al. 2012. Functionalcharacterization of TNF-α in grass carp head kidneyleukocytes: induction and involvement in the regulation ofNF-κB signaling. Fish Shellfish Immunol, 33(5): 1123-1132 |
| Zou J, Peddie S, Scapigliati G et al. 2003. Functionalcharacterisation of the recombinant tumor necrosis factors inrainbow trout, Oncorhynchus mykiss. Dev Comp Immunol,27(9): 813-822 |
 2015, Vol. 46
2015, Vol. 46


