
中国海洋湖沼学会主办。
文章信息
- 丁聪聪, 徐年军, 张琳, 孙雪, 李亚鹤. 2015.
- DING Cong-Cong, XU Nian-Jun, ZHANG Lin, SUN Xue, LI Ya-He. 2015.
- 水杨酸对蛋白核小球藻(Chlorella pyrenoidosa) 生长及抗逆相关基因的影响
- EFFECTS OF SALICYLIC ACID ON GROWTH AND STRESS-RELATED GENES OF CHLORELLA PYRENOIDOSA
- 海洋与湖沼, 46(6): 1451-1460
- Oceanologia et Limnologia Sinica, 46(6): 1451-1460.
- http://dx.doi.org/10.11693/hyhz20150300082
-
文章历史
- 收稿日期:2015-03-18
- 改回日期:2015-06-24
2. 浙江省海洋生物工程重点实验室 宁波 315211
2. Key Laboratory of Marine Biotechnology of Zhejiang Province, Ningbo 315211, China
小球藻(Chlorella)为绿藻门(Chlorophyta)、 Trebouxiophyceae 纲、小球藻科(Chlorellaceae)的一类单细胞藻类,在自然界广泛分布。小球藻中常见种主要有普通小球藻(C. vulgaris)、蛋白核小球藻(C. pyrenoidosa)、椭圆小球藻(C. ellipsoidea)等。蛋白核小球藻因生长快、易培养,及其独有的具有很高药用价值的小球藻生长因子(CGF)而广受关注。温度作为重要的环境因素之一,在小球藻生长和光合作用中发挥了重要作用(欧阳峥嵘等,2010)。水杨酸作为一种新型植物激素已成为植物体内的重要信号分子来诱导逆境防御机制,参与并调节逆境胁迫。大量的研究证实水杨酸可以提高植物对低温(Lei et al,2010)、高温(Li et al,2015)、盐害(Jayakannan et al,2015)等胁迫的抗性。
热激蛋白(heat stock proteins,HSPs)作为植物体对逆境短期响应的一种分子伴侣,能阻止细胞内变性蛋白发生聚集,并对其进行修复(Fu et al,2009),可提高机体耐热性,减轻逆境胁迫对机体的伤害(Koizumi et al,2014)。大量研究发现,逆境条件如高温、高盐、重金属、干旱和病害等多种胁迫都可诱导 HSPs 的合成(Timperio et al,2008; 周向红等,2010)。 其中HSP70 是热激蛋白家族中的重要成员,参与真核细胞新生肽段折叠、定位等正常生命活动过程,以及DNA 修复、抗氧化活性、光保护物质等多种应激反应。藻类中关于HSP 的研究已经比较多,其中褐藻门的裙带菜(Undaria pinnatifida)和海带(Laminaria japonica)(Henkel et al,2008; Fu et al,2009)、红藻门的龙须菜(Gracilaria lemaneiformis)(Gu et al,2012)、绿藻门的孔石莼(Ulva pertusa)(Tominaga et al,2010)等都有HSP70 基因的相关报道。Liu等(2014)克隆了普通小球藻HSP90 基因,但目前尚无蛋白核小球藻 HSP70 基因克隆和表达的相关报道。
磷酸甘油酸激酶(phosphoglycerate kinase,PGK)是生物体内糖酵解过程中的关键酶,缺乏此酶可引起生物体代谢功能紊乱。磷酸甘油酸激酶在催化1,3-二磷酸甘油酸转变成3-磷酸甘油酸时,产生一分子的 ATP。逆境条件下,植物需消耗大量能量来提高抗性,而能量主要来源为糖酵解途径(Wang et al,2009)。目前关于PGK 的研究主要集中在动物方面(Wang et al,2014),植物方面有部分蛋白组学相关研究(蒋际谋等,2014),基因表达水平研究较少(Ding et al,2014),而藻类中的研究更少。Shingaki-Wells等(2011)发现,缺氧环境下,水稻胚芽鞘中PGK活性提高,并证实了在适应缺氧环境的过程中水稻胚芽鞘酵解和酒精发酵增强。而高温下水杨酸对糖代谢分子水平的影响方面的研究还很少。
本文从蛋白核小球藻中分离鉴定了其HSP70和PGK 基因序列,并研究了高温胁迫下水杨酸对蛋白核小球藻生长、可溶性糖和蛋白含量及HSP70和PGK 基因转录水平的影响。相关研究结果可为水杨酸在抗高温胁迫方面的应用及其作用机制等提供一定的参考。
1 材料与方法 1.1 材料蛋白核小球藻820 藻株来自宁波大学海洋生物工程重点实验室藻种室,培养基为f/2 培养基,培养温度为25°C,光照强度为3500 lx,光照周期为 12L: 12D。
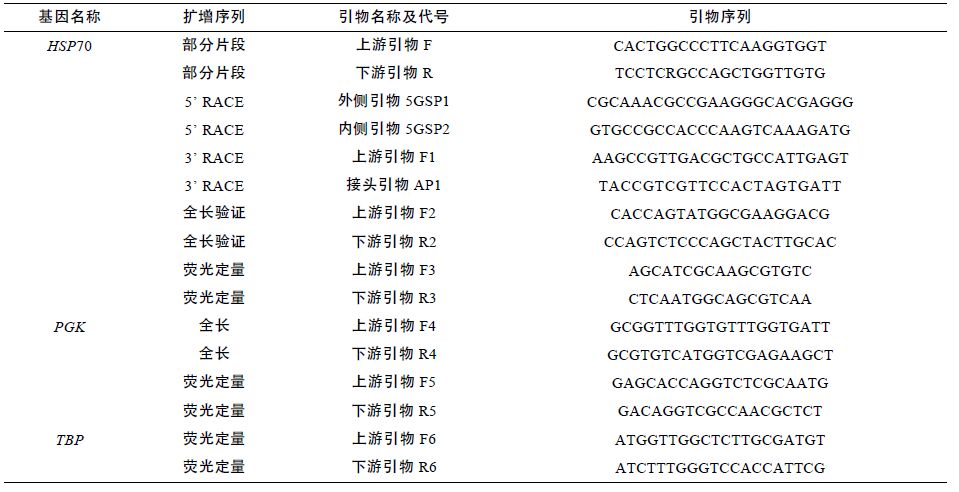
1.2 引物序列从GenBank数据库中搜索莱茵衣藻(Chlamydomonas reinhardtii)、普通小球藻等的HSP70 序列,利用 ClustalX 1.83 软件进行比对,根据其保守核苷酸序列设计简并引物,扩增出两条基因的部分cDNA 序列,然后根据这部分cDNA 序列使用Primer Premier 5.0 软件来设计5′ RACE和3′ RACE 引物(所用各引物序列见表 1)。
 |
首先8000 r/min 离心5min 收集对数期的蛋白核小球藻,无菌水洗涤藻细胞后再次离心。再按Trizol 试剂说明提取小球藻总RNA,检测总RNA 质量合格后根据PrimeScript® RT reagent Kit(TaKaRa)反转录试剂盒说明书反转录为cDNA,以该cDNA 为模板利用简并引物进行PCR 扩增。1%琼脂糖凝胶电泳检测PCR 产物后,GenClean 琼脂糖凝胶回收试剂盒回收目的片段,连接至pMD18-T 载体,连接后的产物导入大肠杆菌(E. coli)DH5α 感受态细胞,阳性克隆送去华大基因(上海)科技服务有限公司测序。
1.4 HSP70 的RACE 扩增利用SMARTerTM RACE cDNA 扩增试剂盒(Clontech 公司)获得基因的5’ 端序列。根据 PrimeScript® RT reagent Kit(Takara)反转录试剂盒说明书进行3’ RACE cDNA的制备,3’ RACE adaptor 代替试剂盒中的OligodT Primer和R and om6 mers 进行反转录反应。以合成的cDNA 为模板,特异性引物F、接头引物AP1 作为上下游引物进行3’ RACE PCR 扩增。
1.5 HSP70和PGK 基因全长的获得及验证将测序得到的HSP70 基因的部分片段、5’ RACE和3’ RACE 片段一起拼接得到其全长cDNA 序列。 PGK 基因序列来自实验室已测蛋白核小球藻的转录组测序结果。为了验证两条基因序列的正确性,再从基因两端的非翻译区(UTR)区设计一对引物,利用 Pyrobest Polymerase(TaKaRa)进行PCR 扩增。产物的回收、转化等同1.3,将阳性克隆送去测序。
1.6 HSP70和PGK 基因的序列分析将HSP70和PGK 基因在NCBI 的Blastx 中(http://www.ncbi.nlm.nih.gov/blastx)进行同源性比对; 用 ORF Finder(http: //www.ncbi.nlm.nih.gov/gorf/gorf.html)推测开放阅读框; 利用ExPASy Proteomics Server(http: //web.expasy.org)进行氨基酸序列分析; 利用 ClustalX和MEGA 5.0 软件中的邻接法(NJ)分别进行多序列比对和系统进化树构建。
1.7 HSP70和PGK 基因转录水平的定量分析样品处理: 处理温度为35°C,在处于对数中期的蛋白核小球藻中加入水杨酸母液,使其终浓度分别为0、1、5、10、15和20μg/mL,每组设三个平行,培养12h和24h 后取样。根据获得的HSP70和PGK 基因设计荧光定量PCR 引物(表 1)。以TATA 结合蛋白(TATA-binding protein,TBP)做内参基因,根据其 cDNA 序列设计荧光定量PCR 引物(表 1)。将TBP、 HSP70和PGK 的荧光定量PCR 引物扩增序列进行克隆与测序鉴定。
荧光定量PCR采用SYBR® Premix Ex TaqTM试剂盒,反应体系: 10 μL SYBR Premix Ex Taq,正反向引物(10 μmol/L)各0.4 μL,2 μL cDNA 模板,RNA-free 水补足体积至20 μL。PCR 循环参数为95°C 预变性 2min; 然后按95°C 变性15s,55°C 复性15s,72°C 延伸 20s 的程序进行40 个循环; PCR 结束后进行熔解曲线分析95°C 15s,60°C 15s,95°C 15s(一个循环)。每个样品三个平行。采用2–ΔΔCt 方法分析HSP70和PGK 的相对表达量。并用Origin 7.0 软件进行差异显著性分析。
1.8 生长及生化指标的测定不同浓度水杨酸处理蛋白核小球藻24h和48h 后,利用分光光度计测定680nm 下藻的吸光值。根据吸光值与藻细胞密度的标准曲线图计算出细胞密度,并根据μ=(lnN–lnN0)/(t–t0)计算藻的比生长速率。其中 N0 为初始培养时间t0 时的细胞密度,N 为t 时的细胞密度。可溶性糖含量测定采用硫酸蒽酮法,可溶性蛋白含量测定用考马斯亮蓝法(李合生,2000)。
1.9 统计分析数据处理和统计分析采用Origin7.0 软件,差异显著水平检验用的是单因素方差分析(one-way ANOVA),P<0.05 为差异显著,P<0.01 为差异极显著。
2 结果 2.1 HSP70和PGK 基因的扩增使用HSP70 简并引物扩增得到1518 bp 长的 cDNA 部分片段,将其与3′ RACE 扩增得到的长为 611 bp 的产物与长900 bp 的5′ RACE 产物一起拼接,得到全长为2405 bp 的HSP70 基因(GenBank 号: KP694307),包括1959 bp 的开放阅读框(ORF)、60 bp 的5’端非编码区(5’-UTR)和386 bp 的3′端非编码区(3’-UTR)。其中ORF 区编码652 个氨基酸,Expasy 分析显示其分子量大小为71.59 kDa,理论等电点为 5.12。利用引物F4和R4 扩增得到全长1664 bp 的 PGK 基因(GenBank 号: KP694308),包括35 bp 的 5’-UTR,1398 bp 的ORF和231 bp 的 3’-UTR,其中 ORF 编码465 个氨基酸,推测其分子量为49.16 kDa,理论等电点为7.01。
2.2 HSP70和PGK 基因的分析将由HSP70 的cDNA 序列推导出的氨基酸序列与其它物种的HSP70 氨基酸序列进行多序列比对(图 1),结果表明该蛋白核小球藻与普通小球藻和小球藻C. variabilis 的同源性均高达91%,与拟南芥(Arabidopsis thaliana)的同源性为83%。我们在HSP70 氨基酸的多序列比对中发现序列保守性强的区域,包含了三个典型的 HSP70 家族签名基序,其氨基酸残基序列分别为10—17(IDLGTTYS)、203—216(IFDLGGGTFDVSLL)、339—354(VVLVGGSTRIPKVQQ),及细胞质定位的C-末端的特征基序(EEVD)。

|
|
图 1 蛋白核小球藻与其它物种的HSP70 氨基酸的多序列比对结果
Fig. 1 Alignment of HSP70 amino acid sequences of C. pyrenoidosa and other species
“*”表示保守的氨基酸残基, “: ”表示保守替换的氨基酸残基, “.”表示相似性氨基酸, 方框中为三个家族签名基序 C. vulgaris (ABR01232.1); C. variabilis (XP_005843891.1); A. thaliana (NP_187864.1); Gossypium hirsutum (ACJ11745.1); Oryza sativa Japonica Group (NP_001044757.1); Zea mays (XP_008674843.1); Ch. reinhardtii (AAB00730.2); Chlamydomonas sp. ICE-L (ACX42438.1) |
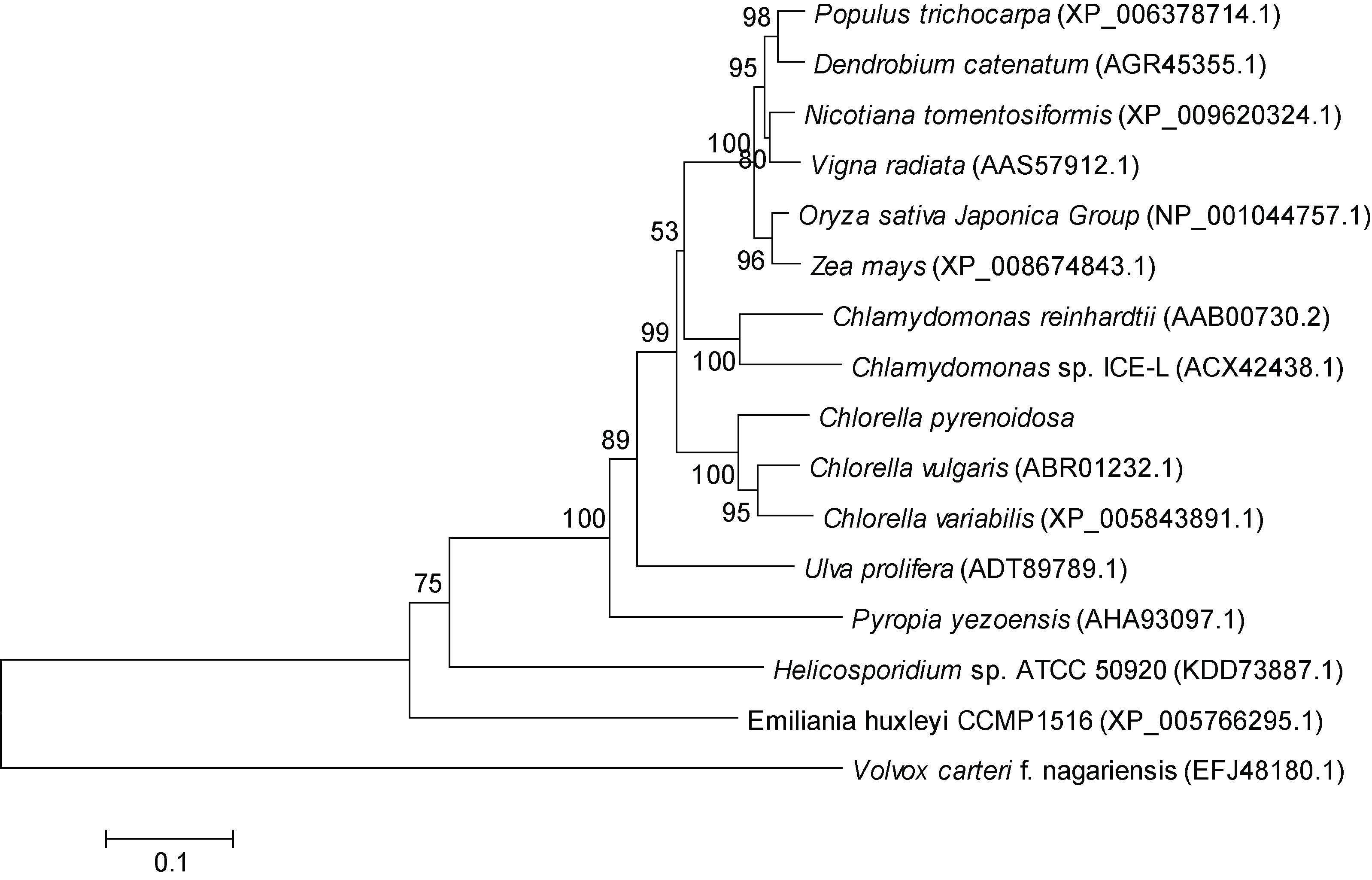
利用邻接法构建了基于HSP70 氨基酸序列的系统进化树。进化树分析显示,蛋白核小球藻HSP70 氨基酸序列与普通小球藻和小球藻C. variabilis 亲缘关系最近,先聚为一支,然后再与其它植物聚为一组,符合其传统的分类地位(图 2)。
|
| 图 2 不同物种基于HSP70 氨基酸序列的系统进化树 Fig. 2 Phylogenetic tree of different species based on HSP70 amino acid sequences |
Blastx 分析结果表明蛋白核小球藻的PGK 氨基酸序列与团藻(Volvox carteri f. nagariensis)有75%的相似性,与莱茵衣藻(Ch. reinhardtii)相似性为73%。氨基酸多序列比对中连续序列YVNDAFG、AHRAHAST、 WNGPMGVFEF、TIIGGGDSV、MSHISTGGGASLEL 保守性较强(图 3)。分析基于PGK 氨基酸序列构建的进化树,发现蛋白核小球藻与莱茵衣藻和团藻亲缘关系最近,聚为一支,其它高等植物则聚在一起(图 4)。以上结果表明不同物种的HSP70和PGK 在进化过程中是比较保守的,其氨基酸序列同源性较高。

|
|
图 3 蛋白核小球藻与其它物种的PGK 氨基酸的多序列比对结果
Fig. 3 Alignment of PGK amino acid sequences of C. pyrenoidosa and other species
“*”表示保守的氨基酸残基, “: ”表示保守替换的氨基酸残基, “.”表示相似性氨基酸 A. thaliana (NP_176015.1); Theobroma cacao (XP_007022578.1); Zea mays (AFW78532.1); Pinus massoniana (AIZ74346.1); Pinus pinaster (CBL95264.1); V. carteri f. nagariensis (XP_002951648.1); Ch. reinhardtii (XP_001699523.1); Coccomyxa subellipsoidea C-169 (XP_005651456.1) |

|
| 图 4 不同物种基于PGK 氨基酸序列构建的系统进化树 Fig. 4 Phylogenetic tree of different species based on PGK amino acid sequences |
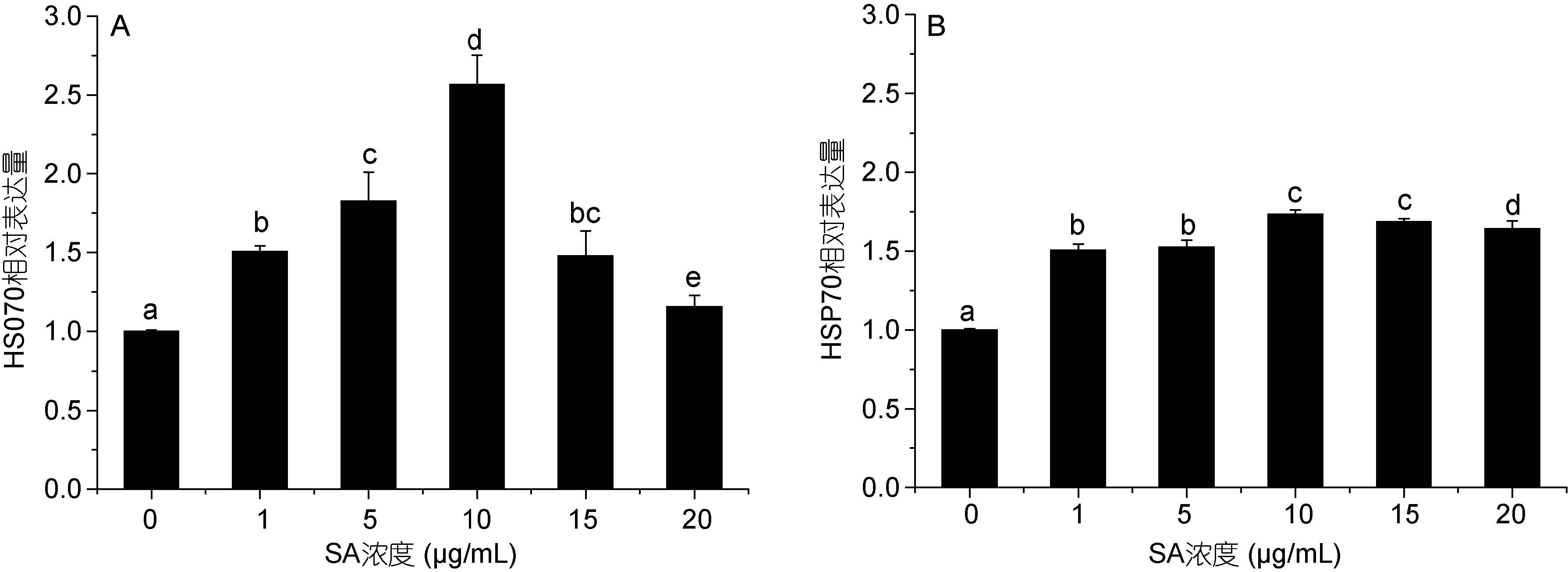
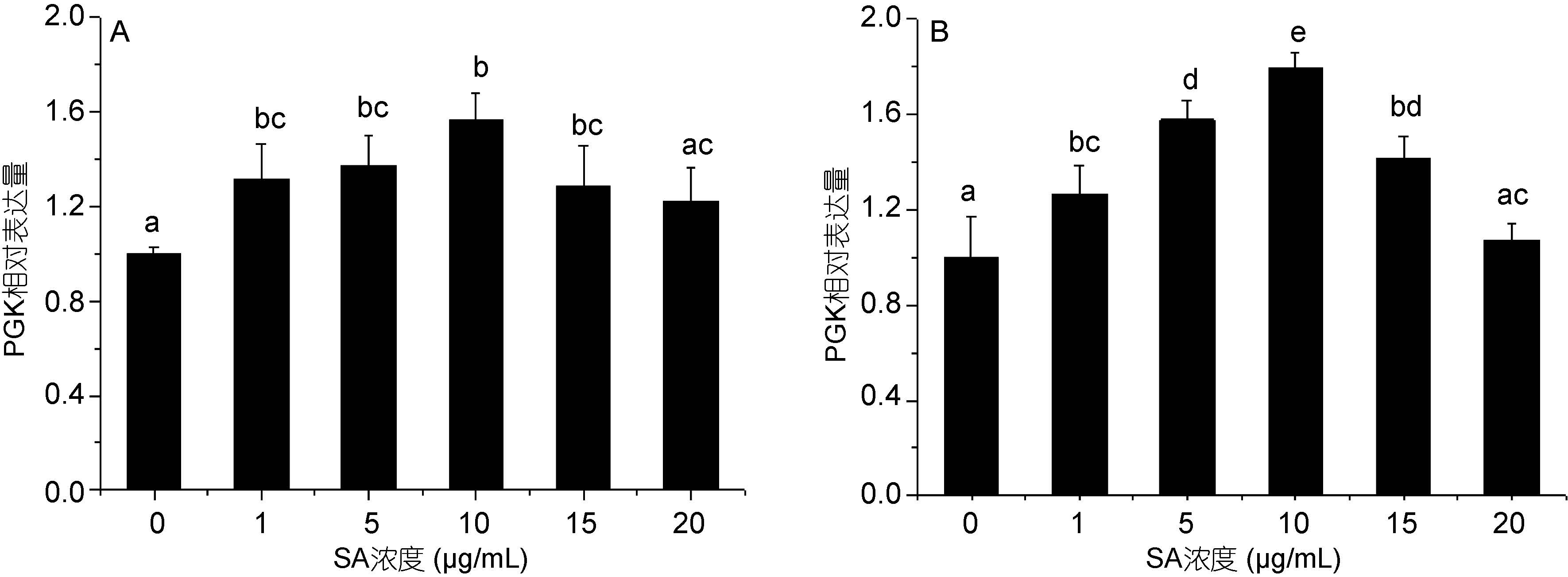
影响不同浓度水杨酸对HSP70(图 5)和PGK(图 6)基因表达的影响在12h和24h 均呈现相同的趋势。水杨酸添加后,HSP70和PGK 基因表达量均增加,在0— 10μg/mL 浓度范围内两基因的表达水平随着水杨酸浓度的升高而增加,随着水杨酸浓度的继续升高两者的表达量有所下降。其中10 μg/mL 水杨酸浓度下两基因的表达量最高。
|
| 图 5 不同浓度水杨酸对高温培养蛋白核小球藻HSP70 基因表达的影响(A: 12h, B: 24h) Fig. 5 Effects of salicylic acid concentration on HSP70 relative expression of C. pyrenoidosa under high temperature (mean±SD) (A: 12h, B: 24h) 图中不同字母a、b、c、d、e 表示有显著性差异。下同 |
|
| 图 6 不同浓度水杨酸对高温培养蛋白核小球藻PGK 基因表达的影响(A: 12h, B: 24h) Fig. 6 Effects of salicylic acid concentration on PGK relative expression of C. pyrenoidosa under high temperature (mean±SD) (A: 12h, B: 24h) |
在水杨酸处理12h和24h 时,HSP70 的相对表达量与对照组均有显著性差异(P<0.05),且12h 时(图 5A)1、5、10、15μg/mL 水杨酸处理组与对照组差异极显著(P<0.01); 而24h 时(图 5B)5 个处理组与对照组差异均极显著(P<0.01)。在水杨酸处理12h 时,10μg/mL 水杨酸浓度组中HSP70 表达量为对照组的
2.57 倍,在24h 则为对照组的1.71 倍。在水杨酸处理12h(图 6A)和24h(图 6B)时,PGK 的相对表达量在1、5、10、15 μg/mL 水杨酸处理组和对照组均有显著性差异(P<0.05),且5、10 μg/mL 水杨酸处理组与对照组差异极显著(P<0.01)。12h 时,10μg/mL 水杨酸浓度下PGK 表达量为对照组的 1.56 倍,24h 则为对照组的1.79 倍。以上结果说明 水杨酸促进了HSP70和PGK 的表达,且10 μg/mL 效果最好。
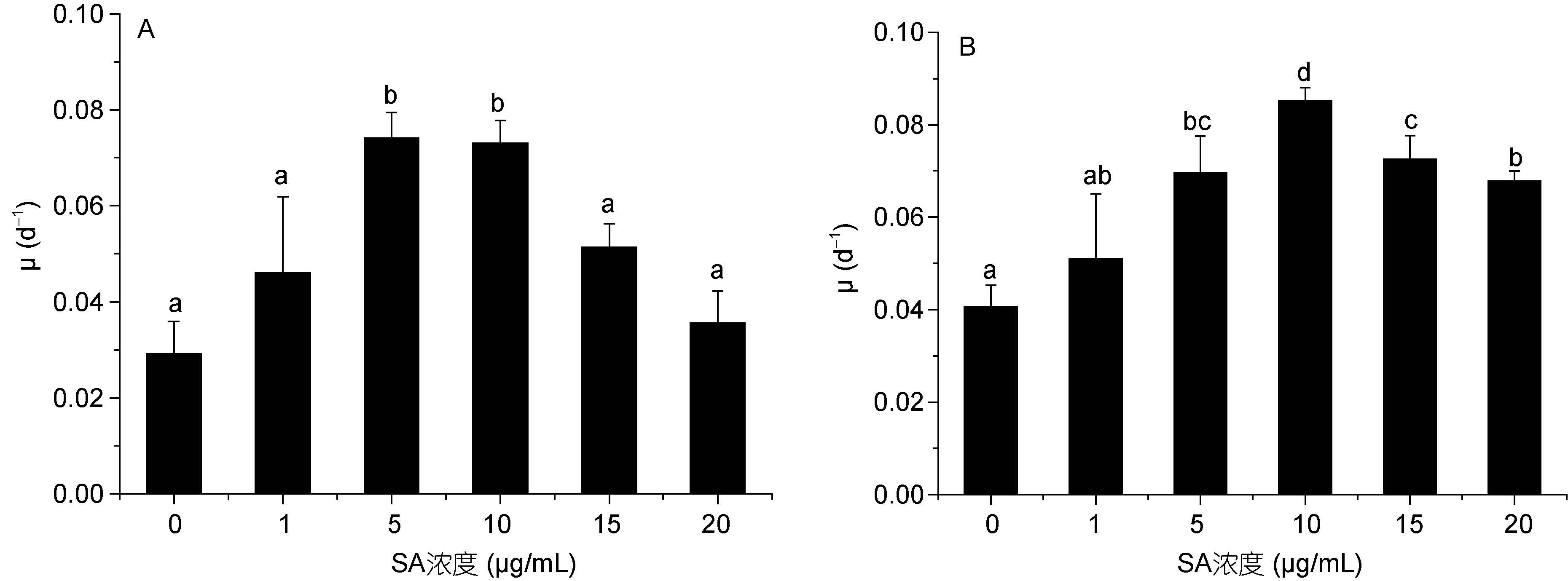
2.4 不同浓度水杨酸对蛋白核小球藻生长的影响不同浓度水杨酸处理对高温胁迫后蛋白核小球藻生长有明显的影响(图 7)。随着水杨酸浓度的升高,蛋白核小球藻比生长速率(μ)均有所提高,且在一定范围内随着水杨酸浓度的增加而增加。其中高温胁迫 24h 时(图 7A),5和10μg/mL 水杨酸添加后,藻的比生长速率均显著高于对照组(P<0.05),且在5 μg/mL 浓度下达到最高,为对照组的2.55 倍。在48h 时,5-20μg/mL 水杨酸添加后藻的比生长速率显著高于对照组(P<0.05),而在10μg/mL 浓度下最高,为对照组的2.07 倍。该结果说明一定浓度的水杨酸促进了高温培养蛋白核小球藻的生长,其中5和10 μg/mL 水杨酸促进作用最好。
|
| 图 7 不同浓度水杨酸对高温培养蛋白核小球藻生长的影响(A: 24h, B: 48h) Fig. 7 Effects of salicylic acid concentration on C. pyrenoidosa grown in high temperature (mean±SD) (A: 12h, B: 24h) |
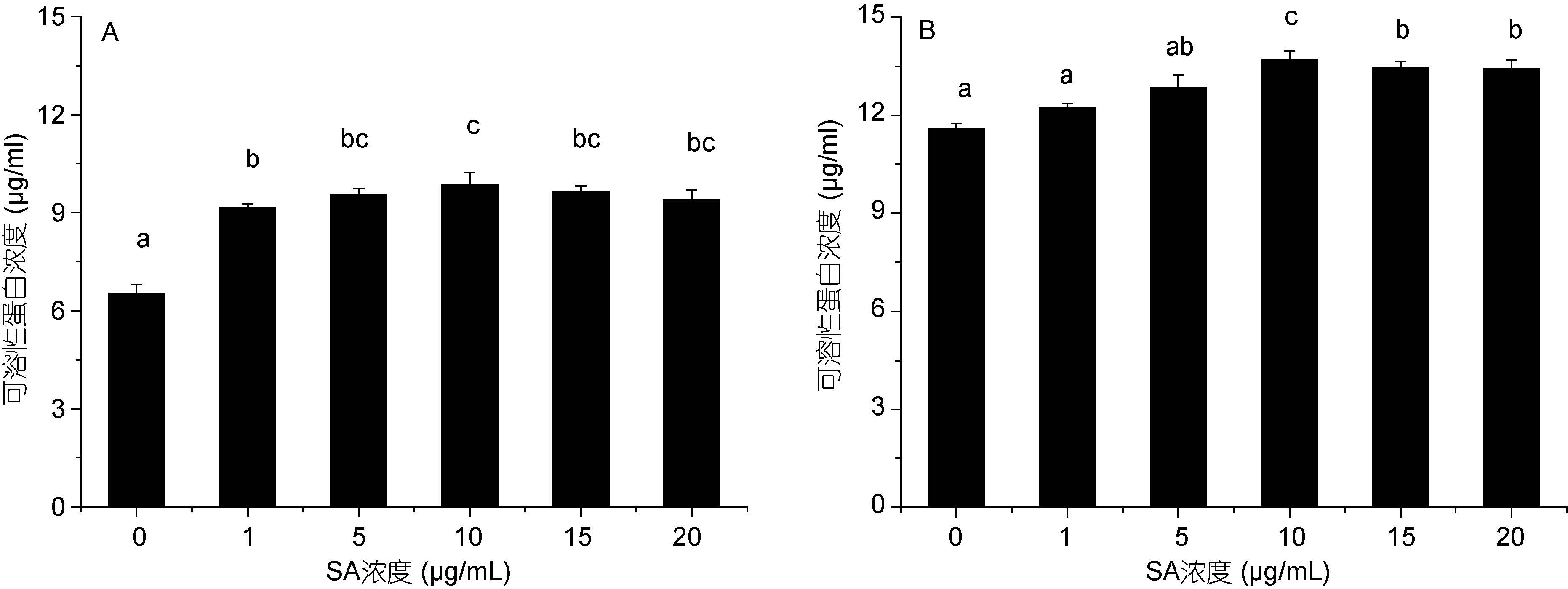
的影响不同浓度水杨酸处理对高温胁迫后蛋白核小球藻可溶性蛋白(图 8)和可溶性糖含量(图 9)有一定的影响。随着水杨酸浓度的增加,小球藻的可溶性蛋白和糖含量均有所增加,且在一定浓度范围内,蛋白和糖含量的增加量与水杨酸浓度呈正相关。其中高温胁迫 24h和48h 时,5 个水杨酸处理组藻的蛋白含量均高于对照组(P<0.05),且在10μg/mL 水杨酸组中最高,分别是对照组的1.51和1.18 倍。
|
| 图 8 不同浓度水杨酸对高温培养蛋白核小球藻可溶性蛋白含量的影响(A: 24h, B: 48h) Fig. 8 Effects of salicylic acid concentration on soluble protein content of C. pyrenoidosa under high temperature (mean±SD) (A: 12h, B: 24h) |
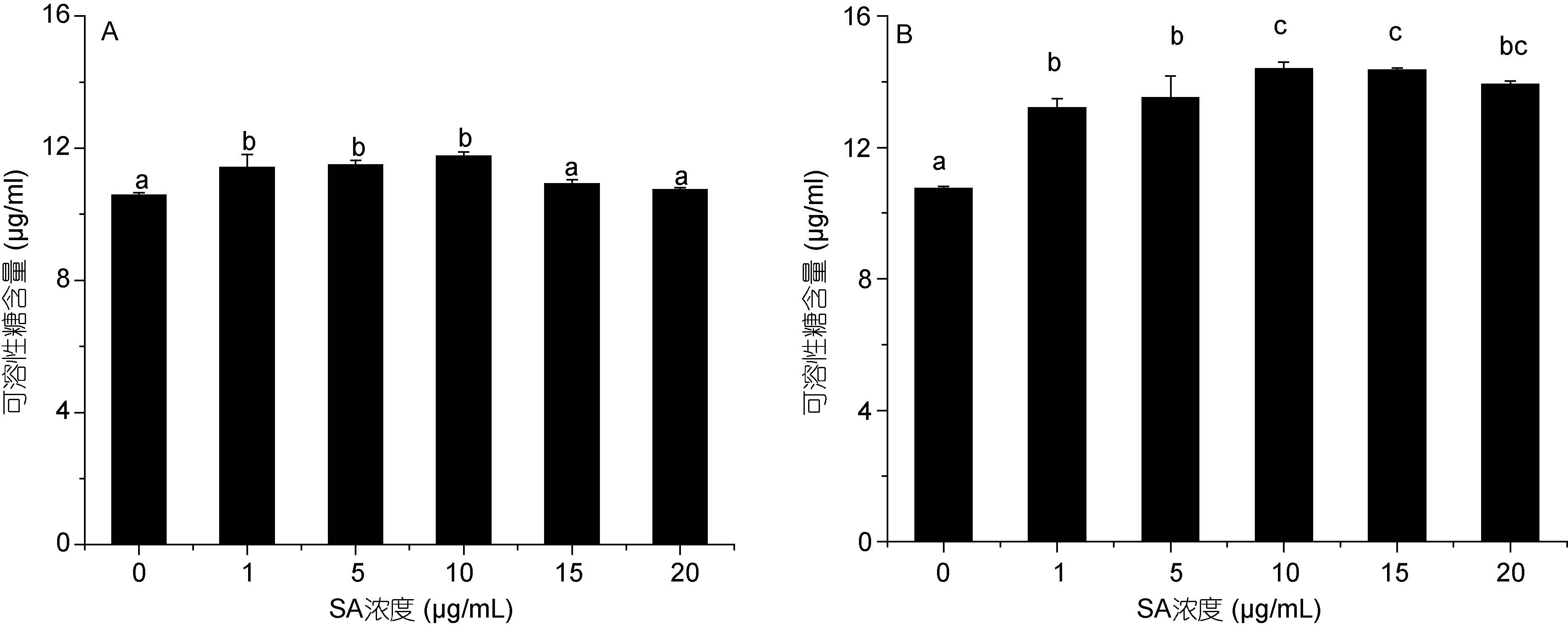
|
| 图 9 不同浓度水杨酸对高温培养蛋白核小球藻可溶性糖含量的影响(A: 24h, B: 48h) Fig. 9 Effects of salicylic acid concentration on soluble sugar content of C. pyrenoidosa under high temperature (mean±SD) (A: 12h, B: 24h) |
在高温胁迫24h 时,仅1、5、10μg/mL 水杨酸处理组藻的可溶性糖含量有所增加(P<0.05); 在48h 时,5 个水杨酸处理组藻的可溶性糖含量均高于对照组。在 10μg/mL 水杨酸组中,小球藻的糖含量最高,分别是对照组的1.10和1.34 倍。以上结果说明一定浓度的水杨酸促进了蛋白核小球藻可溶性蛋白和可溶性糖含量的增加。
3 讨论藻类在生长过程中往往受到多种逆境(高温、低温、高盐等)的影响,作为一种胁迫生物指示物,HSPs 已得到广泛关注(Dahlhoff,2004; Elyse Ireland et al,2004)。在逆境胁迫状态时,生物体大量表达HSPs 阻止变性蛋白的聚集,修复变性蛋白,并运送未成熟的蛋白质完成包装、代谢、修复,增加细胞抗逆性。有研究发现水杨酸参与植物的抗热反应,它可通过调节活性氧、抗氧化物质含量及活性来提高植物抗逆性(Qu et al,2013)。何亚丽等(2002)研究认为,SA 通过促进植物在高温胁迫下合成大量的热激蛋白,保持较高的超氧化物歧化酶和过氧化氢酶活性,提高抗氧化能力,降低高温对细胞产生的伤害,从而提高植物抗热性。Pan等(2006)发现豌豆受到高温胁迫时,SA 处理可诱导HSP70 的合成。而番茄在面临高温环境时,外施SA 可诱导HSP70 mRNA 转录和热休克因子基因表达增强,积累HSP70 蛋白(Snyman et al,2008)。 本研究发现水杨酸添加后,蛋白核小球藻HSP70 的表达量不同程度地得到提高,且在水杨酸处理浓度为10 μg/mL 时HSP70 表达量最高。该结果说明高温条件下水杨酸可以促进HSP70 的转录水平表达,从而大量合成HSP70 蛋白,修复受损细胞使生物体抵御高温环境,从而维持正常的生命活动状态。
高温条件下植物呼吸作用急剧升高,分解代谢增强,能量消耗增加。Gammulla等(2010)认为高温对水稻糖酵解途径具有负面的影响,且降低细胞能量的产生。磷酸甘油酸激酶(PGK)的编码基因在整个高温处理过程中表达持续上调(Zhang et al,2012)。而关于水杨酸处理后PGK 的变化研究较少。Suzuki等(2014)认为水杨酸促进了PGK 的表达,Fahraji等(2014)研究则表明水杨酸显著刺激PGK 参与种子的萌发。本研究中PGK 在水杨酸处理12h和24h 时表达增强,反映了高温胁迫过程中,水杨酸促进细胞呼吸,减轻高温逆境胁迫对机体产生的伤害。
高温条件下小球藻生长受到胁迫,新陈代谢活性降低,比生长速率较小,而水杨酸添加后比生长速率升高,高温对生长的抑制作用得到缓解,这与小麦中的研究结果一致。高温下淀粉水解作用增强,可溶性糖含量升高,而淀粉的水解为呼吸作用提供能源,增加细胞渗透压,对细胞产生保护作用。有研究认为,高温处理下可溶性糖含量下降(Chaitanya et al,2001)。而本研究中高温胁迫48h 比24h 可溶性蛋白含量有所提高,高温下体内可溶性蛋白含量的提高可增加细胞渗透势等,维持机体正常代谢,提高细胞抗逆性,抵御不良环境胁迫。本研究中经水杨酸处理后可溶性糖和蛋白含量均呈现不同程度的提高,说明水杨酸通过调节渗透调节物质,改变质膜透性,从而提高机体对逆境胁迫的抗性,与Czerpak等(2001)的研究结果相符。
综上所述,本文克隆了蛋白核小球藻HSP70和PGK 全长基因,并研究了水杨酸对高温胁迫下蛋白核小球藻中HSP70和PGK 的表达、及藻的生长、生化指标的影响。结果表明适宜浓度的水杨酸对蛋白核小球藻高温胁迫具有一定的缓解作用,且在一定程度上增强了HSP70和PGK的表达,其中5—10 μg/mL 时作用最显著,这为利用水杨酸缓解小球藻温度胁迫的研究提供了一定的资料。
| 李合生. 2000. 植物生理生化实验原理和技术. 北京: 高等教育出版社, 195-197 |
| 何亚丽, 刘友良, 陈权等. 2002. 水杨酸和热锻炼诱导的高羊茅幼苗的耐热性与抗氧化的关系. 植物生理与分子生物学学报, 28(2): 89-95 |
| 欧阳峥嵘, 温小斌, 耿亚红等. 2010. 光照强度、温度、pH、盐度对小球藻(Chlorella)光合作用的影响. 武汉植物学研究, 28(1): 49-55 |
| 周向红, 李信书, 王萍等. 2010. 条斑紫菜HSP90 基因的克隆与表达分析.水产学报, 34(12): 1844-1852 |
| 蒋际谋, 邓朝军, 林永祥等. 2014. 枇杷果皮响应高温强光胁迫的蛋白质组分析. 热带亚热带植物学报, 22(4):383-390 |
| Chaitanya K V, Sundar D, Reddy A R. 2001. Mulberry leafmetabolism under high temperature stress. BiologiaPlantarum, 44(3): 379-384 |
| Czerpak R, Bajguz A, Gromek M et al. 2001. Activity of salicylicacid on the growth and biochemism of Chlorella vulgarisBeijerinck. Acta Physiologiae Plantarum, 24(1): 45-52 |
| Dahlhoff E P. 2004. Biochemical indicators of stress andmetabolism: applications for marine ecological studies.Annual Review of Physiology, 66: 183-207 |
| Ding M, Jiang Y, Cao Y et al. 2014. Gene expression profileanalysis of Ligon lintless-1 (Li1) mutant reveals importantgenes and pathways in cotton leaf and fiber development.Gene, 535(2): 273-285 |
| Elyse Ireland H, Harding S J, Bonwick G A et al. 2004.Evaluation of heat shock protein 70 as a biomarker ofenvironmental stress in Fucus serratus and Lemna minor.Biomarkers, 9(2): 139-155 |
| Fahraji S S, Kheradmand M A, Raoofi M M et al. 2014. Effect ofsalicylic acid on germination, leaf area, shoot and rootgrowth in crop plants. International Research Journal ofApplied and Basic Sciences, 8(9): 1454-1458 |
| Fu W, Yao J, Wang X et al. 2009. Molecular cloning andexpression analysis of a cytosolic Hsp70 gene fromLaminaria japonica (Laminariaceae, Phaeophyta). MarineBiotechnology, 11(6): 738-747 |
| Gammulla C G, Pascovici D, Atwell B J et al. 2010. Differentialmetabolic response of cultured rice (Oryza sativa) cellsexposed to high- and low-temperature stress. Proteomics,10(16): 3001-3019 |
| Gu Y H, Zhang X, Lu N et al. 2012. Cloning and transcriptionanalysis of hsp70-1 and hsp70-2 of Gracilarialemaneiformis under heat shock. Aquaculture, 358-359:284-291 |
| Henkel S K, Hofmann G E. 2008. Thermal ecophysiology ofgametophytes cultured from invasive Undaria pinnatifida(Harvey) Suringar in coastal California harbors. Journal ofExperimental Marine Biology and Ecology, 367(2): 164-173 |
| Jayakannan M, Bose J, Babourina O et al. 2015. TheNPR1-dependent salicylic acid signalling pathway is pivotalfor enhanced salt and oxidative stress tolerance inArabidopsis. Journal of Experimental Botany, 66(7):1865-1875 |
| Koizumi S, Ohama N, Mizoi J et al. 2014. Functional analysis ofthe Hikeshi-like protein and its interaction with HSP70 inArabidopsis. Biochemical and Biophysical ResearchCommunications, 450(1): 396-400 |
| Lei T, Feng H, Sun X et al. 2010. The alternative pathway incucumber seedlings under low temperature stress wasenhanced by salicylic acid. Plant Growth Regulation, 60:35-42 |
| Li Z G, Xie L R, Li X J. 2015. Hydrogen sulfide acts as adownstream signal molecule in salicylic acid-induced heattolerance in maize (Zea mays L.) seedlings. Journal of PlantPhysiology, 177: 121-127 |
| Liu Z, Zhang L, Pu Y et al. 2014. Cloning and expression of acytosolic HSP90 gene in Chlorella vulgaris. BioMedResearch International. 2014: 487050, http://dx.doi.org/10.1155/2014/487050 |
| Pan Q, Zhan J, Liu H et al. 2006. Salicylic acid synthesized bybenzoic acid 2-hydroxylase participates in the developmentof thermotolerance in pea plants. Plant Science, 171(2):226-233 |
| Qu A L, Ding Y F, Jiang Q et al. 2013. Molecular mechanisms ofthe plant heat stress response. Biochemical and BiophysicalResearch Communications, 432(2): 203-207 |
| Shingaki-Wells R N, Huang S, Taylor N L et al. 2011.Differential molecular responses of rice and wheatcoleoptiles to anoxia reveal novel metabolic adaptations inamino acid metabolism for tissue tolerance. Plant Physiology,156(4): 1706-1724 |
| Snyman M, Cronjé M J. 2008. Modulation of heat shock factorsaccompanies salicylic acid-mediated potentiation of HSP70in tomato seedlings. Journal of Experimental Botany, 59(8):2125-2132 |
| Suzuki H, Takashima Y, Ishiguri F et al. 2014. Proteomicanalysis of responsive proteins induced in Japanese birchplantlet treated with salicylic acid. Proteomes, 2(3):323-340 |
| Tominaga H, Coury D A, Amano H et al. 2010. Isolation andcharacterization of a cDNA encoding a heat shock protein 70from a sterile mutant of Ulva pertusa (Ulvales, Chlorophyta).Ecotoxicology, 19(3): 577-588 |
| Timperio A M, Egidi M G, Zolla L. 2008. Proteomics applied onplant abiotic stresses: role of heat shock proteins (HSP).Journal of Proteomics, 71(4): 391-411 |
| Wang Y T, Huang H Y, Tsai M A et al. 2014. Phosphoglyceratekinase enhanced immunity of the whole cell ofStreptococcus agalactiae in tilapia, Oreochromis niloticus.Fish & Shellfish Immunology, 41(2): 250-259 |
| Wang Y X, Sun Y, Tian Y C et al. 2009. Cloning and expressingof putative enolase gene from cotton (Gossypium hirsutumL.). Cotton Science, 21(4): 275-278 |
| Zhang X, Li J, Liu A et al. 2012. Expression profile in ricepanicle: insights into heat response mechanism atreproductive stage. PLoS One, 7(11): e49652 |
 2015, Vol. 46
2015, Vol. 46


