
中国海洋湖沼学会主办。
文章信息
- 杨洋, 孙晓霞, 郑珊, 赵永芳. 2016.
- YANG Yang, SUN Xiao-Xia, ZHENG Shan, ZHAO Yong-Fang. 2016.
- 南黄海夏初网采浮游植物分布与长期变化
- DISTRIBUTION AND LONG-TERM VARIATION OF NET PHYTOPLANKTON IN SOUTH YELLOW SEA IN EARLY SUMMER
- 海洋与湖沼, 47(4): 755-763
- Oceanologia et Limnologia Sinica, 47(4): 755-763.
- http://dx.doi.org/10.11693/hyhz20160200028
-
文章历史
- 收稿日期:2016-02-04
- 改回日期:2016-03-18
2. 中国科学院大学 北京 100049;
3. 青岛海洋科学与技术国家实验室 海洋生态与环境科学功能实验室 青岛 266071
2. University of Chinese Academy of Sciences, Beijing 100049, China;
3. Laboratory for Marine Ecology and Environmental Science, Qingdao National Laboratory for Marine Science and Technology, Qingdao 266071, China
浮游植物是海洋生态系统中最主要的初级生产者,其生物量及群落结构的变动将对海洋生态系统的结构和功能产生影响。浮游植物的分布对生态环境具有指示作用,海洋环境的变化也影响着浮游植物群落的稳定性(Gao et al,2005; Litchman et al,2008),因而对浮游植物生物量和群落结构的研究一直是海洋生态调查研究的重点。
黄海是太平洋的边缘海,具有显著季节性变化的冷水团(赫崇本等,1959; Bai et al,2004)。黄海受到人类活动的显著影响,在全球碳循环中起着重要作用(Liu,2013)。对南黄海浮游植物开展的大规模调查最早为1958年的全国海洋综合调查(朱树屏等,1959),进行了浮游植物分类及分布的研究,为该海域浮游植物的长期变化研究打下了宝贵的基础。之后开展的许多海洋调查进一步加深了人们对黄海浮游植物生态状况的了解(黄文祥等,1984; 俞建銮等,1993; 王俊,2001)。
针对浮游植物网采样品,传统的分析方法是在显微镜下进行种类鉴定和计数。这一方面为浮游植物的研究积累了珍贵的基础资料,另一方面也存在不足,即仅以细胞丰度来表征浮游植物的生物量会高估小个体藻细胞对群落的贡献(Smayda,1978)。因此,许多学者建立了浮游植物细胞体积、丰度与细胞含碳量的经验转换公式(Mullin et al,1966; Eppley et al,1970; Verity et al,1992; Montagnes et al,1994; Menden-Deuer et al,2000; Yang et al,2016),可根据体积参数和丰度数据最终获得以碳含量为指标的浮游植物现存量。在显微镜下对浮游植物样品中的细胞进行分类并逐一测量不仅耗时、耗力,也对分析人员有较高的技术要求,因此转换生物量在室内试验及单一种的分析上应用较广(Chiang et al,2002; Fahnenstiel et al,2010; Jakobsen et al,2015),而在大范围的海洋生态调查中应用较少。利用流式影像术(Flow Cytometry and Microscopy,FlowCAM)可以实现对浮游植物细胞的快速计数和体积参数测量(Álvarez et al,2011; Spaulding et al,2012)。在国内,基于体积转换生物量法,孙军等(2000)研究了胶州湾海域浮游植物各类群生物量的变动,宋书群(2010)研究了黄、东海浮游植物功能群的组成和分布。而针对南黄海浮游植物生物量和群落结构长时间变化的研究相对匮乏,且以碳含量为表征的浮游植物现存量的长期变化情况尚未见报道。
本文根据2012年与2013年6月份两个航次的调查,与2002—2003年以及1959年全国海洋综合调查时期的浮游植物历史调查数据进行整合处理,分析了夏初南黄海网采浮游植物丰度、碳含量分布以及硅甲藻相对比例和种属组成的变化。同时结合理化因子,讨论影响夏初南黄海浮游植物群落结构的因素,以期为全球变化影响下的我国近海生态系统演变研究提供依据。
1 材料与方法 1.1 研究海域与站位设计于2012年和2013年6月,分别搭载“北斗”号调查船展开两个航次的调查,同时与来自1959年(全国海洋综合调查,由中国科学院海洋研究所档案室提供)、2002年和2003年(中国科学院海洋研究所973项目课题G1999043706,由973计划资源环境领域项目数据汇交服务网www.973geodata.cn提供)的相同月份航次数据做比较分析。采样区域位于33°—37°N,120°—124°E之间的南黄海海域。本研究选取了1959、2002、2003、2012和2013年5个航次中经纬度一致的9个站位进行分析,站位标号为s1—s9,见图 1。所选站位在黄海冷水团的内外均有分布,受不同水文环境的影响。
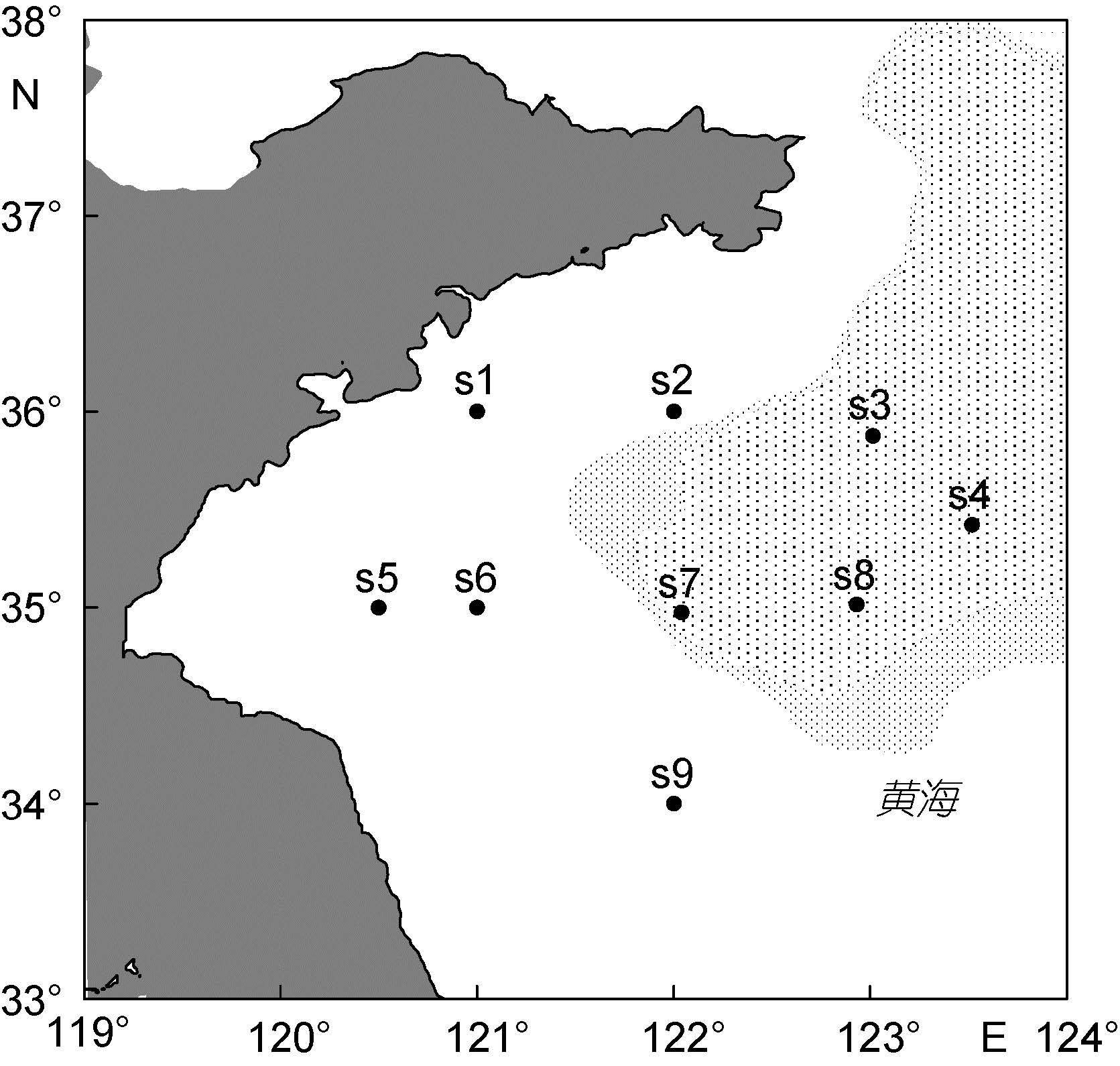 |
| 图 1 南黄海区域9个站位的分布图(阴影部分指示了冷水团的大致范围) Fig. 1 Location of the nine sampling stations in the South Yellow Sea area(the grey shaded area indicates the Yellow Sea Cold Water Mass) |
浮游植物样品的采集和保存按照海洋调查规范(GB/T12763.6-2007)进行。在各个采样站位,用小型浮游生物采集网(孔径0.076mm,网口面积0.1m2,网长2.8m)由底层至表层垂直拖网,采集后的样品立即用5%中性福尔马林溶液固定。在采集浮游植物的同时,由船载SBE911 CTD(Sea-Bird Electronics Inc.,美国)测得各站位的深度、温度、盐度数据。用Niskin(KC-Denmark,丹麦)10L采水器按照海洋调查规范中规定的标准水层进行采水,用于营养盐的测定。营养盐的测定方法遵照海洋调查规范(GB/T12763.4-2007),硅酸盐、磷酸盐分别采用硅钼蓝法和抗坏血酸还原磷钼蓝法测定,铵盐、硝酸盐和亚硝酸盐分别采用次溴酸钠氧化法、锌镉还原法和重氮-偶氮法测定。
1.3 浮游植物计数与含碳量的计算1959、2002和2003年的浮游植物丰度数据来自于显微镜镜检记录,2012和2013年浮游植物丰度利用FlowCAM(Fluid Imaging Technologies Inc.,美国)进行分析。为验证FlowCAM计数结果与显微镜计数结果的可比性,利用校准后的FlowCAM在自动模式下对网采样品藻细胞进行计数,与以BX-51显微镜(Olympus,日本)计数的结果做差异性检验,结果表明两者计数结果差异不显著,即FlowCAM计数结果与显微镜计数结果具有可比性(Yang et al,2016)。各站位硅藻、甲藻的碳含量根据Yang等(2016)的公式进行换算,换算公式为
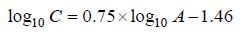 (Ⅰ)
(Ⅰ)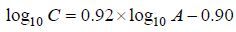 (Ⅱ)
(Ⅱ)其中,公式(Ⅰ)适用于硅藻碳含量的转换,公式(Ⅱ)适用于甲藻碳含量的转换。其中,C为海水中藻细胞碳含量的转换值,单位为μgC/m3,A为海水中藻细胞的丰度值,单位为cell/m3。
2012年和2013年的浮游植物细胞经FlowCAM分析,可以获得单个细胞的尺寸信息,因此每个藻属的碳含量可以根据Eppley等(1970)提出的体积转换法获得。需要说明的是,夜光藻属(Noctiluca)细胞个体较大且具有大液泡,鉴于其特殊性不适于利用上述公式进行碳含量的转换,故本文中的碳含量不包括夜光藻的碳含量。
1.4 生物数据和环境因子数据的排序分析数据的分析利用SAS 9.1.3(SAS Institute Inc.,美国)统计分析软件进行。为满足方差分析及相关分析的前提条件,对数据进行正态性转换。其中,丰度与碳含量数据均经过对数(log10)转换,百分数经过平方根反正弦转换。应用Canoco5(Microcomputer Power,美国)软件分析浮游植物与环境因子的关系,包括除趋势对应分析(detrended correspondence analysis,DCA)及冗余分析(redundancy analysis,RDA)等。参与排序的种属经过筛选,本文中用于排序的站位含有的种属数目不少于2个,用于排序的种属在各站位出现的频率大于10%,且满足在至少一个站位的相对碳含量大于2%。物种矩阵进行log10(x+1)的转换处理。
2 结果与讨论 2.1 温盐特征调查海域处于不同的水文环境,将其按照离岸远近及受冷水团影响的程度,分为南黄海近岸海域(W区,s1、s5、s6、s9站位)、南黄海中部海域(M区,s2、s7站位)和南黄海东部外海海域(E区,s3、s4、s8站位)三个区域。各区域海水的温度、盐度如图 2所示,W区域受近岸淡水输入的影响,盐度较低,受海水冷水团的影响较弱,仅在s1站位有个别水团低于10°C; E区海水盐度值最高,是冷水团的控制区域; M区位于前两者之间,亦受到冷水团的影响。
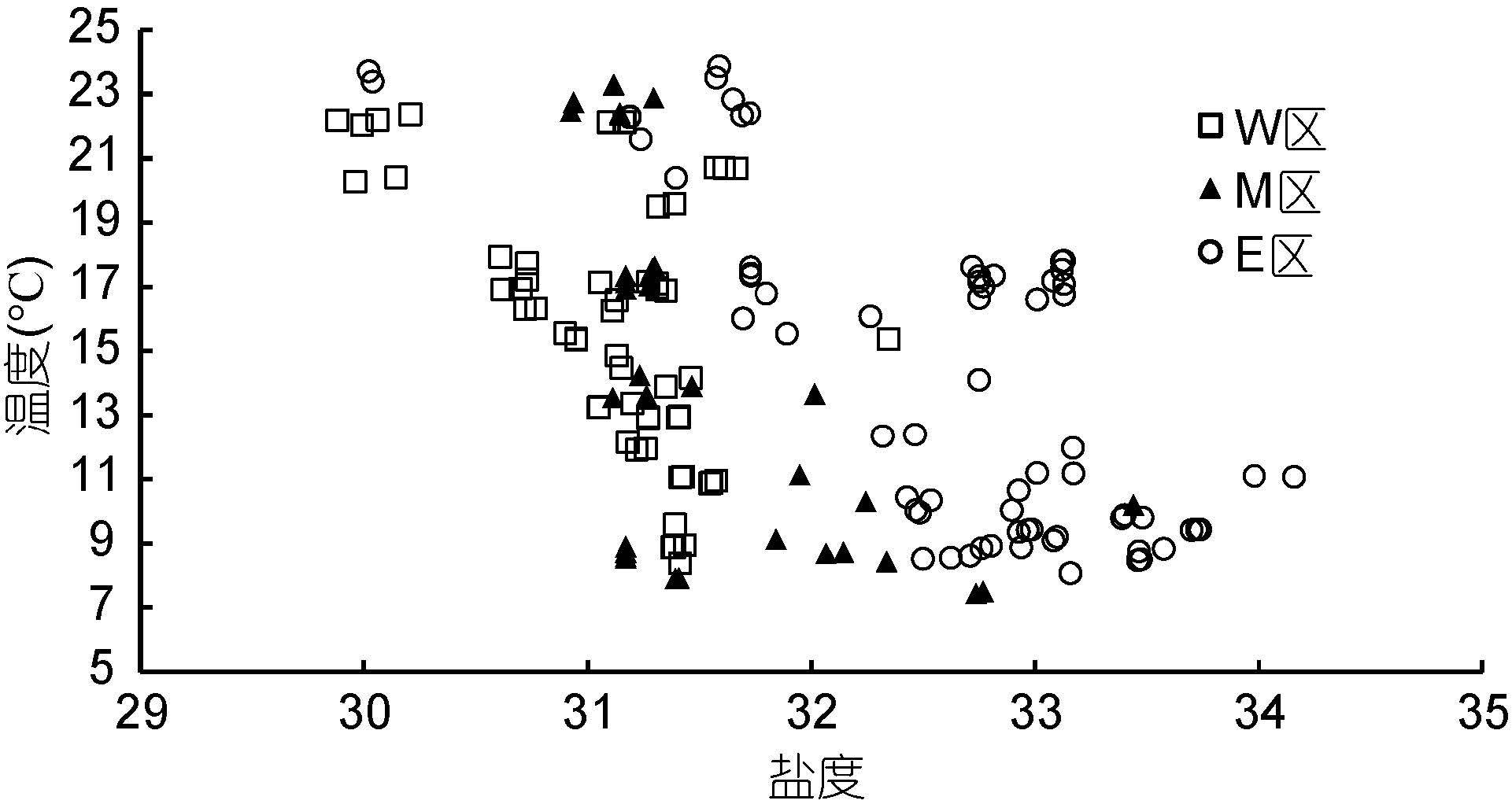 |
| 图 2 2012、2013年南黄海三个区域(W区、M区和E区)内站位的海水温度-盐度图(W区: 南黄海近岸海域; M区: 南黄海中部海域; E区: 南黄海东部外海海域) Fig. 2 T-S diagram of stations in three regions(W,M and E)of the South Yellow Sea in 2012 and 2013(W: coastal area of South Yellow Sea; M: middle area of South Yellow Sea; E: the east open area of South Yellow Sea) |
2012和2013年,调查站位浮游植物丰度变化范围为(0.36—142.51)×104cell/m3,平均值分别为(6.16± 5.05)×104和(18.73±46.68)×104cell/m3。这一时期与1959年及2002—2003年两个时期的丰度数据的统计分析结果表明,三个时期浮游植物丰度差异显著(F=3.37,P=0.04)。两两比较采用q检验,结果表明,2002—2003年与2012—2013年差异不明显; 1959年与2012—2013年的差异有统计学意义,该年调查站位浮游植物丰度变化范围为(0.01—8.32)×104cell/m3,平均值为(2.02±3.31)×104cell/m3。浮游植物碳含量方面,2012和2013年,碳含量的变化范围为47.25—3324.32μgC/m3,平均值分别为(845.70±988.84)和(1110.71±2107.82)μgC/m3,在三个时期中为最高; 1959年的浮游植物总碳含量变化范围为(0.82—188.88)μgC/m3,平均值为(62.99±71.33)μgC/m3,在三个时期中为最低。统计分析结果表明,三个时期浮游植物碳含量差异显著(F=9.68,P=0.003)。由误差分析可以看出,同一年份不同站位之间浮游植物群落特征的变动较大,尤其是近岸站位与外海站位的生物量相差悬殊,所以接下来进行分区域讨论。
浮游植物丰度分区域结果如图 3所示,W区的浮游植物丰度值远远高于其它区域,这表明近岸区域是南黄海浮游植物生物量的主要贡献区。W区同样表现出年际间波动较大的特点。1959年全国海洋调查时期获得的浮游植物丰度最低,为(2.36±3.32)× 104cell/m3,2003年的丰度最高,为(61.38±115.83)× 104cell/m3,约为前者的26倍。M区和E区的浮游植物丰度在各年份均维持在较低水平。M区丰度的最大值出现在1959年,为(4.29±5.70)×104cell/m3,约为其它调查年份丰度的2倍。E区在2012年的丰度值最大,为(9.31±7.60)×104cell/m3,其它调查年份均处于1×104cell/m3以下。可见,南黄海海域各时期浮游植物的丰度变化主要体现在近岸海域。中国近海普遍存在浮游植物生物量升高且年际间波动大的特点,胶州湾海域(吴玉霖等,2005; 孙晓霞等,2011)、长江口及其邻近海域(Zhou et al,2008; 章飞燕,2009)以及台湾海峡所属海域(林更铭等,2011)均有相关报道,被认为是近海海域浮游植物对全球气温升高的一种响应。
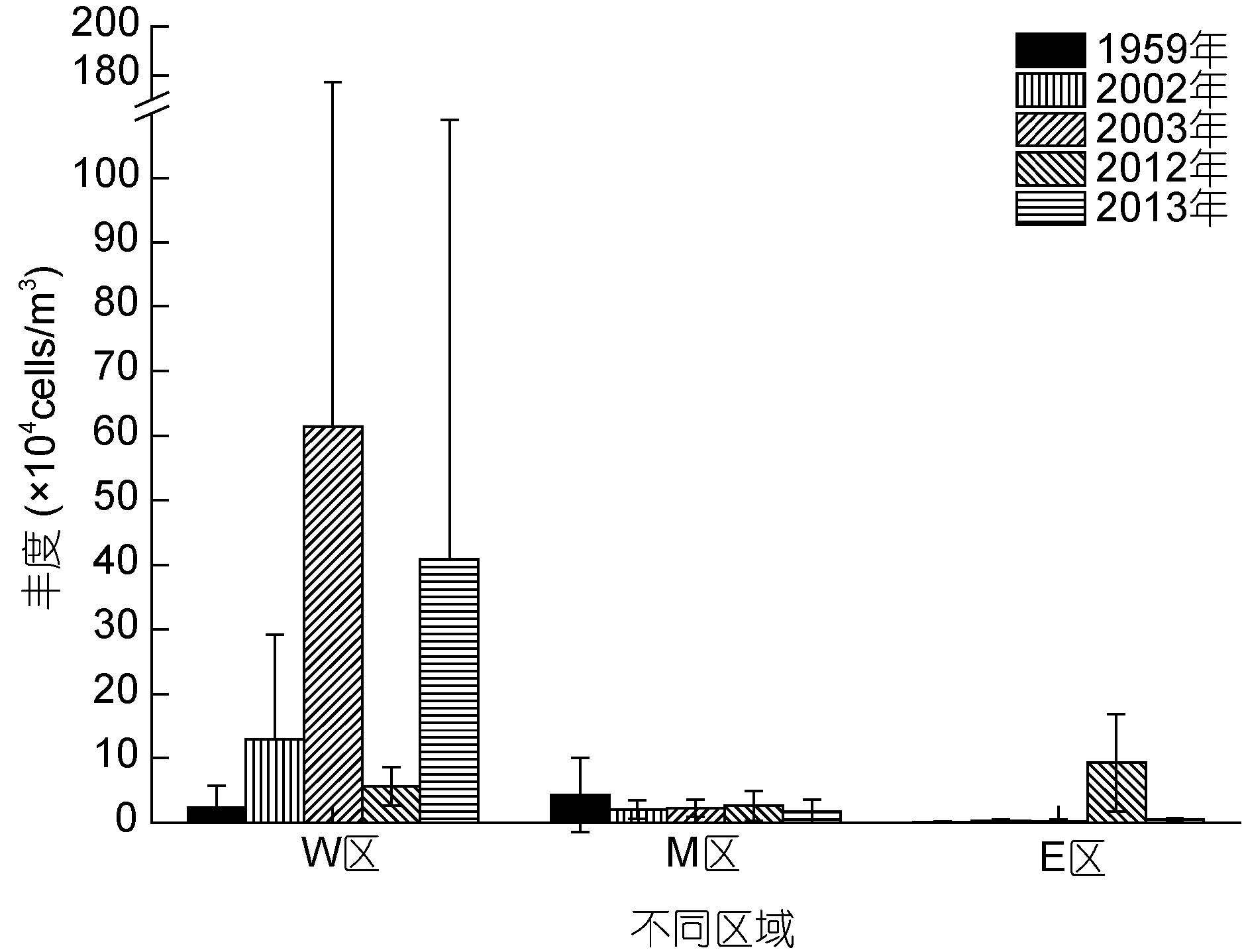 |
| 图 3 南黄海三个区域不同年份浮游植物的丰度变化 Fig. 3 Interannual changes in phytoplankton abundance of three different regions in South Yellow Sea |
浮游植物碳含量在各区域的分布与丰度分布大致相似(图 4)。W区的浮游植物碳含量对南黄海海域碳含量有主要贡献作用。1959年全国海洋调查时期的碳含量值最低,为(85.91±59.55)μgC/m3,2013年的碳含量值最大,为(2303.68±2901.77)μgC/m3,约为前者的27倍。M区和E区的碳含量值均维持在较低水平。M区碳含量的最大值出现在2012年,为(292.34± 119.34)μgC/m3,其它年份大致相当。E区在2012年和2013年分别出现碳含量的最大值和次大值,分别为(372.90±201.42)μgC/m3和(185.90±120.26)μgC/m3,而以往年份该海域浮游植物的碳含量值极低,在30μgC/m3以下。碳含量较为明显地反应出E区浮游植物生物量的增加。另外,W区在2003年的丰度值最高,而该年的碳含量值较低; 2012年的丰度值较低,而该年的碳含量值较高,这表明衡量浮游植物生物量的变化要综合考虑丰度和类群组成的变动。
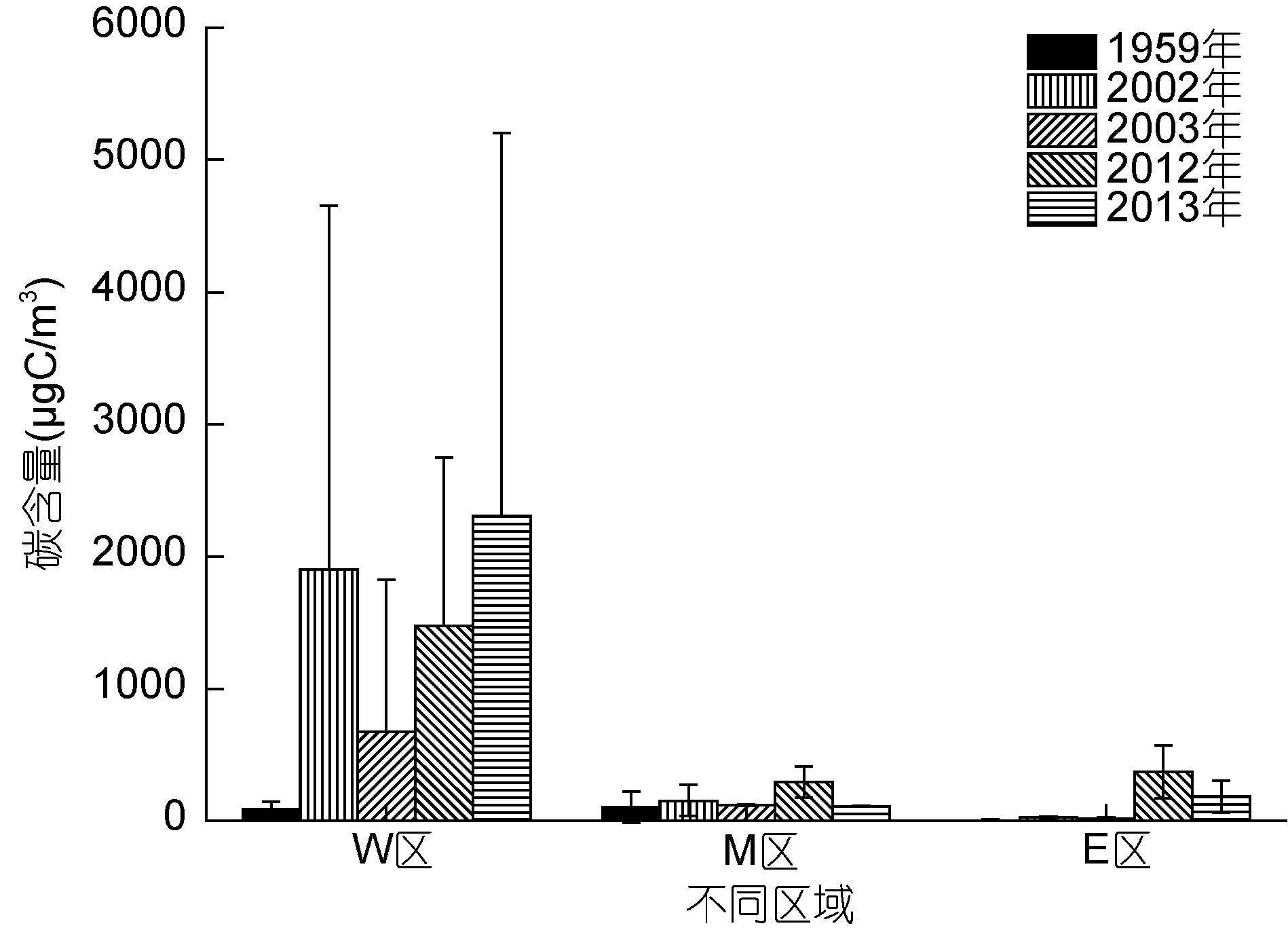 |
| 图 4 南黄海三个区域不同年份浮游植物碳含量的变化 Fig. 4 Interannual changes in phytoplankton carbon biomass of three different regions in South Yellow Sea |
从硅甲藻比例的分布及变化来看(图 5),1959、2002和2003年硅藻在南黄海海域占优势,M区站位的浮游植物中硅藻均占到90%以上,甲藻仅在W区和E区有少量出现。相比之下,近年来甲藻所占优势明显增长。2012和2013年,海域中出现了甲藻占优势的站位,甲藻的分布区域扩大。同样,在常年以硅藻占绝对优势的胶州湾海域,自2003年之后,甲藻在夏季经常成为一些站位的优势种类,其数目和分布范围均呈增长趋势(孙晓霞等,2011)。
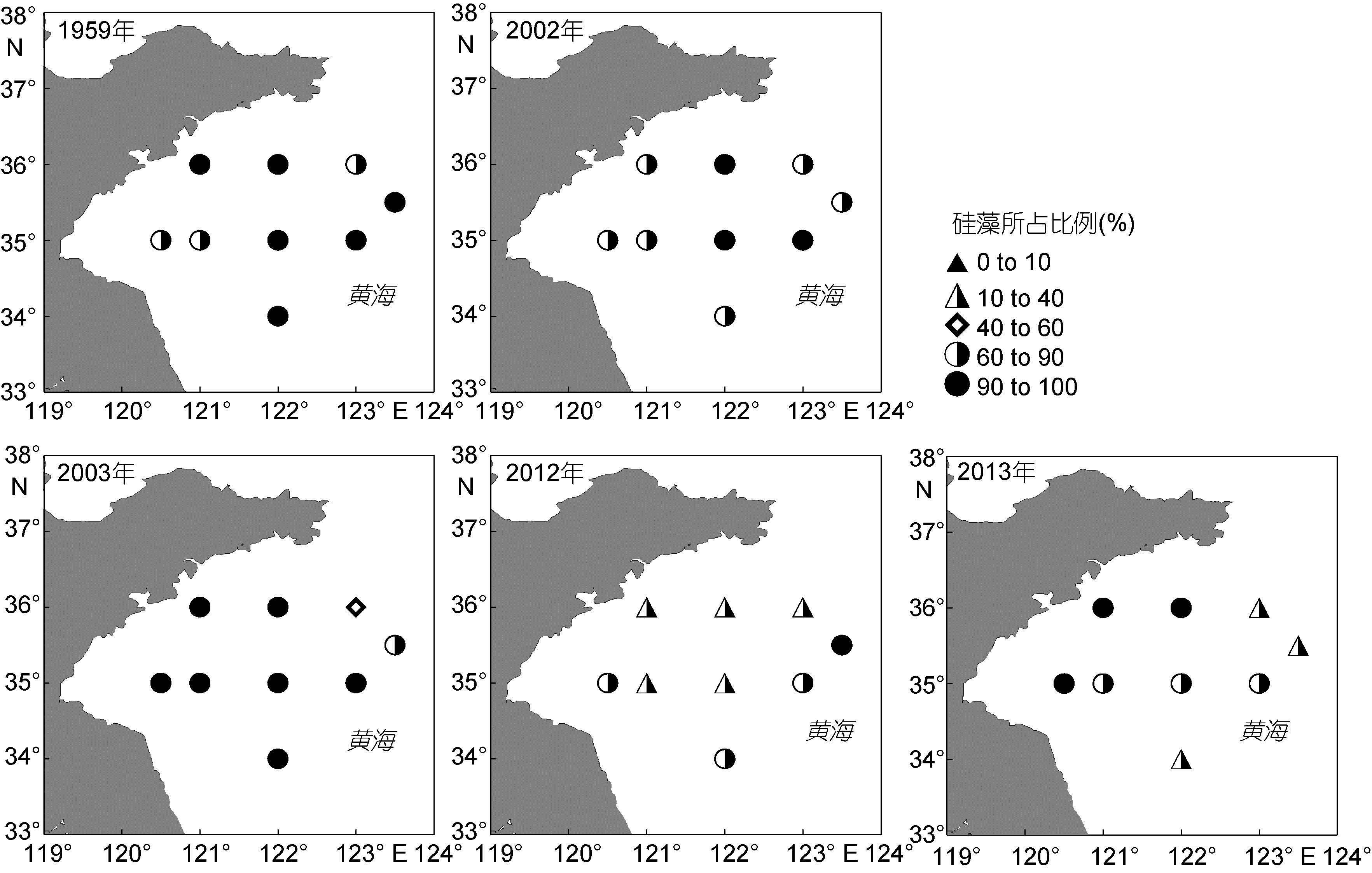 |
| 图 5 调查年份各站位的硅藻所占比例 Fig. 5 The proportion of diatom abundance in each station of each year |
统计分析结果表明,三个时期的硅藻丰度比例差异显著(F=6.97,P=0.0041),q检验下的两两比较显示1959年与2002—2003年结果的差异不存在统计学意义,20122013年的结果与前两个时期差异显著。三个时期分区域的硅藻丰度所占比例如图 6所示。同一时期各区域硅藻的相对丰度大体相当。相较于其它时期,W区、M区和E区三个区域的硅藻所占比例均在2012—2013年最低,相应地,该时期甲藻在群落中所占的比例为最高。1959年各区域硅藻所占的比例均在93%以上,占绝对优势地位; 2012—2013年各区域硅藻的比例为50%—60%,甲藻在丰度上的优势地位已与硅藻相当。可见,近年南黄海海域夏初浮游植物中的硅藻比例较以往时期有下降趋势。
 |
| 图 6 硅藻丰度所占比例在三个时期的变化 Fig. 6 The proportion of diatom abundance in three different regions in the three periods |
统计分析结果表明,三个时期的硅藻碳含量比例差异显著(F=15.89,P<0.0001),q检验下的两两比较显示2002—2003年与2012—2013年结果的差异不存在统计学意义,1959年的结果与后两个时期差异显著。三个时期各区域硅藻碳含量所占比例如图 7所示。1959年硅藻碳含量比例最高,硅藻有绝对优势地位,各区域平均比例在70%—85%之间; 2012—2013年,南黄海各区域硅藻的优势地位已明显被甲藻取代,硅藻碳含量比例仅为18%—28%。其中,2012年W区域角藻属(Ceratium)大量暴发,s1站位角藻丰度达到6.16×104cell/m3,造成该时期硅藻碳含量所占比例处于较低水平。碳含量表征的浮游植物变化趋势和丰度表征的变化趋势在总体上是一致的,即硅藻所占优势下降,甲藻比例升高。由于类群的差异,不同物种对浮游植物生物量的贡献要综合考虑群落结构、自身个体大小和数量等因素(孙军等,2000)。本研究中,相对于丰度,以碳含量表征的硅藻生物量的下降幅度明显较大。一方面,硅藻细胞的液泡较大(Strathmann,1967),其碳含量密度被认为低于其它浮游植物类群; 另一方面,甲藻在数目上相对增多(图 6),共同导致硅藻在碳含量上的优势地位明显下降。
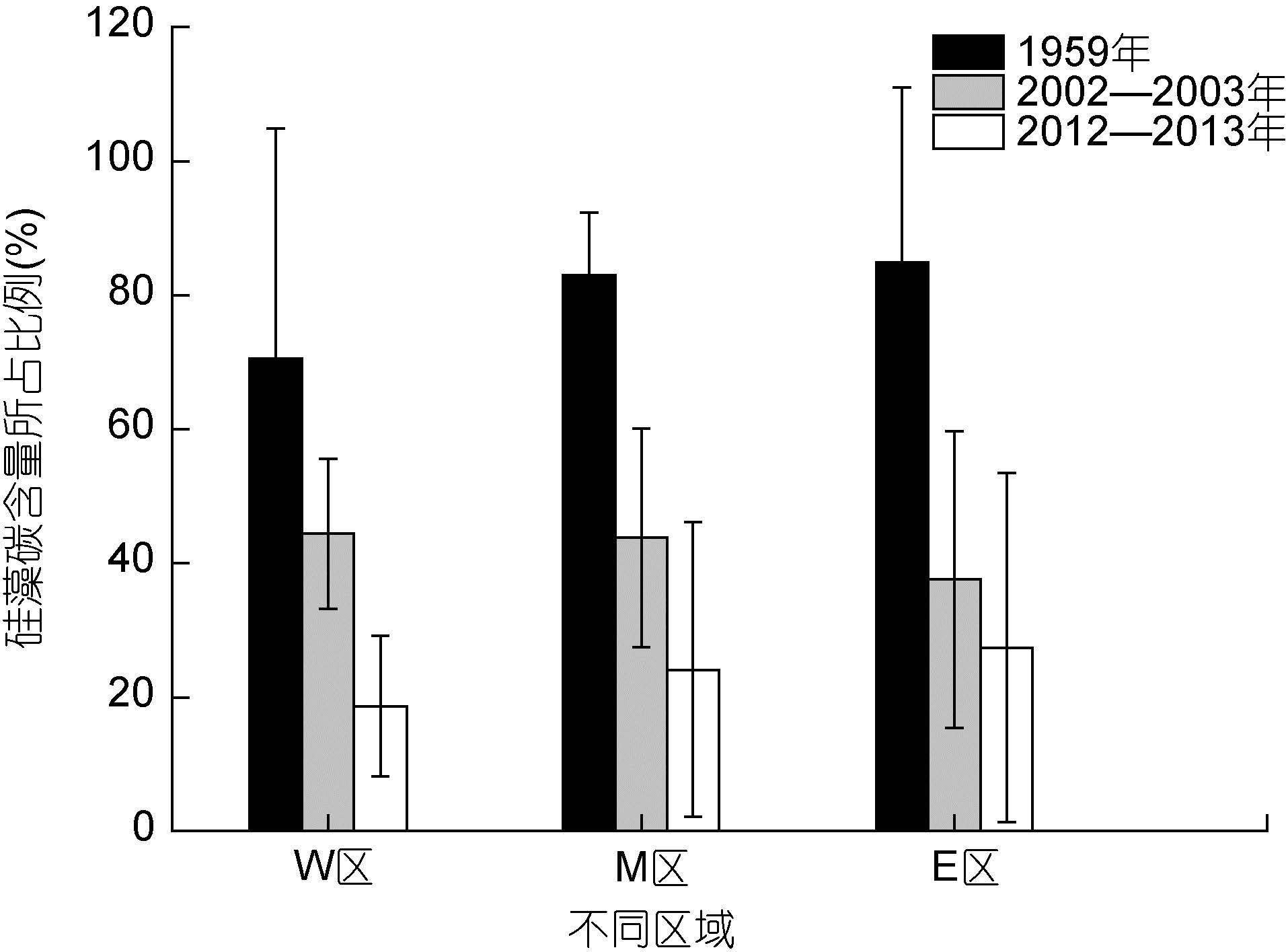 |
| 图 7 硅藻碳含量所占比例在三个时期的变化 Fig. 7 The proportion of carbon biomass in diatom from three different regions in the three periods |
表 1显示了1959年、2012年及2013年6月份南黄海网采浮游植物的优势种属及其优势度。优势度Y的计算公式(孙儒泳,1992)为:
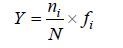
| 优势种属 | 1959年 | 2012年 | 2013年 | |||
| 平均丰度(×104cell/m3) | 优势度Y | 平均丰度(×104cell/m3) | 优势度Y | 平均丰度(×104cell/m3) | 优势度Y | |
| 硅藻 | ||||||
| 圆筛藻属Coscinodiscus | 0.158±0.244 | 0.070 | 0.481±0.568 | 0.078 | 0.887±1.495 | 0.042 |
| 根管藻属Rhizosolenia | 0.258±0.518 | 0.071 | — | — | 10.613±29.963 | 0.441 |
| 半管藻属Hemiaulus | 0.262±0.520 | 0.043 | — | — | — | — |
| 角毛藻属Chaetoceros | — | — | 2.947±5.367 | 0.213 | 1.859±5.156 | 0.033 |
| 帕拉藻属Paralia | 1.046±2.051 | 0.172 | — | — | — | — |
| 菱形藻属Nitzschia | 0.188±0.492 | 0.041 | — | — | — | — |
| 伪菱形藻属Pseudonitzschia | — | — | — | — | 3.386±9.874 | 0.060 |
| 甲藻 | ||||||
| 角藻属Ceratium | — | — | 1.287±1.912 | 0.186 | 1.572±4.223 | 0.075 |
| 夜光藻属Noctiluca | — | — | 0.935±1.080 | 0.135 | — | — |
式中,ni为第i属的总丰度,N为浮游植物总丰度,fi为第i属出现的频率。
在种属组成上,1959年调查海域的优势种属均为硅藻类; 2012—2013年出现了在数量上占优势地位的甲藻类。其中圆筛藻属(Coscinodiscus)和根管藻属(Rhizosolenia)在两个时期均居优势地位; 在1959年占优势地位的半管藻属(Hemiaulus)、帕拉藻属(Paralia)和菱形藻属(Nitzschia)在2012—2013年不再占优势; 硅藻中的角毛藻属(Chaetoceros)和伪菱形藻属(Pseudonitzschia),以及甲藻中的角藻属和夜光藻属相对于1959年成为2012—2013年新的优势种属。
角毛藻呈链状,伪菱形藻呈阶梯状群体,它们占优势地位时对丰度具有较大贡献,尤其是角毛藻属,2012年和2013年各站位的角毛藻平均丰度分别达到2.947×104和1.859×104cell/m3,但由于其单个个体的体积较小,对碳含量的贡献相对较小,这两年各站位角毛藻属的平均转换碳含量分别为93.95和24.77μgC/m3。同时甲藻种属数目增加,调查区域角藻属在2012年和2013年平均丰度分别为1.287×104和1.572×104cell/m3,平均转换碳含量分别为518.94和1153.32μgC/m3,可见其在碳含量方面的优势高于丰度相当的小型硅藻。该时期角藻属的组成主要为三角角藻(Ceratium tripos)和梭角藻(C. fusus)。以往研究显示,2009年6月长江口及其邻近海域的三角角藻和夜光藻(N. scintillans)相对于往年也成为了新的网采浮游植物群落优势种(Jiang et al,2014),可见甲藻的优势地位在中国近海明显提升。
2.5 浮游植物群落特征与环境因子的关系浮游植物在丰度与类群结构上的变动受到营养盐的影响,对此在中国近海已有相关研究。20世纪末,渤海海域出现硅、磷限制,硅藻比例明显下降(Ning et al,2010)。长江口及邻近海域的研究表明,自1984至2002年,春季末浮游植物生物量增多,硅藻比例由85%下降到60%,其潜在原因是较高的氮磷比及磷限制的出现(Zhou et al,2008)。珠江入海口及邻近海域也存在磷限制和硅的缺乏,甲藻等不依赖硅酸盐的藻类在群落凸显出优势地位(Yin et al,2000)。20世纪末黄海海域氮升高引起的磷限制和硅限制是该海域甲藻比例升高的可能原因(Lin et al,2005)。本文根据2012年6月份南黄海海域的浮游植物数据和温度、盐度及营养盐浓度做相关性分析,其结果如表 2所示。在调查区域,浮游植物生物量与海水平均温度呈显著的正相关关系,与海水平均盐度呈显著的负相关关系。夏初南黄海的硅藻类群和甲藻类群均受到温度和盐度的影响。营养盐方面,硅藻丰度与硅酸盐浓度呈显著的正相关关系,表明硅酸盐是硅藻的限制因素。浮游植物与磷酸盐浓度的相关关系不显著。甲藻与亚硝酸盐浓度呈显著的正相关关系,硅藻与铵盐浓度和硝酸盐浓度呈显著的正相关关系。与以往研究不同,磷限制在南黄海夏初并不明显。同时,浮游植物生物量与氮磷比的相关性不显著(P值均大于0.05)。以往研究表明,人类活动通过影响陆源输入及大气沉降等方式影响近海生态系统,溶解性无机氮和磷酸盐含量的相对升高促进了生物硅的输出,进而推进硅限制的出现,使得硅藻在近海生态系统中的地位下降(Nelson et al,1996; Humborg et al,2000; Tréguer et al,2013),进一步解释了本研究中观察到的现象。
| 海水平均温度 | 海水平均盐度 | 硅酸盐 | 磷酸盐 | 亚硝酸盐 | 铵盐 | 硝酸盐 | |
| 总丰度 | 0.875** | -0.470* | 0.630** | 0.084 | 0.107 | 0.936** | 0.932** |
| 硅藻丰度 | 0.831** | -0.445* | 0.614** | 0.097 | 0.077 | 0.724** | 0.682** |
| 甲藻丰度 | 0.621** | -0.609** | 0.222 | -0.301 | 0.670** | -0.370 | 0.174 |
| 总碳含量 | 0.737** | -0.536* | 0.360 | -0.132 | -0.357 | -0.232 | -0.108 |
| 硅藻碳含量 | 0.803** | -0.616** | 0.475 | -0.093 | -0.066 | 0.265 | 0.214 |
| 甲藻碳含量 | 0.569** | -0.540* | 0.163 | -0.272 | 0.648** | -0.341 | 0.200 |
| 注: *表示P<0.05,差异显著; **表示P<0.01,差异极显著 | |||||||
对2012年及2013年6月份的物种数据和环境数据进行DCA分析,其中物种数据采用浮游植物碳含量指标。排序轴梯度长度最大值小于3,因而采用基于线性模型的RDA分析(Lepš et al,2003)。排序结果(图 8)表明,受温度影响最明显的藻属为角藻属、双尾藻属(Ditylum)和圆筛藻属。营养盐方面,硅酸盐对角毛藻属的影响较为明显,硅藻中的盒形藻属(Biddulphia)、双尾藻属与硝酸盐和亚硝酸的浓度呈正相关关系,角毛藻属、根管藻属和伪菱形藻属与氨盐
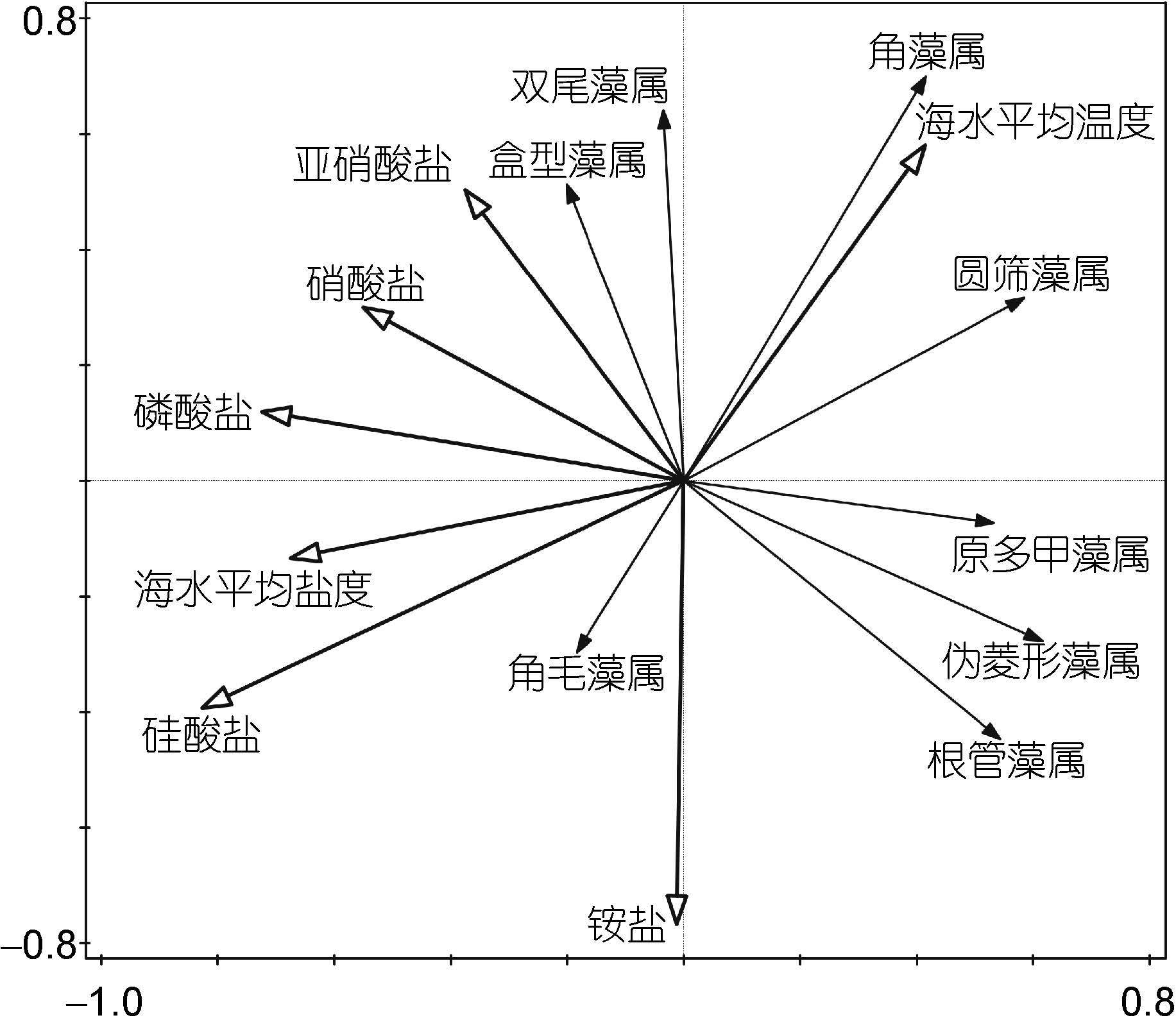 |
| 图 8 浮游植物种类与环境因子的RDA二维排序图 Fig. 8 Biplot of redundancy analysis on relationship between environmental factors and phytoplankton species |
浓度呈正相关关系。相似地,胶州湾海域的优势种尖刺伪菱形藻(Pseudonitzschia pungens)和旋链角毛藻(Chaetoceros curvisetus)有明显的嗜氮性营养生理特征(刘东艳,2004)。综上,浮游植物生物量及群落的变动受到气候变化和人类活动的综合影响,南黄海夏初影响浮游植物结构和分布的关键环境因子是海水温度、盐度、硅酸盐和溶解性无机氮。
3 结论南黄海夏初的网采浮游植物生物量年际变化波动较大,在1959年全国海洋综合调查时期、2002—2003年以及2012—2013年三个不同时期呈现出明显的差异。2012—2013年时期的丰度和碳含量均显著高于1959年海洋综合调查时期。近岸海域是该区域网采浮游植物生物量的主要贡献区域,南黄海中部的浮游植物丰度和碳含量在各个时期均维持在相对稳定且较低的水平,外海区域近年的浮游植物碳含量有较为明显的升高。
近年来南黄海夏初时期甲藻占优势的范围扩大,硅藻失去了绝对优势地位。相对于1959年,2012— 2013年的硅藻所占比例显著降低,且硅藻碳含量的下降幅度相对于丰度更大。硅藻的碳密度较低,且甲藻丰度增大,使得近年甲藻碳含量所占比重明显升高。相对于1959年,近年硅藻中的角毛藻属和伪菱形藻属,以及甲藻中的角藻属和夜光藻属成为新的优势种属。
与环境因子的分析表明,近年南黄海夏初浮游植物生物量与海水平均温度呈显著正相关关系,与海水平均盐度呈显著负相关关系。营养盐方面,硅藻与硅酸盐、硝酸盐和铵盐呈显著正相关关系,甲藻与亚硝酸盐呈显著正相关关系。温度、盐度、硅酸盐和溶解性无机氮是影响南黄海夏初浮游植物分布的关键环境因子。
| 王俊. 2001. 黄海春季浮游植物的调查研究. 海洋水产研究, 22 (1) : 56–61 |
| 刘东艳, 2004. 胶州湾浮游植物与沉积物中硅藻群落结构演替的研究. 青岛: 中国海洋大学博士学位论文, 1-127 http://cdmd.cnki.com.cn/article/cdmd-10423-2004131357.htm |
| 孙儒泳. 1992. 动物生态学原理(第2版). 北京: 北京师范大学出版社, 356-357 |
| 孙晓霞, 孙松, 吴玉霖, 等. 2011. 胶州湾网采浮游植物群落结构的长期变化. 海洋与湖沼, 42 (5) : 639–646 |
| 孙军, 刘东艳, 钱树本. 2000. 浮游植物生物量研究Ⅱ. 胶州湾网采浮游植物细胞体积转换生物量. 海洋学报, 22 (1) : 102–109 |
| 朱树屏, 郭玉潔. 1959. 十年来我国海洋浮游植物的研究. 海洋与湖沼, 2 (4) : 223–229 |
| 宋书群, 2010. 黄、东海浮游植物功能群研究. 青岛: 中国科学院研究生院海洋研究所博士学位论文, 1-149 http://cdmd.cnki.com.cn/Article/CDMD-80068-2010147131.htm |
| 吴玉霖, 孙松, 张永山. 2005. 环境长期变化对胶州湾浮游植物群落结构的影响. 海洋与湖沼, 36 (6) : 487–498 |
| 林更铭, 杨清良. 2011. 全球气候变化背景下台湾海峡浮游植物的长期变化. 应用与环境生物学报, 17 (5) : 615–623 |
| 俞建銮, 李瑞香. 1993. 渤海、黄海浮游植物生态的研究. 黄渤海海洋, 11 (3) : 52–59 |
| 章飞燕, 2009. 长江口及邻近海域浮游植物群落变化的历史对比及其环境因子研究. 上海: 华东师范大学硕士学位论文, 1-75 http://cdmd.cnki.com.cn/article/cdmd-10269-2009188335.htm |
| 黄文祥, 沈亮夫, 朱琳. 1984. 黄海的浮游植物. 海洋环境科学, 3 (3) : 19–28 |
| 赫崇本, 汪园祥, 雷宗友, 等. 1959. 黄海冷水团的形成及其性质的初步探讨. 海洋与湖沼, 2 (1) : 11–15 |
| ÁlvarezE, López-UrrutiaÁ, NogueiraE, 等. 2011. How to effectively sample the plankton size spectrum? A case study using FlowCAM. Journal of Plankton Research, 33 : 1119–1133 |
| Bai H, Hu D X, Chen Y L, et al. 2004. Statistic characteristics of thermal structure in the southern Yellow Sea in summer. Chinese Journal of Oceanology and Limnology, 22 (3) : 237–243 DOI:10.1007/BF02842554 |
| Chiang K P, Kuo M C, Chang J, et al. 2002. Spatial and temporal variation of the Synechococcus population in the East China Sea and its contribution to phytoplankton biomass. Continental Shelf Research, 22 (1) : 3–13 DOI:10.1016/S0278-4343(01)00067-X |
| Eppley R W, Reid F M H, Strickland J D H. 1970. Estimates of phytoplankton crop size, growth rate, and primary production. In: Strickland J D H ed. The Ecology of the Plankton off La Jolla, California, in the Period April through September. California: Scripps Institution of Oceanography, 33 : 33–42 |
| Fahnenstiel G, Pothoven S, Vanderploeg H, et al. 2010. Recent changes in primary production and phytoplankton in the offshore region of southeastern Lake Michigan. Journal of Great Lakes Research, 36 (S3) : 20–29 |
| Gao X L, Song J M. 2005. Phytoplankton distributions and their relationship with the environment in the Changjiang Estuary, China. Marine Pollution Bulletin, 50 (3) : 327–335 DOI:10.1016/j.marpolbul.2004.11.004 |
| Humborg C, Conley D J, Rahm L, et al. 2000. Silicon retention in river basins: far-reaching effects on biogeochemistry and aquatic food webs in coastal marine environments. AMBIO: A Journal of the Human Environment, 29 (1) : 45–50 DOI:10.1579/0044-7447-29.1.45 |
| Jakobsen H H, Carstensen J, Harrison P J, et al. 2015. Estimating time series phytoplankton carbon biomass: Inter-lab comparison of species identification and comparison of volume-to-carbon scaling ratios. Estuarine, Coastal and Shelf Science, 162 : 143–150 DOI:10.1016/j.ecss.2015.05.006 |
| Jiang Z B, Liu J J, Chen J F, et al. 2014. Responses of summer phytoplankton community to drastic environmental changes in the Changjiang (Yangtze River) estuary during the past 50 years. Water Research, 54 : 1–11 DOI:10.1016/j.watres.2014.01.032 |
| Lepš J, Šmilauer P. 2003. Multivariate analysis of ecological data using CANOCO. ambridge: Cambridge university press, |
| Lin C, Ning X R, Su J L, et al. 2005. Environmental changes and the responses of the ecosystems of the Yellow Sea during 1976-2000. Journal of Marine Systems, 55 (3-4) : 223–234 DOI:10.1016/j.jmarsys.2004.08.001 |
| Litchman E, Klausmeier C A. 2008. Trait-based community ecology of phytoplankton. Annual Review of Ecology, Evolution, and Systematics, 39 (1) : 615–639 DOI:10.1146/annurev.ecolsys.39.110707.173549 |
| Liu J Y. 2013. Status of marine biodiversity of the China Seas. PloS One, 8 (1) : e50719 DOI:10.1371/journal.pone.0050719 |
| Menden-Deuer S, Lessard E J. 2000. Carbon to volume relationships for dinoflagellates, diatoms, and other protist plankton. Limnology and Oceanography, 45 (3) : 569–579 DOI:10.4319/lo.2000.45.3.0569 |
| Montagnes D J S, Berges J A, Harrison P J, et al. 1994. Estimating carbon, nitrogen, protein, and chlorophyll a from volume in marine phytoplankton. Limnology and Oceanography, 39 (5) : 1044–1060 DOI:10.4319/lo.1994.39.5.1044 |
| Mullin M M, Sloan P R, Eppley R W. 1966. Relationship between carbon content, cell volume and area in phytoplankton. Limnology and Oceanography, 11 (2) : 307–311 DOI:10.4319/lo.1966.11.2.0307 |
| Nelson D M, Dortch Q. 1996. Silicic acid depletion and silicon limitation in the plume of the Mississippi River: evidence from kinetic studies in spring and summer. Marine Ecology Progress Series, 136 : 163–178 DOI:10.3354/meps136163 |
| Ning X R, Lin C L, Su J L, et al. 2010. Long-term environmental changes and the responses of the ecosystems in the Bohai Sea during 1960-1996. Deep Sea Research Part II: Topical Studies in Oceanography, 57 (11-12) : 1079–1091 DOI:10.1016/j.dsr2.2010.02.010 |
| Smayda T J. 1978. What to count. In: Sournia A ed. Phytoplankton Manual. Paris: UNESCO, : 165–166 |
| Spaulding S A, Jewson D H, Bixby R J, et al. 2012. Automated measurement of diatom size. Limnology and Oceanography: Methods, 10 (11) : 882–890 DOI:10.4319/lom.2012.10.882 |
| Strathmann R R. 1967. Estimating the organic carbon content of phytoplankton from cell volume or plasma volume. Limnology and Oceanography, 12 (3) : 411–418 DOI:10.4319/lo.1967.12.3.0411 |
| Tréguer P J, De La Rocha, C L. 2013. The world ocean silica cycle. Annual Review of Marine science, 5 : 477–501 DOI:10.1146/annurev-marine-121211-172346 |
| Verity P G, Robertson C Y, Tronzo C R, et al. 1992. Relationships between cell volume and the carbon and nitrogen content of marine photosynthetic nanoplankton. Limnology and Oceanography, 37 (7) : 1434–1446 DOI:10.4319/lo.1992.37.7.1434 |
| Yang Y, Sun X X, Zhu M L et al, 2016. Estimating the carbon biomass of marine net-phytoplankton from abundance based on samples from China seas. Marine and Freshwater Research, doi:org/10.1071/MF15298 |
| Yin K D, Qian P Y, Chen J C. 2000. Dynamics of nutrients and phytoplankton biomass in the Pearl River estuary and adjacent waters of Hong Kong during summer: preliminary evidence for phosphorus and silicon limitation. Marine Ecology Progress Series, 194 : 295–305 DOI:10.3354/meps194295 |
| Zhou M J, Shen Z L, Yu R C. 2008. Responses of a coastal phytoplankton community to increased nutrient input from the Changjiang (Yangtze) River. Continental Shelf Research, 28 (12) : 1483–1489 DOI:10.1016/j.csr.2007.02.009 |
 2016, Vol. 47
2016, Vol. 47


