中国海洋湖沼学会主办。
文章信息
- 甄晓桐, 李力, 王小静, 任艺君. 2019.
- ZHEN Xiao-Tong, LI Li, WANG Xiao-Jing, REN Yi-Jun. 2019.
- 黄、渤海几种溶解态痕量金属(Cu、Ni、Co、Zn)分布特征及其影响因素
- DISTRIBUTION CHARACTERISTICS AND INFLUENCING FACTORS OF SEVERAL DISSOLVED TRACE METALS (Cu, Ni, Co, Zn) IN THE YELLOW SEA AND THE BOHAI SEA
- 海洋与湖沼, 50(5): 1022-1032
- Oceanologia et Limnologia Sinica, 50(5): 1022-1032.
- http://dx.doi.org/10.11693/hyhz20190300051
文章历史
-
收稿日期:2019-03-12
收修改稿日期:2019-04-26
2. 青岛海洋科学与技术试点国家实验室 青岛 266237
2. Pilot Marine Science and Technology Pilot National Laboratory(Qingdao), Qingdao 266237, China
痕量金属是一种累积性的、无法被降解的污染物, 可由地表径流、大气沉降以及近海污染物的排放等各种途径进入海洋(Stumm et al, 1996), 可通过食物链被生物体吸收和富集, 当某些痕量金属的浓度超过一定水平时, 会成为毒素, 例如Pb、Hg, 其对生物有毒性, 最终在人体内累积导致慢性中毒、危害人类的健康(Hook et al, 2001; 战玉杰等, 2011; Dong et al, 2016)。但同时, 某些痕量金属是微量营养元素(micronutrients), 例如Fe, 在大洋表层海水中相对稀缺, 当其浓度过低时, 成为限制初级生产力的因素(Martin et al, 1988; Morel et al, 2003)。而有些痕量金属则有其两面性, 例如Cu, 浓度过低时会限制生物生长, 浓度过高时会对生物体产生毒性(Brand et al, 1986; Moffett et al, 1997)。随着经济的发展, 沿海城市工农业的兴起, 进而带来的是工业污水及城市生活废水排放的增加, 因此研究近岸海区海水中痕量金属的时空分布对妥善维护我国沿海地区生态环境至关重要。
痕量金属在海水中的含量极低, 一般在nmol/L (10-9mol/L)到pmol/L (10-12mol/L)量级, 而环境中其污染源众多, 所以在采样和测试过程中易受污染。由于痕量金属洁净采样和分析测试技术的匮乏, 导致我国以往发表的海水中高质量痕量金属数据较少。近年来, 随着我国对海洋科学发展的重视, 逐渐建立起痕量超净实验室, 并对采样过程也予以足够重视, 发表了多篇高质量的科研文章。Ren等(2011)研究了黄海中溶解铝的分布特征, 分析表明大气沉降是影响黄海中溶解态铝的主要来源并推算出溶解铝在黄海中的停留时间; Li等(2015)阐述了渤海痕量金属的分布特征, 结果表明渤海海区几种痕量金属(Cu、Co、Ni、Zn、Cd、Pb、Ag)的浓度与之前发表的研究结果不同, 整体偏低, 与欧美较为洁净的海湾中痕量金属含量相似, 以此推断黄河上游大量建坝导致的河流流量减少, 进而导致河床中的溶解态痕量金属在到达海湾之前沉积, 从而使得海湾中痕量金属浓度偏低; Li等(2017)继而发表了南黄海中几种痕量金属(Cu、Co、Ni、Cd、Ag)的分布, 结果表明Cu、Co、Ni的分布与盐度有很强的相关性, 其来源相似, 主要来自河流输入, 其整体浓度为渤海的一半。但总体来看, 在中国近海针对这几种易污染的痕量金属的高质量数据还是极为匮乏。
因痕量金属在海水中浓度极低, 导致在海水高盐度的基体当中测试如此低浓度的含量很有难度, 一般都要先经过富集分离步骤, 将高盐度基体当中的痕量金属萃取出来。从20世纪七十年代末、八十年代初开始, 大多采用液液萃取法[即样品先与焦赖氨酸二硫代氨基甲酸铵(APDC)和二乙基二硫代氨基甲酸酯(DDDC)混合, 再用氯仿或甲基异丁基酮(MIBK)萃取分离](Danielsson et al, 1978), 此方法操作繁琐, 费时费力, 另外所用萃取剂大多为毒性很大的有机溶剂, 对人体造成极大危害和环境污染。Chelex-100具有很好的重金属吸附能力, 在近中性溶液中可富集痕量金属, 再利用稀硝酸将富集金属洗脱, 实现金属离子与高盐度溶液的分离(Díaz-Romero, 1996; Kiptoo et al, 2009)。2008年Nobias PA1树脂问世, 该树脂含有EDTriA和IDA官能团, 几乎能萃取所有的痕量金属包括稀土元素(Sohrin et al, 2008)。相比于其他传统的富集分离方法, 该方法具有样品量需求小(~40mL)、操作相对简单、耗时短, 且不易污染等优点。目前在国际范围内广泛使用, 且已用公司推出该树脂为核心技术的全自动海水前处理系统(seaFAST系列, Elemental Scientific Inc., 美国)。
在本研究中, 我们首次采用了Nobias PA1树脂富集分离的前处理方法, 测试了黄、渤海海水中的几种溶解态痕量金属(Cu、Ni、Co、Zn)的浓度。希望在2011—2013年工作的基础上(Li et al, 2015, 2017), 研究几种痕量金属在黄、渤海海水中的浓度和分布的年纪变化, 并首次报道分析了黄海海水中溶解态Zn的分布特征及其影响因素。
1 材料与方法 1.1 研究区域及样品采集渤海与黄海是我国重要的半封闭陆架海区, 与中国大陆和朝鲜半岛接壤, 具有陆源输入大、海水交换率小、初级生产力高等特点(谢琳萍等, 2012)。渤海海域面积为77000km2, 由渤海湾、莱州湾和辽东湾三个海湾组成, 平均深度为18m, 渤海通过狭窄的渤海海峡与黄海相连。受辽南沿岸流和鲁北沿岸流的影响, 水体从渤海海峡北部流入渤海, 从渤海海峡南部流出(韦钦胜等, 2011), 水体在辽东湾以顺时针方向流动, 在渤海湾和莱州湾以逆时针方向流动(Guan, 1988; Fang et al, 2000)。
黄海海域位于我国东北部沿海地区, 与朝鲜半岛接壤, 表面积为3.8×105km2, 平均深度为44m, 山东半岛将黄海分为北黄海和南黄海。北黄海主要受到辽南沿岸流和鲁北沿岸流的影响(温国义等, 2008; 鲍献文等, 2009)。在夏季北黄海中部底层水体中存在低温高盐的冷水团(缪经榜等, 1990)。南黄海主要的环流系统是黄海暖流以及黄海西部沿岸流和朝鲜半岛西部沿岸流。黄海暖流在冬季沿黄海槽向北侵入, 在夏季向东流入济州岛与朝鲜半岛之间的济州海峡, 黄海西部沿岸流向北流动(汤毓祥等, 2000)。在南黄海中部底层水中存在明显的温跃层, 即南黄海冷水团, 其在春季形成, 夏季最强, 冬季消退(任慧军等, 2005; 韦钦胜等, 2013)。
本研究采样区间包括黄、渤海大部分海域, 尤其在北黄海采集了样品, 在以往的研究中对北黄海表、底层海水痕量金属的研究很少, 本文在北黄海的研究结果将完善我国近海海水中痕量金属数据, 很好的连接渤海与南黄海之间的海流运动趋势以及对痕量金属的影响因素分析。
1.2 样品处理及分析方法本研究于2016年6月29日—7月14日参加了国家自然基金委黄、渤海夏季航次, 随“东方红2号”调查船对对黄、渤海进行了表层和底层海水的采样过程。采样站位分布如图 1所示。采水过程中严格采用痕量金属洁净(trace-metal clean)技术。C-flex®采样管(Cole-Parmer Inc.)采水端装有约20cm的特氟龙硬管, 将其固定为与采样绳垂直方向。在蠕动泵的带动下采集海水样品, 采样管另一端连接囊式过滤器(Acropak®0.2μm, Pall Inc.), 表、底层海水采样方法一致, 详情参照Li等(2017)。将海水样品收集在事先清洗过的低密度聚乙烯500mL采样瓶(Nalgene Inc.)中, 加高纯HNO3 (Optima级别, Fisher Inc.)至pH~2后, 常温密封保存用于溶解态总量的分析。采样瓶清洗步骤详见Li等(2015)。
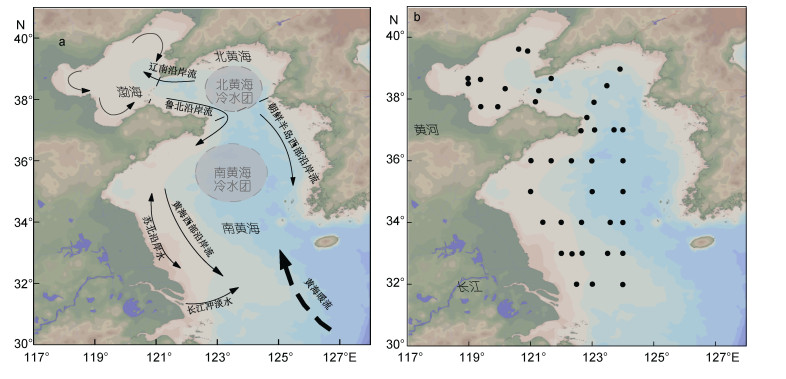 |
| 图 1 黄海和渤海站位分布图 Fig. 1 The location of sampling sites in the Yellow Sea and the Bohai Sea 注: a为黄海和渤海环流图, b为黄海和渤海站位分布图 |
海水样品在超净实验室进行前处理。首先, 样品在紫外消解仪(Jelight Company, Inc.)中消解四个小时以消除样品中的有机质, 然后, 在超净实验室中使用搭载起来的富集分离装置对海水样品进行前处理(Biller et al, 2012)。首先通入10mL 1mol/L硝酸溶液对树脂柱进行清洗, 再通入3—5分钟0.05mol/L醋酸铵缓冲液使树脂柱处于pH为5.6—6.0之间, 通入40mL样品(控制流速为12.0r/min), 待样品全部通过树脂柱后, 再次通入3—5分钟0.05mol/L醋酸铵缓冲液以去除盐分, 最后在氮气的压力下利用洗脱液(1mol/L HNO3)洗脱树脂收集样品约2mL。该方法可同时富集Cu、Zn、Co、Ni四种痕量金属。
溶解态金属总量采用电感耦合等离子体质谱仪ICP-MS(X SeriesⅡ, Thermo Fisher Scientific Inc.)进行分析测定。所有样品都加入In内标(10ppb), 处理和分析了样品数量10%的海水空白样和重复样, 重复样的相对偏差 < 15%。平均空白值和检出限在表 1中报告。对认证的标准海水NASS-6和CASS-5 (National Research Council of Canada)进行了分析, 结果与标准值较为一致(见表 2)。此外, 本实验还采用空白海水加入由低到高的多金属标样(High Purity Standard, Inc.)以追踪回收率并校正其基体效应, Cu、Ni、Co、Zn回收率依次为106%、109%、104%、93%, 所有结果根据回收率进行了校正。叶绿素(chl a)的测定采用萃取荧光法, 采集一定体积海水过滤所得浮游植物用90%丙酮提取其色素, 用荧光计测定提取液酸化前后的荧光值, 从而计算出chl a的浓度(王雪景等, 2018)。
| 名称 | Cu | Co | Ni | Zn |
| 平均空白值(n=21) | 0.21 | 6.73 | 0.07 | 0.15 |
| 检出限 | 0.30 | 0.02 | 0.23 | 0.35 |
| 注: Cu、Ni、Zn的单位为nmol/kg, Co的单位为pmol/kg | ||||
| 名称 | Cu | Co | Ni | Zn |
| CASS 5 (n=6) | 0.370±0.057 | 0.091±0.002 | 0.309±0.017 | 0.691±0.020 |
| 标准值a | 0.371±0.028 | 0.093* | 0.322±0.022 | 0.702±0.067 |
| NASS 6 (n=6) | 0.231±0.040 | 0.016±0.002 | 0.284±0.024 | 0.247±0.045 |
| 标准值a | 0.242±0.025 | 0.015* | 0.294±0.025 | 0.251±0.020 |
| 注: a标准值由加拿大研究委员会发布, 作为标准海水标准值, CASS 5和NASS 6均为标准海水, Cu、Co、Ni、Zn的单位为μg/kg | ||||
研究区表、底层盐度分布如图 2所示。整体来看, 盐度变化范围为26.3—33.3, 平均值为31.4。渤海中部表、底层海水盐度变化较小, 底层水盐度略高于表层水。渤海盐度最低的站点出现在莱州湾、靠近黄河口的站点, 对比Li等(2015)在2013年黄河口的盐度数据(29.1), 本研究黄河口盐度偏高(31.4), 可能是该年度夏季降水较少导致的。
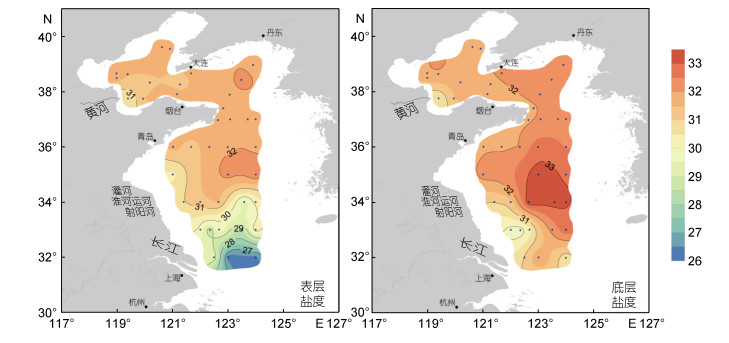 |
| 图 2 黄海和渤海表、底层盐度分布图 Fig. 2 Salinity distribution of surface and bottom layer of the Yellow Sea and the Bohai Sea |
北黄海在远岸海域表、底层海水盐度略有差异, 其位置与北黄海冷水团在夏季出现的海域相仿, 这与马超等(2010)在大连-成山角断面的研究结果类似。北黄海底层盐度呈北高南低的分布特征, 与北黄海海水自渤海海峡北部流入渤海、从南部流出渤海的现象一致(赵保仁, 1991; 韦钦胜等, 2011)。在山东半岛北岸由西向东, 表、底层盐度均出现逐渐升高的趋势, 应是鲁北沿岸水自渤海流入北黄海的影响(鲍献文等, 2009)。
南黄海表、底层盐度分布较为复杂, 在近岸海域表、底层海水存在明显的表层低、底层高的盐度梯度, 在苏北浅滩存在明显的低盐水, 并成舌状向北偏东方向延伸, 入侵较远, 水舌较宽, 在夏季向东北扩展的趋势(刘志亮等, 2009)。在长江口附近海域盐度较往年低(李曌等, 2011), 这是由于在采样期间(2016年6—7月)长江中下游等地连续遭受暴雨洪涝灾害, 导致长江口河流流量增加, 而夏季长江冲淡水有北移的趋势, 导致南黄海部分海域表层海水盐度较低(http://www.chinanews.com/), 该特殊天气现象也影响到了痕量金属在该海域的分布情况(赵保仁, 1991)。
2.2 黄、渤海溶解态痕量金属(Cu、Ni、Co、Zn)分布特征首先, 对研究区溶解态Cu、Ni、Co、Zn与盐度做Spearman相关性分析, 结果如表 3所示。统计结果发现溶解态Cu、Ni、Co、Zn与盐度无显著相关性, 这与Li等(2017)所得到结果不同, 可能是由于在长江中下游连续暴雨天气, 导致苏北沿岸水、长江冲淡水等河流流量增加进而导致表层海水盐度出现较大变化, 从而影响其相关性。其次, 这四种金属之间有显著相关性, 表明其有相似性来源。表、底层海水中四种溶解态痕量金属的空间分布见图 3、图 4。下面, 我们将针对渤海、北黄海、南黄海三个海域进行进一步讨论。
| 名称 | 盐度 | Cu | Co | Ni | Zn |
| 盐度 | 1 | ||||
| Cu | 0.06 | 1 | |||
| Co | −0.04 | 0.55** | 1 | ||
| Ni | 0.04 | 0.79** | 0.63** | 1 | |
| Zn | 0.15 | 0.41** | 0.35** | 0.48** | 1 |
| 注: **表示在置信度(双测)为0.01时, 相关性显著。 | |||||
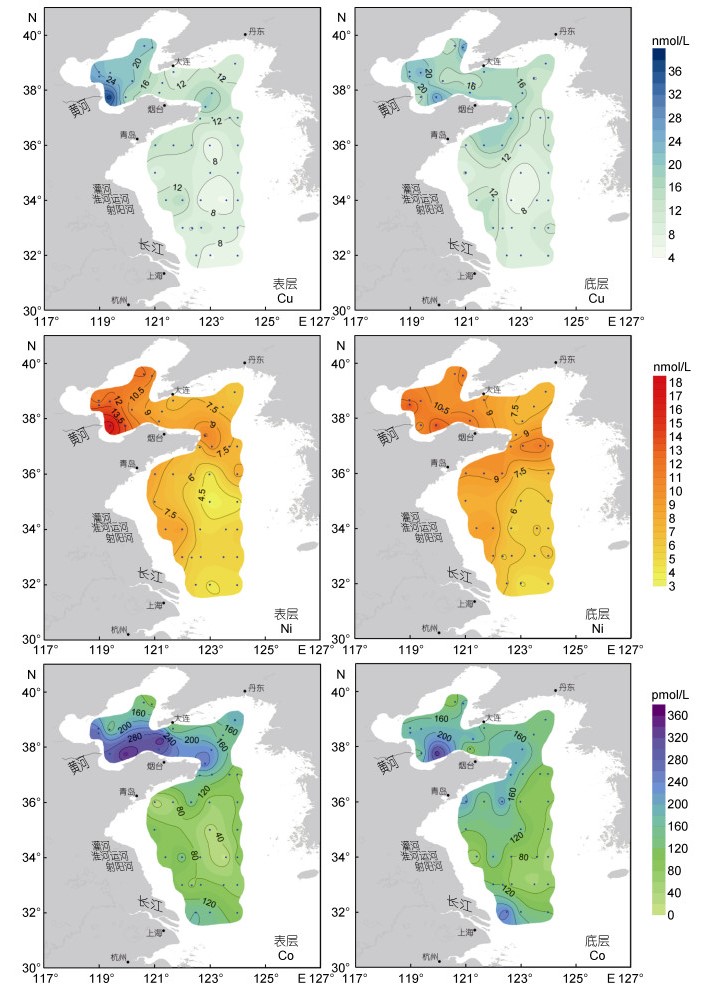 |
| 图 3 黄、渤海表、底层溶解态Cu、Ni、Co的空间分布 Fig. 3 Dissolved Cu, Ni, Co distributions in surface and bottom seawater of the Yellow Sea and the Bohai Sea |
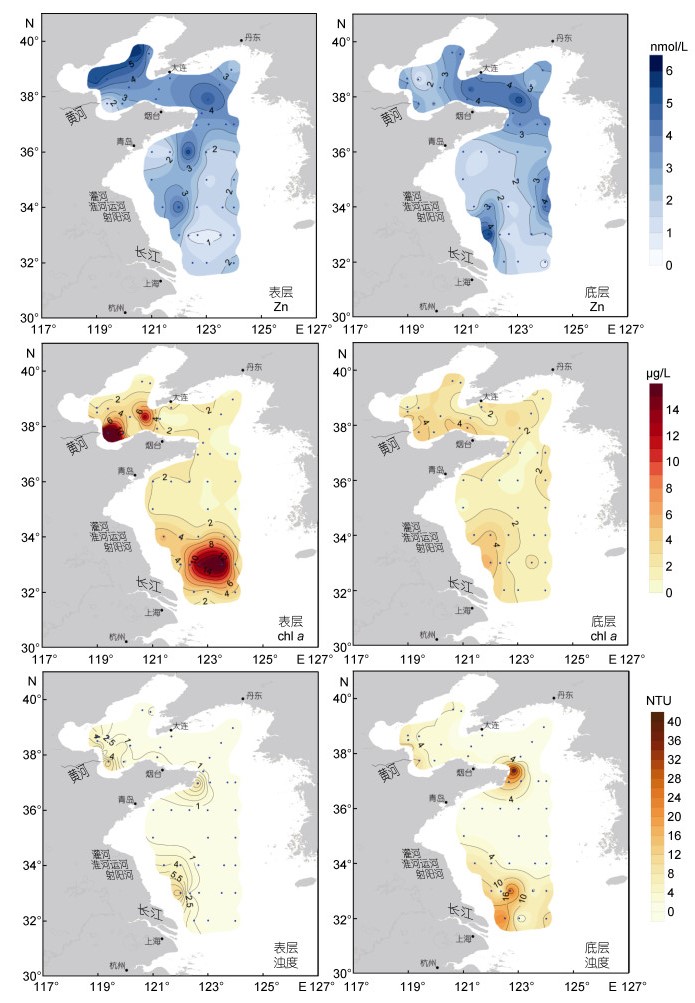 |
| 图 4 黄、渤海表、底层溶解态Zn、chl a和浊度的空间分布 Fig. 4 Dissolved Zn, chl a and turbidity distributions in surface and bottom seawater of the Yellow Sea and the Bohai Sea |
在渤海, 溶解态Cu、Ni、Co有着相似的分布趋势。在黄河口附近站点的表层水中出现三种金属的浓度高值(Cu为37.1nmol/L, Ni为17.5nmol/L, Co为349.5pmol/L)。根据目前仅有的两组较为可靠的黄河河水中痕量金属数据(Zhang, 1995; Li et al, 2015), 与莱州湾海水中痕量金属浓度对比发现Cu、Ni、Co在黄河河水中的浓度高于海水(见表 4), 所以黄河输入可视为这几种痕量金属的一个源。在渤海西北部表层海水中出现了Cu、Ni、Zn的高值, 该站点离岸较近, 无明显河流输入和区域水团影响, 溶解态痕量金属在此区域存留时间较长, 可能受陆源污染、海上石油开采、海洋养殖等因素影响(毛天宇等, 2009)。在渤海南部海域Zn在表、底层无明显变化, 且在表层海水中呈北高南低的分布特征, 与其他几种金属的分布特征相反。从表 4中可以看出, 溶解态Zn在黄河河水[(3.3±1.9)nmol/L]与渤海海水中的平均浓度[(3.2±1.4)nmol/L]相当。同时, 在黄河口附近海域表、底层浊度较高, 悬浮颗粒物可能对海水中溶解态Zn具有吸附作用, 从而导致溶解态Zn浓度较低(Bruland et al, 2003; 夏义雄等, 2012)。
| 海域 | Cu | Ni | Co | Zn | 参考文献 |
| 南黄海(n=50) | 10.8 | 6.8 | 105 | 2.4 | 本研究 |
| (5.5—19.9) | (3.7—11.5) | (12—253) | (0.8—5.8) | ||
| 北黄海(n=14) | 14.5 | 8.3 | 191 | 3.7 | |
| (8.6—18.9) | (6.2—11.5) | (97—339) | (2.2—5.4) | ||
| 渤海(n=16) | 21.6 | 11.6 | 210 | 3.2 | |
| (14.2—37.1) | (9.5—13.6) | (100—349) | (0.7—5.8) | ||
| 南黄海(n=43) | 8.5 | 6.6 | 100 | n.a. | Li et al, 2017 |
| (2.8—15.0) | (3.3—11.7) | (40—300) | n.a. | ||
| 渤海和莱州湾(n=28) | 22.6 | 15.5 | 309 | 1.8 | Li et al, 2015 |
| (17.8—30.4) | (10.9—23.1) | (159—995) | (0.6—3.3) | ||
| 北黄海(春季) | 12.6±9.4 | n.a. | n.a. | 58.1±27.5 | 田琳等, 2009 |
| 北黄海(秋季) | 22.0±14.2 | n.a. | n.a. | 123.9±26.0 | |
| 南黄海 | 22.2 | n.a. | n.a. | 95.0 | 贺志鹏等, 2008 |
| 东海近岸海区 | 61.4 | n.a. | n.a. | 84.1 | 王长友等, 2008 |
| 南海 | 0.78—1.22 | 2.3—2.7 | n.a. | n.a. | Wen et al, 2006 |
| 黄河 | 20.0 | 7.5 | 300.0 | 3.0 | Zhang, 1995 |
| 黄河 | 41.3 | 13.3 | 428.0 | 3.3 | Li et al, 2015 |
| 美国旧金山湾 | 34(16—73) | 27(13—71) | 110(170—530) | 13(5.5—23) | Flegal et al, 1991 |
| 美国加尔维斯顿湾 | 3—27 | 3—32 | 300—3100 | 1—7 | Wen et al, 1999 |
| 美国加州法拉隆湾 | 1.7—5.3 | n.a. | 400—600 | 2.8—3.0 | Hurst et al, 2008 |
| 日本冲绳岛沿岸水 | 0.60—15.0 | 1.9—8.3 | 32—580 | n.a. | Itoh et al, 2009 |
| 美国波士顿港 | 14.7(8.1—54.1) | 6.0(4.3—13.5) | n.a. | 20.8(5.6—51.2) | Li et al, 2010 |
| 西太平洋 | 2.4 | 8.2 | 20 | 5.4 | Fujishima et al, 2001 |
| 天然海水背景值 | 0.16—0.63 | n.a. | n.a. | 0.15 | 于涛, 2003 |
| 国家一类海水水质标准 | 78.74 | 85.19 | 5.1×105 | 305.90 | GB3097-1997 |
| 注: Cu、Ni、Zn的单位为nmol/kg, Co的单位为pmol/kg, n.a.表示未检出。 | |||||
北黄海是链接渤海和南黄海的重要海域。北黄海海水常年由渤海海峡北部进入渤海, 而渤海的海水从渤海海峡南部流出。南黄海海水在黄海暖流的作用下向北黄海输入, 在鲁北沿岸流和朝鲜半岛西部沿岸流的作用下, 北黄海的海水流入南黄海。北黄海很好的将渤海与南黄海连接起来, 如表 4所示, 本研究中北黄海溶解态Cu、Ni、Co的平均浓度介于渤海和南黄海之间, 由北向南逐渐降低。
在渤海海峡, 溶解态Cu、Ni、Co在表层海水中的分布特征整体呈现为南高北低, 北部浓度变化大, 这是由于在夏季辽南沿岸流表层海水流速大、流幅窄的特点(臧家业等, 2001), 将北黄海低浓度海水通过渤海海峡北部向渤海运输, 而渤海海峡南部表层海水主要受到鲁北沿岸水的影响, 将莱州湾高金属浓度海水向北黄海运移。溶解态Cu和Ni在表、底层海水中无明显差异, Co在底层海水中的分布主要受到辽南沿岸流的影响, 受鲁北沿岸水的影响较小。
北黄海表层海水中溶解态Cu和Ni呈现北低南高的分布趋势, Co在江口附近有高值现象, 可能在鸭绿江中Co含量较高(采样站点较少, 表层海水盐度无明显低值)。Co在美国一些近岸海域也发现含量较高, 代表河流带来的污水排放(Hurst et al, 2008)。在北黄海中部50m等深线以深的海槽中存在北黄海冷水团, 其在夏季尤为明显, 冷水团与岸边高温低盐水形成明显锋面, 温、盐呈现双峰结构(姚志刚等, 2012)。在本研究中, 冷水团所在的底层海水中溶解态Cu、Ni、Co的浓度偏低, 但受站位数量所限, 无法明确反映出其具体影响。冷水团对溶解态金属的影响在南黄海比较明显, 下面在2.2.3章节中将具体论述。
在成山角附近海水中溶解态Cu、Co、Ni、Zn均出现高值, 但该海域海水盐度无明显变化, 说明没有特别多的淡水输入导致金属浓度升高。成山角附近海域水深变化剧烈, 在夏季盛行偏南风, 产生上升流(夏综万等, 1983; 武贺等, 2010)。在上升流的作用下, 沉积物发生再悬浮, 表现为浊度在该海域较高, 尤其底层高于表层, 如图 4浊度分布图所示(韦钦胜等, 2011; 王雪景等, 2018)。再悬浮的沉积物可通过解吸或再矿化过程诱导金属从固相中的再活化, 使得底层海水痕量金属浓度升高(Kalnejais et al, 2010)。
2.2.3 南黄海首先, 几种痕量金属在南黄海呈现北高南低、近岸高远岸低的分布趋势。其次, 在黄海中部海域表、底层海水中出现金属的低值区域, 其位置与南黄海的冷水团较为一致。南黄海冷水团春季在青岛附近海域诞生, 在夏季逐渐并入南黄海中部海域, 形成南黄海冷水团, 在秋季范围逐渐缩小(任慧军等, 2005)。在南黄海冷水团存在期间, 垂向水团的分层使得表层水和底层水完全隔离。当表层海水中温度适宜, 藻类的生成可吸收Ni、Co等金属离子, 从而导致表层海水金属浓度低值现象(Bruland et al, 2003)。在底层海水中温度较低, 海水中藻类等浮游生物较少, 但在夏季长期处于低温高盐状态, 猜测海水中的悬浮体颗粒在相对稳定的环境下吸附海水中溶解态Cu和Ni, 从而出现低值, 该现象有待于在未来的研究中进一步分析。
在苏北浅滩表层海水观察到Zn高值, 推测苏北沿岸水是Zn高值的一个来源。该海域海水盐度较低, 在夏季苏北沿岸水在黄海西部沿岸流的作用下向南部流动(邹娥梅等, 1999)。朱建荣等(1997)指出在径流量大时, 长江冲淡水向东南扩展较强, 东北方向扩展较弱, 因此Zn高值主要受到苏北沿岸水的影响。在苏北浅滩底层海水中Cu、Ni、Zn出现高值, 该海域水深浅, 表、底层海水中浊度有明显高值, 水动力复杂(图 4)。受风、海浪、潮流的影响使近岸沉积泥沙再悬浮, 导致溶解态金属含量的增加(韦钦胜等, 2011; 杨红等, 2015)。
在长江三角洲附近海域表层和底层均观测到Co的高值, 并向东北方向扩展, 浓度逐渐降低, 在此站点观察到低盐区域, 因此长江冲淡水可能是Co高值的一个来源。长江冲淡水一般顺河口向东南方向流动, 在夏、秋季(5—9月)转向东北方向流动(赵保仁, 1991)。
2.2.4 浮游植物吸收对溶解态Zn分布的影响溶解态Zn在黄、渤海的分布特征与其他几种金属不尽相同。首先, 黄、渤海海水中溶解态Zn的平均浓度差别不大; 其次, Zn在表层海水中的整体分布与叶绿素(chl a)的分布似呈相反趋势(图 4)。在黄河口chl a高值区, 溶解态Zn值较低, 在长江口附近海域chl a高值区溶解态Cu、Ni、Co、Zn均出现低值。该相反趋势说明, 在黄、渤海水体中浮游植物的吸收在很大程度上影响了Zn的分布。Zn作为一种营养盐型痕量金属(micro-nutrient), 可被海水中的浮游藻类吸收利用, 从而使得其浓度降低(Bruland et al, 2003)。同时, 因为黄、渤海海水中溶解态Zn整体浓度较低[(3.2±1.8)nmol/L], 所以该生物吸收过程被明显的放大出来。
2.3 与其他海区的对比如表 4所示, 本研究印证了本课题组在2011— 2013年间针对黄、渤海海水中溶解态痕量金属浓度的研究结果, 显示平均浓度的年际变化较小, 极个别差异应主要是淡水输入的年际变化所致的。总体表明黄、渤海海水总体上溶解态痕量金属浓度处于良好水平, 均符合国家一类海水水质标准, 且Ni、Co、Zn低于一类海水标准上限至少一个数量级, Cu在渤海中出现最高值, 但也低于一类海水标准一倍。
由表 4可看出, Cu、Ni、Co三种溶解态金属在渤海、北黄海、南黄海呈浓度逐渐降低趋势。溶解态Cu和Ni比我国东海沿岸海区略低, 高于我国南海, 与美国旧金山湾和加尔维斯顿湾以及日本冲绳沿海地区浓度相当, 但都高于西太平洋海水中溶解态痕量金属的浓度。Flegal等(1991)在旧金山湾研究结果表明Cu和Ni主要受到河口人为因素的影响, 与本研究Cu和Ni影响因素一致。而Co在本研究黄河和长江出现局部高值与Farallones湾局部高值类似, 随着离岸距离的增加, 浓度逐渐降低。对比分析表明:黄河的河流输入仍然是渤海痕量金属(Cu、Ni、Co)的主要来源。长江冲淡水是黄海溶解态Co的主要来源。通过对比田琳等(2009)在北黄海春秋两季的研究结果, Cu高于春季海水中痕量金属浓度但低于秋季, 推测季节变化会影响Cu的含量。
黄、渤海溶解态Zn与美国加尔维斯顿湾和Farallones湾相当, 但低于美国旧金山湾沿海地区。作为在采样和分析过程中极易被污染的一种痕量金属元素, 溶解态Zn在黄、渤海整体浓度极低[平均值为(3.2±1.8)nmol/L]。这与之前被广泛报道的中国近海的溶解态Zn数据的数据(30.6—149.9nmol/L)相比, 低1—3个数量级(见表 4)。与国外一些近岸海湾相比(5.5—51.2nmol/L), 也较低(Flegal et al, 1991; Li et al, 2010)。这一方面反映了本研究采样和测试过程的洁净程度较高, 并未引入任何污染; 另一方面, 作为一个有着较长污染历史的半封闭(黄、渤海)海域, 如此低浓度的Zn也是一个较为特别的现象。我们考虑, 应是有某种清除机制存在, 作用于停留时间较长的海水, 不断从海水中清除溶解态Zn。引起该现象的准确原因需要进一步的研究工作来解答。
3 结论(1) 黄、渤海溶解态Cu、Ni、Co的分布较为相似, 呈近岸高、远岸低的特征, 三种金属的平均浓度在渤海-北黄海-南黄海呈逐渐降低的分布特征。渤海高于南黄海远岸海域两倍, 其高值应主要受渤海众多河流输入的影响, 在北黄海成山角附近的高值主要受到常年上升流引起的再悬浮过程的影响, 在苏北浅滩的高值, 应是较浅地势和较高悬浮颗粒物浓度引起的解吸过程所致。在长江口附近海域只发现了Co值稍高, 长江的河流输入是Co的来源。
(2) 溶解态Zn的分布与其他三种金属不同, 在黄、渤海并无明显浓度差异, 而其表层分布与水体中叶绿素(chl a)似呈相反趋势, 应是生物过程吸收利用Zn所致。与之前渤海的研究结果类似, 本研究发现黄海海水中溶解态Zn的含量也极低[(3.1±1.8)nmol/L], 其浓度较之前国内其他研究报道的数据低1—3个数量级。黄海海水中发现如此低浓度的Zn考虑应是存在某种清除机制所致, 而该数据的报道在国内应尚属首次。
(3) 总体来说, 中国近岸黄、渤海海域中溶解态痕量金属的浓度较低, 低于国家一类水质标准。本研究的结果表明, 获取准确可靠的溶解态痕量金属数据需要采取痕量金属洁净的采样和分析测试技术, 而准确数据的获得将为我国近岸海水中的生物地球化学循环过程的研究提供重要信息, 也将为相关环境检测部门提供可信赖的数据, 从而满足中国近岸海洋生态环境长期监测和保护的需要。
致谢 感谢2016年国家自然基金委黄、渤海夏季共享航次船长和全体船员的帮助, 感谢张翠琴参与现场调查和数据分析工作, 感谢中国海洋大学王丽莎对本文叶绿素数据的提供。
于涛. 2003. 南海海水中溶解态铜、铅、锌、镉环境背景值的初步研究. 应用海洋学学报, 22(3): 329-333 DOI:10.3969/j.issn.1000-8160.2003.03.010 |
马超, 鞠霞, 吴德星, 等. 2010. 黄、渤海断面及海洋站的盐度分布特征与变化趋势. 海洋科学, 34(9): 70-75, 81 |
王长友, 王修林, 孙百晔, 等. 2008. Cu、Pb、Zn和Cd对东海原甲藻的生态毒性效应. 中国环境科学, 28(3): 264-268 DOI:10.3321/j.issn:1000-6923.2008.03.016 |
王雪景, 金春洁, 王丽莎, 等. 2018. 2016年夏季黄、渤海颗粒有机碳的分布特征及影响因素. 海洋学报, 40(10): 200-208 DOI:10.3969/j.issn.0253-4193.2018.10.019 |
韦钦胜, 于志刚, 冉祥滨, 等. 2011. 黄海西部沿岸流系特征分析及其对物质输运的影响. 地球科学进展, 26(2): 145-156 |
韦钦胜, 于志刚, 葛人峰, 等. 2013. 黄海西部沿岸冷水在夏季南黄海西部底层冷水形成和季节演变过程中作用的化学水文学分析. 海洋与湖沼, 44(4): 890-905 |
毛天宇, 戴明新, 彭士涛, 等. 2009. 近10年渤海湾重金属(Cu, Zn, Pb, Cd, Hg)污染时空变化趋势分析. 天津大学学报, 42(9): 817-825 DOI:10.3969/j.issn.0493-2137.2009.09.011 |
田琳, 陈洪涛, 杜俊涛, 等. 2009. 北黄海表层海水溶解态重金属的分布特征及其影响因素. 中国海洋大学学报, 39(4): 617-621 |
朱建荣, 沈焕庭. 1997. 长江冲淡水扩展机制. 上海: 华东师范大学出版社
|
任慧军, 詹杰民. 2005. 黄海冷水团的季节变化特征及其形成机制研究. 水动力学研究与进展, 20(S1): 887-896 |
刘志亮, 胡敦欣. 2009. 黄海夏季近岸海区环流的初步分析及其与风速的关系. 海洋学报, 31(2): 1-7 |
汤毓祥, 邹娥梅, 李兴宰, 等. 2000. 南黄海环流的若干特征. 海洋学报, 22(1): 1-16 |
李曌, 张学雷, 王宗灵, 等. 2011. 2008年夏季南黄海叶绿素a垂向分布格局初探. 海洋科学进展, 29(1): 81-89 DOI:10.3969/j.issn.1671-6647.2011.01.010 |
杨红, 阎莉, 王春峰, 等. 2015. 夏、冬季苏北近岸海域悬沙浓度垂直分布特征. 上海海洋大学学报, 24(4): 570-578 |
邹娥梅, 郭炳火, 汤毓祥, 等. 1999. 秋季南黄海水文特征及海水的混合与交换. 海洋学报, 21(5): 12-21 DOI:10.3321/j.issn:0253-4193.1999.05.002 |
武贺, 赵世明, 徐辉奋, 等. 2010. 成山头外潮流能初步估算. 海洋技术, 29(3): 98-100 DOI:10.3969/j.issn.1003-2029.2010.03.022 |
赵保仁. 1991. 长江冲淡水的转向机制问题. 海洋学报, 13(5): 600-610 |
战玉杰, 杨茹君, 王修林, 等. 2011. Hg(Ⅱ)和Pb(Ⅱ)对海洋单细胞藻的急性毒性效应. 生态毒理学报, 6(5): 523-531 |
姚志刚, 鲍献文, 李娜, 等. 2012. 北黄海冷水团季节变化特征分析. 中国海洋大学学报, 42(6): 9-15 |
贺志鹏, 宋金明, 张乃星, 等. 2008. 南黄海表层海水重金属的变化特征及影响因素. 环境科学, 29(5): 1153-1162 DOI:10.3321/j.issn:0250-3301.2008.05.001 |
夏义雄, 陈华林. 2012. 河水中悬浮颗粒物对重金属的吸附行为. 环境研究与监测, 25(2): 16-19, 23 |
夏综万, 郭炳火. 1983. 山东半岛和辽东半岛顶端附近水域的冷水现象及上升流. 黄渤海海洋, 1(1): 13-19 |
温国义, 李广雪, 赵东波, 等. 2008. 根据AVHRRSST探讨中国北部海域冬季环流演变. 海洋环境科学, 27(S2): 19-23 |
谢琳萍, 孙霞, 王保栋, 等. 2012. 渤黄海营养盐结构及其潜在限制作用的时空分布. 海洋科学, 36(9): 45-53 |
鲍献文, 李娜, 姚志刚, 等. 2009. 北黄海温盐分布季节变化特征分析. 中国海洋大学学报, 39(4): 553-562 |
臧家业, 汤毓祥, 邹娥梅, 等. 2001. 黄海环流的分析. 科学通报, 46(S1): 7-15 |
缪经榜, 刘兴泉, 薛亚. 1990. 北黄海冷水团形成机制的初步探讨——Ⅰ.模式解. 中国科学(B辑), (12): 1311-1321 |
Biller D V, Bruland K W, 2012. Analysis of Mn, Fe, Co, Ni, Cu, Zn, Cd, and Pb in seawater using the Nobias-chelate PA1 resin and magnetic sector inductively coupled plasma mass spectrometry (ICP-MS). Marine Chemistry, 130 |
Brand L E, Sunda W G, Guillard R R L, 1986. Reduction of marine phytoplankton reproduction rates by copper and cadmium. Journal of Experimental Marine Biology and Ecology, 96(3): 225-250 DOI:10.1016/0022-0981(86)90205-4 |
Bruland K W, Lohan M C, 2003. Controls of trace metals in seawater. Treatise on Geochemistry, 6: 23-47 |
Díaz-Romero C, 1996. Comparison of APDC/FREON extraction and chelex-100 ion exchange chromatography for preconcentration of heavy metals from seawater. International Journal of Environmental Analytical Chemistry, 64(3): 163-170 DOI:10.1080/03067319608028925 |
Danielsson L G, Magnusson B, Westerlund S, 1978. An improved metal extraction procedure for the determination of trace metals in sea water by atomic absorption spectrometry with electrothermal atomization. Analytica Chimica Acta, 98(1): 47-57 DOI:10.1016/S0003-2670(01)83237-2 |
Dong Y, Rosenbaum R K, Hauschild M Z, 2016. Assessment of metal toxicity in marine ecosystems:comparative toxicity potentials for nine cationic metals in coastal seawater. Environmental Science & Technology, 50(1): 269-278 |
Fang Y, Fang G H, Zhang Q H, 2000. Numerical simulation and dynamic study of the wintertime circulation of the Bohai Sea. Chinese Journal of Oceanology and Limnology, 18(1): 1-9 DOI:10.1007/BF02842535 |
Flegal A R, Smith G J, Gill G A et al, 1991. Dissolved trace element cycles in the San Francisco Bay estuary. Marine Chemistry, 36(1-4): 329-363 DOI:10.1016/S0304-4203(09)90070-6 |
Fujishima Y, Ueda K, Maruo M et al, 2001. Distribution of trace bioelements in the subarctic North Pacific Ocean and the Bering Sea (the R/V Hakuho Maru Cruise KH-97-2). Journal of Oceanography, 57(3): 261-273 DOI:10.1023/A:1012426411228 |
Guan B X, 1988. Major features and variability of the Kuroshio in the East China Sea. Chinese Journal of Oceanology and Limnology, 6(1): 35-48 DOI:10.1007/BF02846566 |
Hook S E, Fisher N S, 2001. Sublethal effects of silver in zooplankton:importance of exposure pathways and implications for toxicity testing. Environmental Toxicology and Chemistry, 20(3): 568-574 DOI:10.1002/etc.5620200316 |
Hurst M P, Bruland K W, 2008. The effects of the San Francisco Bay plume on trace metal and nutrient distributions in the Gulf of the Farallones. Geochimica et Cosmochimica Acta, 72(2): 395-411 DOI:10.1016/j.gca.2007.11.005 |
Itoh A, Ishigaki T, Arakaki T et al, 2009. Determination of trace metals in coastal seawater around Okinawa and its multielement profiling analysis. Bunseki Kagaku, 58(4): 257-263 DOI:10.2116/bunsekikagaku.58.257 |
Kalnejais L H, Martin W R, Bothner M H, 2010. The release of dissolved nutrients and metals from coastal sediments due to resuspension. Marine Chemistry, 121(1-4): 224-235 DOI:10.1016/j.marchem.2010.05.002 |
Kiptoo J K, Ngila J C, Silavwe N D, 2009. Evaluation of copper speciation in model solutions of humic acid by mini-columns packed with Chelex-100 and new chelating agents:application to speciation of selected heavy metals in environmental water samples. Journal of Hazardous Materials, 172(2-3): 1163-1167 DOI:10.1016/j.jhazmat.2009.07.119 |
Li L, Liu J H, Wang X J et al, 2015. Dissolved trace metal distributions and Cu speciation in the southern Bohai Sea, China. Marine Chemistry, 172: 34-45 DOI:10.1016/j.marchem.2015.03.002 |
Li L, Pala F, Jiang M S et al, 2010. Three-dimensional modeling of Cu and Pb distributions in Boston Harbor, Massachusetts and Cape Cod Bays. Estuarine, Coastal and Shelf Science, 88(4): 450-463 DOI:10.1016/j.ecss.2010.05.003 |
Li L, Wang X J, Liu J H et al, 2017. Dissolved trace metal (Cu, Cd, Co, Ni, and Ag) distribution and Cu speciation in the southern Yellow Sea and Bohai Sea, China. Journal of Geophysical Research:Oceans, 122(2): 1190-1205 DOI:10.1002/2016JC012500 |
Martin J H, Fitzwater S E, 1988. Iron deficiency limits phytoplankton growth in the north-east pacific subarctic. Nature, 331(6154): 341-343 DOI:10.1038/331341a0 |
Moffett J W, Brand L E, Croot P L et al, 1997. Cu speciation and cyanobacterial distribution in harbors subject to anthropogenic Cu inputs. Limnology and Oceanography, 42(5): 789-799 DOI:10.4319/lo.1997.42.5.0789 |
Morel F M M, Price N M, 2003. The biogeochemical cycles of trace metals in the oceans. Science, 300(5621): 944-947 DOI:10.1126/science.1083545 |
Ren J L, Zhang G L, Zhang J et al, 2011. Distribution of dissolved aluminum in the Southern Yellow Sea:influences of a dust storm and the spring bloom. Marine Chemistry, 125(1-4): 69-81 DOI:10.1016/j.marchem.2011.02.004 |
Sohrin Y, Urushihara S, Nakatsuka S et al, 2008. Multielemental determination of GEOTRACES key trace metals in seawater by ICPMS after preconcentration using an ethylenediaminetriacetic acid chelating resin. Analytical Chemistry, 80(16): 6267-6273 DOI:10.1021/ac800500f |
Wen L S, Jiann K T, Santschi P H, 2006. Physicochemical speciation of bioactive trace metals (Cd, Cu, Fe, Ni) in the oligotrophic South China Sea. Marine Chemistry, 101(1-2): 104-129 DOI:10.1016/j.marchem.2006.01.005 |
Wen L S, Santschi P, Gill G et al, 1999. Estuarine trace metal distributions in Galveston Bay:importance of colloidal forms in the speciation of the dissolved phase. Marine Chemistry, 63(3-4): 185-212 DOI:10.1016/S0304-4203(98)00062-0 |
Zhang J, 1995. Geochemistry of trace metals from Chinese river/estuary systems:an overview. Estuarine, Coastal and Shelf Science, 41(6): 631-658 DOI:10.1006/ecss.1995.0082 |
 2019, Vol. 50
2019, Vol. 50


