
中国海洋湖沼学会主办。
文章信息
- 翟 宇, 邓蕴彦, 孙园园, LEAW Chui-Pin, LIM Po-Teen, 赵增霞, 胡章喜, 唐赢中. 2019.
- ZHAI Xin-Yu, DENG Yun-Yan, SUN Yuan-Yuan, LEAW Chui-Pin, LIM Po-Teen, ZHAO Zeng-Xia, HU Zhang-Xi, TANG Ying-Zhong. 2019.
- 二种核糖体型的多环马格里夫藻(Margalefidinium polykrikoides)的形态和超微结构比较及分子系统学分析
- MORPHOLOGICAL AND ULTRASTRUCTURAL COMPARISON AND PHYLOGENETIC ANALYSES FOR THE EAST ASIAN AND AMERICAN/MALAYSIAN RIBOTYPES OF MARGALEFIDINIUM POLYKRIKOIDES
- 海洋与湖沼, 50(6): 1252-1262
- Oceanologia et Limnologia Sinica, 50(6): 1252-1262.
- http://dx.doi.org/10.11693/hyhz20190400076
文章历史
-
收稿日期:2019-04-19
收修改稿日期:2019-05-05
2. 青岛海洋科学与技术试点国家实验室 海洋生态与环境科学功能实验室 青岛 266237;
3. 中国科学院大学 北京 100049;
4. 中国科学院海洋大科学研究中心 青岛 266071;
5. 中国科学院实验海洋生物学重点实验室 中国科学院海洋研究所 青岛 266071;
6. Bachok Marine Research Station, Institute of Ocean and Earth Sciences, University of Malaya, 16310 Bachok, Kelantan, Malaysia;
7. 中国科学院海洋研究所胶州湾海洋生态系统国家野外科学观测研究站 青岛 266071
2. Laboratory for Marine Ecology and Environmental Science, Pilot National Laboratory for Marine Science and Technology(Qingdao), Qingdao 266237, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China;
4. Center for Ocean Mega-Science, Chinese Academy of Sciences, Qingdao 266071, China;
5. CAS Key Laboratory of Experimental Marine Biology, Institute of Oceanology, Chinese Academy of Sciences, Qingdao 266071, China;
6. Bachok Marine Research Station, Institute of Ocean and Earth Sciences, University of Malaya, 16310 Bachok, Kelantan, Malaysia;
7. Jiaozhou Bay National Marine Ecosystem Research Station, Institute of Oceanology, Chinese Academy of Sciences, Qingdao 266071, China
马格里夫藻属是新近从旋沟藻属分离出来的新属(Gómez et al, 2017), 与旋沟藻属(Cochlodinium)都隶属于甲藻门、裸甲藻目、裸甲藻科。旋沟藻属最重要的判别特征是横沟环绕细胞1.5圈以上(Schütt, 1896; Kofoid et al, 1921)。该属共有30余种被发现和描述(Schütt, 1896; Kofoid et al, 1921; Margalef, 1961; Iwataki et al, 2007; Gómez, 2012; Kudela et al, 2012)。随着更多旋沟藻纯培养的建立和研究工作的深入, 尤其是精细形态特征如顶沟的形状、横沟和纵沟的相对位置、叶绿体的形状等以及分子系统学的详细研究, 越来越多的研究认为旋沟藻应该被划分成多个属(Reñé et al, 2013, 2015)。最近, 旋沟藻属的模式种Cochlodinium strangulatum在原产地地中海被找到, Gómez等(2017)对其形态和核糖体基因序列进行了详细的观察和分析, 并与多环旋沟藻(Cochlodinium polykrikoides)和褐色旋沟藻(Cochlodinium fulvescens)及其他近缘甲藻的形态和核糖体大亚基序列进行了详细的比较, 根据横沟环绕细胞圈数、是否成链状群体、是否有叶绿体、顶沟形态等特征以及系统进化树上的亲缘关系, 旋沟藻属被分成了两个属:旋沟藻属和马格里夫藻属(Margalefidinium), 从而多环旋沟藻被转移到新建立的马格里夫藻属并成为该属的模式种, 即多环马格里夫藻(Margalefidinium polykrikoides)。
多环马格里夫藻是一种世界性广泛分布的有毒有害藻华原因种(王朝晖等, 2011; Kudela et al, 2012; Iwataki et al, 2015)。多环马格里夫藻由Margalef (1961)在加勒比海的波多黎各被发现和描述, 随后在世界各地沿海不断地被发现和报道。在20世纪90年代以前, 仅有亚洲的韩国、日本、中国香港以及北美的东海岸等几个国家和地区有多环马格里夫藻或由其引起的藻华的报道(Yuki et al, 1989; Kim et al, 1997; Tomas et al, 2008; Law et al, 2013)。但在过去的三十年里, 多环马格里夫藻的分布范围逐渐扩大, 如亚洲的中国、韩国、日本、菲律宾、印度、印度尼西亚、新加坡和阿拉伯湾等国家和地区, 美洲的美国、墨西哥和欧洲的西班牙等(Amato et al, 2008; Gobler et al, 2008; Richlen et al, 2010; Kudela et al, 2012; 王红霞等, 2014; Iwataki et al, 2015; Tan et al, 2016)。多环马格里夫藻对鱼类、贝类和浮游动物都有很强的急性毒性, 形成藻华时导致养殖区鱼类和其他动物大量死亡(Jiang et al, 2009; Tang et al, 2009; Richlen et al, 2010; Rountos et al, 2014)。多环马格里夫藻藻华对水产养殖业和渔业可能造成巨大的损失, 如韩国自1982年第一次暴发多环马格里夫藻藻华, 之后几乎年年都有该藻藻华报道, 导致养殖鱼类大量死亡(Kim et al, 1999)。1993年, 韩国沿海地区爆发的多环马格里夫藻藻华造成的损失约为七百万美元, 1995年达到了六千万美元(NFRDI, 2012), 2013年约为二千三百万美元(NFRDI, 2014); 日本自20世纪90年代首次报道多环马格里夫藻藻华以来, 几乎年年都会发生该藻藻华(Yuki et al, 1989); 2008—2009年, 阿拉伯海湾的多环马格里夫藻藻华持续时间长达9个月, 导致数千吨养殖鱼类的死亡并限制了渔业活动, 同时还破坏了珊瑚礁, 严重影响了沿海旅游业(Richlen et al, 2010)。由此可见, 多环马格里夫藻藻华已经给水产养殖业和渔业带来了巨大的经济损失, 同时严重影响了海洋生态系统健康。因此, 多环马格里夫藻藻华已成为重要的海洋生态灾害, 是少数几个全球性的最重要的藻华种类之一。
已有研究发现, 多环马格里夫藻不同地理来源的种群在核糖体大亚基基因序列上有显著差别(Iwataki et al, 2008, 2015; Kudela et al, 2012)。Iwataki等(2008)基于对核糖体大亚基基因(LSU rDNA)序列的系统学分析, 将多环马格里夫藻分成了3种不同的核糖体型:即(1)东亚型(East Asian ribotype), 主要分布在中国香港、日本西部海域以及韩国南部海域; (2)菲律宾型(Philippines ribotype), 主要分布在菲律宾的马尼拉湾和日本的大村湾; (3)美国/马来西亚型(American/Malaysian ribotype), 主要分布在美国的大西洋沿岸、波多黎各和马来西亚的婆罗岛, 在墨西哥的太平洋沿岸也有藻华报道。2013年, Reñé等(2013)在地中海的加泰罗尼亚海岸发现了多环马格里夫藻的一种新的核糖体型即地中海型(Mediterranean ribotype), 在亲缘关系上与东亚型较为接近。这些不同的核糖体型具有明显的地理分布范围。目前, 四种核糖体型中, 已知东亚和美国/马来西亚核糖体型的种群的藻华都对养殖业和生态系统造成严重危害, 但二者的LSU rDNA序列(D1—D6区)的相似性仅为94%, 显著低于目前被广为接受的同一物种97%相似性的水平, 但是它们在形态上是否有保守的可差别特征还不清楚。到目前为止, 对东亚核糖体型种群有了比较详细的表面形态和超微结构的研究(Iwataki et al, 2007, 2010, 2015; Matsuoka et al, 2008; 王红霞等, 2014), 但对其他核糖体型(包括美国/马来西亚和地中海核糖体型)的表面形态观察还不全面(Gobler et al, 2008; Reñé et al, 2013), 已有图片很难看清包括顶沟、横沟和纵沟的相对位置等重要形态特征, 尤其是还没有针对不同核糖体型的纯培养在同样培养、样品处理和样品观察条件下的比较研究。本实验室从青岛胶州湾的近藻华水平水体分离到一株多环马格里夫藻, 因而本研究对该株藻和从美国和马来西亚近海分离的另外两株多环马格里夫藻(均为美国/马来西亚核糖体型)进行了全面的细胞形态和超微结构特征的比较研究, 以探明不同核糖体型的种群是否已产生细胞形态和超微结构水平上可识别的分化。我们相信本研究对于多环马格里夫藻的分类学和藻华监测及其基础生态学具有重要意义。
1 材料与方法 1.1 藻种及培养条件实验所用多环马格里夫藻藻种均为以毛细管分离法获得的单细胞培养系。多环马格里夫藻中国株MPJZBC3于2015年分离自中国青岛胶州湾, 美国株CP1于2006年分离自美国纽约Paconic湾(Tang et al, 2009), 马来西亚株MPCoKK23于2014年分离自马来西亚Kota Kinabalu海域。藻种置于光照培养箱中培养, 采用不添加Si的f/2培养基(Guillard, 1975), 基础介质为青岛市汇泉湾天然海水(盐度31)。培养温度为(21±1)℃, 光照强度约100μmol/(m2·s), 光暗比12L:12D。每次接种时往培养基中添加1%—2%的青霉素、链霉素混合液(北京索莱宝科技有限公司), 以抑制细菌生长。
1.2 分子测序与系统进化分析 1.2.1 分子测序取2mL处于对数生长期的藻液, 离心收集藻细胞, 使用植物DNA提取试剂盒(天根生化科技(北京)有限公司)提取总DNA。提取的DNA序列作为PCR的模板来扩增大约1400bp的核糖体大亚基序列(LSU rDNA), 扩增引物为D1R (正向, 5′-ACCCGCTGAATTTAAGCATA-3′) (Scholin et al, 1994)和28-1483R (反向, 5′-GCTACTACCACCAAG ATCTGC-3′) (Daugbjerg et al, 2000)。PCR反应体系为25μL, 包括9.5μL ddH2O, 12.5μL 2× Taq PCR MasterMix (0.1U/μL Taq Polymerase, 500μmol/L dNTPs, 20mmol/L Tris-HCl (pH8.3), 100mmol/L KCl, 3mmol/L MgCl2, 稳定剂和增强剂; 天根生化科技(北京)有限公司), 1μL正向引物D1R (10mmol/L), 1μL反向引物28-1483R (10mmol/L)和1μL DNA模板。PCR反应程序为: 94℃预变性5min, 94℃ 20s, 55℃ 30s, 72℃ 2min, 35个循环, 72℃延伸10min。PCR产物在溴化乙锭染色的1.0%琼脂糖平板进行电泳, 最后在凝胶成像分析仪下进行凝胶成像。将目的DNA条带从琼脂糖凝胶中切下, 并使用DNA回收试剂盒(DNA fragment recovery kit, GK2043-50, 上海捷瑞生物工程有限公司)回收纯化PCR产物, 经连接、转化后, 挑取阳性克隆菌液送至上海生工生物公司测序。序列结果上传至GenBank, 多环马格里夫藻中国株(MPJZBC3)、美国株(CP1)和马来西亚株(MPCoKK23)的登录号分别为MK685212, MK685214和MK686612。
1.2.2 序列比对与系统学分析将我们获得的序列在NCBI中进行检索, 选取从不同国家和地区分离的多环马格里夫藻和褐色马格里夫藻进行序列分析(序列号见进化树上物种名后), 甲藻Pyrodinium bahamense (序列号: AY154959)作为外群。首先, 使用MAFFT v.7 (http://mafft.cbrc.jp/alignment/server/; Katoh et al, 2002)对所有序列进行比对, 并使用BioEdit (v7.2.5) (Hall, 1999)对序列进行修剪至1523个碱基(包括缺失(gap))。使用jModelTest 2.1.14 (Darriba et al, 2012)程序中的AIC功能选择最适合的分子进化模型, 分析结果选择GTR+G模型。使用RaxML (v7.2.6; Guindon et al, 2003; Guindon, 2010)构建最大似然树(Maximum likelihood, ML), 选择的最适合替换模型为GTR+G, bootstrap值设置为1000。使用MrBayes 3.2.6 (Ronquist et al, 2003)构建贝叶斯树(Bayesian tree), 选择的最适合替换模型为GTR+G, 四条MCMC链运行10000000代, 每1000代进行一次取样。使用FigTree (v1.4.4) (Rambaut, 2018)对进化树进行分析和编辑。
1.3 光镜观察将处于对数生长期的多环马格里夫藻置于正置显微镜(型号BX53, 奥林巴斯, 东京, 日本)下观察, 使用CCD制冷显微数码相机(型号DP80, 奥林巴斯, 东京, 日本)对细胞进行观察和拍照。为了观察细胞核的形状和位置, 用SYBR Green Ⅰ (北京索莱宝科技有限公司)对细胞进行染色, 然后在荧光显微镜下观察和拍照。
1.4 扫描电镜样品制备取一定体积处于对数生长期的藻液, 加入到等体积的锇酸中固定(使用与培养液相同盐度的海水配制锇酸溶液, 终浓度为2%), 固定时间为40—50min, 使用尼龙膜(孔径为20μm; 密理博, 科克, 爱尔兰)过滤并收集藻细胞, 然后用蒸馏水清洗三遍, 在不同浓度丙酮溶液(10%, 30%, 50%, 70%, 90%, 100%, 100%, 100%, 每个浓度处理15min)中脱水, 经CO2临界点干燥仪(型号EM CPD 300, 莱卡, 维也纳, 奥地利)干燥, 镀膜仪(型号EM ACE200, 莱卡, 维也纳, 奥地利)喷金, 使用扫描电子显微镜(型号S-3400N, 日立, 常陆那珂, 日本)观察藻细胞形态, 并使用电镜软件测量细胞大小。
1.5 透射电镜样品制备取一定体积处于对数生长期的藻液, 加入到戊二醛(终浓度为2.5%)中, 常温下固定3小时, 3000r/min离心, 去掉上清, 加入新鲜培养基清洗3遍, 收集藻细胞加入到4%的锇酸中固定, 终浓度为1%, 4℃过夜后, 3000r/min离心, 去掉上清, 加入新鲜培养基清洗3遍, 在不同浓度丙酮溶液(10%, 30%, 50%, 70%, 90%, 每个浓度处理10min)中脱水, 然后经100%丙酮脱水3次, 每次处理时间为15min。使用树脂包埋(Spurr Formula Kit I, The SPI Supplies Division of Structure Probe, Inc., 西切斯特, 美国; Spurr, 1969), 切片(型号EM UC7, 莱卡, 维也纳, 奥地利), 染色(醋酸铀和柠檬酸铅的终浓度分别为3%和2%), 使用透射电子显微镜(型号HT7700, 日立, 常陆那珂, 日本)观察藻细胞超微结构。
2 结果与分析 2.1 核糖体型的确定和系统进化分析通过正向引物D1R和反向引物28-1483R获得三株多环马格里夫藻的核糖体大亚基(LSU rDNA) D1—D6区, 中国株(MPJZBC3)、美国株(CP1)和马来西亚株(MPCoKK23)长度分别为1508、1522和1522bp。中国株(MPJZBC3)与美国株(CP1)和马来西亚株(MPCoKK23)的相似性均为93.6% (1426bp/1523bp), 美国株(CP1)和马来西亚株(MPCoKK23)的相似性为100% (1508bp/1508bp)。将所获得多环马格里夫藻中国株(MPJZBC3)、美国株(CP1)和马来西亚株(MPCoKK23)序列与GenBank中已报道的其他马格里夫藻的序列进行比较, 发现中国株(MPJZBC3)与GenBank中日本株(登录号AB288383)、韩国株(登录号KJ503268)、中国香港株(登录号EF506623)的相似性分别为100% (1508bp/1508bp)、100% (1226bp/1226bp)、100% (953bp/953bp), 而与波多黎各株(登录号AB295050)、马来西亚株(登录号AB295048)、美国株(登录号JX967271)、菲律宾株(登录号AB295046)、地中海株(登录号KC577590)和褐色马格里夫藻(登录号AB288382)的相似性分别为93.6% (1426bp/1523bp)、93.6% (1426bp/1523bp)、92.9% (1213bp/1306bp)、90.7% (925bp/1020bp)、97.9% (553bp/565bp)和91.9% (756bp/823bp)。由之可以基本判断中国株与日本、韩国种群的近缘性, 和地中海种群也有相对较近的亲缘关系。
用最大似然法(Maximum likelihood, ML)和贝叶斯法(Bayesian inference, BI)构建的系统发育树基本上一致(图 1)。从系统树上看, 不同地理来源的多环马格里夫藻聚在一起, 与褐色马格里夫藻形成姊妹支(图 1)。本研究中的中国株(MPJZBC3)和已报到的分离于日本、韩国及中国香港的藻株聚在一起, 且支持率为100%, 说明我们从胶州湾分离的中国株(MPJZBC3)属于东亚核糖体型; 美国株(CP1)和马来西亚株(MPCoKK23)和已报到的分离于美国、马来西亚、波多黎各、阿拉伯海湾等国家和地区的藻株聚在一起, 且支持率为100%, 说明这两株属于美国/马来西亚核糖体型(图 1)。
 |
| 图 1 基于核糖体大亚基序列所构建的多环马格里夫藻的系统发育树 Fig. 1 Phylogenetic tree of the Margalefidinium polykrikoides based on the large subunit rDNA sequences |
另外, 对中国株(MPJZBC3)、美国株(CP1)、马来西亚株(MPCoKK23)、波多黎各株(美国/马来西亚核糖体型)和日本株进行比对(alignment)发现, 中国株(MPJZBC3)和日本株的序列完全一样, 但与美国、马来西亚和波多黎各株比较, 共存在15个碱基的缺失(gap), 占整个可比较序列的1.1%, 这在同属不同种间是罕见的(图 2)。
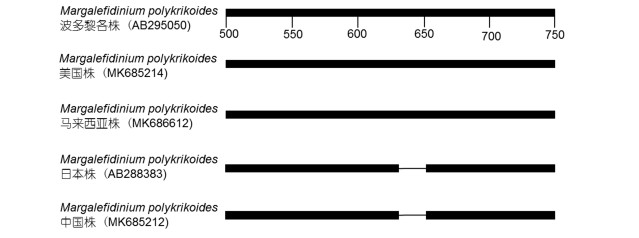 |
| 图 2 对五株多环马格里夫藻(AB295050, MK685214, MK686612, AB288383, MK685212)的部分大亚基核糖体序列的比对分析, 间隔区在638—652 Fig. 2 Alignment for the partial large subunit rDNA sequences of the five strains of Margalefidinium polykrikoides (AB295050, MK685214, MK686612, AB288383, MK685212), showing a gap of 638—652 |
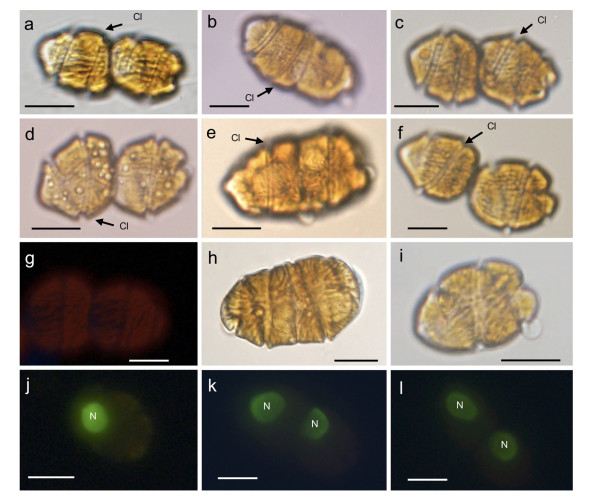
多环马格里夫藻中国株(MPJZBC3)单细胞的上锥呈圆锥形, 下锥近球形, 长为29.2—39.5μm [平均值(34.8±2.9)μm, n=50], 宽为21.8—32.8μm [平均值(27.1±2.2)μm, n=50](图 3, 图 4)。细胞腹面观可见横沟, 较纵沟宽且深, 横沟绕细胞1.5—2.0圈, 横鞭毛镶嵌在横沟当中(图 3a、3d, 图 4a、4d)。纵沟较横沟窄且浅, 在细胞上部与横沟平行, 纵鞭毛从细胞底部伸出(图 3a、3d, 图 4a、4d、4g)。叶绿体为杆状, 分散在整个细胞内(图 3a、3d、3g), 细胞核位于藻细胞的上锥(图 3j)。顶沟呈“U”形(图 4j)。美国株(CP1)单细胞的上锥呈圆锥形, 下锥近球形, 长为27.7—45.1μm [平均值(36.7±3.8)μm, n=50], 宽为22.4—36.9μm [平均值(29.0±3.4)μm, n=50](图 3, 图 4)。细胞横沟与纵沟的形态特征与中国株基本一致(图 3, 图 4)。叶绿体呈杆状(图 3b、3e、3h), 细胞核位于细胞的上锥(图 3k)。顶沟呈“U”形(图 4k)。马来西亚株(MPCoKK23)单细胞上锥呈圆锥形, 下锥近球形, 长为30.2—44.1μm [平均值(37.0±3.8)μm, n=50], 宽为23.5—35.4μm [平均值(29.8±3.1)μm, n=50](图 3和4)。叶绿体为杆状, 分散在整个细胞内(图 3c, 3f, 3i), 细胞核位于藻细胞的上锥(图 3l)。顶沟呈“U”型(4l)。
 |
|
图 3 光学和荧光显微镜下三株多环马格里夫藻(中国株、美国株和马来西亚株)的细胞形态 Fig. 3 Morphology of three strains of Margalefidinium polykrikoides (Chinese strain, American strain and Malaysian strain) under optical and fluorescence microscope. 注:从左至右依次为中国株(a、d、g和j)、美国株(b、e、h和k)和马来西亚株(c、f、i和l); a、b、c:细胞背面观, 横沟(CI, cingulum); d、e、f:细胞腹面观; g、h、i:细胞叶绿体; j、k、l:细胞核(N, nucleus)。比例尺: 20μm。 |
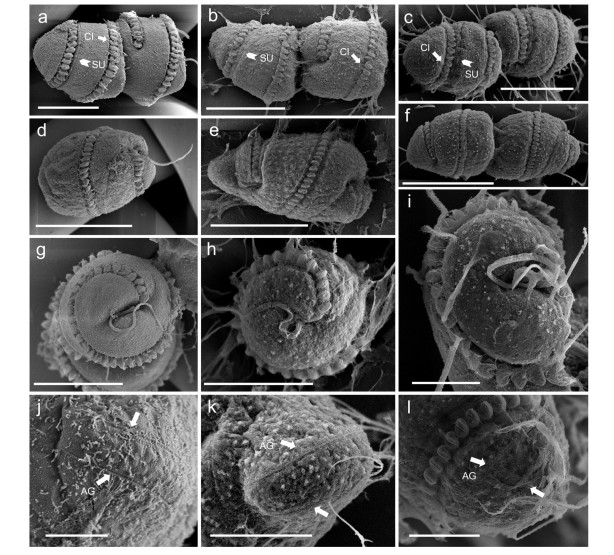 |
| 图 4 扫描电子显微镜下三株多环马格里夫藻(中国株、美国株、马来西亚株)的细胞形态 Fig. 4 Cell morphology of three strains of Margalefidinium polykrikoides (Chinese, American, and Malaysian strains) under scanning electron microscope. 注:从左至右依次为中国株(a、d、g和j)、美国株(b、e、h和k)和马来西亚株(c、f、i和l); a、b、c:细胞背面观, 横沟(CI, cingulum), 纵沟(SU, sulcus); d、e、f:细胞腹面观, 横沟(CI), 纵沟(SU); g、h、i:细胞底面观; j、k、l:细胞顶沟(AG, apical groove)。比例尺, a、g、h: 20μm; b、c、d、e: 30μm; f: 40μm; i、k、l: 10μm; j: 5μm。 |
通过透射电镜观察到多环马格里夫藻中国株(图 5a, 5d, 5g, 5j, 5m)、美国株(图 5b, 5e, 5h, 5k, 5n)和马来西亚株(图 5c, 5f, 5i, 5l, 5o)的胞内精细结构。三株多环马格里夫藻的细胞核均较大, 位于细胞的中上部(图 5a, 5b, 5c)。染色体较多, 呈高度浓缩状(图 5g, 5h, 5i)。叶绿体分布在整个细胞中, 呈杆状(图 5a, 5b, 5c), 常与淀粉核相连(图 5j, 5k, 5l), 叶绿体膜为三层(图 5m, 5n, 5o)。
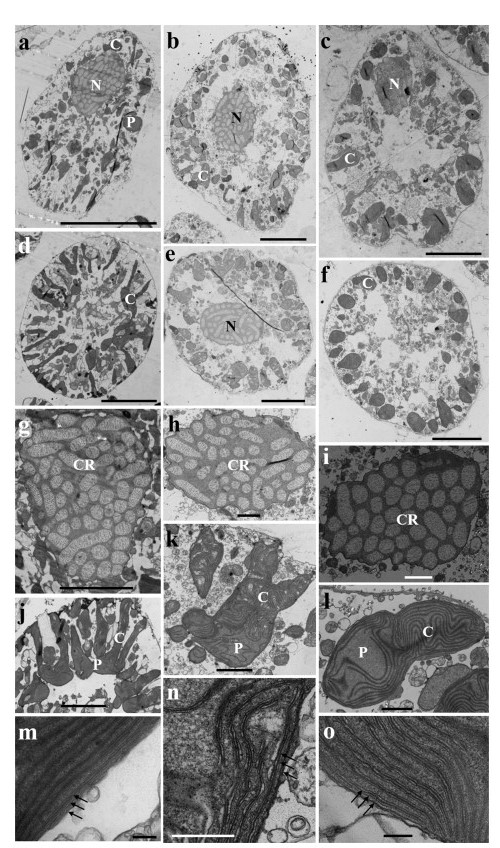 |
| 图 5 透射电子显微镜下三株多环马格里夫藻(中国株、美国株、马来西亚株)的细胞超微结构比较 Fig. 5 Ultrastructure of the three strains of Margalefidinium polykrikoides (Chinese, American and Malaysian strains) under transmission electron microscope. 注:从左至右依次为中国株(a、d、g、j和m)、美国株(b、e、h、k和n)和马来西亚株(c、f、i、l和o); a、b、c:细胞纵切面观, 细胞核(N, nucleus), 叶绿体(C, chloroplast)和淀粉核(P, pyrenoid); d、e、f:细胞横切面观; g、h、i:细胞核中染色体(CR, chromosome)的详细形态; j、k、l:叶绿体(C)和淀粉核(P)的详细形态; m、n、o:叶绿体膜的详细观察。比例尺, a、i: 20μm; b、c、d、e、f: 10μm; g、j: 5μm; h、k: 2μm; l: 1μm; m、o: 200nm; n: 500nm。 |
最近三十年来, 多环马格里夫藻是世界上扩散最为迅速的藻华原因种之一, 在多个国家和地区的沿海形成灾害性藻华, 因此也被认为是世界上最重要的几种藻华原因种之一(王朝晖等, 2011; Kudela et al, 2012; Tang et al, 2012)。在中国, 最早报道多环马格里夫藻藻华是1984年发生在香港吐露港, 随后1998年和2011年在香港南部及东南部水域都发生了几起(Law et al, 2013)。1990年, 福建沿海发生了一次旋沟藻藻华(Du et al, 1993), 但不能确定是多环马格里夫藻。2006年, 广东珠江口发生过几起多环马格里夫藻藻华(广东省海洋与渔业局, 2007), 但由于没有分子序列确证, 该鉴定可以存疑。2010年, 浙江温岭石塘海域首次报道了多环马格里夫藻藻华(余文翎等, 2011), 次年在浙江海域再次发生藻华(王红霞等, 2014)。2012年, 山东青岛浮山湾海域第一次报道了小规模旋沟藻藻华(自然资源部北海局, 2013)。2014年, 在江苏海州湾赤潮监控区发现多环马格里夫藻, 且已成为浮游植物群落中的优势种(生态环境部国家海洋环境监测中心赤潮监控区养殖环境质量通报2014年第8期)。2015年和2016年在渤海均有多环马格里夫藻藻华发生(自然资源部北海局, 2016; 自然资源部北海局, 2017)。综上所述可以看到, 多环马格里夫藻在我国表现出从南到北, 或者从南海到东海再到黄海直至渤海的扩散趋势。
Iwataki等(2008)和Reñé等(2013)将全世界报道的多环马格里夫藻种群基于核糖体大亚基基因序列分成了4种不同的核糖体型:东亚型、菲律宾型、美国/马来西亚型和地中海型。但是, 至今还没有发现不同核糖体型细胞之间可以清楚分辨的形态、表面结构或超微结构特征。从进化的一般规律来看, 同种不同地理种群在基因水平分化却在形态特征上没有平行分化是令人难以理解的。本文研究显示, 多环马格里夫藻中国株(MPJZBC3)与美国株(CP1)和马来西亚株(MPCoKK23)核糖体大亚基序列的相似性为93.6% (1426bp/1523bp), 且共存在15个碱基的间隔区(1.1%), 这在同属不同种之间也甚为罕见。如果仅仅按照目前广为接受的基于基因序列的分种“标准”(97%), 包含中国株的东亚核糖体型和美国/马来西亚核糖体型完全可以分成两个种, 但却缺乏形态学或其他保守性特征的支持。
本文对这两种核糖体型的三株藻详细表面形态和超微结构的比较发现:三株藻之间或者二种核糖体型之间在所有常用的具有分类学意义的细胞形态学和超微结构特征上, 如细胞大小、单细胞或群体及群体细胞数、上下锥形状、横沟位移度(绕细胞圈数)、纵沟形态、顶沟形态、细胞核位置与形状、染色体形状与数目、叶绿体的形状、结构、数目及分布、淀粉核形态等都没有发现明显可区分的差别。比如, 中国株、美国株、马来西亚株均可以单细胞或链状细胞存在, 单细胞大小(长、宽、长宽比)都各表现一定的变异范围, 但没有统计学意义上显著的差别, 与其他报道中的大小也基本一致(Matsuoka et al, 2008)。因此, 我们的结论是东亚核糖体型与美国/马来西亚核糖体型在形态特征上没有具判别性的差异。但是, Tang等(2012)在对美国株(即本研究中用到的同一个来源)纯培养的研究中发现其可以形成表面光滑、球形的休眠孢囊, 而Li等(2014)在韩国海域沉积物中分离、萌发的东亚核糖体型的多环马格里夫藻孢囊表面似有网状凸起。Thoha等(2015)在印度尼西亚澜沧湾多环马格里夫藻藻华区沉积物中找到了表面光滑的疑似多环马格里夫藻孢囊, 与Tang等(2012)报道的孢囊相似。最近, Thoha等(2019)又在印度尼西亚澜沧湾发现了三种形态的多环马格里夫藻孢囊, 分别与Matsuoka等(2000)、Tang等(2012)和Thoha等(2015)报道的三种类型的多环马格里夫藻孢囊一样。有意思的是, 他们从水体中分离的藻株通过测序分析确认属于美国/马来西亚核糖体型, 而沉积物中的孢囊则属于地中海核糖体型, 遗憾的是地中海核糖体型的孢囊却仅有分子信息, 没有孢囊图片从而不知其形态特征。由于现阶段孢囊的形态特征还没有被应用于种的分类, 而且这种差别也可能是由于实验室纯培养和野外沉积物环境的差别所造成。另外菲律宾核糖体型的种群是否形成孢囊尚未知, 故不同核糖体型多环马格里夫藻在孢囊形态特征上的差别需要进一步深入的研究。另外, 由于已有关于多环马格里夫藻有害藻华及毒性的研究主要来自东亚和美国/马来西亚核糖体型, 它们在毒性强弱、毒素种类上是否存在差异也还没有见到报道, 其他两种核糖体型的种群也尚未见到其毒性研究。最后, 东亚核糖体型和美国/马来西亚核糖体型都已经被证明可以产生休眠孢囊, 但不同核糖体型种群之间是否具有杂交相容性(sexual compatibility, 即是否可能通过有性交配形成合子并产生可育后代)也是值得进一步研究的方向。如果它们不能杂交且产生可育的后代, 则应该据此分类为不同的种。
4 结论基于系统进化、细胞表面形态和超微结构结果的分析, 本文从胶州湾分离的多环马格里夫藻属于东亚核糖体型, 采自美国纽约Paconic湾和马来西亚Kota Kinabalu海域的两株多环马格里夫藻均属于美国/马来西亚核糖体型, 中国株与美国株和马来西亚株碱基差异为97bp, 核糖体大亚基相似性为93.6%。多环马格里夫藻中国株与美国株和马来西亚株在所有常用的具有分类学意义的细胞形态学和超微结构特征上都没有发现明显可区分的差别。因此, 我们认为应该在生活史、休眠孢囊形态和生理学特征(如毒素种类及毒性强弱)以及性别相容性或杂交相容性等方面开展进一步比较研究, 以获得对不同核糖体型种群的识别性状。在现阶段有害藻华的野外监测中, 尤其是对于不同核糖体型种群可能造成的生物入侵的监测和追溯, 多环马格里夫藻的鉴定尚必须以核糖体基因序列作为可靠的判决依据。
广东省海洋与渔业局, 2007. 2006年广东省海洋环境质量公报. http://zwgk.gd.gov.cn/006941338/201706/t20170612_708821.html
|
王红霞, 陆斗定, 何飘霞, 等. 2014. 东海多环旋沟藻的形态特征和系统进化分析. 海洋与湖沼, 45(4): 757-763 |
王朝晖, 林朗聪, 康伟, 等. 2011. 有毒有害赤潮藻类旋沟藻(Cochlodinium Schütt)研究进展. 暨南大学学报(自然科学与医学版), 32(1): 109-114 DOI:10.3969/j.issn.1000-9965.2011.01.023 |
余文翎, 龙华, 王红霞, 等. 2011. 我国东海藻华新记录种多环旋沟藻赤潮事件分析. 海洋开发与管理, 28(11): 66-68, 123 DOI:10.3969/j.issn.1005-9857.2011.11.019 |
自然资源部北海局, 2013. 2012年北海区海洋灾害公报. ncs.mnr.gov.cn/n1/upload/180207171729487214/180207173258328778.PDF
|
自然资源部北海局, 2016. 2015年北海区海洋灾害公报. ncs.mnr.gov.cn/n1/upload/180207171729440628/180207172932626510.PDF
|
自然资源部北海局, 2017. 2016年北海区海洋灾害公报. ncs.mnr.gov.cn/n1/upload/180207171729424158/180207172142394444.PDF
|
生态环境部国家海洋环境监测中心赤潮监控区养殖环境质量通报2014年第8期. http://www.chmem.cn/res_base/mem_gov_www/upload/article/image/2014_3/9_5/2014-8.pdf
|
Amato A, Montresor M, 2008. Morphology, phylogeny, and sexual cycle of Pseudo-nitzschia mannii sp. nov. (Bacillariophyceae): a pseudo-cryptic species within the P. pseudodelicatissima complex. Phycologia, 47(5): 487-497 DOI:10.2216/07-92.1 |
Darriba D, Taboada G L, Doallo R et al, 2012. jModelTest 2: more models, new heuristics and parallel computing. Nature Methods, 9(8): 772 |
Daugbjerg N, Hansen G, Larsen J et al, 2000. Phylogeny of some of the major genera of dinoflagellates based on ultrastructure and partial LSU rDNA sequence data, including the erection of three new genera of unarmoured dinoflagellates. Phycologia, 39(4): 302-317 DOI:10.2216/i0031-8884-39-4-302.1 |
Du Q, Huang Y, Wang X, 1993. Toxic dinoflagellate red tide by a Cochlodinium sp. along the coast of Fujian, China. In: Smayda T J, Shimizu Y eds. Toxic Phytoplankton Blooms in the Sea. New York: Elsevier, 235-238
|
Gobler C J, Berry D L, Anderson O R et al, 2008. Characterization, dynamics, and ecological impacts of harmful Cochlodinium polykrikoides blooms on eastern Long Island, NY, USA. Harmful Algae, 7(3): 293-307 DOI:10.1016/j.hal.2007.12.006 |
Gómez F A, 2012. Checklist and classification of living dinoflagellates (Dinoflagellata, Alveolata). CICIMAR Oceánides, 27(1): 65-140 |
Gómez F, Richlen M L, Anderson D M, 2017. Molecular characterization and morphology of Cochlodinium strangulatum, the type species of Cochlodinium, and Margalefidinium gen. nov. for C. polykrikoides and allied species (Gymnodiniales, Dinophyceae). Harmful Algae, 63: 32-44 DOI:10.1016/j.hal.2017.01.008 |
Guillard R R L, 1975. Culture of phytoplankton for feeding marine invertebrates. In: Smith W L, Chanley M H eds. Culture of Marine Invertebrate Animals. Boston: Springer, 29-60
|
Guindon S, 2010. Bayesian estimation of divergence times from large sequence alignments. Molecular Biology and Evolution, 27(8): 1768-1781 DOI:10.1093/molbev/msq060 |
Guindon S, Gascuel O, 2003. A simple, fast, and accurate algorithm to estimate large phylogenies by maximum likelihood. Systematic Biology, 52(5): 696-704 DOI:10.1080/10635150390235520 |
Iwataki M, Hansen G, Moestrup Ø et al, 2010. Ultrastructure of the harmful unarmored dinoflagellate Cochlodinium polykrikoides (Dinophyceae) with reference to the apical groove and flagellar apparatus. Journal of Eukaryotic Microbiology, 57(4): 308-321 DOI:10.1111/j.1550-7408.2010.00491.x |
Iwataki M, Kawami H, Matsuoka K, 2007. Cochlodinium fulvescens sp. nov. (Gymnodiniales, Dinophyceae), a new chain-forming unarmored dinoflagellate from Asian coasts. Phycological Research, 55(3): 231-239 DOI:10.1111/j.1440-1835.2007.00466.x |
Iwataki M, Kawami H, Mizushima K et al, 2008. Phylogenetic relationships in the harmful dinoflagellate Cochlodinium polykrikoides (Gymnodiniales, Dinophyceae) inferred from LSU rDNA sequences. Harmful Algae, 7(3): 271-277 DOI:10.1016/j.hal.2007.12.003 |
Iwataki M, Takayama H, Takahashi K et al, 2015. Taxonomy and Distribution of the unarmored dinoflagellates Cochlodinium polykrikoides and C. fulvescens. In Marine Protists. Springer Japan, 551-565
|
Jiang X D, Tang Y Z, Lonsdale D J et al, 2009. Deleterious consequences of a red tide dinoflagellate Cochlodinium polykrikoides for the calanoid copepod Acartia tonsa. Marine Ecology Progress Series, 390: 105-116 DOI:10.3354/meps08159 |
Katoh K, Misawa K, Kuma K I et al, 2002. MAFFT: a novel method for rapid multiple sequence alignment based on fast Fourier transform. Nucleic Acids Research, 30(14): 3059-3066 DOI:10.1093/nar/gkf436 |
Kim C S, Lee S G, Lee C K et al, 1999. Reactive oxygen species as causative agents in the ichthyotoxicity of the red tide dinoflagellate Cochlodinium polykrikoides. Journal of Plankton Research, 21(11): 2105-2115 DOI:10.1093/plankt/21.11.2105 |
Kim H G, Lee S G, An K H et al, 1997. Recent red tides in Korean coastal waters. Pusan: National Fisheries Research and Development Agency, 237-239
|
Kofoid C A, Swezy O, 1921. The free-living unarmored Dinoflagellata. Memoirs of the University of California, 5: 1-564 |
Kudela R M, Gobler C J, 2012. Harmful dinoflagellate blooms caused by Cochlodinium sp.: global expansion and ecological strategies facilitating bloom formation. Harmful Algae, 14: 71-86 DOI:10.1016/j.hal.2011.10.015 |
Law P C, Lee Y K, 2013. Harmful marine microalgae in Hong Kong. Hong Kong, China: Agriculture, Fisheries and Conservation Department, the Government of the Hong Kong Special Administrative Region, 47
|
Li Z, Han M S, Matsuoka K et al, 2015. Identification of the resting cyst of Cochlodinium polykrikoides Margalef (Dinophyceae, Gymnodiniales) in Korean coastal sediments. Journal of Phycology, 51: 204-210 DOI:10.1111/jpy.12252 |
Margalef R, 1961. Hidrografía y fitoplancton de un área marina de la costa meridional de Puerto Rico. Invest Pesq, 18: 33-96 |
Matsuoka K, Iwataki M, Kawami H, 2008. Morphology and taxonomy of chain-forming species of the genus Cochlodinium (Dinophyceae). Harmful Algae, 7(3): 261-270 DOI:10.1016/j.hal.2007.12.002 |
National Fisheries Research & Development Institute (NFRDI), 2012. Monitoring, Management and Mitigation of Red Tide. Annual report of NFRDI on red tide of Korea, Busan, Korea (written in Korean).
|
National Fisheries Research & Development Institute (NFRDI), 2014. Monitoring, Management and Mitigation of Red Tide. Annual report of NFRDI on red tide of Korea, Busan, Korea (written in Korean).
|
Rambaut A, 2018. FigTree v1.4.4. http://tree.bio.ed.ac.uk/software/figtree/Reñé A, Camp J, Garcés E, 2015. Diversity and phylogeny of Gymnodiniales (Dinophyceae) from the NW Mediterranean Sea revealed by a morphological and molecular approach. Protist, 166(2): 234-263
|
Reñé A, Garcés E, Camp J, 2013. Phylogenetic relationships of Cochlodinium polykrikoides Margalef (Gymnodiniales, Dinophyceae) from the Mediterranean Sea and the implications of its global biogeography. Harmful Algae, 25: 39-46 DOI:10.1016/j.hal.2013.02.004 |
Richlen M L, Morton S L, Jamali E A et al, 2010. The catastrophic 2008-2009 red tide in the Arabian gulf region, with observations on the identification and phylogeny of the fish-killing dinoflagellate Cochlodinium polykrikoides. Harmful Algae, 9(2): 163-172 DOI:10.1016/j.hal.2009.08.013 |
Ronquist F, Huelsenbeck J P, 2003. MrBayes 3: bayesian phylogenetic inference under mixed models. Bioinformatics, 19(12): 1572-1574 DOI:10.1093/bioinformatics/btg180 |
Rountos K J, Tang Y Z, Cerrato R M et al, 2014. Toxicity of the harmful dinoflagellate Cochlodinium polykrikoides to early life stages of three estuarine forage fish. Marine Ecology Progress Series, 505: 81-94 DOI:10.3354/meps10793 |
Scholin C A, Herzog M, Sogin M et al, 1994. . Identification of group- and strain-specific genetic markers for globally distributed Alexandrium (Dinophyceae). Ⅱ. sequence analysis of a fragment of the LSU rRNA gene. Journal of Phycology, 30(6): 999-1011 DOI:10.1111/j.0022-3646.1994.00999.x |
Schütt F, 1896. Bacillariales (diatomeae). In: Engler A, Prantl K eds. Die Naturlichen Pflanzenfamilien. Leipzig: Engelmann, 31-153
|
Tan T H, Leaw C P, Leong S C Y et al, 2016. Marine micro-phytoplankton of Singapore, with a review of harmful microalgae in the region. Raffles Bulletin of Zoology, 34: 78-96 |
Tang Y Z, Gobler C J, 2009. Characterization of the toxicity of Cochlodinium polykrikoides isolates from Northeast US estuaries to finfish and shellfish. Harmful Algae, 8(3): 454-462 DOI:10.1016/j.hal.2008.10.001 |
Tang Y Z, Gobler C J, 2012. The toxic dinoflagellate Cochlodinium polykrikoides (Dinophyceae) produces resting cysts. Harmful Algae, 20: 71-80 DOI:10.1016/j.hal.2012.08.001 |
Thoha H, Muawanah, Bayu Intan M D et al, 2019. Resting cyst distribution and molecular identification of the harmful dinoflagellate Margalefidinium polykrikoides (Gymnodiniales, Dinophyceae) in Lampung Bay, Sumatra, Indonesia. Frontiers in Microbiology, 10: 306 DOI:10.3389/fmicb.2019.00306 |
Thoha H, Rachman A, Sidabutar T et al, 2015. First record of the harmful dinoflagellate Cochlodinium polykrikoides in Lampung Bay, Indonesia. Harmful Algae News, 50: 14-15 |
Tomas C R, Smayda T J, 2008. Red tide blooms of Cochlodinium polykrikoides in a coastal cove. Harmful Algae, 7(3): 308-317 DOI:10.1016/j.hal.2007.12.005 |
Yuki K, Yoshimatsu S, 1989. Two fish-killing species of Cochlodinium from Harima-Nada, Seto Inland Sea, Japan. In: Okaichi T, Anderson D M, Nemoto T eds. Red Tides: Biology, Environmental Science, and Toxicology. New York: Elsevier, 451-454
|
 2019, Vol. 50
2019, Vol. 50


