中国海洋湖沼学会主办。
文章信息
- 祁梅, 吴嘉伟, 龚森森, 柴毅, 罗静波, 谭凤霞, 杨军, 杨德国, 何勇凤. 2020.
- QI Mei, WU Jia-Wei, GONG Sen-Sen, CHAI Yi, LUO Jing-Bo, TAN Feng-Xia, YANG Jun, YANG De-Guo, HE Yong-Feng. 2020.
- 长湖浮游植物功能群特征及其与环境因子的关系
- RELATIONSHIP BETWEEN CHARACTERISTICS OF PHYTOPLANKTON FUNCTIONAL GROUPS AND THEIR ENVIRONMENTAL FACTORS IN CHANGHU LAKE
- 海洋与湖沼, 51(1): 75-84
- Oceanologia et Limnologia Sinica, 51(1): 75-84.
- http://dx.doi.org/10.11693/hyhz20190700150
文章历史
-
收稿日期:2019-07-30
收修改稿日期:2019-11-22
2. 长江大学湿地生态与农业利用教育部工程研究中心 荆州 434025;
3. 中国水产科学研究院长江水产研究所 农业部淡水生物多样性保护重点实验室 武汉 430223
2. Engineering Research Center of Wetland Ecology and Agricultural Utilization, Ministry of Education, Changjiang University, Jingzhou 434025, China;
3. Yangtze River Fisheries Research Institute, Chinese Academy of Fishery Sciences; Key Laboratory of Freshwater Biodiversity Conservation, Ministry of Agriculture, Wuhan 430223, China
浮游植物(phytoplankton)是水域生态系统中初级生产者的主要组成部分, 同时作为水域环境监测评价的重要生物指标已被广泛认可(刘建康, 1999)。浮游植物功能群(functional group)是将依据形态学、生理学和生态学特征分组, 每组物种有相同或相近的生态位且对应为特定的生境类型。功能群的划分及其结构特征能够客观表达浮游植物对所在生境的适应性, 也反映了该物种所在生态系统的功能特征, 具有积极的生态学意义(Reynolds et al, 2002; 胡韧等, 2015)。国外相关研究从水库和湖泊发展到河流以及激流生态系统等水体环境质量评价并在此基础上提出了浮游植物生境模板概念(Becker et al, 2010; Costa et al, 2009; Stanković et al, 2012; Qu et al, 2019; Stankovićet al, 2012)。我国现阶段的研究主要集中在浮游植物功能群的演替特征及水质评价等方面, 其中淡水生态系统以典型富营养化内陆湖泊为主(汪星等, 2016; 王徐林等, 2018; 钱奎梅等, 2019), 海洋生态系统也有相关报道(Lin L et al, 2018)。
长湖是湖北省第三大天然淡水湖泊, 是长江中游地区生态平衡的重要湿地生态系统, 2010年农业部批准在长湖建立鮊类种质资源保护区。同我国大多数内陆浅水湖泊一样, 富营养化也是长湖面临的最主要的生态环境问题, 多项研究结果显示, 长湖鱼类资源呈衰退状态, 优势鱼类有小型化趋势, 高等水生植物多样性降低, 浮游动物各季节优势种单一, 局部区域处于重度富营养化(刘建峰等, 2014; 何勇凤等, 2015; 周淼等, 2016; 郭坤等, 2017)。目前围绕长湖浮游植物的相关研究主要集中在群落结构特征及生态位等方面(柴毅等, 2014; 郭坤等, 2016; 魏志兵等, 2019; Guo et al, 2019), 主要通过浮游植物的种类组成、丰度、生物量以及优势种等指标对进行水质评价, 而这种常规传统科属分类方法存在一定的局限性(胡韧等, 2015)。浮游植物功能群可以从物种的功能性更精确地反映出与环境因子的相关性, 进而预测水域生态系统发展趋势。本研究首次通过功能群概念对长湖浮游植物进行划分并阐明其季节演替规律, 分析优势功能群在不同季节与环境因子的关系, 以期为长湖水环境保护和生态系统修复以及未来可持续发展利用提供科学参考依据。
1 材料与方法 1.1 研究区域概况长湖地处长江和汉江之间(30.37°—30.53°N, 112.25°—112.50°E), 为亚热带湿润性气候, 光照充足, 平均水深2.1m (刘建峰等, 2014)。图 1所示整个长湖自西向东可分为庙湖、海子湖、马洪台以及圆心湖共4个湖区(各区域以虚线隔开)。由于引江济汉工程的建设, 庙湖大部分面积已被两条堤坝(图 1中实线表示)拦截形成静水, 故未在此区域设置采样点。
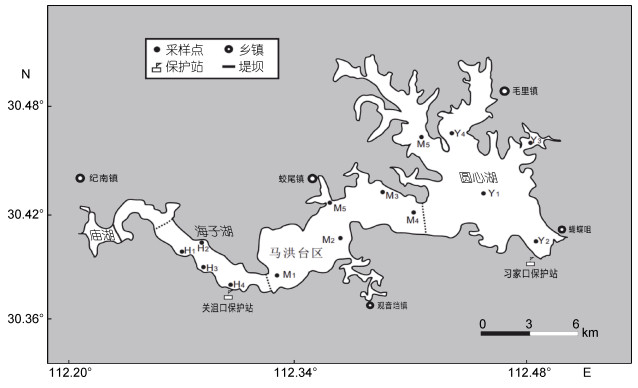 |
| 图 1 长湖采样点示意图 Fig. 1 The sampling sites in Changhu Lake |
参照《水域生态系统观测规范》(中国生态系统研究网络科学委员会, 2007)并根据长湖实际水域形态、进出水口以及水文特征共设置14个采样点(图 1), 其中海子湖(H1、H2、H3、H4)4个、马洪台(M1、M2、M3、M4、M5)5个以及圆心湖(Y1、Y2、Y3、Y4、Y5)5个, 分别于2015年4月(春季)、7月(夏季)、11月(秋季)和2016年1月(冬季)进行采样。
1.3 实验采集与分析浮游植物定性样本使用25号浮游生物网(网目直径0.064mm)在距水体表层0.5m处采集, 用4%甲醛固定后带回实验室进行种类鉴定。定量样本使用有机玻璃采水器(1.0L)在表层至0.5m处和距底层0.5m处各采样一次, 充分混均后取1.0L加入15.0mL鲁哥氏液, 带回实验室后经沉淀、浓缩至30—50mL后进行定量计数。使用光学显微镜(XSM-20, 宁波舜宇仪器有限公司, 宁波, 浙江)进行种类鉴定和计数(胡鸿钧等, 2006; 赵文, 2016), 所有种类鉴定到种。藻类生物量(B)采用细胞近似体积公式法推算(Hillebrand et al, 1999)。
使用多参数水质分析仪(HQ40D, Hach Loveland, 美国)现场测定溶解氧(DO)、pH值和水温(WT), 使用塞氏盘测定透明度(WD)和水深(SD)。总悬浮物(TSS)、磷酸盐(
某一功能群在其采样点相对生物量占比在5%以上即为优势功能群(黄享辉等, 2013)。藻类丰度(D)和生物量(B)评价水质参照湖泊营养评价标准与藻类生物学评价标准(况琪军等, 2005)。
1.5 功能群划分浮游植物功能群的划分依据参考Reynolds (Reynolds et al, 2002)提出的Functional Group(FG)分类方法, 目前公认的FG已达38个(Padisák et al, 2009), FG功能群对解释水体与浮游植物群落结构之间的联系可信度最高(胡韧等, 2015)。
1.6 数据分析冗余分析(redundancy analysis, RDA)主要是分析不同物种对环境的需求, 再现物种分布与其生态环境的内在关系。其分析结果用物种—环境因子关系双序图表示, 带箭头射线代表环境因子, 箭头所在坐标代表该环境因子与排序轴的相关系数的大小, 箭头所指方向为变化趋势。物种代表点垂直投影到环境因子射线上, 投影点在箭头方向上为正相关, 在反向延长线上则为负相关。
功能群与环境因子的多元分析使用R语言软件vegan包进行分析, 浮游植物优势功能群丰度进行lg(x+1)转换处理, 首先对每个季节优势功能群进行除趋势对应分析(divide trend correspondence analysis, DCA), 根据Lengths of gradient第一轴大小选择合适的排序和分析方法, 进行分析作图。本文选用了冗余分析, 并采用蒙特卡洛置换检验, 以逐步迭代的方式筛选出有显著解释性的环境因子, 进行分析作图, 本文其他分析和作图在R_V3.4.3与Excel 2003中完成。
2 结果与分析 2.1 浮游植物种类组成及功能群的划分此次调查共鉴定出浮游植物7门78种(表 1), 绿藻门种类最多(46种, 占比58.97%), 其次为硅藻门和蓝藻门各12种, 占比15.38%。本次调查共鉴定出26个功能群, 其中富营养化水体代表性功能群13个(F、G、H1、J、K、Lo、Lr、M、Tc、W1、W2、X1、X2)。种类组成和所对应的生境特征见表 1, 其中代表种类较多的功能群有J (19种)、X1 (10种)和MP (6种)。
| 功能群(FG) | 种类 | 生境特征 |
| B | 扭曲小环藻Cyclotella comta | 中小型中营养湖泊 |
| 线性菱形藻Nitzschia linearis W. Smith | 浑浊的浅水水体 | |
| 肘状针杆藻Synedra ulna | ||
| D | 窗格平板藻Tabellaria fenestrata | |
| 二角盘星藻Pediastrum duplex | ||
| 被甲栅藻Scenedesmus armatus | ||
| E | 分歧锥囊藻Dinobryon divergensImh | 小型浅水中营养湖泊 |
| 蹄形藻Kirchneriella lunaris | 混合充分、清澈或富营养型湖泊 | |
| F | 月牙藻Selenastrum bibraianum | |
| 椭圆卵囊藻Oocystis elliptica | ||
| G | 空球藻Eudorina elegans | 水体中营养富集的停滞水层 |
| 实球藻Pandorina morum | ||
| H1 | 螺旋鱼腥藻Anabaena spiroides Lemm. | 氮含量低的富营养湖泊 |
| 湖泊伪鱼腥藻Pseudanabaena limnetica Lemm. Komarek | ||
| 双星藻Zygnema | 浅型混合高富集水体 | |
| 华丽四星藻Tetrastrum elegans | ||
| 集星藻Actinastrum hantzschii | ||
| 尖细栅藻Scenedesmus acuminatus | ||
| 二形栅藻Scenedesmus dimorphus | ||
| 粗刺四棘藻Treubaria crssispinaa | ||
| 短刺四星藻Tenadeam staurogeniaefome | ||
| 三角四角藻Tetraedron trigonum | ||
| 空星藻Coelastrum sphaericum | ||
| J | 双列栅藻Scenedesmus bijuga | |
| 四刺顶棘藻Chodatella quadriseta | ||
| 粗刺四棘藻Treubaria crssispinaa | ||
| 四角盘星藻Pediastrum tetras | ||
| 四角十字藻Crucigenia quadrata | ||
| 三叶四角藻Tetraedron trilobulatum | ||
| 四尾栅藻Scenedesmus quadricauda | ||
| 四足十字藻Crucigenia tetrapedia | ||
| 弯曲栅藻Scenedesmus arcuatus | ||
| 斜生栅藻Scenedesmus obliquus | ||
| K | 溪生隐球藻Aphanocapsa rivularis Rabenh. | 营养物质丰富的浅水水体 |
| Lo | 通等片藻Diatoma vnlagare Bory | 寡营养型到富营养型、大型到中型、深水型到浅水型湖泊 |
| 裸甲藻Gymnodinium aeruginosum | ||
| 微小平裂藻Merismopedia tenuissima | ||
| 水华微囊藻Microcystis flos-aquae | ||
| Lr | 颗粒直链藻Melosira.granulata | 水体强烈和持续扰动的富营养水库 |
| M | 铜绿微囊藻Microcystis aeruginosa | 富营养型到高度富营养型、小型到中型水体 |
| MP | 尖异极藻Gomphonema acuminatum | 经常受到搅动的、无机的、浑浊的浅水湖泊 |
| 近缘桥弯藻Gomphonema affinis | ||
| 扁圆舟形藻Navicula placentula | ||
| 缢缩异极藻Gomphonema constrictum | ||
| 两栖颤藻Oscillatoria amphibia | ||
| 细丝藻Ulothrix tenerrima Kutz | ||
| N | 美丽鼓藻Cosmarium formosulum | 浅水湖泊, 中营养性 |
| NA | 纤细角星鼓藻Staurastrum gracile Ralfs | 中度营养化的水体, 对水体变温敏感 |
| 梅尼鼓藻Cosmarium meneghinii | ||
| P | 反曲新月藻Closterium sigmoideum | 浅水湖泊, 中上营养性 |
| S1 | 鞘丝藻Lyugba contarata | 均匀浑浊水体, 适应暗环境的蓝藻 |
| S2 | 螺旋藻Spirulina.major | 温暖的、浅的、中碱度的水体 |
| Sn | 类颤鱼腥藻Anabaena oscillarioide | 温暖的混合的水体 |
| 中华小尖头藻Raphidiopsis sinensia | ||
| Tc | 小席藻Phormidium tenus Gom | 富营养化静止水体, 水流速度慢、大型挺水植物密集的河流 |
| W1 | 尾裸藻Euglena caudata Hubn | 富集有机质或临时形成的水体 |
| 旋形扁裸藻Phacus helicoides | ||
| W2 | 细粒囊裸藻Trachelomonas granulota Playf | 中型到富营养型池塘, 浅水湖泊 |
| Ws | 树状黄管藻Tribonema arbuscula | 非酸性的、腐殖质丰富的池塘 |
| 拟丝状黄丝藻Tribonema ulothrichoides | ||
| X1 | 镰形纤维藻Ankistrodesmus falcatus | 富营养和高度富营养型的浅水水体 |
| 镰形纤维藻变种Ankistrodesmus falcatus | ||
| 螺旋纤维藻Ankistrodesmus spiralis | ||
| 卷曲纤维藻Ankistrodesmus convolutes | ||
| 镰形纤维藻奇异变种Ankistrodesmus falcatus var mirabilis | ||
| 鞘藻Oedogonium | ||
| 狭形纤维藻Ankistrodesmus angustus | ||
| 纤维藻Ankistrodesmus | ||
| 小球藻Chlorella vulgaris | ||
| 针形纤维藻Ankistrodesmus acicularis | ||
| X2 | 简单衣藻Chlamydomonas simplex | 中营养和富营养型的浅水水体 |
| 长绿梭藻Chlorogonium elongaturn | ||
| 小球衣藻Chlamydomonas microsphaera Pasch | ||
| X3 | 细布纹藻Gyrosigma kutzingli Cl. | 充分混合的中营养浅水水体 |
| 弓形藻Schroederia setigera | ||
| 螺旋弓形藻Schroederia spiralis | ||
| Y | 扁圆卵形藻Cocconeis placentula Ehr. | 牧食强度低的静水水体 |
| 二角多甲藻Peridinium bipes |
本次调查共鉴定出16个优势功能群(表 2), 其中B、D、J、Lo、MP、W1和X1是四季共有优势功能群。以最大相对丰度超过50%为评价指标, 优势功能群的季节演替规律为X1/X2/B(春)→X1(夏)→MP/X1/ B(秋)→D/X1(冬)。优势功能群的丰度变化范围为0.008×106—11.16×106ind./L, 呈现夏 > 春 > 秋 > 冬的变化趋势。总生物量呈现夏(12.1mg/L) > 春(5.8mg/L) > 冬(3.1mg/L) > 秋(1.9mg/L)变化趋势, 其中典型浅水富营养化水体代表功能群X1在四季的最大相对丰度(57.39%—70.26%)和出现频率(85.71%—100%)均较高, 夏季出现的主要是蓝藻门类群, MP和W1的生物量占比均超过30%。
| 季节 | 优势功能群 | 出现频率(%) | 丰度(×106ind./L) | 相对丰度max (%) | 生物量(mg/L) | 生物量占比(%) |
| 春 | B | 64.29 | 1.59 | 59.61 | 0.79 | 13.66 |
| D | 14.29 | 0.22 | 32.57 | 0.94 | 16.23 | |
| H1 | 14.29 | 0.08 | 10.67 | 0.02 | 0.28 | |
| J | 64.29 | 0.55 | 24.54 | 0.06 | 0.96 | |
| Lo | 28.57 | 0.16 | 7.14 | 0.01 | 0.13 | |
| Lr | 28.57 | 0.36 | 21.51 | 0.64 | 11.04 | |
| MP | 14.29 | 0.10 | 19.88 | 0.11 | 1.94 | |
| N | 7.14 | 0.01 | 7.92 | 0.01 | 0.17 | |
| Sn | 14.29 | 0.12 | 34.07 | 0.005 | 0.08 | |
| W1 | 57.14 | 0.59 | 33.69 | 2.34 | 40.27 | |
| X1 | 85.71 | 1.28 | 67.95 | 0.08 | 1.34 | |
| X2 | 14.29 | 0.55 | 66.64 | 0.27 | 4.70 | |
| Y | 7.14 | 0.06 | 5.97 | 0.51 | 8.74 | |
| 夏 | B | 50.00 | 3.14 | 30.71 | 1.57 | 12.96 |
| D | 7.14 | 0.56 | 5.15 | 1.13 | 9.32 | |
| J | 71.43 | 2.07 | 21.99 | 0.27 | 2.21 | |
| Lo | 85.71 | 1.91 | 12.39 | 0.05 | 0.42 | |
| MP | 71.43 | 3.77 | 41.00 | 3.72 | 30.65 | |
| Sn | 35.71 | 1.98 | 48.03 | 0.05 | 0.41 | |
| W1 | 35.71 | 1.01 | 9.54 | 4.01 | 33.08 | |
| X1 | 100.00 | 11.16 | 70.26 | 0.35 | 2.91 | |
| 秋 | B | 85.71 | 0.57 | 52.57 | 0.29 | 14.73 |
| D | 64.29 | 0.36 | 21.39 | 1.07 | 55.16 | |
| J | 85.71 | 0.31 | 14.67 | 0.03 | 1.56 | |
| Lo | 78.57 | 0.40 | 27.27 | 0.01 | 0.57 | |
| Lr | 7.14 | 0.05 | 5.21 | 0.08 | 4.34 | |
| MP | 28.57 | 0.26 | 79.24 | 0.27 | 14.09 | |
| Sn | 14.29 | 0.12 | 6.96 | 0.003 | 0.16 | |
| W1 | 92.86 | 0.87 | 49.28 | 0.04 | 2.23 | |
| X1 | 85.71 | 1.40 | 67.53 | 0.07 | 3.74 | |
| X2 | 7.14 | 0.04 | 5.78 | 0.03 | 1.55 | |
| 冬 | B | 42.86 | 0.19 | 29.10 | 0.09 | 3.06 |
| D | 71.43 | 0.13 | 59.53 | 0.43 | 14.17 | |
| E | 14.29 | 0.02 | 25.01 | 0.02 | 0.64 | |
| F | 7.14 | 0.02 | 11.31 | 8×10–5 | 0.00 | |
| J | 50.00 | 0.07 | 37.50 | 0.01 | 0.36 | |
| K | 7.14 | 0.008 | 5.49 | 5×10–5 | 0.00 | |
| Lo | 7.14 | 0.034 | 7.10 | 0.02 | 0.63 | |
| MP | 28.57 | 0.06 | 14.54 | 0.06 | 2.08 | |
| W1 | 78.57 | 0.23 | 31.03 | 0.93 | 30.37 | |
| X1 | 100.00 | 0.47 | 57.39 | 0.03 | 0.86 | |
| X2 | 42.86 | 0.08 | 17.78 | 0.04 | 1.32 | |
| Y | 35.71 | 0.15 | 39.57 | 1.37 | 44.54 | |
| 注:表中丰度代表各季节所有采样点某功能群丰度的平均值, 相对丰度max是所有采样点某功能群丰度与所在采样点总丰度的比值取最大值。 | ||||||
先对浮游植物功能群生物量数据进行除趋势对应分析(DCA), pH值以外的所有理化数据进行lg(x+1)转换, 四个季节排序轴梯度长度最大值为2.522, 因此选择线性模型RDA。RDA分析相关系数如表 3所示, 各个季节轴1、轴2的特征值累积解释变量分别是49.54%、70.39%、77.01%、63.27%, 累计解释率为92%、88%、98%、94%, 表明排序能较好地反映功能群与环境因子的关系。
| 季节 | RDA1、RDA2特征值 | 解释比例(%) | 约束轴与非约束轴比例(%) | 累计解释百分比(%) |
| 春 | 0.062 | 0.30 | 0.92 | 49.54 |
| 0.039 | 0.19 | 0.08 | ||
| 夏 | 0.023 | 0.49 | 0.88 | 70.39 |
| 0.010 | 0.21 | 0.13 | ||
| 秋 | 0.036 | 0.45 | 0.98 | 77.01 |
| 0.026 | 0.32 | 0.03 | ||
| 冬 | 0.061 | 0.39 | 0.94 | 63.27 |
| 0.037 | 0.24 | 0.06 |
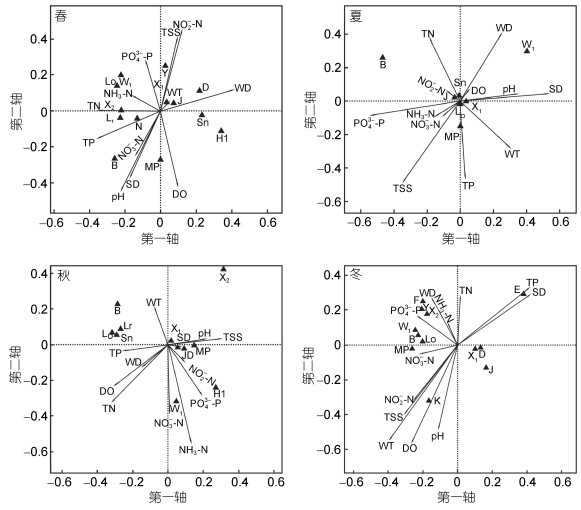
浮游植物优势功能群与环境因子的RDA分析如图 2所示, 春季优势功能群X2与总氮(TN)、N与总磷(TP)以及Y与总悬浮物(TSS)表现出较强的正相关性, 夏季优势功能群MP与总磷(TP)有较明显的正相关性, 秋季优势功能群B、Lr、Lo、Sn与水温(WT)处在同一象限, 表现出不同程度的正相关, W1与氨氮(NH3-N)和硝酸盐氮(
 |
|
图 2 长湖四季浮游植物优势功能群与环境因子RDA图 Fig. 2 RDA diagram of phytoplankton dominant functional groups and environmental factors in the four seasons of Changhu Lake 注: ▲代表功能群, 其中B、D、E、F、H1、J、K、Lo、Lr、MP、N、Sn、W1、X1、X2、Y分别代表优势功能群类别(表 1) ↑代表环境因子相关性, 溶解氧(DO)、pH值、水温(WT)、透明度(WD)、水深(SD)、总悬浮物(TSS)、磷酸盐( |
浮游植物的种类组成、丰度和分布等群落结果特征以及功能群划分对水环境具有较强的指示作用, 本次调查共鉴定出26个功能群, 其中包括13个富营养化水体代表性功能群, 以相对生物量占比超过5%划分出优势功能群16个, 其对应的生境特征较一致, 显示长湖属于浑浊, 含有机质, 中营养-富营养化的浅水水体。这与长湖的浮游动物、水生高等植物、鱼类以及表层底泥(刘建峰等, 2014; 何勇凤等, 2015; 王毅等, 2015; 周淼等, 2016; 郭坤等, 2017)等研究对其水域生态环境评价结果相一致。
本次调查鉴定出的16个优势功能群, 其中B、D、J、Lo、MP、W1和X1是四季共有优势功能群。以夏季和冬季出现频率均为100%的功能群X1为例来看, 主要种类是绿藻门的纤维藻属(Ankistrodesmus), 鞘藻属(Oedogonium)和小球藻(Chlorella vulgaris)等, 这些藻类均为富营养化水体的常见种。从优势功能群的丰度和最大相对丰度来看, 四季共有优势功能群B和X1在各季节占比均较高, 其中夏季X1的丰度为11.16× 106ind./L, 最大相对丰度达70.26%, 其所在生境是中小型中营养湖泊或富营养型的浅水水体。从生物量和生物量占比来看, 四季共有优势功能群W1在春季(2.34mg/L, 40.27%)和夏季(4.01mg/L, 33.08%)的值均最高, 其所代表的生境特征是富营养的静水水体。本次调查结果中浮游植物总丰度呈现夏(26.4×106ind./L) > 春(5.8×106ind./L) > 秋(4.5×106ind./L) > 冬(1.5×106ind./L)变化趋势, 总生物量为夏(12.1mg/L) > 春(5.8mg/L) > 冬(3.1mg/L) > 秋(1.9mg/L)变化趋势, 均以夏季最高, 春季其次。参照湖泊营养评价标准与藻类生物学评价标准(王明翠等, 2002; 况琪军等, 2005), 表明长湖整体处于富营养水平, 夏季富营养化程度最高, 这也与本次研究结果中优势功能群所代表的生境特征相一致。根据何勇凤等(何勇凤等, 2015)应用综合营养状态指数和浮游植物细胞丰度法在2012—2013年对长湖水质的评价显示, 长湖全区处于重度富营养化状态, 2015年的季节演替趋势与其一致。郭坤等(郭坤等, 2017)使用浮游动物(2012—2013年)多样性指数评价长湖处于中度污染, 肥度指数评价长湖处于富营养状态。对比往年结果(柴毅等, 2014; 魏志兵等, 2019)表明, 湖在2015年各季节的富营养化程度变化趋势与往年基本一致, 均为夏季最高, 冬季较低。
3.2 浮游植物功能群季节演替浮游植物功能群可通过自身演替来应对季节更替引起的水环境因子变化, 从而维持生态平衡, 这种伴随季节更替发生的演替往往具有一定的规律性(Reynolds et al, 2002; Padisák et al, 2009)。从本次研究结果来看, 以最大相对丰度超过50%为评价指标, 优势功能群的季节演替规律为X1/X2/B(春)→X1 (夏)→MP/X1/B(秋)→D/X1(冬), 其中除了X2之外, 其余均为四季共有优势功能群, 而X1则在四个季节均出现。春季优势功能群的代表种类有扭曲小环藻(Cyclotella comta)、衣藻属(Chlamydomonas)和小球藻等小型单细胞种类, 其代表生境特征为中营养-富营养浅水水体。这一时期随着水温升高和光照增强, 个体较小的浮游植物可充分利用水体中的营养而快速生长, 丰度与生物量都有较明显的增长。夏季以单一优势功能群X1占绝对优势, 最大相对丰度超过70%, Sn和MP的最大相对丰度也超过40%, 代表种类主要是绿藻门小球藻和蓝藻门颤藻(Oscillatoria)、鱼腥藻(Anabaena)以及硅藻门异极藻(Gomphonema)、舟形藻(Navicula)、桥弯藻(Cymbella)等典型富营养化水体指示种。夏季优势功能群的丰度和生物量均为最高, 这与降雨量及周边河流汇集、水体受扰动程度、水深等环境因子关系紧密。此外, 一些群体型、丝状体或单细胞聚集成的多细胞型藻类也大量出现, 这些种类往往不易被鱼类摄食而加水体重富营养化程度, 诸多因素导致长湖夏季富营养化程度最高, 局部水域为重度富营养化状态。秋季优势功能群中以硅藻门小型单细胞种类如舟形藻、异极藻、桥弯藻、扭曲小环藻以及扁裸藻(Phacus)为主, 这些种类具有分布广、适温性广等特点, 一般很少形成优势种群, 因此秋季优势功能群的丰度和生物量均较低, 富营养化程度也有所降低。冬季优势功能群中的D和X1代表种主要是淡水水体常见种类如硅藻门菱形藻(Nitzschia)和绿藻门栅藻(Scenedesmus)、盘星藻(Pediastrum), 其所在生境特征为中营养-富营养浅水水体。这一时期由于日照时间短、水温较低以及降雨量少导致地表径流营养盐输入较少等特点, 丰度和生物量均较低。
环境因子限制理论(Huisman et al, 1999; Moss et al, 2003)认为, 水体紊动通过改变藻类的生长位置使其生境条件频繁变化, 进而影响藻类获取光照和营养条件, 温度升高也可以通过改变蓝藻门喜高温种类群落结构组成, 进而影响整个生态系统结构功能, 这些环境因子的改变都是诱使藻类群落演替发生的关键。从本次研究得出的浮游植物功能群季节演替规律可以看出, 温度、光照、营养盐水平以及水文等环境因子是功能群发生演替的主要驱动力。
3.3 环境因子与浮游植功能群的相关性RDA排序是分析不同物种对环境的需求, 能很好的展现出生态环境对物种分布、组成的相互关系, 并可分析出不同功能群对环境的适应性, 以及理化因子的影响。此次RDA排序两轴的累积解释率在50%以上, 表明排序能较好地反映优势功能群与环境因子的关系。
此次RDA分析表明, 春季环境因子水温(WT)和透明度(WD)与四季共有优势功能群X1和D的相关性均较高, 表明此时期温度回升, 水位升高, 有利于藻类生长, 水温和水深是主要限制因子。在夏季总磷(TP)与功能群MP表现出明显正相关性, MP代表种类主要是硅藻门单细胞小型种类和典型富营养化浅水湖泊代表种两栖颤藻(Oscillatoria amphibia), 其对应的生境特征为经常受搅动、浑浊的浅水湖泊, 这与通过浮游植物丰度和生物量的水质评价结果表现出较好的一致性。夏季的环境因子对大部分优势功能群影响不明显, 可能是夏季高温及高度富营养化满足藻类生长需求, 导致环境因子变化对藻类功能群组成影响不显著。秋季总氮(TN)、总磷(TP)、溶解氧(DO)、透明度(WD)与其他优势功能群均无明显正相关关系, 其可能原因是温度下降, 导致喜高温藻类(主要是蓝藻)丰度大量死亡并释放出耗氧有机质, 而此时水体悬浮物水平较高, 大量悬浮物对氮、磷等营养物质进行吸附, 影响营养盐的分布与转化, 这种正反馈作用使藻类生物量达到年度较低值(高小丰等, 2015)。冬季功能群F、Y、X2、W1、B和Lo与磷酸盐(
(1) 长湖2015年浮游植物调查分析共划分出26个功能群, 其中13个富营养化水体代表性功能群, B、D、E、F、H1、J、K、Lo、Lr、MP、N、Sn、W1、X1、X2和Y共计16个为优势功能群。
(2) 以最大相对丰度超过50%为评价指标, 优势功能群的季节演替规律为X1/X2/B(春)→X1(夏)→ MP/X1/B(秋)→D/X1(冬)。
(3) RDA分析结果显示, 总悬浮物(TSS), 磷酸盐(
王毅, 罗静波, 郭坤, 等. 2015. 长湖表层底泥营养元素分布特征分析. 凯里学院学报, 33(6): 77-80 DOI:10.3969/j.issn.1673-9329.2015.06.23 |
王明翠, 刘雪芹, 张建辉. 2002. 湖泊富营养化评价方法及分级标准. 中国环境监测, 18(5): 47-49 DOI:10.3969/j.issn.1002-6002.2002.05.018 |
王徐林, 张民, 殷进. 2018. 巢湖浮游藻类功能群的组成特性及其影响因素. 湖泊科学, 30(2): 431-440 |
中国生态系统研究网络科学委员会. 2007. 水域生态系统观测规范. 北京: 中国环境科学出版社
|
刘建峰, 张翔, 谢平, 等. 2014. 长湖水质演变特征及水环境现状评价. 水资源保护, 30(4): 18-22 |
刘建康. 1999. 高级水生生物学. 北京: 科学出版社
|
何勇凤, 李昊成, 朱永久, 等. 2015. 湖北长湖富营养化状况及时空变化(2012-2013年). 湖泊科学, 27(5): 853-864 |
况琪军, 马沛明, 胡征宇, 等. 2005. 湖泊富营养化的藻类生物学评价与治理研究进展. 安全与环境学报, 5(2): 87-91 DOI:10.3969/j.issn.1009-6094.2005.02.024 |
汪星, 李利强, 郑丙辉, 等. 2016. 洞庭湖浮游藻类功能群的组成特征及其影响因素研究. 中国环境科学, 36(12): 3766-3776 DOI:10.3969/j.issn.1000-6923.2016.12.031 |
周淼, 聂细荣, 黄俊, 等. 2016. 长湖马洪台区秋季浮游植物群落结构特征分析. 长江大学学报(自然科学版), 13(27): 28-32 DOI:10.3969/j.issn.1673-1409(s).2016.27.007 |
赵文. 2016. 水生生物学. 2版. 北京: 中国农业出版社
|
胡韧, 蓝于倩, 肖利娟, 等. 2015. 淡水浮游植物功能群的概念、划分方法和应用. 湖泊科学, 27(1): 11-23 |
胡鸿钧, 魏印心. 2006. 中国淡水藻类-系统、分类及生态. 北京: 科学出版社
|
柴毅, 彭婷, 郭坤, 等. 2014. 2012年夏季长湖浮游植物群落特征及其与环境因子的关系. 植物生态学报, 38(8): 857-867 |
钱奎梅, 刘宝贵, 陈宇炜. 2019. 鄱阳湖浮游植物功能群的长期变化特征(2009-2016年). 湖泊科学, 31(4): 1035-1044 |
高小丰, 吴莹, 朱卓毅. 2015. 长江口外浮游植物死亡释放溶解有机质的降解及其溶氧消耗. 海洋与湖沼, 46(5): 1010-1017 |
郭坤, 杨德国, 彭婷, 等. 2016. 湖北省长湖浮游植物优势种生态位分析. 湖泊科学, 28(4): 825-834 |
郭坤, 彭婷, 罗静波, 等. 2017. 长湖浮游动物群落结构及其与环境因子的关系. 海洋与湖沼, 48(1): 40-49 |
黄享辉, 胡韧, 雷腊梅, 等. 2013. 南亚热带典型中小型水库浮游植物功能类群季节演替特征. 生态环境学报.2013, 22(2): 311-318 |
魏志兵, 柴毅, 罗静波等, 2019.长湖浮游植物优势种季节演替及生态位分析[J/OL].水生生物学报, 1-11, http://www.doc88.com/p-6778734143478.html
|
Becker V, Caputo L, Ordóñez J et al, 2010. Driving factors of the phytoplankton functional groups in a deep Mediterranean reservoir. Water Research, 44(11): 3345-3354 DOI:10.1016/j.watres.2010.03.018 |
Costa L S, Huszar V L M, Ovalle A R, 2009. Phytoplankton functional groups in a tropical estuary:hydrological control and nutrient limitation. Estuaries and Coasts, 32(3): 508-521 DOI:10.1007/s12237-009-9142-3 |
Guo K, Wu N C, Wang C et al, 2019. Trait dependent roles of environmental factors, spatial processes and grazing pressure on lake phytoplankton metacommunity. Ecological Indicators, 103: 312-320 DOI:10.1016/j.ecolind.2019.04.028 |
Hillebrand H, Dürselen C D, Kirschtel D et al, 1999. Biovolume calculation for pelagic and benthic Microalgae. Phycology, 35(2): 403-424 DOI:10.1046/j.1529-8817.1999.3520403.x |
Huisman J, Weissing F J, 1999. Biodiversity of plankton by species oscillations and chaos. Nature, 402(6760): 407-410 DOI:10.1038/46540 |
Lin L, Tao J, Yong X et al, 2018. Succession of phytoplankton functional groups from spring to early summer in the central Bohai Sea using HPLC-CHEMTAX approaches. Journal of Oceanography, 74(4): 381-392 DOI:10.1007/s10872-018-0469-x |
Moss B, McKee D, Atkinson D et al, 2003. How important is climate? Effects of warming, nutrient addition and fish on phytoplankton in shallow lake microcosms. Journal of Applied Ecology, 40(5): 782-792 DOI:10.1046/j.1365-2664.2003.00839.x |
Padisák J, Crossetti LO, Naselli-Flores L, 2009. Use and misuse in the application of the phytoplankton functional classification:a critical review with updates. Hydrobiologia, 621(1): 1-19 DOI:10.1007/s10750-008-9645-0 |
Qu Y M, Wu N C, Guse B et al, 2019. Riverine phytoplankton functional groups response to multiple stressors variously depending on hydrological periods. Ecological Indicators, 101: 41-49 DOI:10.1016/j.ecolind.2018.12.049 |
Reynolds C S, Huszar V, Kruk C et al, 2002. Towards a functional classification of the freshwater phytoplankton. Journal of Plankton Research, 24(5): 417-428 DOI:10.1093/plankt/24.5.417 |
Stanković I, Vlahović T, Udovič M G et al, 2012. Phytoplankton functional and morpho-functional approach in large floodplain rivers. Hydrobiologia, 698(1): 217-231 DOI:10.1007/s10750-012-1148-3 |
 2020, Vol. 51
2020, Vol. 51


