
中国海洋湖沼学会主办。
文章信息
- 王朋鹏, 张芳, 孙松, 杨涛. 2020.
- WANG Peng-Peng, ZHANG Fang, SUN Song, YANG Tao. 2020.
- 2018年6月渤海大型水母分布特征
- DISTRIBUTION OF GIANT JELLYFISH IN THE BOHAI SEA IN JUNE 2018
- 海洋与湖沼, 51(1): 85-94
- Oceanologia et Limnologia Sinica, 51(1): 85-94.
- http://dx.doi.org/10.11693/hyhz20190500085
文章历史
-
收稿日期:2019-05-06
收修改稿日期:2019-11-19
2. 青岛海洋科学与技术试点国家实验室 海洋生态与环境科学功能实验室 青岛 266071;
3. 中国科学院大学 北京 100049;
4. 中国科学院海洋大科学研究中心 青岛 266071;
5. 中国科学院海洋研究所 山东胶州湾海洋生态系统国家野外科学观测研究站 青岛 266071;
6. 中国水产科学研究院黄海水产研究所 山东省渔业资源与生态环境重点实验室 青岛 266071
2. Laboratory of Marine Ecology and Environmental Sciences, Pilot National Laboratory for Marine Science and Technology(Qingdao), Qingdao 266071, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China;
4. Center for Ocean Mega-Science, Chinese Academy of Sciences, Qingdao 266071, China;
5. Jiaozhou Bay Marine Ecosystem Research Station, Institute of Oceanology, Chinese Academy of Sciences, Qingdao 266071, China;
6. Key Laboratory for Fishery Resources and Eco-Environment, Yellow Sea Fisheries Research Institute, Chinese Academy of Fishery Sciences, Qingdao 266071, China
自1990年以来, 全球很多海域中水母数量显著增多(Arai, 2001; Purcell et al, 2001a, b; 丁峰元等, 2005), 已给全球范围内的经济、社会和生态带来了严重影响。我国近海暴发的大型水母种类主要有沙海蜇(Nemopilema nomurai)、霞水母(Cyanea spp.)、海月水母(Aurelia spp.)、多管水母(Aequorea spp.)等(Dong et al, 2010; Zhang et al, 2012)。近二十年来, 针对近海暴发的大型水母我国科学家在黄、东海开展了大量野外调查工作, 在其时空分布及物理驱动机制、种群动态、水母旺发引发的渔业资源效应及生态效应等方面的研究卓有成效(李建生等, 2009; 王彦涛等, 2012; Zhang et al, 2012; Sun et al, 2015; 左涛等, 2016a; 张芳等, 2017)。
我国渤海海域同样出现水母暴发现象, 莱州湾、辽东湾作为我国传统意义上渔业生物重要的产卵、孵育和索饵场所, 大型灾害性水母暴发严重影响了该海域海洋渔业资源与渔业生产(董婧等, 2013; 左涛等, 2016b); 水母暴发在影响渔业资源的同时, 更是危及到人类生命安全, 浴场水母蜇伤事件的报道层出不穷(董婧等, 2013; 郑向荣等, 2014b)。因此, 我国科学家在渤海海域同样开展了大量水母自然生态学的研究工作, 但这主要以辽东湾大型水母调查研究为主, 例如, 辽宁省海洋水产科学研究院对辽东湾大型水母的种群变动开展了长期监测, 对该海域不同年份各阶段大型水母的基础生物学信息有了清楚的了解, 并结合室内生态学实验, 在大型水母生活史、繁殖生物学等方面进行了比较系统的探讨(Dong et al, 2006, 2008; 王彬等, 2010, 2012; 董婧等, 2012, 2013; 孙明等, 2013)。郑向荣等(2014a, b)、左涛等(2016b)分别对河北近海、莱州湾大型水母的分布特征进行过报道。到目前为止, 我国对于渤海海域大型灾害水母的监测结果较为分散, 具有明显区域性, 缺少同步、整体性地调查, 限制了大型水母在渤海种群动态的整体性分析, 同时制约了渤海、黄东海大型水母自然生活史的关联性探讨, 从而阻碍了对我国近海大型水母自然生活史的整体性理解。
本研究于2018年6月上旬, 在渤海海域进行了较大范围的定点调查, 调查船舶为“中渔科102”渔业资源调查船, 记录了渤海内大型水母种类组成、渔获密度及伞径大小分布。通过本研究, 以期达到如下目的: (1)系统性了解6月份整个渤海海域大型水母的分布格局, 并探讨渤海各海域水母之间潜在的连通性, 推测渤海海域大型水母可能存在的暴发源头; (2)结合前人研究结果, 对渤海与黄东海大型水母进行了对比, 探讨渤海与黄东海大型水母生长的差异。
1 材料与方法 1.1 调查海域及站位设置本研究于2018年6月上旬, 在渤海海域进行了大型水母种群特征调查, 科考船舶为水科院黄海水产研究所“中渔科102”号。调查站位按0.5°×0.5°设定, 计划调查站位60个, 因部分站位所在海域水较浅或存在渔业养殖区, 因此实际调查站位为47个, 且实际走航站位与理论设定的0.5°×0.5°有所不同, 详如图 1所示, 拖网时间均为白天。为对比渤海不同海域水母生物学信息是否具有差异, 将整个渤海海域划分为渤海中部、辽东湾、渤海湾、莱州湾四部分海域, 详见图 1。
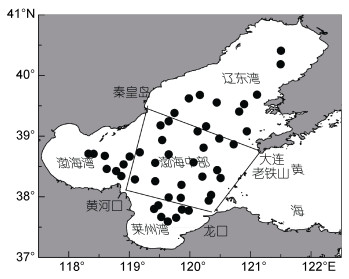 |
| 图 1 水母调查站位图 Fig. 1 Sampling stations in the Bohai Sea |
水母样品采用渔业资源调查底拖网(网目: 200mm× 440目, 囊网网目: 2mm×287目, 网口周长: 46.6m, 网长: 51.7m)采集, 各站位拖网时间控制在0.5—1h, 部分站位受恶劣天气、底泥等因素影响拖网时间略短, 拖速控制在3kn左右。各站位起网后将所有出现的水母进行收集, 在船载实验室中测定记录水母种类、个数, 并分别测量各类水母伞径(cm)。海区中大型水母的渔获量用渔获密度[CPUE, 单位: ind./(net·h)]表示, 即每小时每网大型水母的渔获数量。停船时使用船载CTD测量所在站位表、底层温度、盐度。
1.3 数据统计本研究数据统计、处理所使用软件为Surfer12、SPSS Statistics19。本文使用Surfer12进行调查站位图、环境参数分布图以及水母伞径与密度分布图的绘制; 分别使用SPSS Statistics19中KolmogorovSmirnov检验和Levene检验进行渤海各海域(辽东湾、渤海中部、渤海湾、莱州湾)温盐数据组内正态分布检验和组间方差齐性检验, 然后利用One-Way ANOVA分析各海域温盐的差异显著性; 使用Pearson相关性分析检验温盐与水母密度之间所存在的相关关系; 使用非参数Kruskal-Wallis检验用来对比渤海各海域(辽东湾、渤海中部、渤海湾、莱州湾)水母伞径大小是否具有显著差异性。P < 0.05表征具有显著差异。
2 结果 2.1 调查海域温、盐分布特征图 2展示了2018年6月渤海海域表、底层温度、盐度分布特征。结果显示, 渤海各海域表温无明显差异(F=2.780, P=0.052), 均值为(19.5±1.4)℃, 最高温度22.0℃ (站位: 39.16°N, 120.27°E), 最低温度16.2℃ (站位: 39.08°N, 120.94°E); 渤海各海域底层温度变化较大, 10—20℃均有分布, 莱州湾底层温度要显著高于其他海域(F=4.438, P=0.008)。渤海各海域表、底层盐度变化较大, 最大差值可达3.2;莱州湾表、底层盐度均要显著低于其他海域(表层: F=13.470, P < 0.001;底层: F=48.842, P < 0.001), 黄河入海口附近海域形成盐度低值区。
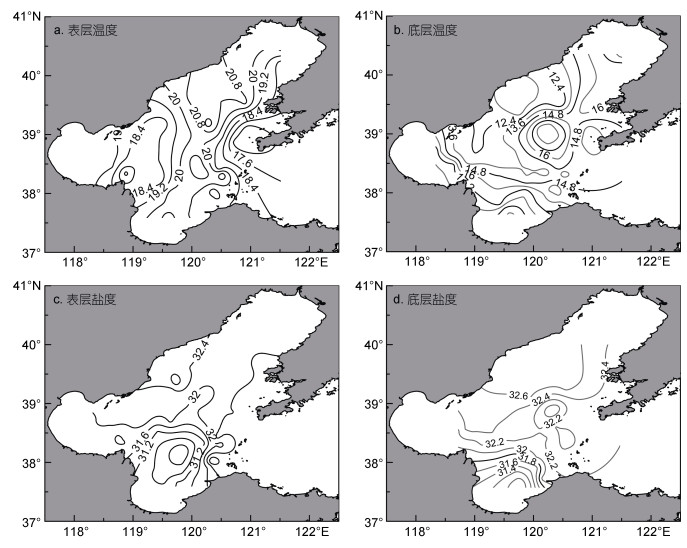 |
| 图 2 调查海域表、底层温度与盐度分布 Fig. 2 Distribution of temperatures (℃) and salinity at the sea surface and bottom |
本航次共发现四种大型水母:海月水母(Aurelia coerulea); 沙海蜇(Nemopilema nomurai)、海蜇(Rhopilema esculentum); 多管水母(Aequorea sp.)。
本次调查共有9个站位出现海月水母, 19个站位出现沙海蜇, 分别占调查站位的19%、40% (图 3a, 3b)。海月水母密度最大为221.21ind./(net·h), 出现在站位(38.34°N, 118.86°E), 其次为38ind./(net·h), 出现在站位(38.30°N, 119.06°E), 其余海月水母出现站位密度在1—5ind./(net·h); 渤海海域6月份海月水母密度地理分布特征为:高密度区域集中于渤海湾外部海域, 莱州湾、辽东湾海域海月水母密度较小, 辽东湾北部、渤海湾内部、渤海中东部海域未见海月水母出现(图 3a)。Pearson相关性分析结果表明, 温度、盐度对海月水母密度影响不显著(P > 0.05)。
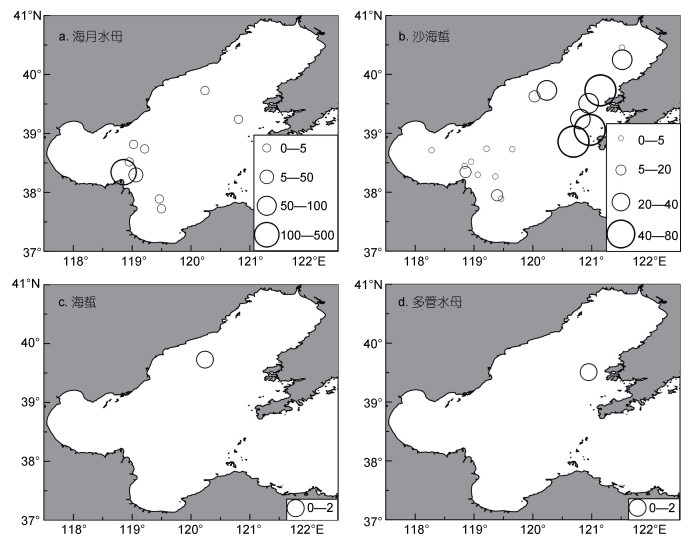 |
| 图 3 2018年6月渤海海域大型水母渔获密度[ind./(net·h)]分布图 Fig. 3 Distributions of densities [ind./(net·h)] of Aurelia coerulea (a), Nemopilema nomurai (b), Rhopilema es culentum (c) and Aequorea sp. (d) in the Bohai Sea in June 2018 注:圆圈表示站位平均值 |
沙海蜇密度最大为75.6ind./(net·h), 出现在站位(39.73°N, 121.15°E); 辽东湾海域沙海蜇出现站位密度均值为(35.32±21.64)ind./(net·h); 渤海湾外侧、渤海中部海域沙海蜇出现站位密度均值为(3.68±3.34)ind./ (net·h); 在渤海海域沙海蜇高密度分布区域为莱州湾、渤海湾外侧海域以及辽东湾海域(图 3b)。Pearson相关性分析结果表明, 除表层盐度对沙海蜇密度具有显著影响外(P < 0.05), 温度与底层盐度均对沙海蜇密度影响不显著(P > 0.05)。
海蜇在测区仅在一个站位出现(39.73°N, 120.24°E), 且密度较低[1-2ind./(net·h)]; 多管水母同样只有一个站位出现, 密度在[1-2ind./(net·h)], 位于站位(39.51°N, 120.95°E) (图 3c, 3d)。
2.3 伞径大小分布18年6月渤海海域海月水母伞径均值最大为8.3cm, 出现在站位(38.34°N, 118.86°E); 均值最小为1.8cm, 出现在站位(38.34°N, 119.02°E)(图 4a); 辽东湾南部海月水母平均伞径(7.00±1.00)cm, 渤海中部均值为(6.03±2.99)cm, 渤海湾均值为(4.95±2.57)cm, 莱州湾(5.33±0.58)cm (图 5a), 非参Kruskal-Wallis检验结果显示, 渤海各海区海月水母伞径大小无显著差异(H=2.453, df=3, P=0.484 > 0.05)。总体来讲, 6月份渤海海域海月水母伞径较小, 大部分个体在10cm以下, 各海区伞径大小无显著差异。
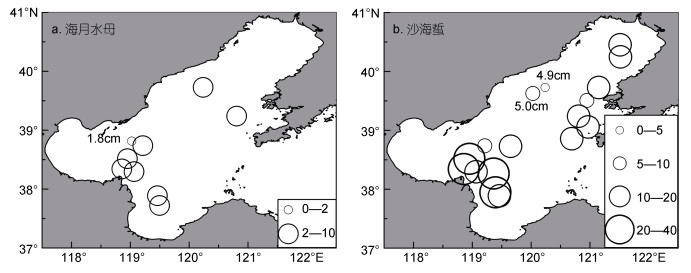 |
| 图 4 2018年6月渤海海域各站位海月水母(a)与沙海蜇(b)平均伞径大小(cm)分布图 Fig. 4 Distributions of mean diameters (cm) of Aurelia coerulea (a), Nemopilema nomurai (b) in the Bohai Sea in June 2018 注:圆圈表示站位平均值 |
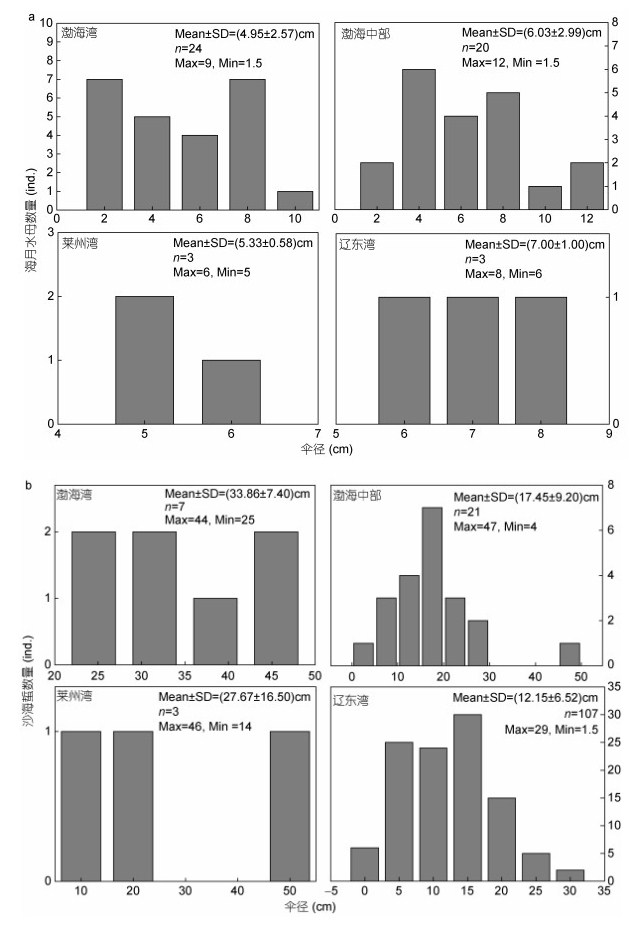 |
| 图 5 海月水母(a)与沙海蜇(b)在渤海各海域(渤海湾、莱州湾、辽东湾、渤海中部)伞径频度分布图 Fig. 5 Frequencies of Aurelia coerulea (a), Nemopilema nomurai (b) in the central part of Bohai Sea, Laizhou Bay, Bohai Bay and Liaodong Bay, in June 2018, respectively |
2018年6月份渤海海域沙海蜇伞径均值最大为39cm, 出现在站位(38.34°N, 118.86°E); 均值最小为4.9—5cm, 出现在辽东湾西侧、秦皇岛外侧海域(图 4b); 辽东湾沙海蜇平均伞径(12.15±6.52)cm, 渤海中部均值为(17.45±9.20)cm, 渤海湾均值为(33.86± 7.40)cm, 莱州湾(27.67±16.50)cm (图 5b), 非参Kruskal-Wallis检验结果显示渤海湾、莱州湾外侧交界海域沙海蜇伞径要显著大于辽东湾海域(H=27.5, df=3, P < 0.001)。总体来讲, 6月份渤海海域沙海蜇伞径分布极不均匀, 具体呈现为渤海湾、莱州湾外侧交界海域沙海蜇伞径要显著大于辽东湾海域, 且在秦皇岛外侧海域(39.63°—39.73°N, 120.03°—120.23°E)发现沙海蜇个体伞径在1—3cm之间。
3 讨论 3.1 渤海大型水母分布及源地探讨 3.1.1 海月水母6月份渤海海月水母在三湾海域均有分布, 渤海湾东南部为海月水母密度高值区, 可达38—221.21ind./(net·h), 其他站位密度较低, 多在5ind./(net·h)以下(图 3a)。虽然Pearson相关性分析显示温度均对海月水母密度不具有显著影响, 但渤海湾东南部海域底层温度要显著高于其他海域(图 2b), Wang等(2015b)指出海月水母水螅体在8—17℃均能产生横裂生殖, 但13℃是其最适横裂温度; 董婧等(2013)指出海月水母水螅体在15—20℃横裂生殖产生的碟状体比例最高。调查时发现, 辽东湾海域多数站位底层温度在13℃以下, 而莱州湾、渤海湾交界海域底层温度均在15℃以上, 这可能导致此处海月水母水螅体横裂发生时间要早于其他源地, 因此呈现出密度高值区。此外, 此部分海域盐度要显著低于其他海域, 最大差值可达3以上(图 2c, 2d)。但众多研究表明, 海月水母是一种广盐性生物, 具有很强盐度适应性(董婧等, 2013), 因此, 在本研究中Pearson相关性分析显示盐度对海月水母分布不具有显著影响。
各海域海月水母伞径均值较小, 多为10cm以下的水母幼体(图 4a), 但海月水母在野外海域伞径最大可达30cm以上, 这表明6月上旬海月水母在渤海处于发生初期阶段。渤海湾东南部海域海月水母伞径多集中于4.95—6.03cm, 最大可达12cm, 最小值为1.5cm (图 4a, 5a), 据此推测, 此处出现的海月水母应为土著种, 莱州湾与渤海湾交界海域可能是渤海海月水母种群发源地之一。渤海湾内部测区未见海月水母, 东侧河北沿岸海域有两个站位出现, 密度为2—4.8ind./(net·h) (图 3a), 值得注意的是所有出现的海月水母伞径仅有1.5—3cm (图 4a, 5a), 作者推测, 附近海域同样可能为渤海海月水母种群源头之一。
本次调查发现, 辽东湾海月水母仅出现于湾南, 在秦皇岛外海与大连外海两个站位有所显现, 密度在1.5—2ind./(net·h), 且均为海月水母幼体(伞径均值为7cm±1cm; 图 4a, 5a), 在湾北测区未见海月水母(图 3a), 这可能由于本研究未在湾北近海设置调查站位所致。事实上, 这与辽宁水科院长期对辽东湾海月水母观测结果类似, 2004—2011年调查中, 同样发现海月水母主要分布于辽东湾湾南, 湾北海域较少出现(王彬等, 2012; 董婧等, 2013), 例如: 2010年海月水母在湾南密度可达533ind./(net·h), 而湾北仅有1— 15ind./(net·h) (王彬等, 2012)。王彬等(2012)于2009—2011年6月下旬调查时发现湾北海月水母有增加的趋势, 这可能由于湾北温度要低于湾南, 因此海月水母在湾北发生时间要晚于湾南, 推迟到6月下旬。作者认为辽东湾南部海月水母于6月上旬开始出现, 这与前人调查结果一致; 由于此次调查对辽东湾站位调查时间集中于6月中上旬, 此时海月水母在辽东湾尚未大规模出现, 因此所测密度要显著低于前人调查结果。
莱州湾内只有两个站位出现海月水母, 密度在1—4ind./(net·h) (图 3a), 伞径均值为(5.33±0.58)cm (图 5a), 但据左涛等(2016b)的调查结果, 6月份莱州湾未发现有海月水母出现, 直到7月份才有一个站位出现海月水母, 而到9、10月份海月水母会在个别站位集中出现, 生物量最高可达45454kg/km2, 这表明不同年份该海域海月水母的发生时间、旺发时间会有所不同。
一方面海月水母水螅体具有很强的环境适应性, 其最适盐度范围可在17.5—37 (董婧等, 2013), 即使在本研究中发现各海域盐度有所差异(30—34), 但这并不影响水螅体生存与生殖; 另一方面, 各地人工设施的建造, 如防波堤、海港、码头等, 为水螅体的附着提供了适宜的栖息地(Uye et al, 2004; Holst et al, 2007), 因此, 海月水母在渤海沿岸可能存在多个源头, 诸如:莱州湾与渤海湾交界近岸海域、河北近岸、辽东湾大连近岸以及北部近岸, 此处所提出的海月水母源头是基于本研究所给出的推测, 当然在渤海其他近岸海域可能同样存在海月水母水螅体栖息地, 这需要更加深入的调查才能清楚的了解渤海海月水母的发生地。在6月上旬温度适宜时, 渤海海月水母水螅体逐渐横裂生殖释放碟状体。
3.1.2 沙海蜇6月份沙海蜇在渤海分布范围较广, 集中出现于两部分海域:辽东湾、莱州湾和渤海湾交界外侧海域, 且辽东湾沙海蜇密度要显著高于莱州湾与渤海湾外侧(图 3b), 但前者沙海蜇伞径要显著大于后者(图 5b)。前人研究指出沙海蜇水螅体更适合在低盐海水中生长(董婧等, 2013), Feng等(2016)同样指出河口附近低盐海区可能成为沙海蜇发生源头, 莱州湾和渤海湾交界外侧海域由于黄河淡水注入, 形成盐度低值区; 但本次调查并未在此近海发现沙海蜇幼体的存在, 因此作者推测, 莱州湾和渤海湾交界海域所出现的沙海蜇并非土著种。Pearson相关性分析表明, 虽然表层盐度对沙海蜇密度具有显著影响, 但温度与底层盐度均对其无显著影响, 作者认为温盐条件并不能对沙海蜇的分布特征作出很好的解释。但水母自主游动能力很弱, 其分布很大程度受到风流、海流的影响。6月调查时发现, 渤海湾伞径均值为(33.86±7.40)cm, 伞径最小也有25cm, 莱州湾采集到的沙海蜇伞径均值为(27.67±16.50)cm, 渤海中部出现的沙海蜇伞径均值也有(17.45±9.2)cm (图 5b), 沙海蜇伞径要显著大于辽东湾, 渤海湾、莱州湾出现的沙海蜇伞径最小分别为25、14cm, 最大可达46cm (图 5b)。春、夏季渤海中部存在较为明显的顺时针大流环和逆时针小流环, 辽东湾内部存在明显的逆时针流环(Wei et al, 2001); 渤海湾湾口北部存在一支形态清晰的沿岸南下入流, 其在湾内仅到达南堡附近便转向东南, 从湾口中部流出, 夏季在老黄河口外侧流向发生转变, 向北汇入渤海中部顺时针大流环(Zhou et al, 2017)。作者推测在此环流作用下, 辽东湾或者其他海域的沙海蜇进入到渤海湾、莱州湾湾口附近海域, 由于此部分沙海蜇出现较早, 经过长时间漂移伞径自然要大于辽东湾, 但整体密度并不高。
本次调查发现, 沙海蜇在大连外海形成密度高值区, 密度在39—80ind./(net·h) (图 3b), 其伞径分布极不均匀, 从1.5cm到29cm均有出现; 在辽东湾北部有两个站位出现沙海蜇, 密度范围在3—37ind./(net·h), 伞径均值为10—20cm, 最小个体为8cm (图 4b)。王彬等(2012)于2009—2011年对辽东湾北部海域调查时发现, 5月底未见沙海蜇, 海区中能采集到沙海蜇幼体最早的时间为6月上旬, 且在湾北近海双台子河口有大量沙海蜇幼体聚集, 形成数量高峰(王彬等, 2013), 但本次调查发现, 6月上旬湾南沙海蜇个体最大可达29cm, 这表明湾南沙海蜇发生时间要明显早于湾北, 这可能是由于温度差异导致水螅体横裂时间的不同。可以看出, 虽然沙海蜇在辽东湾分布范围较广, 但同时具有分布不均匀的特点。另外, 我们在秦皇岛东侧海域同样采集到沙海蜇, 其密度为7.5— 26ind./(net·h) (图 3b), 该海域沙海蜇伞径均值不足5cm(图 4b), 最小个体只有1.5cm。作者推测, 秦皇岛东侧海域出现的沙海蜇可能与辽东湾北部为不同的两个群体, 同样在6月上旬逐渐开始出现。
郑向荣等(2014a, b) 2012年8—9月对河北沿岸调查时发现, 该海区沙海蜇生物量要显著高于其他水母, 且分布较广, 从秦皇岛浴场到渤海湾大部均有分布, 滦河口附近生物量更是高达15—75t/km2, 而本次调查在渤海湾内只有一个站位采集到沙海蜇, 且密度只有0.67ind./(net·h), 一方面可能由于本次调查时间处于6月上旬, 沙海蜇处于发生初期, 因此尚未形成如此高密度, 另一方面沙海蜇分布可能具有较大的年际差异性。沙海蜇在莱州湾内部并未采集到, 只有湾外站位出现, 这与左涛等(2016b)在2011年调查结果类似。
通过本研究, 作者认为沙海蜇在渤海海域发源地主要集中于辽东湾, 在湾南大连近岸海、秦皇岛近岸, 以及湾北都有分布, 6月初逐渐显现。渤海中部、莱州湾、渤海湾所出现的沙海蜇并非本地种, 很可能是在海流作用下由辽东湾或其他源头漂流至此。
3.1.3 海蜇与多管水母海蜇属暖水性大型水母, 幼体多栖息于河口咸淡水交汇海域(李培军等, 1988; Dong et al, 2009)。本次调查中, 所采集到的海蜇出现在站位(39.73°N, 120.24°E) (图 3c), 位于秦皇岛外侧海域, 伞径为5.5cm。海蜇作为我国具有很高经济价值的渔业资源, 总体来讲, 在渤海的自然资源量下降明显, 渤海湾、莱州湾海蜇资源难以形成汛期(纪灵等, 1994), 只是零星出现, 长期对海蜇资源进行增殖放流, 使得辽东湾成为尚能形成海蜇集中渔汛的代表性渔场(姜连新等, 2007)。多管水母在本次调查中只采集到一只, 出现在大连瓦房店外侧海域(图 3d), 伞径为7cm, 渤海其他海域未见。
3.2 渤海与黄东海海月水母、沙海蜇对比海月水母与沙海蜇在我国近海分布较广, 在统计历史调查数据的基础上, 对两种水母在渤海与黄、东海的生长进行了对比。黄海海月水母的报道多见于胶州湾, 据万艾勇等(2012)于2009年调查时发现海月水母碟状体在胶州湾4月份开始出现, 到6月份达到高峰, 6月上旬伞径为(8.74±1.72)cm, 下旬可达(15.21±4.29)cm; 2010年6月中旬海月水母伞径可达(11.5±2.5)cm (表 1); Wang等(2015a)在2011年对胶州湾调查时报道, 海月水母幼体在5月下旬伞径为(0.97± 0.2)cm, 7月初可达(16.2±1.8)cm。而王彬等(2012)在2009—2011年对辽东湾北部调查时发现, 5月下旬未见海月水母幼体, 到6月下旬伞径只有5—10cm; 同样, 本次调查发现6月份渤海所出现的海月水母伞径多数在10cm以下, 最大个体也不过12cm, 渤海湾东南部海月水母伞径只有1.5cm。因此, 胶州湾海水母发生时间要早于渤海, 且在同一月份伞径要高于渤海。
| 调查时间 | 调查海域 | 水母种类伞径(cm) | 文献 | ||||
| 海月水母 | 沙海蜇 | 海蜇 | 多管水母 | 霞水母 | |||
| 2000.05下旬、6月 | 长江口、舟山渔场 | — | — | — | 14 | 25 | 周永东等, 2004 |
| 2001.05—08 | 浙江中北部近岸海域 | — | — | — | — | 20—50 | 周永东等, 2004 |
| 2003.06中旬 | 29.5°N以北附近海域 | — | 40—50 | — | — | — | 程家骅等, 2004 |
| 2004.06.16—26 | 东海海域(28°—34°N) | — | 50—70 | — | 20—25 | 45—60 | 程家骅等, 2005 |
| 2006.06 | 长江口附近海域 | — | 32.2±3.4 | — | — | 18.2±12.7 | Zhang et al, 2012 |
| 2007.05 | 黄海南部、 长江口附近海域 |
— | 7 | 16.0±6.3 | Zhang et al, 2012 | ||
| 2008.06中旬 | 东海北部 | — | 10—51 | — | — | — | 李建生等, 2009 |
| 2009.06.20 | 胶州湾 | 12.53±5.74 | — | — | — | — | 未发表数据 |
| 2010.06中旬 | 胶州湾 | 11.5±2.5 | 胶州湾调查数据 | ||||
| 2011.05.22—07.2 | 胶州湾 | 5月底0.97±0.2, 7月初16.2±1.8 |
— | — | — | — | Wang et al, 2015a |
| 2012.06 | 黄海南部、东海 (27.42°—37.00°N, 120.50°—124.50°E) |
— | 32±20 | — | — | — | Sun et al, 2015 |
| 2013.05 | 江苏沿岸 | — | 1—2.5 | — | — | — | Sun et al, 2015 |
| 2013.06 | 东海北部 30°—32°N |
— | 32±20 | — | — | — | Sun et al, 2015 |
| 2015.05 | 黄海、东海北部 (30°—39°N) |
— | 12.7 ± 6.20 | — | 东海北部11.67±4.32; 黄海7.74±3.65 |
40±14.17 | 左涛等, 2016a |
| 2005.06中上旬 | 辽东湾北部海域 | — | — | — | — | 水母幼体 | 姜连新等, 2007 |
| 2006.06上旬 | 辽东湾北部海域 | — | 2—10 | 2—3 | — | — | 王彬等, 2010 |
| 2009, 2010.06中旬 | 辽东湾 | — | 6—12 | 4—6.2 | — | — | 王彬等, 2013 |
| 2009, 2010.06下旬 | 辽东湾 | 5—10 | 18—27 | 11.3—11.4 | — | 5—10 | 王彬等, 2012 |
| 2013.06初 | 秦皇岛附近海域 | 5 | — | — | — | — | 郑向荣等, 2014b |
| 2013.07 | 秦皇岛附近海域 | 20—30 | — | — | — | — | 郑向荣等, 2014b |
| 2018.06 | 渤海海域 | 5.52±2.65 | 14.39±8.95 | 5.5 | 7 | — | 本研究 |
| 注: ”—“表示本次调查未发现或者没有该种水母记 | |||||||
6月份黄海与东海北部沙海蜇发生时间同样要早于渤海, 且同期伞径明显要大(表 1)。据程家骅等(2004)报道, 2003年6月中旬东海北部沙海蜇伞径可达40—50cm, 2004年可达50—70cm; 据Zhang等(2012)在2007年调查时报道, 5月份在南黄海、东海西北部均有沙海蜇分布, 到6月份其伞径可达30cm以上; 李建生等(2009)报道2008年6月中旬在东海北部沙海蜇伞径范围在10—50cm。而在辽东湾最早的沙蜇发现记录是在6月上旬, 此时沙海蜇伞径在2—10cm, 而到6月中旬伞径也只有6—12cm (王彬等, 2010)。本次调查发现, 在渤海海域沙海蜇伞径大小分布具有不均匀性, 辽东湾海域沙海蜇平均伞径只有(12.15±6.25)cm, 在秦皇岛外海位采集到的沙海蜇伞径均值甚至不足5cm, 而在莱州湾与渤海湾交界海域出现的沙海蜇其伞径均值在17—34cm, 最大可达47cm (图 5b), 但从总体来看, 黄海、东海北部沙海蜇种群出现时间要先于渤海沙海蜇种群。
作者认为海月水母、沙海蜇发生时间与伞径最大值的出现期, 随着纬度增加均有推迟的现象。温度对水螅体横裂、水母体生长起到至关重要的作用, 随纬度升高温度降低, 这可能是导致水母发生时间推迟的主要原因。另外, 浮游动物的组成在黄、东海与渤海有很大差异(代鲁平等, 2016), 这为水母提供了不同的饵料环境, 饵料差异不仅能够影响水螅体阶段的分裂生殖(Wang et al, 2015b), 对于水母体的生长发育更会产生很大影响, 这也可能是导致黄、东海与渤海水母种群差异的原因之一。
4 结论2018年6月海月水母、沙海蜇、海蜇、多管水母在渤海均有分布, 但以海月水母、沙海蜇为主。总体来讲, 6月份渤海海月水母分布主要集中于渤海湾东南侧海域, 辽东湾海月水母主要出现于湾南, 各海域海月水母伞径均较小, 多为水母幼体; 沙海蜇分布广泛, 但其密度分布与伞径分布具有不均匀的特点, 辽东湾为沙海蜇密度高值区, 但其伞径较小, 渤海湾与莱州湾外侧海域沙海蜇密度虽小, 但伞径要显著大于辽东湾; 海月水母、沙海蜇在渤海发生时间要晚于黄、东海。
致谢 感谢中国水产科学研究院黄海水产研究所承担的青岛海洋科学与技术试点国家实验室共享搭载航次和环境数据, 及相关调查人员和“中渔科102”号调查船全体船员的辛勤外业工作。
丁峰元, 程家骅. 2005. 东海区夏、秋季大型水母分布区渔业资源特征分析. 海洋渔业, 27(2): 120-128 DOI:10.3969/j.issn.1004-2490.2005.02.006 |
万艾勇, 张光涛. 2012. 胶州湾海月水母(Aurelia sp.1)丰度周年变化及对浮游动物群落的影响. 海洋与湖沼, 43(3): 494-501 DOI:10.11693/hyhz201203014014 |
王彬, 秦宇博, 董婧, 等. 2013. 辽东湾北部近海沙蜇的动态分布. 生态学报, 33(6): 1701-1712 |
王彬, 董婧, 王文波, 等. 2012. 辽东湾北部近海大型水母数量分布和温度盐度特征. 海洋与湖沼, 43(3): 568-578 |
王彬, 董婧, 刘春洋, 等. 2010. 夏初辽东湾海蜇放流区大型水母和主要浮游动物. 渔业科学进展, 31(5): 83-90 DOI:10.3969/j.issn.1000-7075.2010.05.013 |
王彦涛, 孙松, 王世伟, 等. 2012. 2011年春季黄、东海墨绿多管水母(Aequorea coerulescens)分布特征. 海洋与湖沼, 43(6): 1096-1102 |
左涛, 王俊, 吴强, 等. 2016a. 2015年5月黄海及东海北部大型水母分布及生物量估算. 海洋与湖沼, 47(1): 195-204 |
左涛, 吴强, 王俊, 等. 2016b. 莱州湾水母种类多样性及群集结构的季节变化. 生态学报, 36(18): 5646-5656 |
代鲁平, 李超伦, 王世伟, 等. 2016. 基于ZooScan图像技术的南黄海夏季浮游动物群落结构分析. 海洋与湖沼, 47(4): 764-773 |
孙明, 董婧, 柴雨, 等. 2013. 温度、投饵频次对白色霞水母无性繁殖与螅状体生长的影响. 生态学报, 33(10): 3222-3232 |
纪灵, 葛仁英. 1994. 1993年渤海海蜇消失的原因何在. 海洋信息, (1): 15 |
李建生, 凌建忠, 程家骅, 等. 2009. 2008年夏秋季东海区北部沙海蜇资源状况分析. 海洋渔业, 31(4): 444-449 DOI:10.3969/j.issn.1004-2490.2009.04.015 |
李培军, 谭克非, 叶昌臣. 1988. 辽东湾海蜇生长的研究. 水产学报, 12(3): 243-250 |
张芳, 李超伦, 孙松, 等. 2017. 水母灾害的形成机理、监测预测及防控技术研究进展. 海洋与湖沼, 48(6): 1187-1195 |
周永东, 刘子藩, 薄治礼, 等. 2004. 东、黄海大型水母及其调查监测. 水产科技情报, 31(5): 224-227 DOI:10.3969/j.issn.1001-1994.2004.05.018 |
郑向荣, 李燕, 张海鹏, 等. 2014a. 河北沿海大型水母生物量调查. 河北渔业, (1): 15-18, 42 |
郑向荣, 李燕, 饶庆贺, 等. 2014b. 秦皇岛近海大型水母暴发性增长原因探析. 河北渔业, (2): 16-20 |
姜连新, 叶昌臣, 谭克非, 等. 2007. 海蜇的研究. 北京: 海洋出版社, 158-200
|
董婧, 孙明, 赵云, 等. 2012. 中国北部海域灾害水母沙蜇(Nemopilema nomurai)及其它钵水母繁殖生物学特征与形态比较. 海洋与湖沼, 43(3): 550-555 |
董婧, 姜连新, 孙明, 等. 2013. 渤海与黄海北部大型水母生物学研究. 北京: 海洋出版社, 175-205
|
程家骅, 丁峰元, 李圣法, 等. 2005. 东海区大型水母数量分布特征及其与温盐度的关系. 生态学报, 25(3): 440-445 DOI:10.3321/j.issn:1000-0933.2005.03.009 |
程家骅, 李圣法, 丁峰元, 等. 2004. 东、黄海大型水母暴发现象及其可能成因浅析. 现代渔业信息, 19(5): 10-12 DOI:10.3969/j.issn.1004-8340.2004.05.003 |
Arai M N, 2001. Pelagic coelenterates and eutrophication:a review. Hydrobiologia, 451(1-3): 69-87 |
Dong J, Jiang L X, Tan K F et al, 2009. Stock enhancement of the edible jellyfish (Rhopilema esculentum Kishinouye) in Liaodong Bay, China:a review. Hydrobiologia, 616(1): 113-118 DOI:10.1007/s10750-008-9592-9 |
Dong J, Liu C Y, Wang Y Q et al, 2006. Laboratory observations on the life cycle of Cyanea nozakii (Semeostomida, Scyphozoa). Acta Zoologica Sinica, 52(2): 389-395 |
Dong J, Sun M, Wang B et al, 2008. Comparison of life cycles and morphology of Cyanea nozakii and other scyphozoans. Plankton and Benthos Research, 3(S1): 118-124 |
Dong Z J, Liu D Y, Keesing J K, 2010. Jellyfish blooms in China:dominant species, causes and consequences. Marine Pollution Bulletin, 60(7): 954-963 DOI:10.1016/j.marpolbul.2010.04.022 |
Feng S, Wang S W, Zhang G T et al, 2016. Selective suppression of in situ proliferation of scyphozoan polyps by biofouling. Marine Pollution Bulletin, 114(2): 1046-1056 |
Holst S, Jarms G, 2007. Substrate choice and settlement preferences of planula larvae of five Scyphozoa (Cnidaria) from German Bight, North Sea. Marine Biology, 151(3): 863-871 DOI:10.1007/s00227-006-0530-y |
Purcell J, Arai M N, 2001a. Interactions of pelagic cnidarians and ctenophores with fish:a review. Hydrobiologia, 451(1-3): 27-44 |
Purcell J, Sturdevant M V, 2001b. Prey selection and dietary overlap among zooplanktivorous jellyfish and juvenile fishes in Prince William Sound, Alaska. Marine Ecology Progress Series, 210: 67-83 DOI:10.3354/meps210067 |
Sun S, Zhang F, Li C L et al, 2015. Breeding places, population dynamics, and distribution of the giant jellyfish Nemopilema nomurai (Scyphozoa:Rhizostomeae) in the Yellow Sea and the East China Sea. Hydrobiologia, 754(1): 59-74 DOI:10.1007/s10750-015-2266-5 |
Uye S I, Ueta U, 2004. Recent increase of jellyfish populations and their nuisance to fisheries in the Inland Sea of Japan. Bulletin of Japanese Society of Fisheries Oceanography, 68(1): 9-19 |
Wang Y T, Sun S, 2015a. Population dynamics of Aurelia sp.1 ephyrae and medusae in Jiaozhou Bay, China. Hydrobiologia, 754(1): 147-155 DOI:10.1007/s10750-014-2021-3 |
Wang N, Li C L, 2015b. The effect of temperature and food supply on the growth and ontogeny of Aurelia sp.1 ephyrae. Hydrobiologia, 754(1): 157-167 DOI:10.1007/s10750-014-1981-7 |
Wei H, Wu J P, Pohlmann T, 2001. A Simulation on the Seasonal Variation of the Circulation and Transport in the Bohai Sea. Journal of Oceanography of Huanghai & Bohai Seas, 19(2): 1-9 |
Zhang F, Sun S, Jin X S et al, 2012. Associations of large jellyfish distributions with temperature and salinity in the Yellow Sea and East China Sea. Hydrobiologia, 690(1): 81-96 DOI:10.1007/s10750-012-1057-5 |
Zhou F, Huang D J, Xue H J et al, 2017. Circulations associated with cold pools in the Bohai Sea on the Chinese continental shelf. Continental Shelf Research, 137: 25-38 DOI:10.1016/j.csr.2017.02.005 |
 2020, Vol. 51
2020, Vol. 51


