中国海洋湖沼学会主办。
文章信息
- 徐奎栋. 2021.
- XU Kui-Dong. 2021.
- 印太交汇区海洋生物多样性中心形成演化机制研究进展与展望
- FORMATION AND EVOLUTION MECHANISMS OF MARINE BIODIVERSITY CENTER IN THE INDO-PACIFIC CONVERGENCE REGION: PROGRESS AND PROSPECTS
- 海洋与湖沼, 52(2): 262-273
- Oceanologia et Limnologia Sinica, 52(2): 262-273.
- http://dx.doi.org/10.11693/hyhz20200900256
文章历史
-
收稿日期:2020-09-24
收修改稿日期:2020-12-20
2. 青岛海洋科学与技术试点国家实验室 海洋生物学和生物技术功能实验室 青岛 266237;
3. 中国科学院大学 北京 100049;
4. 中国科学院海洋大科学研究中心 青岛 266071
2. Laboratory for Marine Biology and Biotechnology, Pilot National Laboratory for Marine Science and Technology(Qingdao), Qingdao 266237, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China;
4. Center for Ocean Mega-Science, Chinese Academy of Sciences, Qingdao 266071, China
印度-西太平洋区(Indo-West Pacific region, 又称印度-太平洋区)包括西自印度洋非洲东岸(含红海), 东至太平洋中部的复活节岛, 北起日本南半部, 南至澳大利亚北半部的热带及亚热带海域, 是世界海洋动物地理区中面积最大、多样性最高的区域。印太交汇区是热带西太平洋和东印度洋交汇的区域, 处于印度-西太平洋区的中心地带, 是全球海洋的热量中心, 长期地质历史和剧烈的板块构造过程在此塑造了生境多样的大面积浅海, 形成全球海洋生物多样性中心。
海洋生物多样性最高的区域处于印太交汇区的珊瑚大三角(Coral Triangle), 即由菲律宾、马来西亚、印度尼西亚、巴布亚新几内亚和所罗门群岛组成的三角海域(Green et al, 2008), 地处印澳群岛(Indo-Australian Archipelago, IAA) 的中心区域。印澳群岛又称马来群岛(Malay Archipelago)或东印度群岛(East Indies), 包括文莱、东帝汶、印度尼西亚、马来西亚、巴布亚新几内亚、菲律宾、新加坡和泰国半岛, 区域较之珊瑚大三角略大, 均为海洋生物多样性和海洋生物地理学研究的高关注区(Briggs, 1966, 2003)。
珊瑚大三角的物种多样性为何比全球其他任何地方都高, 一直是海洋生物地理学中的热点问题(Bellwood et al, 2009)。这里生活着全球种类繁多的珊瑚, 以及以珊瑚礁为栖息地的高多样性海洋生物, 包括占全球76%的造礁石珊瑚物种(Veron et al, 2009)、全球37%的珊瑚礁鱼类物种(Allen et al, 2002; Allen, 2008)、全球近75%的红树林物种、45%以上的海草物种、58%的热带海洋软体动物, 全球7种海龟中的6种, 以及至少22种海洋哺乳动物, 惊人的多样性水平集中在不到世界1%的海洋面积中(wwf.panda.org/coraltriangle)。
印太交汇区海洋生物多样性中心的形成是长期地质历史、构造过程、气候与海洋环境及生命过程等共同作用的结果, 对其成因和驱动机制的探究一直是海洋科学乃至地球科学的热点。有关其成因有多个竞争性假说, 热带物种分化快, 随时间的稳定性, 地理隔离及适应辐射, 以及较长的进化历史等, 推动了珊瑚大三角多样性热点的形成。构造过程和气候事件驱动的地理和海洋环境变化在中心的形成演化中起了不同程度的作用, 但一些关键过程与驱动机制依然不明。
本文综述了印太交汇区生物多样性的分布格局、形成演化、物种多样性成因及驱动机制等方面的研究进展, 就存在的问题进行了总结和梳理, 并对未来研究提出一些想法和建议。希冀能为印太交汇区海洋生物多样性的系统深入研究提供参考。
1 海洋生物多样性分布格局及起源演化 1.1 海洋生物多样性时空分布格局从赤道向两极减少是当前全球生物多样性的一个基本格局, 是认识和预测气候变化驱动的生物多样性变异的关键。纬度梯度模式是海洋生物多样性分布的一个显著特点, 但相关认识主要来自近岸浅海。Tittensor等(2010)通过对从有孔虫到哺乳类共13个类群11567种海洋生物的分布研究, 发现海洋生物总体上呈现两种分布模式: 一种如近海珊瑚和鱼类等大多数海洋生物, 主要集中在印太珊瑚大三角, 在物种丰富度和较高分类阶元的特异性上都很高, 呈明显的纬度梯度分布模式; 另一种如金枪鱼、头足类、鲸等大洋游泳动物, 并不呈现从赤道向两极减少的分布模式, 其多样性峰值出现在中纬度海域。
除珊瑚大三角外, 海洋生物在西太平洋中纬度海域(如日本群岛南部) 也常呈现高多样性。海葵目在近海有类似的分布特点, 其物种丰富度自南北纬30º—40º向低纬度和高纬度均呈降低趋势, 不同于其所隶属的珊瑚纲及刺胞动物门从赤道向两极减少的纬度梯度分布模式(李阳等, 2020)。受限于资料不足, 对于很多生物类群的地理分布特征仍不明了。通常, 底栖生物较之浮游生物在地理分布上更具限定性, 但对于海洋微型底栖生物和浮游生物是否有明确的限定性分布仍有广泛争议(徐奎栋, 2011; Moss et al, 2020)。
从时空尺度上, 海洋生物多样性从赤道向两极减少的分布格局在5.4亿年以来并非一成不变, 多样性峰值区的转移可能是构造过程、气候环境和生物进化历史等综合作用的结果(Naimark et al, 2011)。基于海洋大型底栖有孔虫化石和现生生物分子证据及数值模拟均显示, 近5千万年以来全球海洋生物多样性峰值区经历了数次转移, 几乎横跨半个地球, 并至少出现在三个热点: 从始新世(55—33 Ma)位于古地中海, 到始新世晚期和中新世中晚期(37—11 Ma)转移到阿拉伯半岛和西印度洋, 后从渐新世(33—23 Ma)至早中新世(23—16 Ma)转移到印太交汇区(Renema et al, 2008; McMonagle et al, 2011; Leprieur et al, 2016)。海洋生物多样性热点转移的时间和地点与构造过程和气候事件一致。
海洋生物多样性的纬度梯度分布模式的动力机制一直是研究关注点(Willig et al, 2003; Hillebrand, 2004)。对海洋生物多样性纬度梯度的解释多侧重于宏观进化或生物地理过程。从宏观进化角度来看, 物种多样性的大尺度空间梯度是物种产生率和灭绝率及地理分布随时间变化共同作用的结果(Goldberg et al, 2005; Jablonski et al, 2006, 2013; Roy et al, 2007)。环境及生境之间大尺度的生物多样性梯度通常归因于一系列复杂的生态和进化因素。Stevens(1989)提出这是由于生活在高纬度的生物因较大的季节波动而具有更高的环境耐受性, 因而多样性低, 而热带物种由于环境相对稳定, 无明显季节变化, 可能有更特化的生境要求和更窄的耐受度, 从而使更多物种共存。
化石生物对于理解长时间尺度海洋生物多样性纬度梯度及进化提供了独特视角, 但也有其自身的局限性, 而与现生生物谱系地理研究相结合可相互印证。整合古生物学和现生生物的系统发育信息被认为是认识物种产生、灭绝和生物地理在形成多样性梯度中相对贡献的最好途径(Barber et al, 2015; Jablonski et al, 2017), 但在印太交汇区相关化石记录研究甚少。在缺乏化石数据情况下, 拟合生物动态分布模型和系统发育数据, 也可估算区域的物种产生率和灭绝率(Goldberg et al, 2005, 2011), 从而验证各种假说。因此, 未来需更多研究来整合现代生物学和古生物学在不同时空尺度上的生物多样性, 预测不同世系在多样性热点转移中的进化响应。
1.2 深海生物多样性分布格局深海严格意义上是指水深超过1000 m的海洋, 将超过200 m的深水区也常称之深海。迄今, 对于浅海的生物多样性分布格局已基本清楚, 但有关深海的生物区系和多样性分布格局依然不明, 盖因采样和调查不足、数据欠缺所致。深海面积巨大, 环境异质性加之不同时空尺度的干扰产生了斑块状群落, 因此被认为具有高生物多样性(Grassle, 1991; Gray, 1994; Levin et al, 2001)。但也有观点认为, 深海环境同质性强及缺乏明显的扩散障碍, 物种常具有较大的分布范围(McClain et al, 2010)。
水深及其关联的环境因子是用于划分底栖生物群落的主要依据。栖息于半深海(1000—3000 m)和深海平原(~4000 m)的生物具有不同的地理分布范围, 自双壳类和腹足类的研究显示深海物种的分布范围较半深海物种大(Etter et al, 1990, 2005)。深海底栖生物大都依赖于上层水体生产并输运的有机物质, 食物通常是深海底栖生物的限制因子。据此, Watling等(2013)按水深将深海底栖生物划分为半深海(Lower bathyal: 801—3500 m)和深海区(Abyssal: 3501—6500 m)两个区系, 又按上层水体向下输运的有机物质通量划分为许多地理省; 在半深海区, 印太深海被划分为西太平洋省和印度洋省, 而在深海区, 印太交汇区被划分到四个地理省中。这一分区是否与实际生物分布吻合需进一步验证。
对深海底栖动物的地理区划大多基于单一类群(Kussakin, 1973; Zezina, 1997; Woolley et al, 2016), 基于多个类群的分析常面临海域覆盖不全或数据欠缺的问题(Vinogradova, 1979; Watling et al, 2013)。基于全球海蛇尾分布的大数据分析, 显示深海底栖生物多样性具有随纬向和深度的分布模式: 在200—2000 m的半深海(陆架以下到陆坡上坡), 物种多样性以热带印度-西太平洋和加勒比海为最高; 而在2000—6500 m的深海则以纬度30°—50°为最高, 集中于碳通量高及近陆海域。据此提出的“物种—能量框架假说”认为水温决定了浅海的物种丰富度, 而化学能与邻近陆坡驱动了深海的物种丰富度(Woolley et al, 2016)。该结果是否可推及其他生物类群仍需验证。印太交汇区相较其两侧的印太海域初级生产力以及向海底输入的碳通量更高, 可能颠覆了这一假说, 形成独特的热带深海动物地理分布模式。
基于65000种海洋动植物分布数据的集成分析, Costello等(2017)将海洋生物划分为18个陆架区和12个深海区。其中, 印太交汇区的近海和深海被划到一个分区中, 其范围包括印度洋西部和北部浅海及热带西太平洋的大片深海区。受限于数据的不均衡和不全面, 这种划分可能与实际的生物区系不符。印太交汇区的深海生物在全球深海的生物区系地位和地理分布格局如何, 是否具有类似浅海的高物种多样性分布格局, 仍待验证。深海包含深海平原、海山、海沟、热液和冷泉等多样化生境, 各自具有相较独特的生态系统和生物区系, 因此需针对不同类型生境开展独立的生物区划(Bachraty et al, 2009; Wu et al, 2019)。
1.3 深海生物起源与演化深海的物种多样性是由时空因素共同作用并演化形成的, 包括时间的稳定性和生境的异质性(Sanders, 1968; Grassle et al, 1992)。绝大部分研究显示, 海洋底栖动物(如软体动物、甲壳动物和棘皮动物)起源于浅海(Little et al, 2003), 并向深水/深海发展并多样化, 呈“近岸浅海深海(onshore-offshore-deep sea)”的演化模式(Jablonski et al, 1983)。对该演化模式的主要解释为: (1) 晚白垩纪前的深海缺氧事件(清除大量底栖生物), 使浅海生物优先起源, 即现代深海生物来自浅海生物的孑遗种(Jacobs et al, 1998); (2) 浅海生物的高捕食压力迫使其向深海转移(Vermeij, 1987)。第二种解释的一个典型案例是棘皮动物海百合类, 其祖先在古生代和中生代大都生活在浅海, 为躲避捕食压力而逐渐迁移至深海, 在深海演化形成高多样性(Baumiller et al, 2004)。
深海动物的浅海起源假说在许多类群中获得验证, 以浅海中鲜见而深海中多样性极高的等足类栉水虱亚目为例, 基于核基因的系统发育研究发现, 该类群起源于浅海, 在深海高度多样化(Raupach et al, 2009)。迄今, 海洋生物的深海起源证据仍十分有限, 基于系统发育分析获得的首个证据是刺胞动物的柱星螅科(Stylasteridae), 其祖先起源于深海并多样化, 随后三次入侵热带浅海, 一次入侵温带浅海, 呈“深海浅海”演化模式(Lindner et al, 2008)。尽管如此, 基于海洋无脊椎动物化石属的研究表明, 虽然热带浅海的物种源始率更高, 但向深海输出的属仅比自深海输入的略高, 因此从“深海浅海”的演化可能较预想的更普遍(Kiessling et al, 2010)。
珊瑚大三角作为海洋生物多样性最高的区域, 如果其周边深海生物遵循“近岸浅海深海”的演化模式, 则可能有极高的多样性。同样地, 如果其周边深海生物存在“深海浅海”的演化模式, 则其对浅海生物多样性的贡献也是值得关注的问题。印太珊瑚大三角、北太平洋和南极海域是全球海洋的三个主要物种起源中心, 通过其持续的物种产生, 成为保持全球海洋生命系统运转的主要引擎(Briggs, 2003)。Dueñas等(2016)对南极丑柳珊瑚的研究证实南极绕极流是深海八放珊瑚多样化的诱因。这三大起源中心保持着物种交换, 但其对印太交汇区深海生物多样性的相对贡献还是一个谜。此外, 深海不同生境间生物的源汇关系也是较为关注的问题。
2 印太交汇区海洋生物多样性中心成因假说对印太交汇区海洋生物多样性中心的判定主要基于近岸浅海的研究。有关其多样性成因有四个主要的竞争性假说, 包括起源假说(Center-of-Origin hypothesis)、保存假说(Center-of-Survival hypothesis)、汇聚假说(Center-of-Accumulation hypothesis)和重叠假说(Center-of-Overlap hypothesis)。这些假说各有其理论依据, 但各有难以解释的问题, 尚无任一假说获得普遍认可。
2.1 物种起源假说和保存假说起源假说集中在高物种形成速率及向外的地理扩布, 是最早提出并被广泛接受的假说(Briggs, 1966, 2003; Bowen et al, 2013)。保存假说将珊瑚大三角比作生物多样性博物馆, 认为高多样性是由于低物种灭绝率形成的(Bellwood et al, 2012; Di Martino et al, 2018)。珊瑚大三角在上新世和更新世冰期可能起到保存生物多样性的作用。现今的海洋物种被认为主要是在气候变冷的更新世出现的, 珊瑚大三角起了生物避难所的作用, 成为海洋物种的保存中心(Bellwood et al, 2009)。
基于起源假说可以预测, 珊瑚大三角由新产生的物种主导, 并向外扩布, 大三角中心的物种应较外围的亲缘种更年轻(Stehli et al, 1971; Goldberg et al, 2005)。保存假说与此正相反, 大三角中心应较其外围的更古老(Roy et al, 2007)。对印太海洋45个礁栖物种的314个种群进行的系统发育重建, 支持珊瑚大三角是印度-太平洋生物多样性的起源中心, 但最古老的种群更靠近大三角中心而非外围(也支持保存假说), 表明珊瑚大三角兼具起源和保存中心的作用(Evans et al, 2016)。
起源假说和保存假说如同一个硬币的两个面, 彼此难以割裂, 争论的大多是哪一个更占主导。Jablonski等(2006)利用海洋双壳类的431个化石属/亚属, 提出“走出热带模式(Out of the Tropics model)”, 即海洋生物优先起源于热带, 向更高纬度扩布而不失去其在热带的存在, 热带海洋在产生多样性的同时也在不断保存多样性, 起着生物多样性源和汇的双重作用。因此, 强调热带海洋是物种产生率更高的地方(源), 或者是物种不易消亡的地方(汇), 可能都有失偏颇, 更应是二者兼而有之。
高特有种比例曾被用于解释起源中心的主要依据之一, 其假设是大三角如果是起源中心, 则必然有更多特有种且物种较外围的更年轻。基于印度尼西亚和菲律宾海域礁栖鱼类的研究显示, 珊瑚大三角有最高的特有种比例, 支持起源假说(Mora et al, 2003)。而另一份同样基于礁栖鱼类的研究却得出相反的结论(Hughes et al, 2002)。基于印太交汇区石珊瑚的研究结果也不支持起源假说, 分析的605种含虫黄藻的石珊瑚中, 特有种仅占2.5% (Veron et al, 2009)。在石珊瑚主要类群——鹿角珊瑚科中亦如此, 289种鹿角珊瑚中仅3.5%为珊瑚大三角所特有, 而78.5%的物种在周边海域也有(Huang et al, 2018)。这些相悖结论产生的根源在于如何界定特有种, 这不仅受所选择区域大小的显著影响, 也受所选类群的影响。另外, 将特有种标记为物种的起源地也未必正确, 尤其是对那些扩布能力强且进化历史长的分类群而言。如何将物种的起源时间与其起源地一一对应, 仍是一个待解决的问题。因此, 特有种比例可能并非是一个可靠的依据(Goldberg et al, 2005; Bellwood et al, 2009; Cowman, 2014)。
另外, 基于不同类群、不同分子标记或不同数据库分析可能得出不一样的结论。以鱼类为例, 对于热带海洋鱼类相较高纬度冷水群落更多样化, 更普遍的解释是温暖的珊瑚礁环境是物种形成的热点, 即起源中心(Alfaro et al, 2007; Kiessling et al, 2010; Cowman, 2014)。然而, Rabosky等(2018)基于时间校准的海洋辐鳍鱼类系统发育分析, 并研究了纬度、物种丰富度和鱼类物种形成速率间的关系, 发现海洋鱼类物种形成速率最快的区域并非在热带, 而是在高纬度海域。该研究颠覆了普遍将热带作为海洋鱼类多样性进化摇篮的假设, 由此也提出了新的问题, 即为何寒冷的海洋是物种形成的热点?产生的新物种是否或如何扩布至热带海域?
然而, 高纬度海域更高的物种产生率显然并未产生更高的物种多样性。通常, 生态分化被认为是高物种形成速率的原因和/或结果。Knope等(2020)基于海洋动物30074个现生属和19992个化石属的分析表明, 现代海洋中较高的生态分化实际上与较低的物种产生率有关。产生生态分化的进化支在灭绝时(特别是大灭绝期间)得到更好的缓冲, 随时间的推移变得多样化; 大灭绝主要影响了物种丰富但生态上同质的进化支。生态分化与分类丰富度的关系在动物进化早期很弱, 但是当相继发生的灭绝事件重塑了海洋动物区系, 便随地质时间的推移而加强。由此可见, 高物种保存率(或低灭绝率)可能是形成高物种多样性更重要的因素。
2.2 物种重叠假说和汇聚假说重叠假说认为, 珊瑚大三角的高物种多样性是太平洋和印度洋的物种在地理上交叉形成的, 即两洋物种因冰期形成地理屏障, 在大三角隔离分化并重叠形成(Woodland, 1983)。该假说强调气候对地理环境的塑造, 物种分布范围扩展在形成高多样性中的作用, 而非关注物种产生或灭绝(Woodland, 1983; Hughes et al, 2002; Bellwood et al, 2009; Hodge et al, 2016)。重叠假说如成立, 则物种在大三角应相较其外围分化更少。这一点在礁栖鱼类中获得印证, 对668种珊瑚礁鱼类的DNA条形码研究显示, 印度-太平洋外围的物种较之大三角区分化更大(Hubert et al, 2012)。印太交汇区复杂的地质历史、连接热带两大洋的位置以及冰期作为陆桥等因素, 促成了物种的异域分化和在大三角的交汇。
汇聚假说认为, 物种分化于珊瑚大三角外的群岛海域, 随板块堆积和洋流扩布, 长期缓慢汇聚形成。汇聚假说涉及了物种产生率和灭绝率在物种输入和输出中的相对贡献, 强调构造过程尤其是洋流的作用将物种自外围扩布至此, 且因较低的灭绝率而随时间维持下来(Ladd, 1960; Pandolfi, 1992; Bellwood et al, 2009)。通过对造礁石珊瑚的系统发育分析, 比较了现生珊瑚的特有种、区外的特有种和广布种年龄分布, 并拟合物种产生、灭绝和分布区转移的动态系统发育模型, 显示珊瑚大三角的物种产生率低于周边地区, 特有种比例低, 不支持起源中心假说; 大三角的珊瑚主要是由区域外形成的物种扩展而来, 支持汇聚假说(Huang et al, 2018)。汇聚假说如成立, 对于海洋生物多样性保护具有重要意义, 即要保护珊瑚大三角生物多样性, 除了热点区, 还要保护其周边的珊瑚礁生物。
礁栖鱼类是研究大三角物种起源形成的主要类群。金鳞鱼科在珊瑚大三角物种多样性最高, 也是原西特提斯海(古地中海)最丰富的化石类群之一。基于时间校正的现生种和化石种的系统发育重建显示, 从古地中海到现今珊瑚大三角的多样性热点区域中, 金鳞鱼科既有起源又有汇聚特征(Dornburg et al, 2015)。然而, 对长海胆属物种的线粒体CoxI基因的系统进化分析结果, 表明遗传分化和物种形成可能在整个印度-西太平洋发生, 不支持重叠假说与汇聚假说(Palumbi, 1996)。
不同生物类群可能具有不同的进化历史, 基于某一类群的研究结果可能无法推及其他类群, 对同一类群基于不同视角的研究也可能得出不同的结论。这也是迄今对珊瑚大三角生物多样性成因仍存广泛争议的原因。迄今, 结合时间和空间异质性, 开展随进化时间尺度的海洋生物多样性热点的研究很少(Renema et al, 2008), 对形成物种多样性模式背后的动力机制仍然所知不多。认识不同生物进化枝如何反映多样性热点的转移, 对于理解海洋生物多样性形成和维持很重要, 但相关推理因缺乏化石证据, 难以洞察其多样性分布的历史格局。通过化石结合现生生物分子地理研究有助于解决这一问题。另外, 基于单一或几个基因的数据难以反映生物谱系地理的全貌, 未来结合多组学的研究有望提供更全面的证据。
3 印太交汇区海洋生物多样性中心形成的环境驱动机制印太交汇区海洋生物多样性中心的形成是构造过程、气候和环境、生命过程等共同作用的结果, 既有生物内在进化动力, 又有外部环境驱动。相关生物进化动力学研究主要来自礁栖鱼类以及珊瑚等无脊椎动物(Cowman, 2014; Bowen et al, 2013; Briggs et al, 2013), 在此不做赘述。此处主要从构造和气候变化驱动的地理隔离及适应辐射、栖息地广阔且生境多样、物质和能量驱动的物种形成等角度予以综述。
3.1 构造与气候变化印太交汇区地处欧亚板块、印澳板块、太平洋板块和菲律宾海板块的汇聚区, 构造复杂且板块活跃。板块运动可引起海洋环境巨变, 塑造新的生境和生物多样性。“寒武纪生命大暴发”被认为是板块构造发生巨大变化造成氧气水平上升, 驱动了寒武纪动物的高度多样化(Williams et al, 2019)。Leprieur等(2016)利用计算机模型, 推演了140 Ma以来大陆板块漂移强烈改变了全球热带浅海的分布, 推动了热带礁栖生物多样性的转移; 在距今60—50 Ma前, 古地中海西部曾分布大量珊瑚礁, 是多样性热点区, 板块构造过程促成新栖息地及新物种出现, 热点转到现今的珊瑚大三角。
构造过程不仅塑造了地理和环境变化, 还显著影响了气候, 从而对物种多样性及分布格局产生影响(Wilson et al, 1998; Keith et al, 2013)。许多研究表明多样性与气候有关的环境变量间有很强的关联性, 存在“气候–丰富度关系(climate–richness relationships)” (Currie et al, 2004; Roy et al, 2007)。基于化石记录的深时(deep-time)研究显示, 自显生宙以来海洋物种多样性的峰值与地球温度曲线呈密切关联: 峰值区通常在冰期处于热带, 暖期则处于温带, 凸显了气候对海洋生物多样性分布的影响(Mannion et al, 2014)。中新世晚期地球持续冷却, 至距今约7—5.4 Ma时海洋温度下降到接近现代的温度, 很可能进一步助推了海洋生物多样性热点往珊瑚大三角的转移(Herbert et al, 2016)。
气候对海洋生物多样性的影响还在于, 热带海洋使物种在冰期易于保存, 并因海平面下降形成地理隔离, 从而独立分化发展; 而暖期时海平面上升, 不同海盆的水体混合, 使来自不同地理分区的物种汇聚和重叠。这是印太交汇区高生物多样性形成的重要推动力, 但关键过程还不清楚。另外, 板块构造过程是一个长尺度、极其缓慢的过程, 而取自海洋的沉积物岩芯常因长度所限, 年代不够久远, 可能无法反映长时间尺度的构造事件和过程。因此, 需结合生物的分子记录相互印证, 取长补短。
3.2 大面积浅海与多样化生境印太珊瑚大三角的高多样性还与其大面积热带浅海及丰富的珊瑚礁有关。栖息地广阔是维持高物种多样性的重要因素。大三角所在的马来群岛总面积约248万km2, 是全球最大的群岛, 也是海洋生物多样性最高的区域; 而位于加勒比海的西印度群岛(West Indies)是全球第二大群岛, 总面积约24万km2, 海洋生物多样性居全球第二位。珊瑚大三角的珊瑚物种占全球总物种数的76%, 而加勒比海则仅为8% (Veron et al, 2000, 2009), 与二者面积之比基本吻合, 由此支持物种–面积假说(species-area hypothesis; Rosenzweig, 1992, 1995)。此外, 珊瑚大三角的高多样性符合中域效应假说(mid-domain effect), 即热带的高多样性是因其处于中间区域(Colwell et al, 2000)。大三角还处于热带印度洋和太平洋交汇的区域, 形成了独特的多样性纬度梯度及经度梯度分布格局。
珊瑚礁生态系统被誉为“海洋中的热带雨林”, 造就了物种多样性丰富的生物群落。此外, 大量群岛和海盆、大片红树林和海草床等生态系统, 构筑了丰富多样的生境。与陆地生物多样性热点不同的是, 珊瑚大三角的生物并非由分布范围小的大量特有种构成, 而是由分布广泛的物种融合形成(Hughes et al, 2002)。基于底栖无脊椎动物化石属的研究显示, 热带浅海和碳酸盐基质(珊瑚礁)具有较高的物种产生率, 并形成物种的外溢效应(Kiessling et al, 2010)。面积广大的珊瑚礁形成的大量斑块化生境使物种不易灭绝, 加之更新世冰期和间冰期轮回造成的海平面和生境变化, 使生物不断在隔离分化、交汇融合中发展。
珊瑚礁是印太珊瑚大三角高物种多样性的基石。海水升温和酸化直接影响造礁石珊瑚的生物多样性, 造成珊瑚礁生态系统衰退(孙军等, 2016; McManus et al, 2020)。通常, 珊瑚的多样性可使其更好地适应升温等环境变化, 但其进化适应是有限度的(Dixon et al, 2015; Hume et al, 2016)。升温驱使含共生藻的珊瑚迁移以适应环境: 一是往深处迁移, 二是往更高纬度迁移。然而, 向深处迁移则受到光照的限制, 无法进行光合作用。升温导致的海洋物种向更高纬度迁移已成常态, 对珊瑚大三角的珊瑚而言, 迁移可能面临着无大面积浅海可用的困境, 从而造成毁灭性影响。研究珊瑚及其共生生物的适应性, 推演其在气候环境变化下的演变, 对珊瑚礁生物多样性保护具有重要意义。
3.3 物质和能量基础印太交汇区不仅处于全球最大的暖池区, 也是陆源物质最大的辐聚区, 河流入海的泥沙通量达全球的一半以上(Milliman et al, 2011), 形成了全球陆源物质和海洋热量的汇聚中心。周边河流入海输入的陆源物质, 使通常的热带寡营养海域在此获得了丰富的营养盐, 在某些区域形成高生产力。共生虫黄藻也为珊瑚礁生态系统维持高生物多样性提供了物质基础。“能量–丰富度假说(energy–richness hypothesis)”提出, 生产力更高的地区拥有更多个体, 因此物种更多。但已有数据显示, 从能量到个体数再到物种数的预期因果关系并不一致(Currie et al, 2004)。另外, 温度、盐度、海流、营养盐等环境变量均可影响海洋生物生产(Kinkade et al, 1997; Ayers et al, 2014)。研究印太交汇区生产力及生态过程与生物多样性间的相互作用关系, 是揭示其高生物多样性维持机制的重要环节。
古生物及海洋生物普查结果均显示, 水温是影响全球海洋生物多样性分布格局的首要因子(Tittensor et al, 2010; Mannion et al, 2014; Woolley et al, 2016)。因此, 作为全球热量中心的印太暖池的形成发展, 必然与海洋生物多样性中心的形成演化有关联。暖池形成是印尼海道关闭的结果, 印尼海道呈多期次逐渐关闭的趋势, 但其相对开合、张缩的时间还有争议(李铁刚等, 2020)。基于有孔虫的古海洋学研究显示, 11—9 Ma为原始暖池形成期, 约7 Ma首次衰退, 6 Ma以来为现代暖池孕育和发展期, 1—0.2 Ma穿插着暖池的二次衰退期(周祖翼等, 2004)。这几个时期的海洋环境很可能不同程度影响了海洋生物多样性中心的形成演化, 但相关过程不清楚。
值得关注的是, 现今海洋生物多样性的峰值区并非位于珊瑚大三角中心区, 而是处于其北缘的菲律宾棉兰老岛附近海域(Sanciangco et al, 2013)。这一分布格局除了生境的可得性和复杂性外, 还可能与水温及上升流有关联。全球变暖对珊瑚大三角的生物多样性将产生显著影响, 关系着这一生物多样性热点的存续。对暖池和海洋生物多样性形成关系的研究, 对于认识印太交汇区海洋生物多样性演变及保护具有重要意义。
3.4 环流动力驱动的生物扩布海洋大型生物大都通过幼体被动地利用海流来扩布, 种群扩布与连通是环境与生物及生物与生物之间相互作用的结果。幼体发育时间、浮游期、存活能力等相关特性决定了其随海流扩布的能力, 在宏观进化中发挥重要作用。印太交汇区处于太平洋和印度洋的“十字路口”, 有热带环流、西边界流和印尼贯穿流等复杂的水文动力环境。南、北赤道流等可将源自太平洋的幼体扩布至交汇区, 而南、北赤道逆流和赤道潜流等则可将生物向交汇区外输送。但有关海流与生物输运的关系, 尤其是海流结构与生物多样性分布的关系尚未见报道。
海流在输运浮游生物或大型生物幼体过程中, 可形成物理屏障影响生物的分布甚至演化。Martín等(2020)利用水体环境DNA (eDNA)和宏条形码技术对物种多样性进行评估, 并通过创建数学模型, 模拟了来自海洋特定样本中的个体动态, 发现洋流导致原生生物物种数急剧增加, 但每一物种的个体数量却减少了。对此有两种解释: 一是洋流通过制造物理屏障限制生物扩散, 从而增加了物种多样性; 二是洋流可能减少了生物间的竞争, 使每种浮游生物与其他物种共存。该研究将宏基因组学与生物海洋学及物理海洋学相结合, 属典型的多学科交叉, 可为印太海洋生物多样性中心成因研究提供借鉴。
印尼贯穿流是连通印度洋和太平洋的主要海流, 将太平洋的物种直接输运到印度洋。印太交汇区有一条著名的华莱士线(Wallace's line), 于1860年由英国动物地理学者华莱士最先提出, 是世界动物地理分区中东洋区和大洋洲区的分界线。巧合的是, 华莱士线及后来修正的韦伯线(Weber's line)与印尼贯穿流的流向基本一致。Barber等(2000)通过对印度尼西亚珊瑚礁螳螂虾的种群遗传结构分析, 发现这些珊瑚礁系统由强大的洋流连接起来的, 形成一条海上华莱士线。迄今, 对于生物随印尼贯穿流向的演化, 形成的物理屏障是否分隔了两侧的海洋生物区系等还是待解的问题, 亟待开展多学科交叉研究。
4 未来研究展望有关浅海的生物多样性成因和机制, 虽已开展大量研究, 但大多局限于单一学科, 缺少对生物内在适应演化和外部环境作用机制的系统认知。诸多假说的验证和科学问题的解决, 需打破常规, 基于新视角、新手段, 通过今古结合、学科交叉和相互印证, 阐释印太交汇区海洋生物多样性中心形成和演化机制, 并推演其未来演变效应。有关印太交汇区深海的生物多样性及分布格局仍然不明, 也是未来研究的突破点。
4.1 今古耦合, 交叉融通印太交汇区海洋生物多样性中心的形成是历史的产物, 是多圈层共同作用的结果。板块构造过程、气候和海洋环境及生命过程如何共同作用, 以及生物内在的适应演化过程与外部环境的作用机制, 均属多学科交叉领域的问题。单一学科的研究仅能从一个侧面去回答, 而无法给以系统阐释。化石生物提供了时间序列的生物和环境信息, 而现生生物的遗传信息也往往记录了地质历史和气候环境事件驱动的变化。通过环境和生命过程的今古研究和多学科交叉融合, 有望在印太海洋生物多样性中心形成的理论方面取得突破。
海洋生物多样性热点的时空转移与气候事件和环境变化有明确关联。利用有孔虫等海洋环境指示生物(Wycech et al, 2020), 分析其时间序列的群落结构和物种演化, 针对印太交汇区典型时段和特殊事件, 尤其是暖池形成以来的演化序列, 探寻古生物演化过程与气候环境的耦联, 回答: (1) 驱动印太交汇区海洋生物多样性形成演化的环境要素; (2) 暖池形成与海洋生物多样性演化的耦合过程; (3) 气候及海平面与地理变化对海洋生物多样性形成的塑造; (4) 现今珊瑚大三角北缘的多样性峰值到底是暖期驱动的北移, 还是间冰期效应的延续?厘清这些问题, 揭示海洋生物多样性与气候环境的协同演化过程, 并结合现今海洋环境与生物多样性分布的数值模拟, 推演印太交汇区海洋生物多样性的演变趋势。
有关印太交汇区生物多样性形成及分布格局的解释多侧重于宏观进化或生物地理过程, 以及基于单个或少数基因的系统发育地理学研究。未来, 应充分利用多组学技术, 基于时间校准的生物谱系地理学分析, 通过宏观和微观进化研究结合, 并结合古生物和古海洋信息, 回答: (1) 印太交汇区海洋物种产生、灭绝和随时间的地理扩布与地质及气候环境事件的关联; (2) 印太海洋生物多样性形成和维持的内在进化动力学机制; (3) 印太交汇区海洋生物与邻近大洋和海盆生物的源汇关系。
海洋生物与物理因子的耦合也应是未来研究的重点。浮游生物和大型生物幼体及其eDNA均通过海流进行扩布, 不同生物有不同的水平和垂直分布特征(Zhao et al, 2017, 2020), 是长期自然选择和进化的产物, 可印证流体结构, 弥补海流数据瞬时观测的不足。开发基于eDNA的宏条形码检测技术(Zhao et al, 2019), 通过生物分布特征印证环流结构, 结合水文动力模型构建和数值模拟, 追溯和推演生物的扩布路径及其在不同水层中的扩布范围(朱国平等, 2020)。将组学、生物海洋学与物理海洋学等学科交叉, 开展生物与动力环境的耦合研究, 回答: (1) 印太交汇区不同海盆间生物多样性空间分布与流体结构关系; (2) 海流驱动的生物及基因流随纬向和经向梯度的变化; (3) 洋流驱动的跨海盆生物扩布与连通的机制。
通过古今结合研究, 重建古海洋环境和古生物多样性特征, 补足时间序列上的观测资料, 揭示长时间尺度上海洋环境与生物演化的关系及其影响。基于对海洋环境和生物的协同研究, 通过数值模拟和观测结果验证, 预测其未来变化趋势。由此, 将显著提高对印太交汇区海洋生物多样性中心形成和演变等关键科学问题的认识, 在理论上取得突破, 为海洋生物多样性热点的保护提供科学依据。
4.2 关注深海, 重点突破对印太海洋生物多样性中心的判定主要基于近岸浅海的研究, 而深海生物往往体现不同的分布模式(Costello et al, 2017)。印太交汇区浅海和深海生态系统交错, 环流系统复杂, 不同来源的生物可能构成了相较独特的深海生物区系。但迄今对深海生物多样性及分布格局的认知十分匮乏, 对于深海和浅海生物的起源演化、扩布路径以及生物源汇关系仍不明确, 也将是未来的研究重点(图 1)。我国在此方面的最大短板是: 深海生物样品获取有限, 生物多样性数据不多, 缺乏对其构成和连通格局的认知, 离支撑国家需求还有差距(徐奎栋, 2020; 徐奎栋等, 2020)。
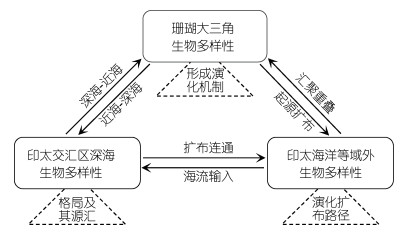 |
| 图 1 印太交汇区浅海和深海的生物多样性形成演化与扩布及源汇关系图 Fig. 1 Diagram of the formation, evolution, distribution, and source-sink relationships of shallow and deep-sea biodiversity in the Indo-Pacific convergence region |
印太交汇区因区域国家调查能力不足及相关限制, 深海生物多样性研究十分匮乏。这里的海盆、海山和热液区生物多样性极为丰富, 很可能在全球生物区系中具有显著地位, 高生物多样性区也恰是研究的盲点区。在此开展深海的探测研究, 对于认识交汇区多样性中心成因、深海生物起源演化及生物多样性保护均具重要意义。
对于印太深海生物多样性研究, 西太平洋的相关研究基础较好, 而印度洋则极为不足且挑战较大。考虑到采样调查的经济性、安全性和可实现性, 西太平洋仍将是未来深海探测研究的主要区域, 其中南海、密克罗尼西亚群岛、俾斯麦海可作为重点关注区。南海处于珊瑚大三角西部边缘, 记录有3365种鱼类(Randall et al, 2000), 物种丰富度与珊瑚大三角(3000—4000种)相当(Burke et al, 2012); 造礁石珊瑚有571种, 丰富程度亦与珊瑚大三角相媲美(Huang et al, 2015)。南海周边国家多, 因领土争端和冲突等因素阻碍了对其物种多样性的准确估计。我国对南海的深海生物调查极为欠缺, 家底不清楚。
密克罗尼西亚海域面积广大, 岛屿众多, 海山密布, 生境类型多样, 近海和深海生物多样性均十分丰富, 可能是珊瑚大三角的生物起源地之一。巴布亚新几内亚的俾斯麦海具有丰富的深海生物多样性, 已开展海底热液采矿活动, 是深海生物多样性研究和保护的热点区域。苏拉威西海也是生物多样性热点区, 水深大多在2000 m以上, 海底有大量新奇多样的生物(Normile, 2010), 是印尼贯穿流的流经区, 与南海亦有物种交流。该海域分属印尼、马来西亚和菲律宾三国专属经济区, 开展调查不易。
印太海洋生物多样性最显著的海域位于珊瑚大三角, 获得生物样品是开展相关研究的前提, 而域内主要国家限制甚至禁止外国科考船进入。如何获得有研究价值的生物样品将是一个亟待解决的问题。通过发起国际大科学计划, 或者参与国际组织倡导的国际合作, 通过科学家及研究机构之间的广泛交流合作, 有望满足研究的样品需求。组织有效的国际合作不仅可提高研究的影响力, 还有助于推进“海上丝绸之路”建设。
5 结语印太交汇区海洋生物多样性中心的形成是地球地质历史、气候、环境和生物协同进化共同作用的结果。对其形成的关键过程和机制认识仍相当有限, 亟待多圈层视角的研究。相较浅海, 对于印太交汇区深海的生物多样性及分布格局依然不明, 浅海的高多样性是否可推及深海仍然未知。诸多假说的验证和科学问题的解释, 需打破常规, 通过今古结合和多学科交叉互证, 从化石生物与环境耦联、现今生物地理及分子数据、生物与环流动力等因素的多联分析, 阐释印太交汇区海洋生物多样性中心形成和演化过程与机制, 推演其在全球气候变化下的演变趋势及生态效应。开展系统性、多学科交叉研究, 有助于全面提升我国对印太海洋的科学认知水平, 占据海洋科学前沿领域制高点, 服务于国家一带一路建设。
朱国平, 周梦潇. 2020. 海洋数值模型发展及其在海洋生物扩散模拟研究中的应用进展. 海洋渔业, 42(2): 245-256 DOI:10.3969/j.issn.1004-2490.2020.02.012 |
孙军, 林茂, 陈孟仙, 等. 2016. 全球气候变化下的海洋生物多样性. 生物多样性, 24(7): 737-738 |
李阳, 徐奎栋. 2020. 中国海海葵目(刺胞动物门: 珊瑚虫纲)物种多样性与区系特点. 海洋与湖沼, 51(3): 434-443 |
李铁刚, 熊志方, 贾奇. 2020. 晚中新世以来印度洋-太平洋暖池水体交换过程及其气候效应. 海洋科学进展, 38(3): 377-389 |
周祖翼, 金性春, 王嘹亮, 等. 2004. 印尼海道的两度关闭与西太平洋暖池的形成和兴衰. 海洋地质与第四纪地质, 24(1): 7-14 |
徐奎栋. 2011. 海洋微型底栖生物的多样性与地理分布. 生物多样性, 19(6): 661-675 |
徐奎栋. 2020. 西太平洋海沟洋脊交联区海山动物原色图谱. 北京: 科学出版社, 239
|
徐奎栋, 林茂, 王少青, 等. 2020. 中国海及西太平洋生物分类研究进展及展望. 海洋与湖沼, 51(4): 728-739 |
Alfaro M E, Santini F, Brock C D, 2007. Do reefs drive diversification in marine teleosts? Evidence from the pufferfish and their allies (Order Tetraodontiformes). Evolution, 61(9): 2104-2126 DOI:10.1111/j.1558-5646.2007.00182.x |
Allen G R, 2008. Conservation hotspots of biodiversity and endemism for Indo-Pacific coral reef fishes. Aquatic Conservation: Marine and Freshwater Ecosystems, 18(5): 541-556 DOI:10.1002/aqc.880 |
Allen G R, Werner T B, 2002. Coral reef fish assessment in the 'coral triangle' of Southeastern Asia. Environmental Biology of Fishes, 65(2): 209-214 DOI:10.1023/A:1020093012502 |
Ayers J M, Strutton P G, Coles V J et al, 2014. Indonesian throughflow nutrient fluxes and their potential impact on Indian Ocean productivity. Geophysical Research Letters, 41(14): 5060-5067 DOI:10.1002/2014GL060593 |
Bachraty C, Legendre P, Desbruyeres D, 2009. Biogeographic relationships among deep-sea hydrothermal vent faunas at global scale. Deep Sea Research Part Ⅰ: Oceanographic Research Papers, 56(8): 1371-1378 DOI:10.1016/j.dsr.2009.01.009 |
Barber P H, Meyer C P, 2015. Pluralism explains diversity in the Coral Triangle. In: Mora C ed. Ecology of Fishes on Coral Reefs. Cambridge, UK: Cambridge University Press, 258-263
|
Barber P H, Palumbi S R, Erdmann M V et al, 2000. A marine Wallace's line?. Nature, 406(6797): 692-693 DOI:10.1038/35021135 |
Baumiller T K, Gahn F J, 2004. Testing predator-driven evolution with paleozoic crinoid arm regeneration. Science, 305(5689): 1453-1455 DOI:10.1126/science.1101009 |
Bellwood D R, Meyer C P, 2009. Searching for heat in a marine biodiversity hotspot. Journal of Biogeography, 36(4): 569-576 DOI:10.1111/j.1365-2699.2008.02029.x |
Bellwood D R, Renema W, Rosen B R, 2012. Biodiversity hotspots, evolution and coral reef biogeography: a review. In: Gower D J, Johnson K, Richardson J et al eds. Biotic Evolution and Environmental Change in Southeast Asia. Cambridge, UK: Cambridge University Press, 216-245
|
Bowen B W, Rocha L A, Toonen R J et al, 2013. The origins of tropical marine biodiversity. Trends in Ecology & Evolution, 28(6): 359-366 |
Briggs J C, 1966. Zoogeography and evolution. Evolution, 20(3): 282-289 DOI:10.1111/j.1558-5646.1966.tb03366.x |
Briggs J C, 2003. Marine centres of origin as evolutionary engines. Journal of Biogeography, 30(1): 1-18 DOI:10.1046/j.1365-2699.2003.00810.x |
Briggs J C, Bowen B W, 2013. Marine shelf habitat: biogeography and evolution. Journal of Biogeography, 40(6): 1023-1035 DOI:10.1111/jbi.12082 |
Burke L, Reytar K, Spalding M et al, 2012. Reefs at Risk Revisited in the Coral Triangle. Washington, DC: World Resources Institute
|
Colwell R K, Lees D C, Colwell R K et al, 2000. The mid-domain effect: geometric constraints on the geography of species richness. Trends in Ecology & Evolution, 15(2): 70-76 |
Costello M J, Tsai P, Wong P S et al, 2017. Marine biogeographic realms and species endemicity. Nature Communications, 8(1): 1057 DOI:10.1038/s41467-017-01121-2 |
Cowman P F, 2014. Historical factors that have shaped the evolution of tropical reef fishes: a review of phylogenies, biogeography, and remaining questions. Frontier in Genetics, 5: 394 |
Currie D J, Mittelbach G G, Cornell H V et al, 2004. Predictions and tests of climate-based hypotheses of broad-scale variation in taxonomic richness. Ecology Letters, 7(12): 1121-1134 DOI:10.1111/j.1461-0248.2004.00671.x |
Di Martino E, Jackson J B C, Taylor P D et al, 2018. Differences in extinction rates drove modern biogeographic patterns of tropical marine biodiversity. Science Advances, 4(4): eaaq1508 DOI:10.1126/sciadv.aaq1508 |
Dixon G B, Davies S W, Aglyamova, G V et al, 2015. Genomic determinants of coral heat tolerance across latitudes. Science, 348(6242): 1460-1462 DOI:10.1126/science.1261224 |
Dornburg A, Moore J, Beaulieu J M et al, 2015. The impact of shifts in marine biodiversity hotspots on patterns of range evolution: evidence from the Holocentridae (squirrelfishes and soldierfishes). Evolution, 69(1): 146-161 DOI:10.1111/evo.12562 |
Dueñas L F, Tracey D M, Crawford A J et al, 2016. The Antarctic Circumpolar Current as a diversification trigger for deep-sea octocorals. BMC Evolutionary Biology, 16: 2 DOI:10.1186/s12862-015-0574-z |
Etter R J, Rex M A, 1990. Population differentiation decreases with depth in deep-sea gastropods. Deep Sea Research Part A. Oceanographic Research Papers, 37(8): 1251-1261 DOI:10.1016/0198-0149(90)90041-S |
Etter R J, Rex M A, Chase M R et al, 2005. Population differentiation decreases with depth in deep-sea bivalves. Evolution, 59(7): 1479-1491 DOI:10.1111/j.0014-3820.2005.tb01797.x |
Evans S M, McKenna C, Simpson S D et al, 2016. Patterns of species range evolution in Indo-Pacific reef assemblages reveal the Coral Triangle as a net source of transoceanic diversity. Biology Letters, 12(6): 20160090 DOI:10.1098/rsbl.2016.0090 |
Goldberg E E, Lancaster L T, Ree R H, 2011. Phylogenetic inference of reciprocal effects between geographic range evolution and diversification. Systematic Biology, 60(4): 451-465 DOI:10.1093/sysbio/syr046 |
Goldberg E E, Roy K, Lande R et al, 2005. Diversity, endemism, and age distributions in macroevolutionary sources and sinks. The American Naturalist, 165(6): 623-633 DOI:10.1086/430012 |
Grassle J F, 1991. Deep-sea benthic biodiversity. Bioscience, 41(7): 464-469 DOI:10.2307/1311803 |
Grassle J F, Maciolek N J, 1992. Deep-sea species richness: regional and local diversity estimates from quantitative bottom samples. The American Naturalist, 139(2): 313-341 DOI:10.1086/285329 |
Gray J S, 1994. Is deep-sea species diversity really so high? Species diversity of the Norwegian continental shelf. Marine Ecology Progress Series, 112: 205-209 DOI:10.3354/meps112205 |
Green A L, Mous P J, 2008. Delineating the Coral Triangle, its ecoregions and functional seascapes. Version 5.0. TNC Coral Triangle Program Report 1/08, 44 |
Herbert T D, Lawrence K T, Tzanova A et al, 2016. Late Miocene global cooling and the rise of modern ecosystems. Nature Geoscience, 9(11): 843-847 DOI:10.1038/ngeo2813 |
Hillebrand H, 2004. On the generality of the latitudinal diversity gradient. The American Naturalist, 163(2): 192-211 DOI:10.1086/381004 |
Hodge J R, Bellwood D R, 2016. The geography of speciation in coral reef fishes: the relative importance of biogeographical barriers in separating sister-species. Journal of Biogeography, 43(7): 1324-1335 DOI:10.1111/jbi.12729 |
Huang D W, Goldberg E E, Chou L M et al, 2018. The origin and evolution of coral species richness in a marine biodiversity hotspot. Evolution, 72(2): 288-302 DOI:10.1111/evo.13402 |
Huang D W, Licuanan W Y, Hoeksema B W et al, 2015. Extraordinary diversity of reef corals in the South China Sea. Marine Biodiversity, 45(2): 157-168 DOI:10.1007/s12526-014-0236-1 |
Hubert N, Meyer C P, Bruggemann H J et al, 2012. Cryptic diversity in Indo-Pacific coral-reef fishes revealed by DNA-barcoding provides new support to the Centre-of-Overlap hypothesis. PLoS One, 7(3): e28987 DOI:10.1371/journal.pone.0028987 |
Hughes T P, Bellwood D R, Connolly S R, 2002. Biodiversity hotspots, centres of endemicity, and the conservation of coral reefs. Ecology Letters, 5(6): 775-784 DOI:10.1046/j.1461-0248.2002.00383.x |
Hume B C C, Voolstra C R, Arif C et al, 2016. Ancestral genetic diversity associated with the rapid spread of stress-tolerant coral symbionts in response to Holocene climate change. Proceedings of the National Academy of Sciences of the United States of America, 113(16): 4416-4421 DOI:10.1073/pnas.1601910113 |
Jablonski D, Belanger C L, Berke S K et al, 2013. Out of the tropics, but how? Fossils, bridge species, and thermal ranges in the dynamics of the marine latitudinal diversity gradient. Proceedings of the National Academy of Sciences of the United States of America, 110(26): 10487-10494 DOI:10.1073/pnas.1308997110 |
Jablonski D, Huang S, Roy K et al, 2017. Shaping the latitudinal diversity gradient: new perspectives from a synthesis of paleobiology and biogeography. The American Naturalist, 189(1): 1-12 DOI:10.1086/689739 |
Jablonski D, Sepkoski Jr J J, Bottjer D J et al, 1983. Onshore-offshore patterns in the evolution of phanerozoic shelf communities. Science, 222(4628): 1123-1125 DOI:10.1126/science.222.4628.1123 |
Jablonski D, Roy K, Valentine J W, 2006. Out of the tropics: evolutionary dynamics of the latitudinal diversity gradient. Science, 314(5796): 102-106 DOI:10.1126/science.1130880 |
Jacobs D K, Lindberg D R, 1998. Oxygen and evolutionary patterns in the sea: onshore/offshore trends and recent recruitment of deep-sea faunas. Proceedings of the National Academy of Sciences of the United States of America, 95(16): 9396-9401 DOI:10.1073/pnas.95.16.9396 |
Keith S A, Baird A H, Hughes T P et al, 2013. Faunal breaks and species composition of Indo-Pacific corals: the role of plate tectonics, environment and habitat distribution. Proceedings of the Royal Society B: Biological Sciences, 280(1763): 20130818 DOI:10.1098/rspb.2013.0818 |
Kiessling W, Simpson C, Foote M, 2010. Reefs as cradles of evolution and sources of biodiversity in the Phanerozoic. Science, 327(5962): 196-198 DOI:10.1126/science.1182241 |
Kinkade C, Marra J, Langdon C et al, 1997. Monsoonal differences in phytoplankton biomass and production in the Indonesian Seas: tracing vertical mixing using temperature. Deep Sea Research Part Ⅰ: Oceanographic Research Papers, 44(4): 581-592 DOI:10.1016/S0967-0637(97)00002-2 |
Knope M L, Bush A M, Frishkoff L O et al, 2020. Ecologically diverse clades dominate the oceans via extinction resistance. Science, 367(6481): 1035-1038 DOI:10.1126/science.aax6398 |
Kussakin O G, 1973. Peculiarities of the geographical and vertical distribution of marine isopods and the problem of deep-sea fauna origin. Marine Biology, 23(1): 19-34 DOI:10.1007/BF00394108 |
Ladd H S, 1960. Origin of the Pacific island molluscan fauna. American Journal of Science, 258-A: 137-150 |
Leprieur F, Descombes P, Gaboriau T et al, 2016. Plate tectonics drive tropical reef biodiversity dynamics. Nature Communications, 7: 11461 DOI:10.1038/ncomms11461 |
Levin L A, Etter R J, Rex M A et al, 2001. Environmental influences on regional deep-sea species diversity. Annual Review of Ecology and Systematics, 32: 51-93 DOI:10.1146/annurev.ecolsys.32.081501.114002 |
Lindner A, Cairns S D, Cunningham C W, 2008. From offshore to onshore: multiple origins of shallow-water corals from deep-sea ancestors. PLoS One, 3(6): e2429 DOI:10.1371/journal.pone.0002429 |
Little C T S, Vrijenhoek R C, 2003. Are hydrothermal vent animals living fossils?. Trends in Ecology & Evolution, 18(11): 582-588 |
Mannion P D, Upchurch P, Benson R B J et al, 2014. The latitudinal biodiversity gradient through deep time. Trends in Ecology & Evolution, 29(1): 42-50 |
Martín P V, Buček A, Bourguignon T et al, 2020. Ocean currents promote rare species diversity in protists. Science Advances, 6(29): eaaz9037 DOI:10.1126/sciadv.aaz9037 |
McClain C R, Hardy S M, 2010. The dynamics of biogeographic ranges in the deep sea. Proceedings of the Royal Society B: Biological Sciences, 277(1700): 3533-3546 DOI:10.1098/rspb.2010.1057 |
McManus L C, Vasconcelos V V, Levin S A et al, 2020. Extreme temperature events will drive coral decline in the Coral Triangle. Global Change Biology, 26(4): 2120-2133 DOI:10.1111/gcb.14972 |
McMonagle L B, Lunt P, Wilson M E J et al, 2011. A re-assessment of age dating of fossiliferous limestones in eastern Sabah, Borneo: implications for understanding the origins of the Indo-Pacific marine biodiversity hotspot. Palaeogeography, Palaeoclimatology, Palaeoecology, 305(1-4): 28-42 DOI:10.1016/j.palaeo.2011.02.009 |
Milliman J D, Farnsworth K L, 2011. River discharge to the coastal ocean: a global synthesis. Cambridge: Cambridge University Press, 143-144
|
Mora C, Chittaro P M, Sale P F et al, 2003. Patterns and processes in reef fish diversity. Nature, 421(6926): 933-936 DOI:10.1038/nature01393 |
Moss J A, Henriksson N L, Pakulski J D et al, 2020. Oceanic microplankton do not adhere to the latitudinal diversity gradient. Microbial Ecology, 79(2): 511-515 DOI:10.1007/s00248-019-01413-8 |
Naimark E B, Markov A V, 2011. Northward shift in faunal diversity: a general pattern of evolution of phanerozoic marine biota. Biology Bulletin Reviews, 1(1): 71-81 DOI:10.1134/S2079086411010075 |
Normile D, 2010. Joint expedition discovers deep-sea biodiversity, new volcanoes. Science, 329(5997): 1270-1271 |
Palumbi S R, 1996. What can molecular genetics contribute to marine biogeography? An Urchin's tale. Journal of Experimental Marine Biology and Ecology, 203(1): 75-92 DOI:10.1016/0022-0981(96)02571-3 |
Pandolfi J M, 1992. Successive isolation rather than evolutionary centres for the origination of Indo-Pacific reef corals. Journal of Biogeography, 19(6): 593-609 DOI:10.2307/2845703 |
Rabosky D L, Chang J, Title P O et al, 2018. An inverse latitudinal gradient in speciation rate for marine fishes. Nature, 559(7714): 392-395 DOI:10.1038/s41586-018-0273-1 |
Randall J E, Lim K K P, 2000. A checklist of the fishes of the South China Sea. The Raffles Bulletin of Zoology, Supplement, 8: 569-667 |
Raupach M J, Mayer C, Malyutina M et al, 2009. Multiple origins of deep-sea Asellota (Crustacea: Isopoda) from shallow waters revealed by molecular data. Proceedings of the Royal Society B: Biological Sciences, 276(1658): 799-808 DOI:10.1098/rspb.2008.1063 |
Renema W, Bellwood D R, Braga J C et al, 2008. Hopping hotspots: global shifts in marine biodiversity. Science, 321(5889): 654-657 DOI:10.1126/science.1155674 |
Rosenzweig M L, 1992. Species diversity gradients: we know more and less than we thought. Journal of Mammalogy, 73(4): 715-730 DOI:10.2307/1382191 |
Rosenzweig M L, 1995. Species Diversity in Space and Time. Cambridge, UK: Cambridge University Press, 460
|
Roy K, Goldberg E E, 2007. Origination, extinction, and dispersal: integrative models for understanding present-day diversity gradients. The American Naturalist, 170(S2): S71-S85 DOI:10.1086/519403 |
Sanciangco J C, Carpenter K E, Etnoyer P J et al, 2013. Habitat availability and heterogeneity and the Indo-Pacific Warm Pool as predictors of marine species richness in the tropical Indo-Pacific. PLoS One, 8(2): e56245 DOI:10.1371/journal.pone.0056245 |
Sanders H L, 1968. Marine benthic diversity: a comparative study. The American Naturalist, 102(925): 243-282 DOI:10.1086/282541 |
Stehli F G, Wells J W, 1971. Diversity and age patterns in hermatypic corals. Systematic Zoology, 20(2): 115-126 DOI:10.2307/2412052 |
Stevens G C, 1989. Integrating the supply chain. International Journal of Physical Distribution & Materials Management, 19(8): 3-8 |
Tittensor D P, Mora C, Jetz W et al, 2010. Global patterns and predictors of marine biodiversity across taxa. Nature, 466(7310): 1098-1101 DOI:10.1038/nature09329 |
Vermeij G J, 1987. Evolution and Escalation: An Ecological History of Life. Princeton, USA: Princeton University Press
|
Veron J E N, Devantier L M, Turak E et al, 2009. Delineating the Coral Triangle. Galaxea, Journal of Coral Reef Studies, 11: 91-100 |
Veron J E N, Stafford-Smith M, 2000. Corals of the World. Townsville, Australian: Australian Institute of Marine Science
|
Vinogradova N G, 1979. The geographical distribution of the abyssal and hadal (ultra-abyssal) fauna in relation to the vertical zonation of the ocean. Sarsia, 64(1-2): 41-50 DOI:10.1080/00364827.1979.10411361 |
Watling L, Guinotte J, Clark M R et al, 2013. A proposed biogeography of the deep ocean floor. Progress in Oceanography, 111: 91-112 DOI:10.1016/j.pocean.2012.11.003 |
Williams J J, Mills B J W, Lenton T M, 2019. A tectonically driven Ediacaran oxygenation event. Nature Communications, 10: 2690 DOI:10.1038/s41467-019-10286-x |
Willig M R, Kaufman D M, Stevens R D, 2003. Latitudinal gradients of biodiversity: pattern, process, scale, and synthesis. Annual Review of Ecology, and Systematics, 34: 273-309 DOI:10.1146/annurev.ecolsys.34.012103.144032 |
Wilson M E J, Rosen B R, 1998. Implications of paucity of corals in the Paleogene of SE Asia: plate tectonics or Centre of Origin?. In Hall R, Holloway J D eds. Biogeography and Geological Evolution of SE Asia. Leiden: Backhuys Publishers, 165-195
|
Woodland D J, 1983. Zoogeography of the Siganidae (Pisces): an interpretation of distribution and richness patterns. Bulletin of Marine Science, 33(3): 713-717 |
Woolley S N C, Tittensor D P, Dunstan P K et al, 2016. Deep-sea diversity patterns are shaped by energy availability. Nature, 533(7603): 393-396 DOI:10.1038/nature17937 |
Wu X W, Zhan Z F, Xu K D, 2019. Two new and two rarely known species of Branchinotogluma (Annelida: Polynoidae) from deep-sea hydrothermal vents of the Manus Back-Arc Basin, with remarks on the diversity and biogeography of vent polynoids. Deep Sea Research Part Ⅰ: Oceanographic Research Papers, 149: 103051 DOI:10.1016/j.dsr.2019.05.011 |
Wycech J, Kelly D C, Fournelle J et al, 2020. Reconstructing Pliocene West Pacific warm pool hydroclimate using in situ microanalyses on fossil planktic foraminifer shells. Paleoceanography and Paleoclimatology, 35(7): e2019PA003772 |
Zezina O N, 1997. Biogeography of the bathyal zone. Advances in Marine Biology, 32: 389-426 |
Zhao F, Filker S, Xu K D et al, 2017. Patterns and drivers of vertical distribution of the ciliate community from the surface to the abyssopelagic zone in the Western Pacific Ocean. Frontiers in Microbiology, 8: 2559 DOI:10.3389/fmicb.2017.02559 |
Zhao F, Filker S, Xu K D et al, 2019. Effects of intragenomic polymorphism in the SSU rRNA gene on estimating marine microeukaryotic diversity: a test for ciliates using single-cell high-throughput DNA sequencing. Limnology and Oceanography: Methods, 17(10): 533-543 DOI:10.1002/lom3.10330 |
Zhao F, Filker S, Xu K D et al, 2020. Microeukaryote communities exhibit phyla-specific distance-decay patterns and an intimate link between seawater and sediment habitats in the Western Pacific Ocean. Deep Sea Research Part Ⅰ: Oceanographic Research Papers, 160: 103279 DOI:10.1016/j.dsr.2020.103279 |
 2021, Vol. 52
2021, Vol. 52

