中国海洋湖沼学会主办。
文章信息
- 彭海, 尤凯, 符子峻, 王品杰, 张沛东, 张云岭. 2023.
- PENG Hai, YOU Kai, FU Zi-Jun, WANG Pin-Jie, ZHANG Pei-Dong, ZHANG Yun-Ling. 2023.
- 唐山祥云湾海洋牧场海域网采浮游植物群集特征研究
- STUDY ON THE ASSEMBLAGE CHARACTERISTICS OF NET-PHYTOPLANKTON IN MARINE RANCHING AREA OF XIANGYUN BAY, TANGSHAN, CHINA
- 海洋与湖沼, 54(4): 1070-1084
- Oceanologia et Limnologia Sinica, 54(4): 1070-1084.
- http://dx.doi.org/10.11693/hyhz20221200343
文章历史
-
收稿日期:2022-12-30
收修改稿日期:2023-02-16
2. 唐山海洋牧场实业有限公司 河北唐山 063600
2. Tangshan Marine Ranching Industrial Limited Company, Tangshan 063600, China
浮游植物通过光合作用将二氧化碳固定为有机碳, 进而开启了海洋食物网中的物质循环和能量流动, 是海洋生态系统中最重要的初级生产者, 供应了地球上近50%的初级生产量(Field et al, 1998), 且浮游植物对环境的变化较为敏感(吴玉霖等, 2005), 对其群落特征及变化的研究是评价水体富营养化状态以及生态系统的健康状况的重要依据(Garmendia et al, 2013), 也是掌握研究区域浮游生态系统结构的基础。
随着海洋牧场和人工鱼礁区建设, 该类水域浮游生物监测研究也逐渐引起了国内研究者的重视。目前海洋牧场和人工鱼礁区关于浮游生物的研究主要通过投礁前后以及投礁区与对照区浮游生物群落结构进行对比(雷安平等, 2009; 张皓宇等, 2016; 谢斌等, 2017), 分析投礁所带来的生态修复效果, 并通过浮游生物与投礁区环境因子的相关性分析探讨鱼礁建设对浮游生物产生的生态效应关系(陈传曦等, 2021), 但这些研究报道多是基于该类水域浮游生物的季度调查进行的(宋秀贤等, 2007; 陈海峰等, 2013; 李大鹏等, 2017)。由于浮游生物可快速对环境变化作出响应, 其群落的变动方面具有快速和短时效性的特征, 因此, 以基于季度月调查为主的低频次的浮游生物调查对于解析该类水域浮游生物的动态过程就受到较大的局限。而这些重要信息的缺乏, 必然会对合理地解析和认识这类海洋牧场或人工鱼礁区水域的生态过程产生制约, 影响着人们对于海洋牧场或人工鱼礁水域的基础生物效应的正确理解。张雪等(2016)通过对獐子岛海域浮游植物进行周年逐月调查完整地呈现出了全年浮游植物丰度波动情况以及优势种演替特征; 罗璇等(2016)对胶州湾周年逐月调查发现浮游植物丰度变化与该区域前期报道的典型双峰型特征并不相同, 这说明对研究区域浮游植物进行高频次的连续监测才能提高对其生态评价的准确性, 而这一方面的研究资料亟待补充。
唐山祥云湾海洋牧场位于乐亭县京唐港南部海域, 为首批国家级海洋牧场示范区, 水深6~13 m, 海洋牧场于2018年6月完成礁体投放工作, 鱼礁区面积为57.33 km2。本研究中鱼礁区分为3 000亩礁区以及860亩礁区, 其中, 3 000亩礁区位于海洋牧场的东南侧海域, 860亩礁区位于海洋牧场的南侧海域, 礁体主要为牡蛎礁。从目前的研究来看, 对该区域的研究主要聚焦于水质状况的监测以及鱼礁的生态效应分析等方面(杨心愿, 2019; 叶敏等, 2021), 浮游植物周年逐月的研究尚未见报道。鉴于以上, 我们选取祥云湾海洋牧场作为典型调查海域, 拟通过“半月-逐月”的高频次浮游生物监测, 来获得高频次的浮游生物数据, 并基于这些监测数据来解析典型海洋牧场海域浮游生物的关键生态过程, 进而探讨该类水域的基础生物效应, 并为海洋牧场海域的基础生物效应研究提供基础支撑数据。
1 材料与方法 1.1 采样站位于2020年11月至2021年11月进行连续13个月(2021年5~10月为半月采样, 其余月份为逐月)的采样调查, 采样站位分为3个鱼礁区和3个对照区。具体采样站位见图 1。
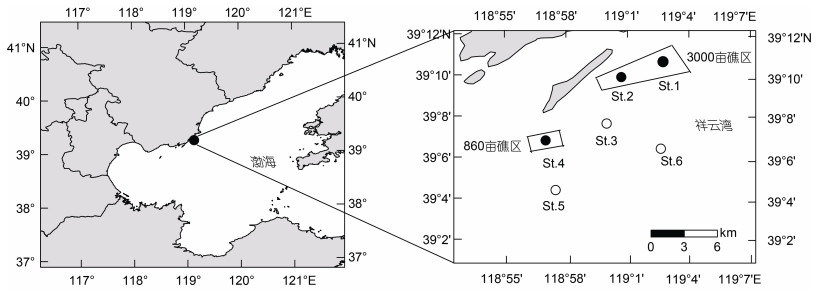 |
| 图 1 采样站位图 Fig. 1 Map of sampling stations |
浮游植物样品采集按照《海洋调查规范第6部分》(GB/T 12763.1–2007), 使用浅水Ⅲ型浮游生物网(网长140 cm, 网口内径37 cm, 网口面积0.1 m2, 筛绢规格JP80, 孔径0.077 mm)自离底2 m至表层垂直拖曳。网采浮游植物样品用浓度为5%的甲醛固定浓缩后在光学显微镜下进行鉴定和计数; 浮游桡足类样品的采集与浮游植物采集同步进行, 5~10月为半月采样, 其余月份为逐月采样, 采用浅水Ⅲ型浮游生物网采集, 样品用浓度为5%的甲醛固定浓缩, 在光学显微镜下进行鉴定和计数。环境因子方面, 水温(T)、盐度(S)和pH采用便携式水质分析仪(YSI-556型)现场测定, 悬浮物(SS)、溶解有机碳(DOC)、亚硝酸盐(NO2)、氨氮(NH4)、硝酸盐(NO3)、磷酸盐(DIP)、硅酸盐(DSi)、总氮(TN=DIN+DON)和总磷(TP)以上项目分析方法按照《海洋监测规范第4部分》(GB 17378.4–2007)。
1.3 数据处理分析群落结构指数分别采用Shannon-Wiener多样性指数(H')、Pielou均匀度指数(J)、Margalef丰富度指数(D)及优势度指数(Y)分析, 计算公式如下:
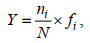 (1)
(1)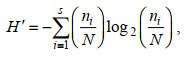 (2)
(2)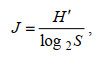 (3)
(3)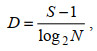 (4)
(4)式中: Y为优势度, 将优势度Y≥0.02的优势类群作为优势种。N为所有种的个体总数, ni为第i种的个体数, fi为第i种的出现频率, S为物种种类总数。
由于浮游植物单个优势种与其他浮游植物种间存在空间、营养盐等方面竞争, 会使得单个优势种的演替变化趋势持续较短, 不利于展现变化规律, 而浮游植物优势类群的连续性变化和规律性效果更好, 更利于发掘规律, 结果和分析中均以圆筛藻、角毛藻、角藻等优势类群来探讨。本研究中圆筛藻类群出现数量较多的种主要有: 星脐圆筛藻、格氏圆筛藻、虹彩圆筛藻、威利圆筛藻4个种。角毛藻类群出现数量较多的种主要有: 劳氏角毛藻、旋链角毛藻、卡氏角毛藻、柔弱角毛藻、密联角毛藻、并基角毛藻、窄隙角毛藻7个种。角藻类群出现数量较多的种主要有: 梭角藻、三角角藻、长角角藻3个种。舟形藻类群下仅有1个种。文中的“链状浮游植物”指在自然状态下, 形态上由单个细胞形成链状的浮游植物群体; “非链状浮游植物”指在自然状态下, 形态上细胞不形成链状的浮游植物群体。本研究把能形成链状群体的硅藻和甲藻归为链状浮游植物, 其余归为非链状浮游植物。
文中的Pearson相关性分析、冗余分析(RDA)以及浮游生物与部分环境因子指标的差异部分的数据计算为全年19个航次的原始数据, 其余图形绘制中5~10月的半月数据为逐月平均结果。
采用CANOCO 4.5软件分析浮游植物与环境因子的相关性, 首先建立物种丰度矩阵进行去趋势对应分析(DCA), 根据其排序轴梯度长度均小于3, 选择基于线性模型的冗余分析(RDA)进行排序。利用forward selection选项中的自动筛选功能选出通过进行999次蒙特卡罗置换检验(Monte Carlo Permutation test)(P < 0.05)的环境因子。采样站位图采用ARCGIS 10.2绘制, 用ORIGIN 2018软件进行绘图。
2 结果 2.1 浮游植物丰度、优势类群、群落结构指数周年变化 2.1.1 浮游植物丰度变化调查共鉴定浮游植物41属78种, 其中硅藻33属62种, 甲藻7属15种, 硅鞭藻1属1种, 浮游植物类群以硅藻为主, 其次为甲藻。礁区与对照区浮游植物丰度逐月变化见图 2。礁区浮游植物丰度最低值出现在12月, 为12.62×104 cells/m3, 最高值出现在10月, 为885.46×104 cells/m3, 全年丰度平均为202.39×104 cells/m3; 对照区浮游植物丰度最低值出现在2月, 为22.63×104 cells/m3, 最高值出现在8月, 为940.52×104 cells/m3, 平均为208.68× 104 cells/m3。两区域浮游植物丰度全年差异不明显, 但礁区浮游植物丰度峰值出现时间较对照区推迟2个月。整体上, 两区域浮游植物丰度全年均在秋季时期最高, 其次为冬季, 春季最低。
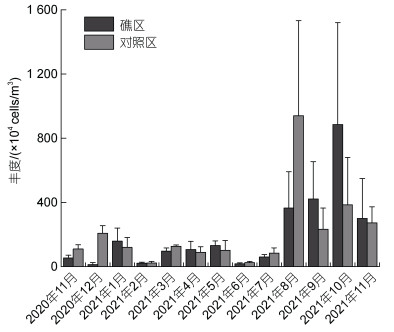 |
| 图 2 礁区与对照区浮游植物丰度逐月变化 Fig. 2 Monthly variation of phytoplankton abundance between reef and control areas |
优势类群及优势度逐月变化见图 3。角藻(3个种)全年在低温的12月优势度最高, 达到0.26; 对照区角藻优势度最高出现在1月, 达到0.23, 其丰度从3月开始逐渐下降趋势。1月和2月礁区与对照区暖水近岸性的优美旭氏藻以及底栖性的具槽帕拉藻均成为优势类群, 3~5月北方近岸冷水性的诺氏海链藻占优势, 随后其丰度迅速消退不再成为优势类群。6月圆筛藻成为绝对优势类群, 在礁区和对照区优势度分别达到0.836、0.518。6月后, 角毛藻丰度迅速增加, 礁区角毛藻在2021年11月优势度达到最高, 为0.631, 对照区优势度最高在8月, 为0.587。9~10月广温广布的中肋骨条藻迅速增殖也成为优势类群, 11月丰度迅速下降, 不再成为优势类群。整体上, 周年水平圆筛藻和角毛藻优势度最高, 分别为0.25、0.20。优势类群的周年演替存在明显的非渐进变化时段, 圆筛藻在11~6月为主要优势类群, 角毛藻在6月后占据主要优势, 两区域浮游植物优势类群在不同时期变化特征基本一致。
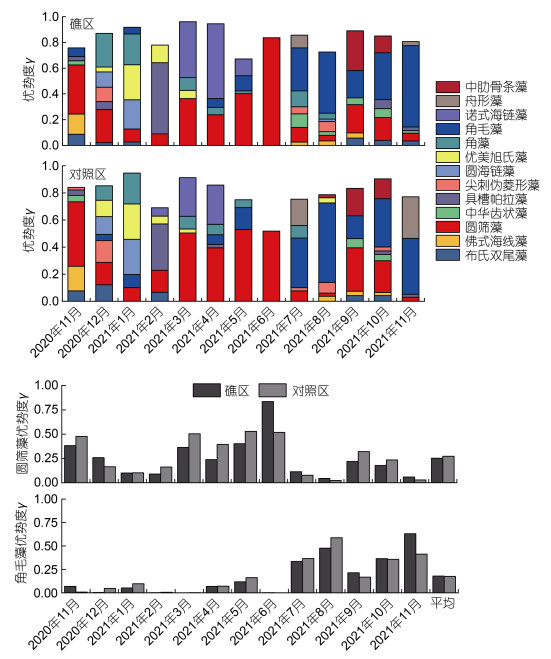 |
| 图 3 礁区与对照区浮游植物优势类群及优势度逐月变化 Fig. 3 Monthly variation of phytoplankton dominant groups and dominance between reef and control areas |
浮游植物群落结构指数变化见图 4。礁区H'变化范围为0.96~3.85, 均值为2.84, 最高值出现在12月, 最低值出现在6月, J变化范围为0.25~0.77, 均值为0.59, 最高值也出现在12月, 最低值在6月, D变化范围为0.65~2.12, 均值为1.34, 最高值出现在8月, 最低值出现在4月; 对照区H'变化范围为1.70~4.10, 均值为2.92, J变化范围为0.43~0.76, 均值为0.61, 其H'、J最高值和最低值与礁区同步。D变化范围为0.40~1.95, 均值为1.30, 最高值出现在12月, 最低值出现在5月, 与礁区略有差异。整体上, 礁区与对照区浮游植物群落结构指数周年变化均呈现出11~5月、7~11月高, 6月低的特征, 两区域浮游植物群落结构指数逐月变化趋势基本一致。
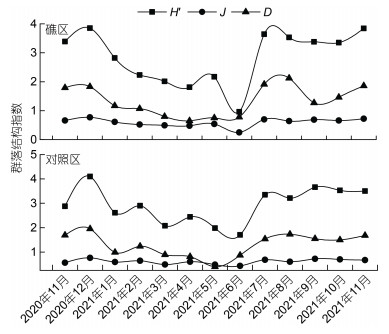 |
| 图 4 礁区与对照区浮游植物群落结构指数逐月变化 Fig. 4 Monthly variation of phytoplankton community structure index between reef and control areas |
通过将礁区与对照区浮游植物群落种类的丰度进行聚类, 群落聚类结果见图 5。礁区在群落距离为0.80的水平上所有月份可划分为3个时期, 分别为11~2、3~6、7~11月; 对照区在群落距离为0.80的水平上所有月份与礁区一致, 也可划分为3个时期, 即11~2、3~6、7~11月。11~2月, 该时期主要特征为水温全年最低, 平均为2.73 ℃, 生物活动强度也低; 3~6月主要特征为温度上升, 浮游桡足类及牡蛎等生物活动频繁, 生长快、新陈代谢旺盛; 7~11月主要特征为生物仍然有适宜其活动的温度, 但温度逐步下降; 可见, 礁区和对照区浮游植物群落种类均可划分为3个一致的时期, 即泛冬季低温期(11~2月)、春夏季繁生期(3~6月)以及泛秋季降温期(7~11月)。
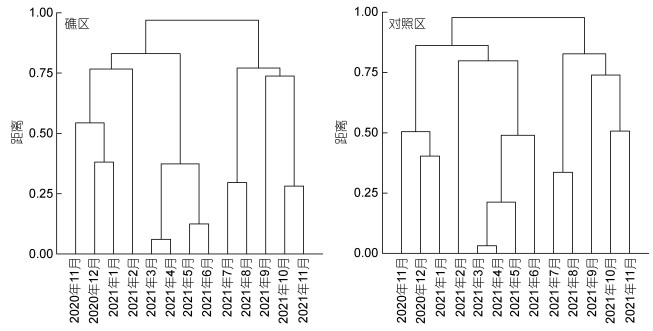 |
| 图 5 礁区与对照区浮游植物群落聚类 Fig. 5 Cluster analysis of phytoplankton community between reef and control areas |
礁区与对照区浮游植物群落丰度占比及群落结构指数差异见图 6。礁区硅藻、甲藻在3个不同时期浮游植物群落中的平均丰度占比分别为92.33%、7.67%, 对照区分别为93.33%、6.67%, 差异不明显。具体时期上, 泛冬季低温期, 硅藻在对照区丰度占比达到90%, 而礁区为86%, 丰度占比差异最大; 甲藻在礁区的占比(14%)明显高于对照区(10%), 也在该时期占比差异达到最大。链状、非链状浮游植物在礁区浮游植物群落中的平均丰度占比分别为47%、53%, 对照区分别为42.67%、57.33%, 总体表现出链状浮游植物礁区高于对照区, 非链状浮游植物礁区低于对照区的特征。在泛秋季降温期, 链状浮游植物丰度占比在礁区明显高于对照区, 差异达到10%, 而非链状浮游植物丰度占比礁区明显低于对照区, 占比差异也达到10%。礁区与对照区仅多样性指数在春夏季繁生期差异最大(礁区高于对照区0.31), 其余指数在3个时期差异均不明显; H'、J、D均表现出泛秋季降温期>泛冬季低温期>春夏季繁生期的特征。
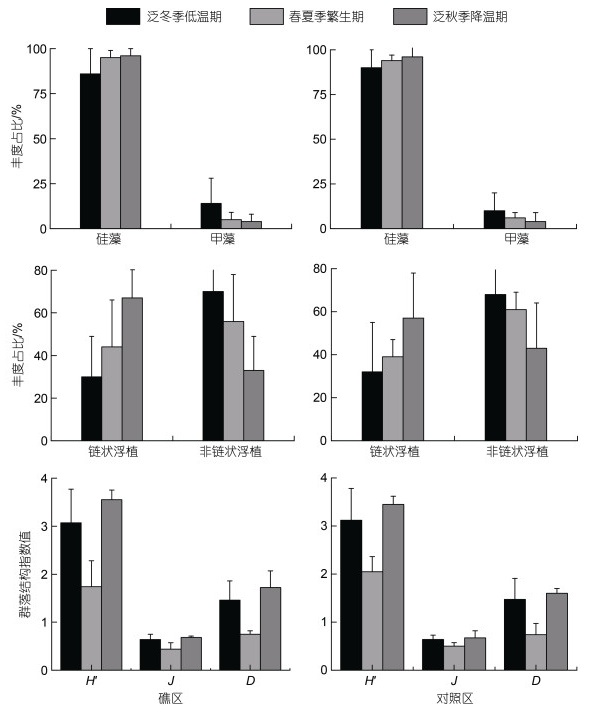 |
| 图 6 浮游植物群落丰度占比及群落结构指数差异 Fig. 6 Proportion of phytoplankton community abundance and differences in community structure index |
礁区与对照区浮游生物指标的差异见图 7a。浮游生物指标方面, 链状浮游植物的丰度在礁区明显高于对照区, 丰度均值百分比差异达到8.82%, 礁区其余浮游生物丰度均值均低于对照区; 其中, 礁区甲藻丰度均值低于对照区丰度均值的差异最大, 达到23.45%。丰度频次方面, 浮游植物、硅藻以及链状浮游植物礁区高于对照区, 浮游桡足类、甲藻以及非链状浮游植物则相反; 其中, 链状浮游植物频次礁区高于对照区的百分比差异最大, 达到71.43%。
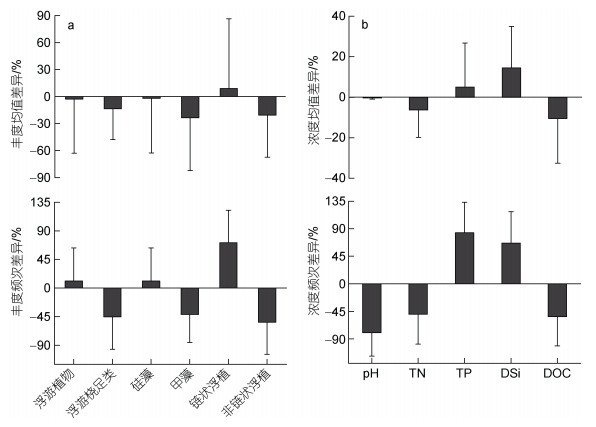 |
| 图 7 礁区与对照区浮游生物与部分环境因子指标的差异 Fig. 7 Difference of indices to plankton and some environmental factors between reef and control areas 注: 丰度、浓度均值差异即全年礁区浮游生物丰度均值、环境因子浓度高于全年对照区浮游生物丰度均值、环境因子浓度均值的百分比; 频次差异即全年礁区浮游生物、环境因子出现的次数多于全年对照区浮游生物、环境因子出现的次数的百分比。均值差异以及频次差异百分比计算方法为: (礁区-对照区)/对照区×100% |
为分析礁区生物活动对浮游植物群集的影响, 选取与生物作用关系密切的环境因子进行比较, 礁区与对照区部分环境因子指标的差异见图 7b。pH、TN、DOC在礁区的均值低于对照区, 而TP、DSi礁区均值高于对照区; 其中, 礁区DSi均值高于对照区DSi均值百分比差异最大, 达到14.49%。环境因子频次方面, pH、TN、DOC礁区也低于对照区, 与环境因子均值同步, TP、DSi礁区也高于对照区; 其中, TP频次礁区高于对照区百分比差异最大, 达到83.33%, 其次为DSi, 达到66.67%。
2.4 礁区和对照区浮游植物与浮游桡足类、环境因子关系的差异 2.4.1 浮游植物与浮游桡足类丰度关系浮游植物与浮游桡足类丰度逐月变化见图 8。礁区与对照区浮游植物在泛冬低温期至春夏季繁生期(6月前)丰度均较低, 泛秋季降温期(6月后)丰度迅速上升, 礁区浮游植物丰度在10月达到最高值, 而对照区最高值在8月, 较礁区提前2个月出现峰值; 礁区与对照区浮游桡足类丰度均在春夏季繁生期的3月达到最高, 分别为45.8×103、44.4×103 ind./m3, 泛秋季降温期浮游桡足类丰度上下波动, 但均低于春夏季繁生期。整体上, 浮游植物与浮游桡足类的丰度逐月变化未表现出生态学上捕食者与被捕食者之间典型的消长关系。此外, 礁区与对照区浮游植物和浮游桡足类的丰度变化在6月前一致性较高, 但6月后出现差异, 主要表现在浮游植物丰度在峰值出现的时间上差异明显。
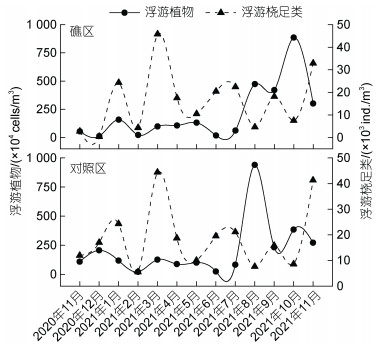 |
| 图 8 礁区与对照区浮游植物及浮游桡足类丰度逐月变化 Fig. 8 Monthly variation in abundance of phytoplankton and copepods between reef and control areas |
礁区与对照区浮游植物与环境因子Pearson相关比较结果见表 1。总体上, 3个时期相关关系差异明显。泛冬季低温期, 两区域浮游植物与环境因子的显著相关关系在3个时期中出现较少, 礁区浮游植物与营养盐因子中的TP呈显著正相关关系, 而对照区与TN达到显著正相关; 礁区非营养盐环境因子中仅SS与甲藻呈显著正相关关系, 而对照区非营养盐环境因子中的DO、SS均与浮游生物呈显著正相关关系。春夏季繁生期, 浮游植物与环境因子的显著相关关系在3个时期中出现最多, 且主要呈现出负相关关系。礁区链状浮游植物以及甲藻与营养盐因子中的DIP呈现显著负相关关系, 而对照区则未达到显著相关水平。礁区非营养盐因子中的pH对浮游桡足类呈现显著负相关关系, 对照区浮游植物与T呈显著负相关关系。泛秋季降温期, 礁区浮游植物与TN、NH4以及DIN均未达到显著相关水平, 而对照区浮游植物与NH4以及DIN达到显著负相关关系。
| 时期 | 区域 | 项目 | T | DO | pH | SS | S | DOC | NH4 | NO2 | NO3 | TN | DIP | TP | DSi | DIN | N/P |
| 泛冬季低温期 | 礁区 | 浮游植物 | ▲ | ||||||||||||||
| 浮游桡足类 | ▲ | ||||||||||||||||
| 链状浮植 | ▲ | ||||||||||||||||
| 非链状浮植 | ▲ | ||||||||||||||||
| 硅藻 | ▲ | ||||||||||||||||
| 甲藻 | ▲ | ▲ | |||||||||||||||
| 对照区 | 浮游植物 | ▲ | ▲▲ | ▲ | |||||||||||||
| 浮游桡足类 | ▲ | ▲ | ▲ | ||||||||||||||
| 链状浮植 | ▲▲ | ▲▲ | ▲ | ||||||||||||||
| 非链状浮植 | ▲ | ||||||||||||||||
| 硅藻 | ▲ | ▲▲ | |||||||||||||||
| 甲藻 | ▲ | ▲▲ | |||||||||||||||
| 春夏季繁生期 | 礁区 | 浮游植物 | ▲ | ∆∆ | ∆∆ | ||||||||||||
| 浮游桡足类 | ∆ | ∆ | ∆∆ | ▲ | |||||||||||||
| 链状浮植 | ▲ | ∆ | ∆ | ∆∆ | ∆ | ∆ | ∆ | ▲ | |||||||||
| 非链状浮植 | ▲ | ∆ | ∆ | ||||||||||||||
| 硅藻 | ▲ | ∆∆ | ∆∆ | ||||||||||||||
| 甲藻 | ∆∆ | ∆ | ▲▲ | ∆∆ | ▲▲ | ∆∆ | ∆ | ∆∆ | ∆ | ||||||||
| 对照区 | 浮游植物 | ∆ | ▲ | ∆ | ∆∆ | ∆∆ | |||||||||||
| 浮游桡足类 | |||||||||||||||||
| 链状浮植 | ∆∆ | ∆ | |||||||||||||||
| 非链状浮植 | ∆ | ▲ | ∆ | ∆ | |||||||||||||
| 硅藻 | ∆ | ▲ | ∆∆ | ∆ | |||||||||||||
| 甲藻 | ∆∆ | ▲ | ∆ | ∆ | ∆ | ∆∆ | ∆ | ||||||||||
| 泛秋季降温期 | 礁区 | 浮游植物 | ∆ | ||||||||||||||
| 浮游桡足类 | ∆ | ||||||||||||||||
| 链状浮植 | |||||||||||||||||
| 非链状浮植 | ∆ | ||||||||||||||||
| 硅藻 | ∆ | ||||||||||||||||
| 甲藻 | ∆∆ | ∆ | ∆ | ||||||||||||||
| 对照区 | 浮游植物 | ∆ | ∆ | ||||||||||||||
| 浮游桡足类 | ▲ | ||||||||||||||||
| 链状浮植 | ∆ | ||||||||||||||||
| 非链状浮植 | ∆ | ||||||||||||||||
| 硅藻 | ∆ | ∆ | |||||||||||||||
| 甲藻 | ▲ | ∆∆ | ∆∆ | ∆ | ▲ | ∆∆ | |||||||||||
| 注: “▲”正相关性显著, “▲▲”正相关性极显著; “∆”负相关性显著, “∆∆”负相关性极显著。T: 水温; DO: 溶解氧; S: 盐度; SS: 悬浮物; DOC: 溶解有机碳; NO2: 亚硝酸盐; NH4: 氨氮; NO3: 硝酸盐; DIN: 溶解无机氮; DIP: 磷酸盐; DSi: 硅酸盐; TN: 总氮; TP: 总磷; N/P: 氮磷比 | |||||||||||||||||
礁区与对照区不同时期浮游植物与环境因子的RDA排序见图 9。RDA排序结果亦显示3个时期两区域浮游植物与环境因子的相关关系差异明显。泛冬季低温期, 礁区(图 9a)浮游植物群落与TP表现出明显正相关关系, 对照区(图 9b)浮游植物群落与营养盐因子显著相关性不明显; 礁区浮游植物群落与SS表现出明显正相关关系, 对照区SS和DO为浮游植物群落为主要影响因子。春夏季繁生期, 礁区(图 9c)浮游植物群落与DIP、DSi表现出显著负相关关系, 对照区(图 9d)浮游植物群落与TN、DSi表现出显著负相关关系; 礁区浮游植物群落与S表现出显著正相关关系, 而与T为显著负相关关系, 对照区浮游植物群落与S也表现出显著正相关关系, T为显著负相关关系。泛秋季降温期, 礁区(图 9e)浮游植物群落与NO2表现出明显的负相关关系, 对照区(图 9f)浮游植物群落与TN呈现正相关关系, 而与DIN、NH4主要表现出显著负相关关系。总体上, RDA分析显示的两区域浮游植物与环境因子的相关关系与Pearson相关分析显示的相关关系基本一致。
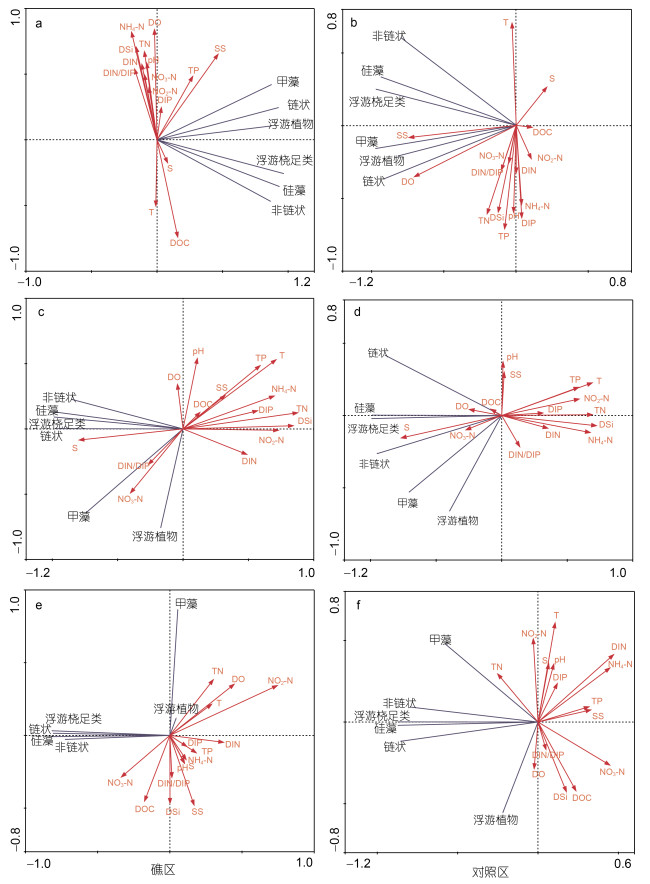 |
| 图 9 礁区与对照区浮游植物与环境因子的RDA排序 Fig. 9 RDA ordination of phytoplankton and environmental factors between reef and control areas 注: 图a为礁区泛冬季低温期; b为对照区泛冬季低温期; c为礁区春夏季繁生期; d为对照区春夏季繁生期; e为礁区泛秋季降温期; f为对照区泛秋季降温期 |
浮游植物会显著受到贝类等生物滤食的影响, 如郭皓等(1999)在辽宁李家湾近岸贝类筏式养殖区发现筏区内浮游植物的数量略少于筏区外, 且高峰期的出现较筏区外滞后1个月; 关莹莹等(2022)在浙江枸杞岛贝类养殖区调查发现筏式养殖区内所处水层中的浮游植物平均丰度较养殖场外表层浮游植物丰度显著偏低。类似地, 增养殖海域浮游植物丰度受到增养殖对象的下行作用影响已有较多报道(张玲等, 2015; 潘玉龙等, 2019; 许钰涵, 2021)。本研究中浮游植物丰度在春夏季繁生期处于全年最低水平, 这应与本研究海域的人工鱼礁为典型的牡蛎礁, 礁体上也附着大量的周丛生物, 春夏季繁生期随着水温升高其摄食活动增强, 对浮游植物产生明显的摄食压力, 从而导致该时期浮游植物丰度现存量最低有关。
优势类群演替方面, 从逐月来看, 2月冰期之后, 3~5月北方冷水性的诺氏海链藻逐渐占优势, 7~11月角毛藻持续成为优势类群。其中, 诺氏海链藻在初春成为优势种应与泛冬季外海水的汇入有密切关系, 在泛冬季外海性的诺氏海链藻与梭角藻数量也增多, 显示外海水的汇入可能是该时期诺氏海链藻以及梭角藻成为优势种的重要原因。7~8月水体悬浮物浓度达到48.58 mg/L, 明显高于前期月份浓度, 显示水体混合增强, 同时, 7~8月靠近外海一侧的对照区的角毛藻丰度持续高于靠近近岸一侧的礁区, 且对照区角毛藻的优势度上升明显, 可见泛秋季角毛藻持续成为优势类群, 应与7~8月主要来自外部海水的角毛藻的汇入有密切关系。
全年来看, 圆筛藻和角毛藻类群为最占优势的类群, 优势度分别达到0.26、0.18。其中, 7月前主要是圆筛藻类群占优势, 优势度平均达到0.34。已有研究表明, 牡蛎对细胞粒径偏小的浮游植物具有更高的摄食效率(Riisgård, 1988; 王芳等, 2000), 圆筛藻细胞粒径大, 被牡蛎滤食的几率较细胞粒径小的浮游植物低, 这可能是本研究中圆筛藻在7月前为主要优势类群重要原因。7月后, 角毛藻替代前期的圆筛藻占据优势, 7~11月优势度平均达0.39。该时期N/P比值为21, DIP浓度为0.009 mg/L, 磷含量相对较低, 已有研究表明, 角毛藻对磷营养盐具有低的半饱和常数(Ks)以及对磷吸收表现出高的生长速率(Eppley et al, 1969; Turpin et al, 1979), 且角毛藻细胞为长链状不易被牡蛎等贝类摄食, 以上可能是角毛藻在泛秋季持续成为优势类群的重要原因。
本研究中, 甲藻在泛冬季低温期的优势度高于春夏季繁生期, 这与于湖洋等(2016)在秦皇岛的研究中指出浮游植物全年均值为2.42×108 cells/m3, 而甲藻类群在6月的丰度达到了1.39×108 cells/m3的调查结果截然相反。一方面, 泛冬季水温低, 牡蛎等贝类以及浮游动物活动强度低, 对甲藻下行抑制作用弱; 另一方面, 梭角藻对磷营养盐具有低的半饱和系数(Ks)以及对磷酸盐具有较强亲和力(Huang et al, 2005; Baek et al, 2008), 且牡蛎等聚集的动物也向水体排泄氮、磷等营养盐, 从而较好缓解了甲藻在该时期磷营养盐补给弱的问题, 加上该时期外海水的汇入也使甲藻类的梭角藻数量增加, 就使得泛冬季低温期的甲藻优势度反而高于春夏季繁生期。
许多近岸研究报道显示, 浮游植物群落结构指数一般在春季会达到高峰或次高峰, 如江志兵等(2012)在象山港海域、郑珊等(2014)在胶州湾海域、林虓等(2015)在青岛滨海水域以及刘长东等(2016)在山东荣成俚岛海域的报道等。但本研究中的浮游植物群落结构指数却在春夏季繁生期达到全年最低, 这与以上诸多报道截然相反。与以上缺乏强烈滤食作用的典型近岸自然海域不同, 本研究中, 除浮游动物摄食之外, 人工鱼礁上附生的牡蛎等贝类在春夏季繁生期会对浮游植物产生明显的下行抑制作用(张玲等, 2015), 使其在该时期的丰度显著降低, 并导致其群落结构单一, 群落结构指数亦显著降低, 这应是本研究与以往报道不同的重要原因。此外, 本研究中浮游植物群落物种多样性指数水平仍较高, 年均值达到2.88, 高于邻近海域报道的浮游植物多样性指数(张建乐等, 2010; 李莉等, 2013; 慕建东等, 2015)。依据《近岸海域环境监测技术规范》(HJ 442-2008)的标准, 该海域的群落结构较为稳定, 海域生境质量良好。对比其他投饵型的典型增养殖区, 祥云湾人工鱼礁海域浮游植物的群落物种多样性指数也明显为高(李希磊等, 2018; 刘萍等, 2019; 潘玉龙等, 2019), 显示人工鱼礁型海洋牧场的建设对海域内水质条件的改善、浮游生物物种多样性的提高以及水域生态系统稳定等方面起到了积极作用。
本研究中礁区与对照区浮游植物的丰度、群落结构差异均不明显, 国内人工鱼礁海域大多研究都有类似的报道(张硕等, 2006; 杨柳等, 2011; 戴媛媛等, 2018; 张智鹏等, 2020), 研究者将其归因于投礁时间短(刘长东等, 2015)、礁区生态效应不稳定(张雪等, 2018)等原因。我们认为另一个重要原因是近岸海域潮汐往复流混合作用带来的影响, 根据邓筱凡(2022)对祥云湾海域的研究结果, 祥云湾海域水体平均流速接近2 km/h, 而多数相关报道中的礁区与对照区距离通常在2 km左右。据以上结果推测, 礁区与对照区在潮汐往复流的作用下一昼夜内可发生多次海水混合, 进而导致监测结果中浮游植物丰度、群落结构差异不明显。
3.2 浮游植物及环境指标在礁区与对照区的差异本研究中, 浮游植物及环境指标在礁区与对照区的差异以链状浮游植物丰度、甲藻丰度、DOC和pH最为明显。其中, 链状浮游植物丰度的年均占比礁区明显高于对照区, 特别是在滤食活动强烈的春夏季繁生期和泛秋季降温期表现更为明显(图 6)。同时, 链状浮游植物的丰度在礁区高于对照区的出现频次也显著多于对照区高于礁区的出现频次(图 7)。
链状浮游植物在春夏季繁生期以及泛秋季降温期的丰度均高于对照区, 牡蛎等贝类对浮游植物的滤食选择性应是其主要原因。许多研究报道表明牡蛎等贝类对细胞粒径偏小的浮游植物的滤食作用更为明显(Fritz et al, 1984; 张莉红等, 2008), 鉴于链状浮游植物的等效粒径偏大, 因此其被滤食的概率较粒径偏小的浮游植物为低, 从而使得链状浮游植物的留存量较高, 而在泛冬季水温的显著降低, 牡蛎等贝类通过滤食对浮游植物产生的下行作用明显减弱, 礁区链状浮游植物丰度则未出现明显高于对照区的情况。此外, Takabayashi等(2006)报道在营养盐供给充足的条件下, 链状浮游植物在浮游植物的种间竞争中更易取得优势, 而本研究中磷、硅等营养盐浓度礁区高于对照区, 这可能也是链状浮游植物在礁区出现数量较高的另一个重要原因。礁区附着贝类的滤食作用以及营养盐浓度均高于对照区是人工鱼礁海域的典型生物环境特征, 而强滤食作用与高营养盐更有利于礁区链状浮游植物的留存和生长, 本研究也很好地验证了这一结果。因此, 今后对于人工鱼礁海域的研究, 建议可将链状浮游植物作为考查礁区与对照区差异的一个重要指标。
甲藻在全年以及春夏季繁生期的丰度均表现出礁区低于对照区的特征, 且礁区与对照区的甲藻丰度均在春夏季繁生期达到最低, 牡蛎等贝类的滤食选择性也是主要原因。相关研究报道指出, 牡蛎等贝类对浮游植物摄食具有选择性, 更偏向于摄食甲藻(张玲等, 2015; 王兆慧等, 2020), 礁区的牡蛎礁上有大量的牡蛎等贝类以及周丛生物, 甲藻受到牡蛎等贝类的下行抑制作用强烈, 这就导致礁区甲藻丰度低于对照区。此外, 春夏季繁生期水温逐渐回暖, 礁区牡蛎等贝类生物活动强度不断增加, 新陈代谢加快, 对浮游植物产生强烈的摄食压力, 从而导致礁区与对照区的甲藻丰度均在春夏季繁生期达到最低。
溶解有机物(DOM)主要来源于各类海洋生物的代谢释出, 通常某海域内的生物越多、活动越频繁, 其浓度亦越增高。生态研究中, 通常以DOC作为溶解有机物的表征指标(Hansell et al, 2015)。本研究中, 总体上DOC的浓度在礁区低于对照区, 这与礁区生物聚集多、代谢活动强, 能释出更多的溶解有机物的规律相悖; 但另一方面, 礁区附生贝类的强烈滤食还可下行作用于小粒径的鞭毛藻类和纤毛虫类(Pierce et al, 1992; Doherty et al, 2010), 而后者又对以DOC为主要食物来源的浮游细菌产生摄食下行作用(Azam et al, 1983, Fenchel, 2008), 这可能是导致表观上礁区的DOC浓度低于对照区的重要原因。另外, 环境因子中的pH值在两区域间的差异在全年时段以及各个时期均表现为礁区持续低于对照区。这主要与礁区的生物聚集和生物量持续高于对照区, 其呼吸作用会产生更多的CO2, 从而使得礁区pH值的下降有关。从本研究的结果来看, 礁区生物作用导致的pH下降基本维持在0.02~0.03之间, 且全年及各时段差异不大。
3.3 浮游植物与生物及环境因子的关系在礁区与对照区的差异浮游植物生态研究显示, 浮游植物与浮游动物之间系直接的捕食与被捕食关系(山东省水产学校, 1993), 但本研究中, 两者之间的消长变化却未呈现上述的典型消长关系, 这方面应与礁区附生贝类对浮游植物的大量滤食, 强烈干扰了浮游植物与浮游桡足类两者之间的消长关系有关。本研究中浮游植物与浮游桡足类之间的相互消长关系在7月前表现为礁区与对照区基本一致, 但7月后则呈现出一定差异。该时期角毛藻丰度显著高于6月, 且靠近外海一侧的对照区的角毛藻丰度持续高于靠近近岸一侧的礁区, 此时区域内悬浮物浓度也显著高于6月, 应与角毛藻所指示的外部海水输入增强, 使对照区浮游植物的丰度在7~8月持续高于礁区, 进而促使消长关系在两区域间产生了较大的差异有关。综上可见, 礁区附生贝类等的滤食作用及外部海水携带浮游生物的输入, 均可对调查海域浮游植物与浮游桡足类之间呈现典型的捕食与被捕食关系产生干扰。
本研究中, 浮游植物与环境因子的相关性分析中, 共检出93个达到显著相关关系(表 1), 其中52个在春夏季繁生期, 占比56%。牡蛎的增肥期主要在春季(牛亚丽, 2014), 此时期牡蛎对浮游植物摄食压力最大, 浮游植物在春夏季繁生期的累计生产量也最多(宁修仁等, 1995; 汪益嫔等, 2011), 春夏季繁生期既是牡蛎等贝类摄食活动最活跃的时期, 也是浮游植物生长最快的时期, 浮游植物与环境因子的关系也最为密切, 这应是春夏季繁生期该海域检出更多浮游植物与环境因子达到显著相关数量的重要原因。相反, 泛冬季和泛秋季, 由于牡蛎的累计生产以及滤食活动减弱, 导致浮游植物的累计生产量也较春夏季繁生期显著减少, 相应地, 浮游植物对环境营养盐的吸收也较春夏季减弱, 导致浮游植物与环境营养盐等因子的关系也不如春夏季密切, 这应是泛冬季和泛秋季该海域检出较少的浮游植物与环境因子显著相关数量的重要原因。由上可见, 在摄食活动最强烈的时期, 浮游植物与环境关系越密切, 更易检出显著相关性, 这可能是人工牡蛎礁海域的一个显著特点, 今后有待进一步验证。
礁区、对照区浮游植物与营养盐的相关关系, 在泛冬季低温期礁区主要表现为浮游植物与营养盐因子中的TP呈显著正相关, 对照区浮游植物与营养盐因子中的TN达到显著水平。春夏季繁生期, 主要表现为礁区浮游植物与DIP呈显著负相关, 对照区浮游植物与NH4呈显著负相关。泛秋季降温期, 主要表现为浮游植物在礁区未与DIN达到显著相关, 对照区浮游植物则与DIN呈显著负相关。
泛冬季礁区水体氮磷比值为27, 高于Redfield比值, 磷相对缺乏, 浮游植物的生长更多地取决于磷的含量, 而礁区附生牡蛎、周丛动物等大量聚集, 这些动物向水体排泄的磷的比例相对于排泄的氮的比例高得多(周毅等, 2003; 薛飞等, 2004; 吴丰辉等, 2015), 礁区磷营养盐的补充更为充分, 这就使得排入水体中的磷营养盐含量在礁区高于对照区, 这可能是礁区TP与各浮游植物均呈显著正相关的重要原因。泛冬季对照区SS浓度较礁区平均高出4.79 mg/L, 显示对照区水体混合作用更为强烈, 同时, 对照区的氮营养盐浓度高于礁区, 显示对照区有更多的氮。该时期对照区水体氮磷比值为18, 与礁区相比为磷营养盐相对多、氮营养盐相对少的状态, 该时期硅藻又为主要类群, 根据Klausmeier等(2004)研究结果, 大部分硅藻最适的氮磷比范围基本高于20, 这可能是TN与浮游植物显著正相关的重要原因。
春夏季繁生期, 牡蛎生长旺盛, 对浮游植物摄食的量也大, 导致水体中的营养盐随着浮游植物的被摄食而大量消耗, 这就使得该时期TN、TP、DSi营养盐均达到3个时期中的最低水平。礁区浮游植物与DIP呈显著负相关关系, 监测结果显示礁区与对照区磷营养盐浓度基本持平, 但礁区生物聚集多, 牡蛎等贝类代谢会产生大量磷酸盐(Magni et al, 2000), Wahyudin等(2020)也指出牡蛎及筏上附生动物通过产生的粪便能使水体中磷含量增加60%, 礁区有大量来源于生物代谢的磷补充, 从以上推测礁区的浮游植物吸收了更多的磷, 此时礁区氮磷比值为22, 高于浮游植物最适营养盐氮磷比值(Redfield, 1958), 磷相对缺乏, 因此浮游植物与DIP呈显著负相关关系。浮游植物与NH4呈显著负相关, 已有较多报道(秦雪等, 2016; 宋秀凯等, 2016; 谢斌等, 2017; 潘玉龙等, 2019; 王尽文等, 2022), 氨氮浓度的高低表征着浮游动物丰度的高低, 浮游动物与浮游植物相互消长, 所以两者呈现负相关关系。本研究结果中, 对照区也监测到这种常见的相关关系, 礁区却未监测到, 这可能是该时期牡蛎的摄食作用强烈, 掩盖了这种相关关系, 使得礁区浮游植物与NH4未显现出显著负相关关系, 而该特征在泛秋季降温期也未发现, 这有待于今后进一步研究。
泛秋季降温期, 礁区浮游植物的数量达到最高, 有研究指出, 浮游植物数量越大则越接近饱和浓度, 会导致其生长速率降低(陈明耀, 1995; Andersen, 2005)。本研究中, 浮游植物在泛秋季的丰度达到最高, 其现存量高可能会受到“饱和效应”的抑制, 对营养盐的吸收相对减弱, 而此时礁区动物代谢来源的氮营养盐又高于对照区, 礁区的氮营养盐相对生长速率降低的浮游植物而言相对充足, 这可能是泛秋季礁区浮游植物与氮营养盐未检出显著相关的一个重要原因。对照区浮游植物数量较礁区低, 对营养盐的吸收较礁区强, 该时期浮游植物类群主要为角毛藻, 根据Klausmeier等(2004)研究结果, 硅藻类的角毛藻最适氮磷比在24~25范围之间, 而对照区氮磷比值低于该范围, 氮营养盐相对缺乏, 从而对照区DIN和浮游植物为显著负相关关系。
4 结论(1) 唐山祥云湾海洋牧场共鉴定浮游植物41属78种, 其中硅藻33属62种, 甲藻7属15种, 硅鞭藻1属1种, 浮游植物类群以硅藻为主, 其次为甲藻。鱼礁区浮游植物丰度平均为202.39×104 cells/m3, 对照区平均为208.68×104 cells/m3, 略高于礁区。
(2) 礁区H'均值为2.84, J均值为0.59, D均值为1.34; 对照区H'均值为2.92, J均值为0.61, D均值为1.30, 两区域浮游植物群落结构指数逐月变化趋势基本一致。
(3) 本研究中, 浮游植物群落结构在多方面受到外界因素影响, 礁体附生牡蛎等贝类的滤食使浮游植物丰度以及群落结构指数在春夏季达到最低。圆筛藻和角毛藻为全年主要优势类群; 甲藻在泛冬季的优势度高于春夏季, 这可能是牡蛎摄食选择性、外部海水汇入以及其对磷营养盐吸收具有优势的结果。近岸海域潮汐往复流的混合作用可能是礁区与对照区浮游植物群落结构差异不明显的重要原因。
(4) 链状浮游植物丰度在礁区高于对照区, 而非链状浮游植物则相反, 这可能是牡蛎等贝类摄食选择性以及链状浮游植物不易被牡蛎摄食的结果。建议今后可将链状浮游植物作为考查礁区与对照区差异的一个重要指标。
(5) 浮游植物与浮游桡足类之间未呈现典型的捕食与被捕食关系, 这可能是牡蛎等贝类对浮游植物的强滤食而产生的干扰以及潮汐往复流混合作用所致。春夏季繁生期, 浮游植物与环境因子的相关关系达到显著水平的数量最多。礁区与对照区不同时期浮游植物与环境因子的显著相关关系不同, 其中, 在摄食活跃的春夏季, 礁区表现为浮游植物与DIP呈显著负相关关系, 对照区表现为浮游植物与NH4呈显著负相关关系。
于湖洋, 崔磊, 潘霖, 等, 2016. 秦皇岛海域浮游植物的群落结构特征. 海洋科学, 40(5): 66-75 |
山东省水产学校, 1993. 海洋浮游生物学. 北京: 中国农业出版社, 172-175
|
王兆慧, 张光涛, 2020. 牡蛎对浮游植物群落下行控制作用的围隔实验研究. 海洋科学, 44(9): 47-53 |
王尽文, 黄娟, 姜万钧, 等, 2022. 日照近岸海域冬夏季网采浮游植物群落结构及其与环境因子的关系. 上海海洋大学学报, 31(1): 86-96 |
王芳, 董双林, 张硕, 等, 2000. 海湾扇贝和太平洋牡蛎的食物选择性及滤除率的实验研究. 海洋与湖沼, 31(2): 139-144 DOI:10.3321/j.issn:0029-814X.2000.02.005 |
牛亚丽, 2014. 桑沟湾滤食性贝类碳、氮、磷、硅元素收支的季节变化研究[D]. 舟山: 浙江海洋学院: 11-14.
|
邓筱凡, 2022. 唐山祥云湾海洋牧场人工鱼礁区的流场特征及生境效应的初步研究[D]. 青岛: 中国海洋大学: 19-22.
|
叶敏, 崔晨, 张秀文, 等, 2021. 唐山祥云湾海洋牧场水质的变化规律与评价. 河北渔业(2): 28-32, (2): 28-32, 44 |
宁修仁, 刘子琳, 史君贤, 1995. 渤、黄、东海初级生产力和潜在渔业生产量的评估. 海洋学报, 17(3): 72-84 |
刘长东, 易坚, 郭晓峰, 等, 2016. 荣成俚岛人工鱼礁区浮游植物群落结构及其与环境因子的关系. 中国海洋大学学报, 46(3): 50-59 |
刘长东, 郭晓峰, 唐衍力, 等, 2015. 海州湾前三岛人工鱼礁区浮游植物群落组成及与环境因子的关系. 中国水产科学, 22(3): 545-555 |
刘萍, 孙萍, 宋洪军, 等, 2019. 桑沟湾不同养殖区浮游植物群落时空变化特征. 海洋科学进展, 37(4): 673-680 |
关莹莹, 林军, 焦俊鹏, 等, 2022. 高滤食压力下贻贝筏式养殖场及周边海域浮游植物群落特征. 海洋环境科学, 41(4): 543-553 |
江志兵, 陈全震, 寿鹿, 等, 2012. 象山港人工鱼礁区的网采浮游植物群落组成及其与环境因子的关系. 生态学报, 32(18): 5813-5824 |
许钰涵, 2021. 山东日照近岸增养殖海域浮游植物群落特征的研究[D]. 青岛: 中国海洋大学: 41-42.
|
李大鹏, 张硕, 石一茜, 等, 2017. 海州湾海洋牧场浮游植物群落年际变化特征分析. 生态环境学报, 26(2): 285-295 |
李希磊, 杨俊丽, 于潇, 等, 2018. 烟台四十里湾扇贝养殖区浮游植物群落调查. 海洋科学, 42(8): 30-37 |
李莉, 陈武军, 张永丰, 等, 2013. 滦河口-北戴河海域夏季浮游植物群落变化研究. 海洋环境科学, 32(6): 896-901 |
杨心愿, 2019. 祥云湾海洋牧场人工牡蛎礁群落特征及其生态效应[D]. 青岛: 中国科学院大学(中国科学院海洋研究所): 1-84.
|
杨柳, 张硕, 孙满昌, 等, 2011. 海州湾人工鱼礁区浮游植物与环境因子关系的研究. 上海海洋大学学报, 20(3): 445-450 |
吴丰辉, 阎波, 田胜艳, 2015. 影响鱼、虾、贝类等海洋生物氮、磷代谢的主要因素分析. 海洋信息, 30(2): 21-25 |
吴玉霖, 孙松, 张永山, 2005. 环境长期变化对胶州湾浮游植物群落结构的影响. 海洋与湖沼, 36(6): 9-20 |
汪益嫔, 张维砚, 徐春燕, 等, 2011. 淀山湖浮游植物初级生产力及其影响因子. 环境科学, 32(5): 1249-1256 |
宋秀贤, 俞志明, 2007. 胶州湾东北部养殖海域夏季营养盐分布特征及其对浮游植物生长的影响. 海洋与湖沼, 38(5): 446-452 |
宋秀凯, 汤宪春, 程玲, 等, 2016. 崂山湾网采浮游植物时空分布特征及其与环境因子关系. 海洋与湖沼, 47(6): 1205-1213 |
张建乐, 陈海, 2010. 北戴河养殖海域浮游植物的种类组成和时空分布特征. 海洋通报, 29(4): 407-411 |
张玲, 李政菊, 陈飞羽, 等, 2015. 大鹏澳牡蛎养殖对浮游植物种群结构的影响研究. 海洋与湖沼, 46(3): 549-555 |
张莉红, 张学雷, 朱明远, 2008. 栉孔扇贝对硅藻和甲藻细胞的选择性摄食初探. 海洋科学进展, 26(3): 372-376 |
张硕, 朱孔文, 孙满昌, 2006. 海州湾人工鱼礁区浮游植物的种类组成和生物量. 大连水产学院学报, 21(2): 134-140 |
张雪, 徐晓甫, 戴媛媛, 等, 2018. 天津近岸人工鱼礁海域浮游植物群落及其变化特征. 渔业科学进展, 39(6): 1-10 |
张雪, 栾青杉, 孙坚强, 等, 2016. 獐子岛海域浮游植物群落周年变化及其与环境因子的关系. 大连海洋大学学报, 31(3): 315-323 |
张智鹏, 陈璐, 刘洪军, 等, 2020. 人工鱼礁建设对海洋浮游植物群落变化的影响. 海洋通报, 39(5): 617-626 |
张皓宇, 刘汉超, 刘永虎, 等, 2016. 獐子岛近岸人工鱼礁区浮游动物群落结构特征. 水产科学, 35(5): 473-479 |
陈传曦, 张建柏, 王新萌, 等, 2021. 渤海莱州湾芙蓉岛人工鱼礁区浮游动物群落结构特征及其与环境因子的关系. 中国水产科学, 28(3): 299-313 |
陈明耀, 1995. 生物饵料培养. 北京: 中国农业出版社, 46-51
|
陈海峰, 王云龙, 廖勇, 等, 2013. 象山港人工鱼礁区浮游植物群落特征. 海洋渔业, 35(4): 396-404 |
林虓, 尤凯, 毛霞, 等, 2015. 2010-2012年青岛海滨浴场67周次浮游植物的群集特征. 海洋科学进展, 33(1): 71-80 |
罗璇, 孙晓霞, 郑珊, 等, 2016. 2011年胶州湾网采浮游植物群落结构及其环境影响因子. 海洋与湖沼, 47(5): 915-923 |
周毅, 杨红生, 张福绥, 2003. 海水双壳贝类的N、P排泄及其生态效应. 中国水产科学, 10(2): 165-168 |
郑珊, 孙晓霞, 赵永芳, 等, 2014. 2010年胶州湾网采浮游植物种类组成与数量的周年变化. 海洋科学, 38(11): 1-6 |
秦雪, 徐宾铎, 杨晓改, 等, 2016. 黄河口及其邻近水域夏季浮游植物群落结构及其与环境因子的关系. 水产学报, 40(5): 711-720 |
郭皓, 闫启仑, 沈亮夫, 1999. 贝类浮筏养殖区内、外浮游植物生态特征研究. 黄渤海海洋, 17(3): 64-72 |
谢斌, 张硕, 李莉, 等, 2017. 海州湾海洋牧场浮游植物群落结构特征及其与水质参数的关系. 环境科学学报, 37(1): 121-129 |
雷安平, 陈欢, 陈菊芳, 等, 2009. 大亚湾人工鱼礁区浮游植物的种类组成和生物量研究. 海洋技术, 28(4): 83-88 |
慕建东, 郑向荣, 赵振良, 等, 2015. 秦皇岛海域赤潮期间浮游植物的生态特征. 中国水产科学, 22(2): 288-301 |
潘玉龙, 刘潇, 沙婧婧, 等, 2019. 荣成近岸养殖海域浮游植物群落结构及与环境因子的关系. 渔业科学进展, 40(5): 26-33 |
薛飞, 周维仁, 徐为民, 2004. 鱼类氮、磷营养与水体环境. 河北渔业, (3): 1-3 |
戴媛媛, 杨森, 侯纯强, 等, 2018. 礁区浮游植物群落结构特征及其与环境因子的关系. 海洋湖沼通报, 40(2): 60-66 |
ANDERSEN R A, 2005. Algal Culturing Techniques. Burlington: Academic Press, 269-282
|
AZAM F, FENCHEL T, FIELD J G, et al, 1983. The ecological role of water-column microbes in the sea. Marine Ecology Progress Series, 10(3): 257-263 |
BAEK S H, SHIMODE S, HAN M S, et al, 2008. Growth of dinoflagellates, Ceratium furca and Ceratium fusus in Sagami Bay, Japan: the role of nutrients. Harmful Algae, 7(6): 729-739 |
DOHERTY M, TAMURA M, VRIEZEN J A C, et al, 2010. Diversity of oligotrichia and choreotrichia ciliates in coastal marine sediments and in overlying plankton. Applied and Environmental Microbiology, 76(12): 3924-3935 |
EPPLEY R W, ROGERS J N, MCCARTHY J J, 1969. Half-saturation constants for uptake of nitrate and ammonium by marine phytoplankton. Limnology and Oceanography, 14(6): 912-920 |
FENCHEL T, 2008. The microbial loop-25 years later. Journal of Experimental Marine Biology and Ecology, 366(1/2): 99-103 |
FIELD C B, BEHRENFELD M J, RANDERSON J T, et al, 1998. Primary production of the biosphere: integrating terrestrial and oceanic components. Science, 281(5374): 237-240 |
FRITZ L W, LUTZ R A, FOOTE M A, et al, 1984. Selective feeding and grazing rates of oyster (Crassostrea virginica) larvae on natural phytoplankton assemblages. Estuaries, 7(4): 513-518 |
GARMENDIA M, BORJA Á, FRANCO J, et al, 2013. Phytoplankton composition indicators for the assessment of eutrophication in marine waters: present state and challenges within the European directives. Marine Pollution Bulletin, 66(1/2): 7-16 |
HANSELL D A, CARLSON C A, 2015. Biogeochemistry of Marine Dissolved Organic Matter. 2nd ed. Boston: Academic Press, 65-126
|
HUANG B Q, OU L J, HONG H S, et al, 2005. Bioavailability of dissolved organic phosphorus compounds to typical harmful dinoflagellate Prorocentrum donghaiense Lu. Marine Pollution Bulletin, 51(8/9/10/11/12): 838-844 |
KLAUSMEIER C A, LITCHMAN E, DAUFRESNE T, et al, 2004. Optimal nitrogen-to-phosphorus stoichiometry of phytoplankton. Nature, 429(6988): 171-174 |
MAGNI P, MONTANI S, TAKADA C, et al, 2000. Temporal scaling and relevance of bivalve nutrient excretion on a tidal flat of the Seto Inland Sea, Japan. Marine Ecology Progress Series, 198: 139-155 |
PIERCE R W, TURNER J T, 1992. Ecology of plankton ciliates in marine food webs. Reviews in Aquatic Sciences, 6(2): 139-181 |
REDFIELD A C, 1958. The biological control of chemical factors in the environment. American Scientist, 46: 205-221 |
RIISGÅRD H U, 1988. Efficiency of particle retention and filtration-rate in 6 Species of Northeast American Bivalves. Marine Ecology Progress Series, 45(3): 217-223 |
TAKABAYASHI M, LEW K, JOHNSON A, et al, 2006. The effect of nutrient availability and temperature on chain length of the diatom, Skeletonema costatum. Journal of Plankton Research, 28(9): 831-840 |
TURPIN D H, HARRISON P J, 1979. Limiting nutrient patchiness and its rôle in phytoplankton ecology. Journal of Experimental Marine Biology and Ecology, 39(2): 151-166 |
WAHYUDIN, YAMAMOTO T, 2020. Modeling bottom-up and top-down controls on the low recruitment success of oyster larvae in Hiroshima Bay, Japan. Aquaculture, 529: 735564 DOI:10.1016/j.aquaculture.2020.735564 |
 2023, Vol. 54
2023, Vol. 54


