
中国海洋湖沼学会主办。
文章信息
- 娄恬, 陆欣鑫, 刘妍, 范亚文. 2023.
- LOU Tian, LU Xin-Xin, LIU Yan, FAN Ya-Wen. 2023.
- 拉林河浮游植物三种功能群分布特征及其与环境因子的关系
- DISTRIBUTION CHARACTERISTICS OF THREE FUNCTIONAL GROUPS OF PHYTOPLANKTON IN LALIN RIVER AND THEIR RELATIONSHIP WITH ENVIRONMENTAL FACTORS
- 海洋与湖沼, 54(4): 1085-1100
- Oceanologia et Limnologia Sinica, 54(4): 1085-1100.
- http://dx.doi.org/10.11693/hyhz20221100301
文章历史
-
收稿日期:2022-11-16
收修改稿日期:2023-03-19
2. 黑龙江省水生生物多样性研究重点实验室 黑龙江哈尔滨 150025
2. Key Laboratory of Biodiversity of Aquatic Organisms, Harbin Normal University, Harbin 150025, China
浮游植物作为河流生态系统的初级生产者, 具有分布范围广、生活周期短、对环境因子变化敏感等特点, 对维持河流生态系统的物质循环、能量流动、信息传递及生态系统平衡起着非常重要的作用(Yang et al, 20192; Tian et al, 2021)。浮游植物群落的时空分布变化可以被认为是受环境因素诱导、制约、调控导致的群落组成和生物量发生变化的复杂过程(Nan et al, 2020; Jeon et al, 2021)。环境因素包括物理因素(温度和浊度)、化学因素(磷酸盐、硝酸盐、铵和硅酸盐等营养物质)和生物因素(Wang et al, 2020)1。由于浮游植物对水环境变化具有极敏感的指示作用, 它们的动态演替是河流水环境变化的直接反映(Varol, 201920440; Manier et al, 20211460)。经典分类学研究以浮游植物物种间进化关系、细胞色素体结构、光合作用色素种类和储存物质为依据, 对浮游植物群落分布格局、演替规律进行探索(杨文等, 2014)1834。分子分类学依据分子标记(Tseplik et al, 2021)、DNA条形码、高通量测序(Baird et al, 2012)、生物芯片(Kuntanawat et al, 2014)技术为浮游植物生态学研究提供群落矩阵信息。然而, 两种方法均为根据物种同源性特点形成的, 着重反映不同生物间的进化关系, 没有考虑生理学特点, 尤其是浮游植物的生态学属性(Kim et al, 2020)。
2002年, Reynolds等(2002)418提出了功能群(functional group, FG)划分法, 将传统的浮游植物分类学与现代的水生生物生态学相关联, 将符合某一特定生境类型, 具有相似敏感性的浮游植物物种归为同一功能群, 这不仅能有效地描述典型的生态特征, 还能一定程度地预测浮游植物时空变化规律(Roselli et al, 2017)。2009年, Padisák等(2009)4根据浮游植物的敏感性和耐受性进行了修正和补充。2007年, Salmaso等(2007)110提出了生态功能群(morpho-functional groups, MFG)划分法, 以运动能力、获得碳和营养物质的混合营养能力、特殊的营养需求、大小和形状以及胶被的有无等进行分类。2010年, Kruk等(2010)615根据浮游植物的大小、比表面积、特殊附带结构的有无、鞭毛的有无、硅质外壳的有无、硅质鞭毛的有无以及群体胶质包被的有无, 将浮游植物分为7个功能群, 提出了形态功能群(morphology-based functional group, MBFG)划分法。目前FG、MFG、MBFG功能群划分法被应用于河流(Abonyi et al, 2014)、湿地(贾鹏等, 2021)1042、水库(Liao et al, 2021)1、湖泊(Braga et al, 2020)1的浮游植物群落演替, 与环境因子的耦合关系, 水生态健康评价等研究中, 但是基于浮游植物功能群的研究多采用单一的划分方法(Petar et al, 2014147; Wang et al, 2021)。尤其针对北方受农业面源污染背景下河流浮游植物群落对环境异质性响应规律的比较研究鲜见报道, 这极大地限制功能群划分法在相关区域水生态健康、物种多样性保护、受损生态系统修复方面的应用。
拉林河流域位于北方寒旱区, 土地利用类型主要为耕地和林地, 流域中、下游地区耕地资源丰富, 为黑、吉两省及全国重要的粮食生产基地。随着流域内城市经济的快速发展, 拉林河承泄了大量的工业生产废水、生活污水。近年来, 对拉林河流域采取野外实地调查和室内测试分析相结合的手段评估区域内污染状况(刘洪超, 2016)69,进行底栖硅藻的多样性分布格局及其与环境相关性的研究、应用多种分析方法对水质状况进行初步评价(邢爽, 2019; 赵杨, 2020)103, 发现拉林河水生态系统受到一定污染, 具体表现为耐污物种出现和物种多样性破坏等。然而, 大多数关于拉林河的研究倾向于底栖硅藻和水体理化因子测定而不是关注河流浮游植物群落演替模式。河流浮游植物群落结构的组成类型一般为硅藻-绿藻型, 基于MFG、MBFG功能群只对硅藻的大小、形态进行划分, 未考虑硅藻对环境响应的物种特异性和环境特异性(杨文等, 2014)1837, 我们提出假设: FG功能群比MFG和MBFG功能群能更好地表征拉林河水体环境的时空变化。本研究通过FG、MFG和MBFG功能群划分法对拉林河浮游植物进行归类并阐明其时空变化规律, 并通过冗余分析(redundancy analysis, RDA)明确影响浮游植物功能群演替的主要环境因子, 为河流浮游植物生态特征研究提供最佳功能群研究方法, 为拉林河水生生物多样性及水环境的保护提供重要的生物学参考依据。
1 材料与方法 1.1 采样点设置拉林河为松花江右岸的一级支流, 于哈尔滨上游150 km处注入松花江。流域地理位置介于125°34′~ 128°34′E、44°00′~45°30′N之间。河长450 km, 流域面积19 923 km2。拉林河流域属中温带大陆性季风气候, 冬季较为寒冷, 极端最低气温−40.9 ℃, 年平均气温在3.0 ℃左右, 冰封期长, 一年有两个汛期, 年径流量曲线为双峰型。4月冰雪融化水量补给河流, 形成春汛; 8月降雨集中, 降水量占全年的70%以上, 形成夏汛。拉林河流域上游多为山区, 森林的覆盖率高, 有大型水库, 中下游有水田、旱田等耕地, 受农业污染严重(赵杨, 2020)8。本研究在拉林河流域设置了23个采样点(图 1)。其中S1、S2、S2-1、S2-2、S10、S11、S12、S13位于林地区, 其余样点在耕地区。
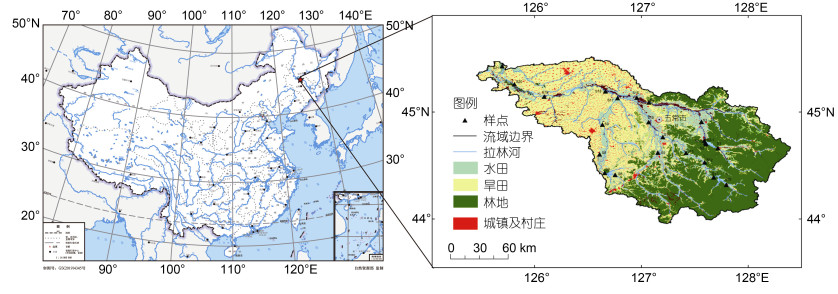 |
| 图 1 拉林河采样点示意图 Fig. 1 Sampling sites in the Lalin River watershed |
于2021年4、8月中下旬对23个采样点进行定量样品与定性样品的采集。定性样品采用25号浮游网在水面表层下0.5 m处作“∞”字形缓慢捞取; 定量样品用1 L的采水器在水表层以下0.5 m处进行采集, 现场加入30 mL的鲁哥氏剂固定, 带回实验室沉淀48 h后, 浓缩至50 mL, 用光学显微镜进行镜检计数(尹航, 2007)。标本鉴定主要依据胡鸿钧等(2006)等著作文献(毕列爵等, 2004; 王全喜等, 2008)。浮游植物的密度近于1, 故可以直接由体积换算为生物量, 细胞的体积测定时依据其体型按照最相似的几何形态测量, 然后按公式计算出体积(金业, 2019)15。
1.3 理化指标的测定采用YSI ProPlus手持式多参数水质分析仪(美国维赛公司)现场测定水温(water temperature, WT)、电导率(specific conductivity, SpCond.)、溶解氧(dissolved oxygen, DO)、酸碱度(pH)。采用便携式浊度计(聚创环保, JC-WGZ-1B型)测定水体浊度(turbidity, Tur.)。现场采集的水样用棕色玻璃瓶避光保存, 带回实验室依据《地表水环境质量标准(GB3838-2002)》(郭晓茆等, 2002)进行总氮(total nitrogen, TN)、总磷(total phosphate, TP)、高锰酸盐指数(chemical oxygen demand, CODMn)、五日生化需氧量(five-day biochemical oxygen demand, BOD5)的测量。
1.4 优势度及数据分析浮游植物优势度通过下述公式计算:
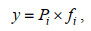 (1)
(1)式中, fi为第i种的出现频率, Pi为第i种个体数量占总个体数量的比例。当y≥0.02时, 定义为优势种(张萍等, 2022)421。
浮游植物功能群优势度根据功能群的出现频率(fn)及相对生物量(Pn)确定。
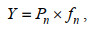 (2)
(2)式中, fn为第n功能群的出现频率, Pn为第n功能群生物量占总生物量的比例。当Y≥0.02时, 定义为优势功能群; 当Y≥0.2时, 定义为绝对优势功能群(金业, 2019)15。
主成分分析(principal component analysis, PCA) (君珊等, 2019)789是一种识别的多维数据统计分析方法, 旨在利用降维的思想, 通过少数几个主成分来揭示多个变量间的内部结构。单因素交叉相似性分析(analysis of similarities, ANOSIM)(贾鹏等, 2021)1045是一种用于分析高维度数据组间相似性的统计方法。通过变量计算样本间距离, 计算关系排名, 进行置换检验判断组间差异是否显著不同于组内差异。相似性百分比分析(similarity percentage analysis, SIMPER) (贾鹏等, 2021)1045可以识别对群落组间差异性和组内相似性贡献率较大的关键物种。非度量多维尺度(non-metric multidimensional scaling, NMDS)(Manier et al, 2021)1455和广义可加模型(generalized additive model, GAM)通过对样本距离进行等级排序, 使样本在低维空间中的排序尽可能符合彼此之间的相似距离的远近关系。冗余分析(redundancy analysis, RDA) (王徐林等, 2018)433是一种将对应分析与多元回归分析相结合的排序方法, 每一步计算均与环境因子进行回归, 又称多元直接梯度分析, 此分析主要是用来反映群落与环境因子之间关系。
本文样点分布及优势种优势度可视化地图采用ArcGIS 10.8.1软件绘制。通过SPSS软件完成独立样本T检验。通过SPSS软件进行KMO检验和Bartlett球形检验法检验理化变量进行因子分析的可行性。采用R软件(ggrepel包)进行PCA分析。使用PRIMER 5.0软件进行ANOSIM和SIMPER分析。应用Canoco 4.5软件进行三种浮游植物功能群与环境因子的RDA分析, 在进行排序分析前, 对解释变量和响应变量数据进行log(x+1)转换, 使样本总体趋于正态分布。采用R软件(vegan包)进行NMDS和GAM分析。
2 结果与分析 2.1 环境因子及梯度独立样本T检验表明在季节、空间上水体理化因子变化明显, 除电导率、TP、浊度外其他理化指标在季节间均存在一定的变化规律(P < 0.05)。DO、BOD5、TN和pH都呈现随春、夏季节变化逐渐降低的规律, 平均值分别为10.87 mg/L、10.77 mg/L、0.60 mg/L和8.04, 变化范围分别在3.91~16.60 mg/L、0.44~ 11.21 mg/L、0.25~0.94 mg/L和7.13~9.36之间; 春季WT介于6.3~13.0 ℃, 平均值为10.0 ℃, 夏季WT介于11.0~29.2 ℃, 平均值为24.9 ℃, 较春季显著升高; 高锰酸盐指数呈现出随着春、夏季节变化逐渐升高的规律, 平均值为6.19 mg/L, 变化范围在2.88~ 11.04 mg/L。电导率、TP、浊度在空间上变化差异显著(P < 0.05)(表 1)。在空间尺度, 电导率、TP及浊度呈现出林地低, 耕地高的规律, 平均值分别为161.33 μS/cm、0.18 mg/L、48.31 NTU, 变化范围分别在29.30~ 405.10 μS/cm、0.01~0.89 mg/L、0.10~200.00 NTU之间。
| 理化指标 | 春季 | 夏季 | 林地 | 耕地 | 独立样本T检验 | |
| 春季×夏季 | 林地×耕地 | |||||
| 水温WT/℃ | 10.00±2.38 | 24.89±4.03 | 14.75±7.97 | 18.89±8.09 | P < 0.05 | P > 0.05 |
| 溶解氧DO/(mg/L) | 13.63±2.03 | 8.11±2.59 | 12.21±3.19 | 10.16±3.68 | P < 0.05 | P > 0.05 |
| 五日生化需氧量BOD5/(mg/L) | 6.34±0.79 | 4.43±2.63 | 6.36±1.70 | 4.86±2.21 | P < 0.05 | P > 0.05 |
| 电导率SpCond./(μS/cm) | 153.19±116.86 | 169.46±107.54 | 72.44±22.36 | 208.73±110.89 | P > 0.05 | P < 0.05 |
| pH值 | 8.28±0.39 | 7.79±0.47 | 8.10±0.47 | 8.00±0.51 | P < 0.05 | P > 0.05 |
| 总氮TN/(mg/L) | 0.76±0.12 | 0.44±0.14 | 0.51±0.18 | 0.65±0.21 | P < 0.05 | P > 0.05 |
| 总磷TP/(mg/L) | 0.19±0.14 | 0.21±0.19 | 0.07±0.04 | 0.23±0.22 | P > 0.05 | P < 0.05 |
| 浊度Tur./NTU | 34.95±34.57 | 64.82±62.05 | 14.79±14.62 | 66.28±57.79 | P > 0.05 | P < 0.05 |
| 高锰酸盐指数CODMn/(mg/L) | 5.45±2.14 | 6.93±1.81 | 5.13±1.29 | 6.76±2.24 | P < 0.05 | P > 0.05 |
| 注: P < 0.05, 表示显著相关 | ||||||
PC1表示第一主成分, PC2表示第二主成分, 百分比表示该主成分对数据集的解释率; 图 2中的每个点表示一个采样点, 同一个组的样品使用同一种颜色表示。PCA分析表明, 拉林河理化因子在季节和空间分布上存在一定的差异, 而浮游植物群落分布特征与不同环境梯度密切相关。
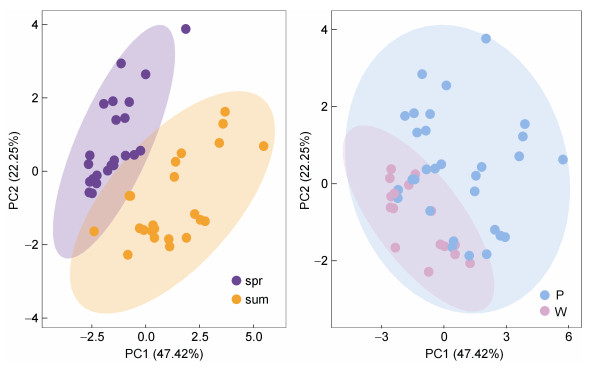 |
| 图 2 拉林河环境变量的PCA分析 Fig. 2 PCA Analysis of Environmental Variables in the Lalin River 注: P为耕地; W为林地; spr为春季; sum为夏季 |
在研究期间共鉴定浮游植物168个分类单位, 包括161种7变种, 隶属于7门10纲18目33科77属。其中, 硅藻门种类最多, 绿藻门和蓝藻门次之。韦恩图分析表明, 春、夏两季浮游植物共有种96种(图 3a); 耕地、林地浮游植物共有种104种(图 3b)。春、夏两季所有样点中没有均出现的种类(图 3c)。
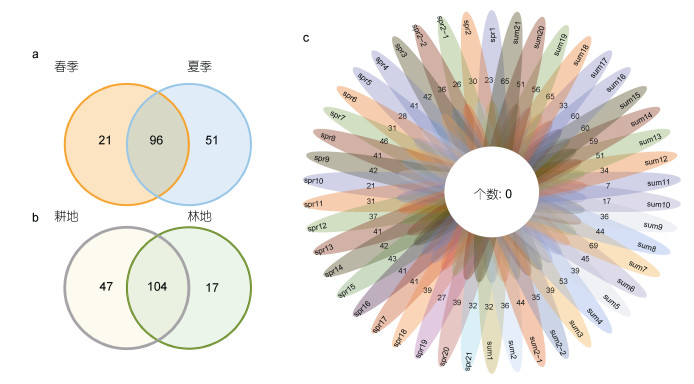 |
| 图 3 拉林河浮游植物群落组成变化 Fig. 3 Changes of phytoplankton community composition in the Lalin River 注: a为不同季节间种类数变化韦恩图; b为不同空间种类数变化韦恩图; c为种类数时空变化韦恩图; spr为春季采样点; sum为夏季采样点 |
浮游植物种类数的季节变化呈现夏季>春季的趋势。春季共鉴定112种5变种, 硅藻门(Bacillariophyta) 51种; 绿藻门(Chlorophyta) 39种; 蓝藻门(Cyanophyta) 13种; 裸藻门(Euglenophyta) 6种; 隐藻门(Cryptophyta) 4种; 金藻门(Chrysophyta) 2种; 甲藻门(Dinophyta) 2种。夏季共鉴定141种6变种, 绿藻门59种; 硅藻门52种; 蓝藻门21种; 裸藻门10种; 隐藻门2种; 金藻门1种; 甲藻门2种。
浮游植物种类数在空间上呈现出耕地区>林地区的规律。耕地区共鉴定145种6变种, 绿藻门60种; 硅藻门51种; 蓝藻门23种; 裸藻门10种; 隐藻门3种; 金藻门2种; 甲藻门2种。林地区共鉴定115种6变种, 硅藻门55种; 绿藻门39种; 蓝藻门14种; 裸藻门7种; 隐藻门2种; 金藻门2种; 甲藻门2种。
浮游植物平均丰度的季节变化呈现出春季(6.10×106 ind./L)>夏季(1.14×106 ind./L)的趋势。春季的变化范围在(0.32~21.37)×106 ind./L; 夏季的变化范围在(0.14~4.06)×106 ind./L。浮游植物平均丰度中占比最高的类群为硅藻门, 春季和夏季分别为5.03×106和0.55×106 ind./L; 其次为绿藻门, 春季和夏季分别为0.85×106和0.30×106 ind./L。
浮游植物平均丰度在空间上呈现出耕地区(4.41× 106 ind./L)>林地区(2.15×106 ind./L)的规律。耕地的变化范围在(0.14~21.37)×106 ind./L; 林地的变化范围在(0.24~6.73)×106 ind./L之间。浮游植物平均丰度中占比最高的类群为硅藻门, 耕地区和林地区分别为3.30×106和1.83×106 ind./L; 其次为绿藻门, 耕地区和林地区分别为0.79×106和0.16×106 ind./L。
2.3 FG、MFG和MBFG功能群时空分布根据Reynolds等(2002)418和Padisák等(2009)2提出的FG功能群划分法, 共划分为25个功能群(表 2), 将优势度大于0.02的功能群定义为优势功能群, 优势功能群为B、C、D、MP、P、T、W1, 将优势度大于0.2的功能群定义为绝对优势功能群, 绝对优势功能群为B、MP。季节演替特征为春季B、C、D, 夏季B、D、MP、P、X1、W1、G。B类群在春、夏季出现频率95%以上, 生物量贡献率在春季高达83.09%。MP类群在春、夏季出现频率均为100%, 但夏季生物量贡献率较低; 空间分布特征为林地B、C、D、MP、P, 耕地B、C、D。C、MP类群在林地出现频率为100%, 生物量贡献率在15%以上。B类群在耕地出现频率为100%, 且生物量贡献率高达84.59%。
| 功能群 | 春季 | 夏季 | 林地 | 耕地 | |||||||
| 出现频率 /% |
生物量贡献率 /% |
出现频率 /% |
生物量贡献率 /% |
出现频率 /% |
生物量贡献率 /% |
出现频率/% | 生物量贡献率 /% |
||||
| B | 100.00 | 83.09 | 95.65 | 26.30 | 93.75 | 26.20 | 100.00 | 84.59 | |||
| C | 100.00 | 8.47 | 82.61 | 2.13 | 100.00 | 34.93 | 86.67 | 4.08 | |||
| D | 100.00 | 4.08 | 95.65 | 9.60 | 93.75 | 8.54 | 100.00 | 4.08 | |||
| MP | 100.00 | 0.55 | 100.00 | 24.72 | 100.00 | 16.80 | 100.00 | 1.02 | |||
| P | 100.00 | 0.92 | 95.65 | 12.65 | 93.75 | 5.36 | 100.00 | 1.63 | |||
| W2 | 95.65 | 0.05 | 82.61 | 0.65 | 81.25 | 0.48 | 93.33 | 0.06 | |||
| J | 91.30 | 0.06 | 95.65 | 1.68 | 87.50 | 0.13 | 97.67 | 0.23 | |||
| S1 | 91.30 | 0.00 | 82.61 | 0.02 | 75.00 | 0.00 | 93.33 | 0.00 | |||
| X1 | 91.30 | 0.00 | 86.96 | 2.32 | 68.75 | 0.74 | 100.00 | 0.16 | |||
| Y | 91.30 | 1.13 | 39.13 | 0.36 | 43.75 | 1.01 | 76.67 | 1.06 | |||
| X2 | 86.96 | 0.32 | 52.17 | 0.33 | 43.75 | 1.11 | 83.33 | 0.21 | |||
| W1 | 82.61 | 0.94 | 86.96 | 10.02 | 68.75 | 2.49 | 93.33 | 1.75 | |||
| Lo | 73.91 | 0.01 | 73.91 | 0.40 | 62.50 | 0.02 | 80.00 | 0.05 | |||
| H1 | 65.22 | 0.00 | 60.87 | 0.03 | 37.50 | 0.00 | 76.67 | 0.00 | |||
| E | 56.52 | 0.17 | 4.35 | 0.03 | 31.25 | 0.00 | 30.00 | 0.15 | |||
| LM | 56.52 | 0.02 | 21.74 | 0.02 | 18.75 | 0.01 | 50.00 | 0.02 | |||
| F | 43.48 | 0.00 | 82.61 | 0.04 | 50.00 | 0.00 | 70.00 | 0.00 | |||
| S2 | 30.43 | 0.00 | 4.35 | 0.00 | 0.00 | 0.00 | 26.67 | 0.00 | |||
| X3 | 30.43 | 0.01 | 69.57 | 0.72 | 43.75 | 0.29 | 53.33 | 0.05 | |||
| K | 26.09 | 0.00 | 4.35 | 0.00 | 18.75 | 0.00 | 13.33 | 0.00 | |||
| TB | 13.04 | 0.06 | 4.35 | 0.02 | 18.75 | 0.43 | 3.33 | 0.00 | |||
| T | 8.70 | 0.12 | 82.61 | 2.08 | 31.25 | 0.17 | 53.33 | 0.33 | |||
| G | 4.35 | 0.00 | 65.22 | 5.57 | 12.50 | 1.06 | 46.67 | 0.48 | |||
| N | 0.00 | 0.00 | 21.74 | 0.31 | 6.25 | 0.04 | 13.33 | 0.03 | |||
| Wo | 0.00 | 0.00 | 17.39 | 0.00 | 6.25 | 0.00 | 10.00 | 0.00 | |||
根据Salmaso等(2007)110提出MFG功能群划分法, 共划分为24个功能群(表 3), 优势功能群为1c、6a、6b、6c、7a、8a、11c, 绝对优势功能群为7a、6b。季节演替特征为春季6b、6c、7a, 夏季1c、3b、6a、6b、7a、8a、11a。7a类群在春、夏季出现频率60%以上, 生物量贡献率在春季高达82.09%。6b类群在春、夏季出现频率均为100%, 夏季生物量贡献率达35.07%; 空间分布特征为林地1c、6b、6c、7a, 耕地6b、6c、7a。6b、6c类群在林地出现频率均为100%, 生物量贡献率达30%以上。7a类群在耕地出现频率为76.67%, 生物量贡献率达84.25%。
| MFG功能群 | 春季 | 夏季 | 林地 | 耕地 | |||||||
| 出现频率 /% |
生物量贡献率 /% |
出现频率 /% |
生物量贡献率 /% |
出现频率 /% |
生物量贡献率 /% |
出现频率 /% |
生物量贡献率 /% |
||||
| 6b | 100.00 | 5.18 | 100.00 | 35.07 | 100.00 | 30.99 | 100.00 | 5.25 | |||
| 6c | 100.00 | 8.00 | 82.61 | 1.98 | 100.00 | 33.00 | 86.67 | 4.13 | |||
| 7a | 100.00 | 82.89 | 65.22 | 13.05 | 93.75 | 26.94 | 76.67 | 84.25 | |||
| 1c | 95.65 | 0.91 | 86.96 | 8.90 | 81.25 | 2.88 | 96.67 | 1.59 | |||
| 11a | 91.30 | 0.02 | 95.65 | 2.73 | 81.25 | 0.70 | 100.00 | 0.24 | |||
| 2d | 91.30 | 1.13 | 26.09 | 0.33 | 37.50 | 1.06 | 70.00 | 1.07 | |||
| 5a | 91.30 | 0.00 | 95.65 | 0.05 | 87.50 | 0.02 | 96.67 | 0.01 | |||
| 9b | 86.96 | 0.01 | 86.96 | 1.20 | 68.75 | 0.21 | 96.67 | 0.12 | |||
| 3a | 82.61 | 0.29 | 69.57 | 0.41 | 50.00 | 1.14 | 90.00 | 0.20 | |||
| 6a | 82.61 | 0.29 | 91.30 | 14.19 | 81.25 | 1.20 | 90.00 | 1.76 | |||
| 1b | 73.91 | 0.05 | 30.43 | 0.05 | 31.25 | 0.02 | 63.33 | 0.05 | |||
| 5d | 73.91 | 0.00 | 73.91 | 0.40 | 56.25 | 0.01 | 83.33 | 0.05 | |||
| 5e | 65.22 | 0.00 | 60.87 | 0.03 | 37.50 | 0.00 | 76.67 | 0.00 | |||
| 1a | 56.52 | 0.17 | 4.35 | 0.03 | 31.25 | 0.18 | 30.00 | 0.15 | |||
| 2a | 47.83 | 0.00 | 0.00 | 0.00 | 18.75 | 0.02 | 26.67 | 0.00 | |||
| 11b | 43.48 | 0.00 | 82.61 | 0.04 | 50.00 | 0.00 | 70.00 | 0.00 | |||
| 8a | 43.48 | 0.86 | 78.26 | 11.53 | 50.00 | 0.00 | 66.67 | 0.00 | |||
| 7b | 39.13 | 0.00 | 47.83 | 0.01 | 62.50 | 0.01 | 33.33 | 0.00 | |||
| 2c | 26.09 | 0.07 | 65.22 | 1.76 | 18.75 | 0.25 | 60.00 | 0.24 | |||
| 11c | 8.70 | 0.12 | 69.57 | 1.93 | 25.00 | 0.18 | 46.67 | 0.32 | |||
| 3b | 4.35 | 0.00 | 65.22 | 5.57 | 12.50 | 1.12 | 46.67 | 0.49 | |||
| 9a | 4.35 | 0.00 | 26.09 | 0.34 | 12.50 | 0.05 | 16.67 | 0.03 | |||
| 10a | 0.00 | 0.00 | 43.48 | 0.39 | 6.25 | 0.01 | 30.00 | 0.04 | |||
| 5c | 0.00 | 0.00 | 8.70 | 0.00 | 0.00 | 0.00 | 6.67 | 0.00 | |||
根据Kruk等(2010)615提出的MBFG功能群划分法, 共划分为7个功能群(表 4), 优势功能群为Ⅳ、Ⅴ、Ⅵ, 绝对优势功能群为Ⅵ。季节演替特征为春季Ⅴ、Ⅵ, 夏季Ⅳ、Ⅴ、Ⅵ。Ⅵ类群在春、夏季出现频率100%, 生物量贡献率均在60%以上。Ⅳ类群在春、夏季出现频率均为90%, 夏季生物量贡献率较高。Ⅰ、Ⅲ、Ⅴ、和Ⅶ类群出现频率均在60%以上。空间分布特征为林地Ⅳ、Ⅴ、Ⅵ, 耕地Ⅴ、Ⅵ。Ⅵ类群在林地、耕地出现频率100%, 生物量贡献率均在85%以上。
| MBFG功能群 | 春季 | 夏季 | 林地 | 耕地 | ||||
| 出现频率 /% |
生物量贡献率 /% |
出现频率 /% |
生物量贡献率 /% |
出现频率 /% |
生物量贡献率 /% |
出现频率 /% |
生物量贡献率 /% |
|
| Ⅵ | 100.00 | 96.36 | 100.00 | 64.31 | 100.00 | 87.70 | 100.00 | 94.65 |
| Ⅴ | 100.00 | 2.46 | 86.96 | 17.01 | 81.25 | 6.16 | 100.00 | 3.52 |
| Ⅳ | 95.65 | 1.01 | 95.65 | 17.78 | 87.50 | 5.91 | 100.00 | 1.70 |
| Ⅲ | 86.96 | 0.00 | 60.87 | 0.01 | 50.00 | 0.01 | 86.67 | 0.00 |
| Ⅰ | 65.22 | 0.00 | 78.26 | 0.42 | 68.75 | 0.02 | 73.33 | 0.05 |
| Ⅱ | 65.22 | 0.17 | 4.35 | 0.03 | 31.25 | 0.19 | 36.67 | 0.03 |
| Ⅶ | 60.87 | 0.00 | 86.96 | 0.44 | 56.25 | 0.02 | 83.33 | 0.05 |
本研究运用非度量多维尺度法(NMDS)和广义可加模型(GAM)来分析拉林河浮游植物功能类群的时空异质性及其环境驱动机制。NMDS结果的可靠性通过stress来检验, 数值越接近0模型效果越好。FG功能群组的stress值为0.160 3, MFG功能群组的stress值为0.169 1, MBFG功能群组的stress值为0.188 7, 表明模型拟合效果良好(stress < 0.2)。NMDS结果显示, 基于FG、MFG和MBFG功能群分析, 不同季节的样点分布具有一定差异性, 表明季节和空间变化对浮游植物群落演替驱动作用明显, 与MFG、MBFG功能群相比, FG功能群与环境因子的拟合效果较好。GAM分析结果显示, 浮游植物三种功能群的季节分布与WT和TN等主要环境因子之间具有显著的相关关系(图 4a), 浮游植物三种功能群的空间分布与浊度和电导率等主要环境因子之间具有显著的相关关系(图 4b)。
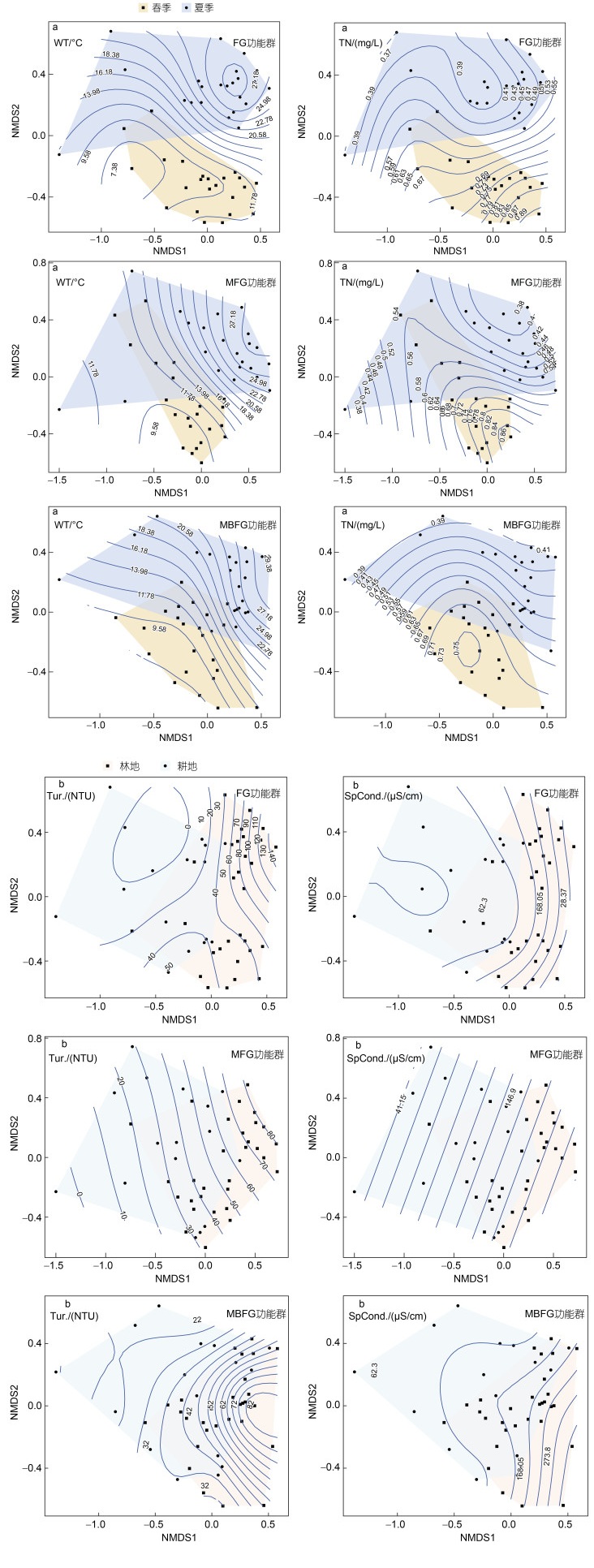 |
| 图 4 浮游植物功能群的非度量多维标尺排序(NMDS)及环境因子在时空中的可加模型曲线 Fig. 4 Non-metric multidimensional scaling (NMDS) plots of phytoplankton functional group overlain by smooth response curves of the environmental variables 注: a图为三种浮游植物功能群与WT、TN在时间上的分布差异; b图为三种浮游植物功能群与Tur.、SpCond.在空间上的分布差异; WT为水温; TN为总氮; Tur.为浊度; SpCond.为电导率 |
对FG、MFG和MBFG功能群进行去趋势对应分析(DCA), 结果显示排序轴<3, 故对浮游植物功能群与环境因子间的关系采用冗余分析(RDA)。通过Monte Carlo置换检验, 筛选出影响FG功能群时间和空间分布格局的主要环境变量为: WT(P=0.002)、TN(P=0.002)、浊度(P=0.024); 影响MFG功能群时间和空间分布格局的主要环境变量为: WT(P=0.002)、TN(P=0.002)、BOD5(P=0.048)。影响MBFG功能群时间和空间分布格局的主要环境变量为: WT (P=0.002)、TN(P=0.002)。FG和MFG功能群与环境因子的RDA分析结果显示: 环境因子集中在第二、三、四象限; 春季采样点位于第二、三象限; 夏季采样点在坐标轴的第一、四象限; 耕地和林地采样点分布杂乱在四个象限内。MBFG功能群与环境因子的RDA分析结果显示: 环境因子集中在第一、三、四象限; 春季采样点位于第一、四象限; 夏季采样点在坐标轴的第二、三象限; 耕地和林地采样点分布杂乱在四个象限内。
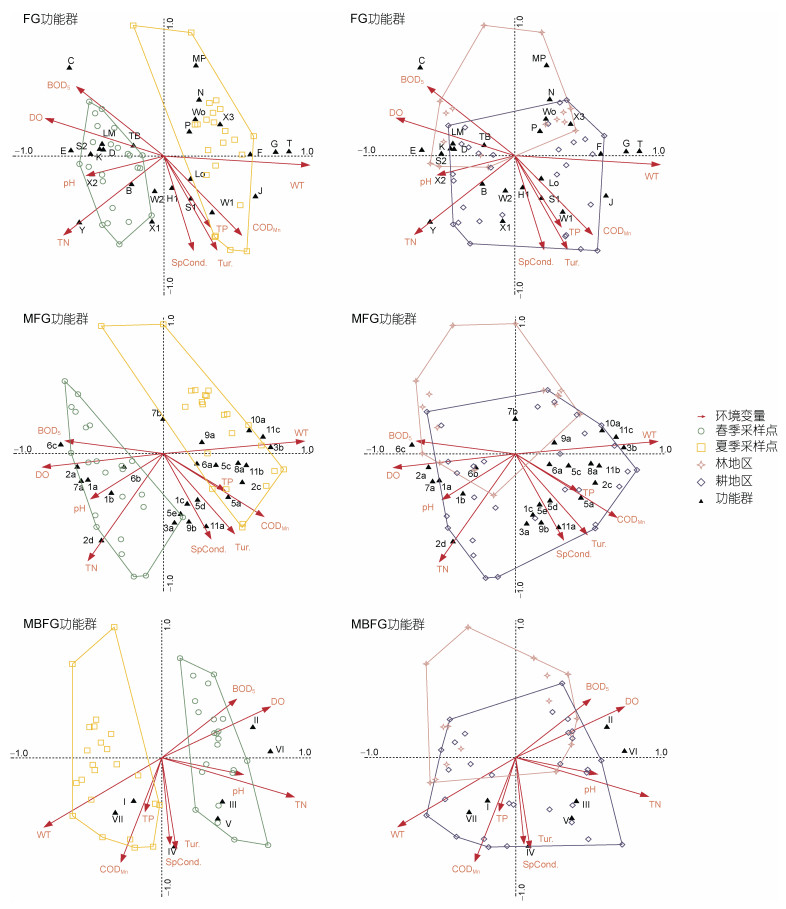 |
| 图 5 浮游植物功能群与环境变量的RDA分析 Fig. 5 RDA of representative functional groups and environmental variables |
浮游植物群落可以通过自身演替来应对季节更替引起的水环境因子变化, 从而维持水生态系统平衡(王徐林等, 2018)438。本研究发现, 浮游植物群落的动态变化规律为从春季硅藻门占绝对优势, 演替到夏季硅藻门占优势, 绿藻门和蓝藻门的比例逐渐升高。拉林河浮游植物群落结构的组成类型为硅藻-绿藻型, 与同纬度地区的多瑙河(Abonyi et al, 2018)456、密西西比河(Manier et al, 2021)1451等(Améziane et al, 2003)以及我国内陆(朱为菊等, 2017637; 君珊等, 2019790; 代亮亮等, 2021)4的淮河、汾河等大型河流浮游植物群落结构组成相似, 符合河流群落分布特征。寒区河流春季经历河冰解冻的过程导致水体温度相对较低, 不利于浮游植物生存; 而夏季温度升高伴随着高强度光照, 有助于浮游植物定植建群。Tian等(2021)7对滦河的研究表明夏季较高的TN含量, 促使夏季的浮游植物丰度高于春季。但本研究中春季浮游植物平均丰度显著高于夏季。大量研究表明(纪道斌等, 2013; Brasil et al, 2020; 张萍等, 2022), 高降水量不仅会对浮游植物进行稀释, 对营养物质也有稀释作用, 从而对浮游植物生长产生抑制作用。水体的稀释超过了浮游植物的生长速度, 导致其丰度显著下降。有数据统计拉林河流域春季降水量在10~50 mm, 夏季降水量在30~100 mm, 且夏季上游降水量在50~100 mm (刘洪超, 2016)9, 因此拉林河夏季降雨过程可能是夏季浮游植物平均丰度低于春季的原因之一。而另一方面, 本研究TN的平均含量呈现出春季(0.76 mg/L)>夏季(0.44 mg/L)的规律, 可能是由于春季河流冰雪消融、营养盐积累, 因此较高的TN含量为喜好高营养的浮游植物提供了良好的生存生境。
本次研究共鉴定浮游植物种类数168种, 春季、夏季平均丰度为6.10×106和1.14×106 ind./L。这与松花江哈尔滨段(136种, 春季3.27×106 ind./L、夏季1.15×106 ind./L)浮游植物种类数相比较丰富, 春季平均丰度较高(Meng et al, 2020)。河流连续概念(river continuum concept, RCC)认为河流从上游到下游水体的营养盐及对应生物群落组成呈现纵向梯度变化, 物种多样性通常在源头河段和下游河段相对较低(马煜等, 2021)7, 拉林河于松花江哈尔滨段上游汇入松花江, 这可能是拉林河浮游植物物种多样性高于松花江哈尔滨段的原因; 由于拉林河流域农业活动的开展, 农药、化肥的使用, 外源营养盐尤其是TN过量输入, 拉林河春季(0.76 mg/L) TN平均含量高于松花江哈尔滨段(0.49 mg/L), 较高浓度的TN利于浮游植物生长, 这也是拉林河春季浮游植物平均丰度高于松花江哈尔滨段的原因之一。
浮游植物群落空间分布格局受水体理化因素, 土地利用类型, 人为活动干扰强度等多重因子共同影响(朱为菊等, 2017)638。本研究中, PCA分析得出水体理化环境因子在不同土地利用类型之间存在明显空间差异。ANOSIM分析表明, 拉林河林地与耕地间浮游植物分布特征差异显著(P < 0.05)。农业种植区域, 化肥、农药残留经地表径流及渗漏、淋溶等途径进入水生态系统能改变流域内的营养状态和底质的环境因子, 进而导致河流污染, 这体现在浮游植物群落存在明显的空间梯度(Li et al, 2017)。SIMPER分析表明, 美丽星杆藻、梅尼小环藻、狭形纤维藻是拉林河林地与耕地浮游植物群落差异的主要贡献物种, 贡献率分别为21.64%、19.28%、6.26%。美丽星杆藻为寡污指示种(张囡囡等, 2016), 在春季上游及干流广泛分布且占据优势。梅尼小环藻、狭形纤维藻为富营养化水体指示种(朱为菊等, 2017)642, 在夏季耕地区占据不同程度优势地位, 且TN、TP、SpCond.等理化因子呈现出耕地>林地的规律, 表现出农业活动对拉林河水质产生一定程度的污染。基于底栖硅藻对拉林河研究表明耕地区呈现出轻度污染至重度污染状况(单涛等, 2023), 与本研究基于浮游植物对拉林河的研究结果一致。这进一步证明, 浮游植物和底栖硅藻群落时空分布特征可作为农业活动区河流生态评估的生物指标。
| 河流 | 流域面积/万km2 | 资料来源 | 群落结构 |
| 北美洲-密西西比河 | 322.00 | Manier et al, 20211450 | 浮游植物的种类组成以硅藻为主 |
| 欧洲-多瑙河 | 81.70 | Abonyi et al, 2018466 | 浮游植物的种类组成以硅藻为主, 硅藻丰度在春/冬季高, 夏/秋季低 |
| 欧洲-加龙河 | 5.60 | Améziane, 2003 | 浮游植物的种类组成以硅藻为主, 其次为绿藻和蓝藻 |
| 欧洲-波河 | 7.50 | Tavernini et al, 2011 | 浮游植物的种类组成以硅藻为主、隐藻和绿藻次之 |
| 亚洲-牡丹江 | 4.06 | Yu et al, 2012 | 浮游植物132种, 绿藻52种、硅藻36种、蓝藻30种。春季丰度最高 |
| 滦河 | 0.10 | Tian et al, 20216 | 浮游植物的种类组成以硅藻为主、绿藻次之。夏季62种、秋季61种、春季44种 |
| 黄河流域汾河 | 0.39 | Yang et al, 201913 | 浮游植物群落组成以蓝藻为主、绿藻、硅藻次之。在空间分布上, 河流下游浮游植物丰度比上游高 |
| 高原河流拉萨河 | 0.31 | 君珊等, 2019795 | 浮游植物5门22科46属53种, 夏季硅藻32种、绿藻11种、蓝藻8种 |
| 钱塘江 | 0.55 | 张萍等, 2022426 | 夏季浮游植物95种, 绿藻41种、硅藻38种。梅雨期主要优势种为硅藻门, 梅雨后主要优势种为蓝藻门 |
| 淮河流域 | 1.90 | 朱为菊等, 2017641 | 夏季浮游植物244种, 绿藻101种、硅藻53种 |
| 长江流域湘江河 | 0.49 | 代亮亮等, 20217 | 浮游植物43种, 硅藻18种、绿藻16种 |
| 松花江哈尔滨段 | 5.30 | 马煜等, 20216 | 浮游植物136种, 以硅藻门和绿藻门为主 |
浮游植物功能群演替主要是由水动力学特征、水体温度、生源要素、CO2浓度、光照条件、浮游动物牧食压力等共同作用的结果。浮游植物优势功能群与相应的生境状态相对应, 能够反映水体的水质状况、营养水平(Wang et al, 2020)2。
拉林河流域为北温带季风气候, 春季光照强度和水体温度相对较低。B/7a类群小环藻属的梅尼小环藻形态有利于维持高水平的表面积和体积比值, 同时具有高效的捕光能力, 耐受低光、低温的水体环境(韩丽彬等, 2022)。因此在春季较低光照条件下具有良好的竞争优势; C/6c类群多为星杆藻属的美丽星杆藻, 其喜好生活在中小型水体中(贾鹏等, 2021)1049; D/6b类群多为菱形藻属的谷皮菱形藻、针状菱形藻, 其喜好高营养盐和高pH的中小型浅水水体(Petar et al, 2014)164。春季由于冰雪消融, 营养盐积累, 水体呈碱性, 因此D/6b类群在春季占据优势地位。Ⅴ类群主要是具鞭毛中到大型的单细胞种类(隐藻), Ⅵ类群主要是具硅质外壁且无鞭毛的种类(硅藻)。Ⅴ类群的代表性物种为卵形隐藻和啮蚀隐藻, 耐受低温低光照, 具有鞭毛且运动能力较强, 为广适应性种类(朱忆秋等, 2019)2084, 与Ⅵ类群的硅藻在春季共同占据优势地位。MP类群主要包括硅藻门具有胶柄的桥弯藻、异极藻等, 分泌胞外多聚物的舟形藻、羽纹藻等, 易于依附在基质上, 生活在不稳定且浑浊的水体中(Xiao et al, 2011); X1类群多为绿藻门的纤维藻属, 生长最适温度在25~35 ℃, 通常存在于水体扰动的浅混合层中(Li et al, 2020)。夏季拉林河经常骤降暴雨, 降雨径流所携带的陆源物质发生沉降, 同时引起水体浊度升高, 透明度降低, 因此MP/X1类群易在夏季河流资源竞争及种群适应中占优势地位; P/8a类群多生活于营养丰富的浅水环境中, 且耐受低光照(王徐林等, 2018)438。拉林河夏季耕地区由于水田灌溉用水, 水体透光性差、透明度偏低, 为P/8a类群生长提供了良好的环境。Ⅳ类群主要是无运动器官的绿藻构成(朱忆秋等, 2019)2084, 绿藻适宜生长在中等的水温生境中, 能因此能在拉林河夏季浮游植物群落中占据优势地位。
本研究发现三种功能群在时空分布上具有一定的差异, 季节变化差异显著而空间变化差异相对较小。经RDA分析表明: WT、TN和浊度是驱动三种功能群时空分布格局的主要环境变量, WT和TN在季节间变化差异显著(P < 0.05), 浊度在空间上变化差异显著(P < 0.05)。NMDS与GAM结果与RDA结果一致, 这也进一步证明WT、TN和浊度对流域内浮游植物群落时空演替产生重要的驱动作用。WT是影响浮游植物生长的关键因子, 它能通过影响浮游植物的生理和代谢过程直接影响浮游植物的生长繁殖(君珊等, 2019)795。不同种类的浮游植物有其适合生长和繁殖的温度条件, 较高的WT条件有利于蓝藻、绿藻的生长, 较低的WT条件有利于硅藻的生长(Liao et al, 2021)12。RDA结果显示, MP/P/G/3b/6a/8a/Ⅶ类群与WT变化密切相关, 随着WT的升高各类群占据优势地位。有研究表明(Tian et al, 2018)5 MP类群在较高温度下适宜生长, 这可能是研究区域MP类群在夏季占据优势地位的原因之一。TN是评估河流富营养水平的重要指标, 也是浮游植物生长代谢所必需的营养物质, 与浮游植物群落组成、丰度和生物量等息息相关(赵杨, 2020)70。当水体中TN含量过高或过低时, 都会影响浮游植物群落结构的演替(de Souza et al, 2016)。春季拉林河日照时间相对较少, 水温较低, 水体滞留时间较长, 促进了可溶性物质的富集和积蓄, 导致TN含量升高。夏季光照增强、水温升高、浮游植物迅速繁殖, 消耗大量的营养盐以及降雨稀释作用, 导致TN含量降低。RDA结果显示, B/6b/Ⅵ类群随着TN含量的降低表现出丰度下降的趋势。Varol (2019)20450研究表明B类群对TN浓度敏感, 因此高浓度TN可能是B类群生长的重要因素之一。
浊度是表征水体光线通过时产生的阻碍程度(He et al, 2022)。水体中存在的泥沙与微小颗粒悬浮物质会导致水体透明度降低, 会直接影响浮游植物的丰度(Santos et al, 2022)。适当浊度能够促进如硅藻等浮游植物的生长, 过高的浊度则会抑制浮游植物的生长与繁殖(贾鹏等, 2021)1049。RDA结果显示, W1/X1/P/MP类群与浊度密切相关, 随着水体浊度的升高W1/X1类群的丰度增加, P/MP类群的丰度降低。由于拉林河是一条高泥沙河流, 耕地区受到农业活动以及采沙作业的影响水体流量大且扰动较大, 导致水体的浊度逐渐升高、透明度下降, 进而限制了光照的射入。W1/X1类群的纤维藻和裸藻能够随着光线的强弱自由运动(毛启迪等, 2018), 在相同光照条件下这些类群的光合作用更强, 因此W1/X1类群在浊度较高的耕地区更具有竞争优势, 这也是浮游植物功能群呈现空间分布规律原因之一。此外, 由于P/MP类群的尺寸相对较大, 在相对面积的光照射下这些类群的浮游植物光合作用更弱(Gong et al, 2022), 从而导致P/MP类群在耕地区高浊度的水体中处于不利地位。
3.3 三种功能群对浮游植物群落时空变化过程描述及对环境因子响应关系的比较根据生态位原理, 把生活习性和生存策略相似的浮游植物归于同一个功能群, 可以体现浮游植物在河流生态系统中的生态特征和生境类型(胡韧等, 2015)11。从功能群的划分标准来看: FG功能群依据各种形态、生理和生态因素来判断其所属的功能群(杨文等, 2014)1837; MFG功能群是基于形态和功能特征划分的方法(Salmaso et al, 2007)109; MBFG功能群以浮游植物大小、体积、比表面积以及鞭毛、硅壁、胶被和伪空胞的有无进行划分(Braga et al, 2020)2。MBFG功能群无法把河流的主要优势类群—真浮游型硅藻集群和半浮游型硅藻有效分开, 没有对喜低温低光或喜欢混合搅动水体或喜富营养环境的硅藻进行划分, 会导致水生生态系统营养状态评估存在误差。例如, 将代表富营养状态的梅尼小环藻和代表寡营养或中营养状态的美丽星杆藻划分为Ⅵ类群(胡韧等, 2015)15。FG、MFG相较于MBFG功能群对浮游植物的生理生态属性及功能性状划分更为细致, 可以描述浮游植物群落在响应主要环境驱动因素时的变化。RDA和NMDS结果表明, 三种划分方法都能反应拉林河浮游植物群落分布特征随着季节演替及空间分布发生变化, 但FG功能群更能体现拉林河流域的水体理化环境变化规律。Qu等(2018)、胡长玉等(2019)、Yang等(2020)、Long等(2020)、赵耿楠等(2021)、Wu等(2023)研究也表明FG功能群更好地表征流动水体环境的时空变化, 对环境的解释更全面清晰。
综合分析, FG功能群更适合对河流水环境变化进行监测。以FG功能群为研究手段分析北方河流浮游植物功能群时空分布特征, 基本可以有效地反映浮游植物在河流生态系统中的生态位及对水体变化作出的响应, 并对未来水环境的变化做出预测。
4 结论(1) 本次研究共鉴定浮游植物168个分类单位, 群落结构的组成类型为硅藻-绿藻型, 与同维度地区大型河流浮游植物群落研究相比, 拉林河浮游植物群落结构较为稳定可以作为水环境变化的有效指示信号。
(2) WT和TN为驱动拉林河浮游植物群落结构呈现明显的时空分布差异的环境因子, 浮游植物可以作为区分林地和耕地的生物指示种。
(3) 拉林河三种浮游植物功能群呈现出明显的空异质性。NMDS与GAM和RDA分析表明, 驱动FG、MFG、MBFG功能群季节演替的主要环境因子为WT和TN, 影响浮游植物空间分异的主要环境因子为浊度。
(4) 与MFG、MBFG功能群相比, FG功能群对浮游植物的生理生态属性及功能性状划分更为细致, 对环境的解释更全面清晰, 更适合对河流水环境变化进行监测。
马煜, 陆欣鑫, 范亚文, 2021. 松花江哈尔滨段浮游植物群落格局及其与环境因子的相关性. 生态学报, 41(1): 224-234 |
王全喜, 曹建国, 刘妍, 等, 2008. 上海九段沙湿地自然保护区及其附近水域藻类图集. 北京: 科学出版社, 1-62
|
王徐林, 张民, 殷进, 2018. 巢湖浮游藻类功能群的组成特性及其影响因素. 湖泊科学, 30(2): 431-440 |
毛启迪, 杨苏文, 金位栋, 等, 2018. 北京市翠湖国家湿地公园血红裸藻(Euglena sanguinea)水华衰亡过程. 湖泊科学, 30(2): 394-402 |
尹航, 2007. 环境监测方法标准汇编-水环境. 北京: 中国标准出版社, 224-226
|
代亮亮, 吕敬才, 周维成, 等, 2021. 3种不同营养水平的河流浮游植物群落结构及其与环境因子的相关性. 生态学报, 41(3): 1242-1250 |
邢爽, 2019. 拉林河底栖硅藻时空分布格局及水质初步评价[D]. 哈尔滨: 哈尔滨师范大学: 119-120.
|
毕列爵, 胡征宇, 2004. 中国淡水藻志—第八卷: 绿藻门绿球藻目(上). 北京: 科学出版社, 1-122
|
朱为菊, 庞婉婷, 尤庆敏, 等, 2017. 淮河流域春季浮游植物群落结构特征及其水质评价. 湖泊科学, 29(3): 637-645 |
朱忆秋, 吕俊, 李乔臻, 等, 2019. 亚热带水库浮游植物群落的季节变化及其与环境的关系: 两种功能群分类法的比较. 应用生态学报, 30(6): 2079-2086 |
刘洪超, 2016. 拉林河流域重要省界缓冲区污染特征及负荷模拟研究[D]. 长春: 吉林大学: 9-69.
|
纪道斌, 李媛, 孔松, 等, 2013. 典型暴雨洪水对三峡水库香溪河库湾水华的影响. 中国农村水利水电, (6): 39-44 |
杨文, 朱津永, 陆开宏, 等, 2014. 淡水浮游植物功能类群分类法的提出、发展及应用. 应用生态学报, 25(6): 1833-1840 |
君珊, 王东波, 周健华, 等, 2019. 拉萨河流域浮游植物群落结构特征及与环境因子的关系. 生态学报, 39(3): 787-798 |
张囡囡, 刘宜鑫, 臧淑英, 2016. 黑龙江扎龙湿地不同功能区浮游植物群落与环境因子的关系. 湖泊科学, 28(3): 554-565 |
张萍, 国超旋, 俞洁, 等, 2022. 钱塘江干流夏季浮游植物群落结构特征及其对水文气象的响应. 湖泊科学, 34(2): 418-432 |
金业, 2019. 乌梁素海浮游植物功能群时空变异性及其影响因子研究[D]. 呼和浩特: 内蒙古大学: 14-15.
|
单涛, 袁安龙, 黄子芮, 等, 2023. 拉林河流域底栖硅藻群落结构特征及水生态健康评价. 环境科学, 44(3): 1465-1474 DOI:10.13227/j.hjkx.202205168 |
赵杨, 2020. 城市河段底栖硅藻多样性格局及其环境相关性初步研究——以哈尔滨市4条河流为例[D]. 哈尔滨: 哈尔滨师范大学: 8-103.
|
赵耿楠, 潘保柱, 丁一桐, 等, 2021. 渭河干流和秦岭北麓典型支流浮游植物功能群特征及水质评价. 生态学报, 41(8): 3226-3237 |
胡长玉, 方建新, 李伟, 等, 2019. 新安江(安徽段)及其支流丰水期浮游植物功能群. 生态学杂志, 38(4): 1013-1021 |
胡韧, 蓝于倩, 肖利娟, 等, 2015. 淡水浮游植物功能群的概念、划分方法和应用. 湖泊科学, 27(1): 11-23 |
胡鸿钧, 魏印心, 2006. 中国淡水藻类——系统、分类及生态. 北京: 科学出版社, 1-903
|
贾鹏, 范亚文, 陆欣鑫, 2021. 基于功能类群分析呼兰河口湿地浮游植物群落结构特征. 生态学报, 41(3): 1042-1054 |
郭晓茆, 陈建江, 2002. 执行GB3838-2002《地表水环境质量标准》的思考. 环境监测管理与技术, 14(4): 30-32 |
韩丽彬, 王星, 李秋华, 等, 2022. 贵州高原百花水库浮游植物功能群的动态变化及驱动因子. 湖泊科学, 34(4): 1102-1114 |
ABONYI A, ÁCS É, HIDAS A, et al, 2018. Functional diversity of phytoplankton highlights long-term gradual regime shift in the middle section of the Danube River due to global warming, human impacts and oligotrophication. Freshwater Biology, 63(5): 456-472 |
ABONYI A, LEITÃO M, STANKOVIĆ I, et al, 2014. A large river (River Loire, France) survey to compare phytoplankton functional approaches: do they display river zones in similar ways?. Ecological Indicators, 46: 11-22 |
AMÉZIANE T D, 2003. Origin and transport of phytoplankton in a large river: the Garonne, France. Archiv für Hydrobiologie, 156(3): 385-404 |
BAIRD D J, HAJIBABAEI M, 2012. Biomonitoring 2.0: a new paradigm in ecosystem assessment made possible by next-generation DNA sequencing. Molecular Ecology, 21(8): 2039-2044 |
BRAGA G G, BECKER V, 2020. Influence of water volume reduction on the phytoplankton dynamics in a semi-arid man-made lake: a comparison of two morphofunctional approaches. Anais da Academia Brasileira de Ciências, 92(1): e20181102 |
BRASIL J, SANTOS J B O, SOUSA W, et al, 2020. Rainfall leads to habitat homogenization and facilitates plankton dispersal in tropical semiarid lakes. Aquatic Ecology, 54(1): 225-241 |
DE SOUZA D G, BUENO N C, BORTOLINI J C, et al, 2016. Phytoplankton functional groups in a subtropical Brazilian reservoir: responses to impoundment. Hydrobiologia, 779(1): 47-57 |
GONG D H, GUO Z Q, WEI W X, et al, 2022. Phytoplankton community structure and its relationship with environmental factors in Nanhai Lake. Diversity, 14(11): 927 |
HE R, LUO H A, HE N, et al, 2022. Phytoplankton communities and their relationship with environmental factors in the waters around Macau. International Journal of Environmental Research and Public Health, 19(13): 7788 |
JEON M, IRIARTE J L, YANG E J, et al, 2021. Phytoplankton succession during a massive coastal diatom bloom at Marian Cove, King George Island, Antarctica. Polar Biology, 44(10): 1993-2010 |
KIM H G, HONG S, KIM D K, et al, 2020. Drivers shaping episodic and gradual changes in phytoplankton community succession: taxonomic versus functional groups. Science of the Total Environment, 734: 138940 |
KRUK C, HUSZAR V L M, PEETERS E T H M, et al, 2010. A morphological classification capturing functional variation in phytoplankton. Freshwater Biology, 55(3): 614-627 |
KUNTANAWAT P, RUENIN J, PHATTHANAKUN R, et al, 2014. An electrostatic microwell-based biochip for phytoplanktonic cell trapping. Biomicrofluidics, 8(3): 034108 |
LI F, CHEN L, ZHANG J B, et al, 2017. Bacterial community structure after long-term organic and inorganic fertilization reveals important associations between soil nutrients and specific taxa involved in nutrient transformations. Frontiers in Microbiology, 8: 187 |
LI Q, WANG G, TAN Z, et al, 2020. Succession of phytoplankton in a shallow lake under the alternating influence of runoff and reverse water transfer. Hydrology Research, 51(5): 1077-1090 |
LIAO N, LI H, YOU L H, et al, 2021. Succession of phytoplankton functional groups and driving variables in a young canyon reservoir. International Journal of Environmental Science and Technology, 18(7): 1911-1924 |
LONG S X, ZHANG T, FAN J J, et al, 2020. Responses of phytoplankton functional groups to environmental factors in the Pearl River, South China. Environmental Science and Pollution Research, 27(34): 42242-42253 |
MANIER J T, HARO R J, HOUSER J N, et al, 2021. Spatial and temporal dynamics of phytoplankton assemblages in the upper Mississippi River. River Research and Applications, 37(10): 1451-1462 |
MENG F H, LI Z X, LI L, et al, 2020. Phytoplankton alpha diversity indices response the trophic state variation in hydrologically connected aquatic habitats in the Harbin Section of the Songhua River. Scientific Reports, 10(1): 21337 |
NAN J, LI J H, YANG C T, et al, 2020. Phytoplankton functional groups succession and their driving factors in a shallow subtropical lake. Journal of Freshwater Ecology, 35(1): 409-427 |
PADISÁK J, CROSSETTI L O, NASELLI-FLORES L, 2009. Use and misuse in the application of the phytoplankton functional classification: a critical review with updates. Hydrobiologia, 621(1): 1-19 |
PETAR Ž, MARIJA G U, KORALJKA K B, et al, 2014. Morpho-functional classifications of phytoplankton assemblages of two deep karstic lakes. Hydrobiologia, 740(1): 147-166 |
QU Y M, WU N C, GUSE B, et al, 2019. Riverine phytoplankton functional groups response to multiple stressors variously depending on hydrological periods. Ecological Indicators, 101: 41-49 |
REYNOLDS C S, HUSZAR V, KRUK C, et al, 2002. Towards a functional classification of the freshwater phytoplankton. Journal of Plankton Research, 24(5): 417-428 |
ROSELLI L, LITCHMAN E, 2017. Phytoplankton traits, functional groups and community organization. Journal of Plankton Research, 39(3): 491-493 |
SALMASO N, PADISÁK J, 2007. Morpho-functional groups and phytoplankton development in two deep lakes (Lake Garda, Italy and Lake Stechlin, Germany). Hydrobiologia, 578(1): 97-112 |
SANTOS M, AMORIM A, BROTAS V, et al, 2022. Spatio-temporal dynamics of phytoplankton community in a well-mixed temperate estuary (Sado Estuary, Portugal). Scientific Reports, 12(1): 16423 |
TAVERNINI S, PIEROBON E, VIAROLI P, 2011. Physical factors and dissolved reactive silica affect phytoplankton community structure and dynamics in a lowland eutrophic river (Po River, Italy). Hydrobiologia, 669(1): 213-225 |
TIAN C, HAO D P, PEI H Y, et al, 2018. Phytoplankton functional groups variation and influencing factors in a shallow temperate lake. Water Environment Research, 90(6): 510-519 |
TIAN Y L, JIANG Y, LIU Q, et al, 2021. The impacts of local and regional factors on the phytoplankton community dynamics in a temperate river, Northern China. Ecological Indicators, 123: 107352 |
TSEPLIK N D, MALTSEV Y I, GLUSHCHENKO A M, et al, 2021. Achnanthidium tinea sp. nov.-a new monoraphid diatom (Bacillariophyceae) species, described on the basis of molecular and morphological approaches. PhytoKeys, 174: 147-163 |
VAROL M, 2019. Phytoplankton functional groups in a monomictic reservoir: seasonal succession, ecological preferences, and relationships with environmental variables. Environmental Science and Pollution Research, 26(20): 20439-20453 |
WANG C, JIA H J, WEI J X, et al, 2021. Phytoplankton functional groups as ecological indicators in a subtropical estuarine river delta system. Ecological Indicators, 126: 107651 |
WANG H, ZHAO D D, CHEN L, et al, 2020. Light, but not nutrients, drives seasonal congruence of taxonomic and functional diversity of phytoplankton in a eutrophic highland lake in China. Frontiers in Plant Science, 11: 179 |
WU Z S, WANG F, WANG X L, et al, 2023. Water quality assessment using phytoplankton functional groups in the middle-lower Changjiang River, China. Limnologica, 99: 126056 |
XIAO L J, WANG T, HU R, et al, 2011. Succession of phytoplankton functional groups regulated by monsoonal hydrology in a large canyon-shaped reservoir. Water Research, 45(16): 5099-5109 |
YANG J, WANG F, LV J P, et al, 2019. Interactive effects of temperature and nutrients on the phytoplankton community in an urban river in China. Environmental Monitoring and Assessment, 191(11): 688 |
YANG M Z, XIA J H, CAI W W, et al, 2020. Seasonal and spatial distributions of morpho-functional phytoplankton groups and the role of environmental factors in a subtropical river-type reservoir. Water Science and Technology, 82(11): 2316-2330 |
YU H X, WU J H, MA C X, et al, 2012. Seasonal dynamics of phytoplankton functional groups and its relationship with the environment in river: a case study in Northeast China. Journal of Freshwater Ecology, 27(3): 429-441 |
 2023, Vol. 54
2023, Vol. 54


