
中国海洋湖沼学会主办。
文章信息
- 王一奇, 丁翔翔, 宋会银, 陈楠生. 2023.
- WANG Yi-Qi, DING Xiang-Xiang, SONG Hui-Yin, CHEN Nan-Sheng. 2023.
- 青岛近海球形棕囊藻的宏条形码分析
- METABARCODING ANALYSIS OF PHAEOCYSTIS GLOBOSA IN QINGDAO COASTAL REGIONS
- 海洋与湖沼, 54(5): 1351-1362
- Oceanologia et Limnologia Sinica, 54(5): 1351-1362.
- http://dx.doi.org/10.11693/hyhz20230100014
文章历史
-
收稿日期:2023-01-20
收修改稿日期:2023-07-14
2. 崂山实验室 海洋生态与环境科学功能实验室 山东青岛 266237;
3. 中国科学院海洋大科学研究中心 山东青岛 266071;
4. 中国科学院大学 北京 100049;
5. 江汉大学 湖北武汉 430056
2. Functional Laboratory for Marine Ecology and Environmental science, Laoshan Laboratory, Qingdao 266237, China;
3. Center for Ocean Mega-Science, Chinese Academy of Sciences, Qingdao 266071, China;
4. University of Chinese Academy of Sciences, Beijing 100049, China;
5. Jianghan University, Wuhan 430056, China
隶属于定鞭藻门(Haptophyta)的棕囊藻属(Phaeocystis Lagerheim)物种在包括极地和温带海域在内的全球海域广泛分布, 既是重要的初级生产者, 也是构成海洋生态系统的基础, 为浮游动物提供食物(齐雨藻等, 2001)。棕囊藻属物种具有重要的生态功能, 不仅能够合成和降解二甲基巯基丙酸(DMSP), 释放二甲基硫(DMS)在气候调节中起重要作用(沈萍萍等, 2018), 而且可以引起赤潮, 在包括欧洲北海沿岸海域、荷兰沿海、挪威海等海域频繁暴发, 产生灰白色泡沫, 给海洋环境和渔业造成极大危害(齐雨藻等, 2002)。自1997年10月球形棕囊藻(Phaeocystis globosa)赤潮首次在我国东南沿海海域大规模暴发以来, 球形棕囊藻赤潮在包括福建、广东、广西、海南、河北及天津等省市海域在内的多个海域都频繁暴发(Wang et al, 2021)。
由于球形棕囊藻具有复杂的异型生活周期(heteromorphic life cycle), 既包括游离具有鞭毛的单细胞形态, 也具有囊体形态, 不同形态具有不同的生理和生态特征(Rousseau et al, 2007; Wang et al, 2021), 加上球形棕囊藻细胞很小(直径约3~9 μm), 增加了基于形态特征的检测和鉴定的难度。1997年球形棕囊藻赤潮首次在我国海域暴发时, 曾经根据其形态特征鉴定为波切棕囊藻(Phaeocystis pouchetii) (何家菀等, 1999), 后来通过分子生物学方法确认为球形棕囊藻(王宁等, 2000), 表明分子生物学方法的辅助鉴定大大提升了鉴定的敏感性和准确性。在球形棕囊藻赤潮首次在我国海域暴发时, 赤潮原因种曾被鉴定为一个新纪录种(陈菊芳等, 1999)。不过由于其细胞小, 在浮游植物调查研究中可能被忽视, 因此并不能排除它本来就是我国海域的一个常见物种, 只是长期没有得到准确鉴定。
基于通用分子标记扩增子高通量测序的宏条形码分析(metabarcoding analysis)越来越广泛地应用于鉴定特定海洋生态环境中浮游植物的组成并跟踪浮游植物的时空动态变化(陈楠生, 2020)。与其他种类分子标记相比, 针对海洋浮游植物和赤潮物种的宏条形码分析中应用最多的分子标记18S rDNA V4具有较高的分辨率, 其长度(~380 bp)也适于DNA二代测序技术, 而且参考序列最丰富(Guillou et al, 2013)。不过, 由于包括球形棕囊藻在内的定鞭藻物种的18S rDNA均具有较高的GC含量, 使得基于不同引物的PCR扩增结果出现了不利于定鞭藻物种的扩增偏好性, 导致宏条形码分析容易遗漏掉大量的定鞭藻物种(Liu et al, 2009)。这些研究表明扩增引物的选择对针对定鞭藻物种的宏条形码分析的重要性。为了评估18S rDNA V4不同扩增引物对球形棕囊藻宏条形码分析结果的影响, 我们利用青岛栈桥海域的水样, 比较分析了18S rDNA V4扩增引物对宏条形码分析结果的影响。本研究比较分析了18S rDNA V4两组常用扩增引物: (1) 由Stoeck等开发的扩增引物(简称Stoeck引物), 包括V4F: CCAGCA(G/C)C(C/T) GCGGTAATTCC和V4R: ACTTTCGTTCTTGAT(C/T) (A/G)A (Stoeck et al, 2010; Liu et al, 2021); (2) 由宋伦等开发的扩增引物(简称Song引物), 包括V4-F: GCGGTAATTCCAGCTCCAAT和V4-R: GATCCCC HWACTTTCGTTCTTGA(宋伦等, 2016)。除此之外, 还比较分析了2021年冬季青岛近岸海域(西海岸)首次暴发的球形棕囊藻赤潮(Li et al, 2022; Song et al, 2022; 张清春等, 2022)样本的球形棕囊藻及其时间动态变化。
1 材料与方法 1.1 样品采集为了比较分析通用分子标记18S rDNA V4的扩增引物选择对针对球形棕囊藻的宏条形码分析结果的影响, 我们在青岛栈桥海域系统开展了时间序列的采样。从2021年9月1日至30日, 于青岛栈桥定点(图 1)完成了30天不间断的连续逐日采样。采集时间为每天上午10点, 每次采集表层海水5 L, 采用200 μm筛绢于现场完成藻细胞过滤, 去掉大型的浮游动物和浮游植物, 保留藻细胞样本, 带回实验室进行第2次过滤, 采用0.2 μm的聚碳酸酯膜(Millipore, USA) 对1.5 L海水进行过滤, 携带藻细胞的滤膜迅速放入液氮罐中冷冻保存。除了采集藻细胞, 还于现场完成了温度和盐度的测量, 并于实验室完成了对海水样本进行叶绿素和营养盐测量(附表 1)。
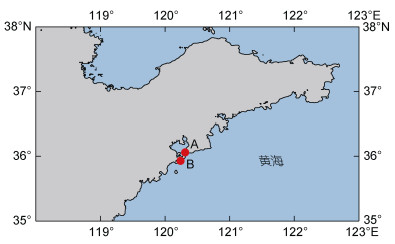 |
| 图 1 本研究采样位点示意图 Fig. 1 Locations of sampling sites in this study 注: 采样点A: 青岛栈桥; 采样点B: 青岛西海岸 |
| 样本 | 水温/℃ | 盐度 | PO43- (μg/L) | NO3- /(μg/L) | NO2- /(μg/L) | NH4+ /(μg/L) | SiO32- /(μg/L) | chl a/(μg/L) |
| S01 | 24.3 | 29.40 | 24.05 | 138.25 | 41.04 | 67.88 | 165.36 | 1.142 |
| S02 | 25.3 | 29.10 | 34.80 | 274.96 | 50.66 | 211.40 | 285.84 | 3.735 |
| S03 | 26.2 | 29.30 | 25.46 | 213.93 | 47.38 | 115.57 | 243.47 | 3.636 |
| S04 | 24.5 | 29.40 | 19.00 | 105.28 | 26.14 | 36.62 | 96.78 | 6.523 |
| S05 | 23.7 | 29.00 | 27.30 | 191.28 | 58.72 | 95.04 | 190.88 | 8.663 |
| S06 | 24.6 | 29.40 | 29.44 | 275.88 | 64.36 | 101.28 | 254.90 | 2.265 |
| S07 | 23.8 | 29.40 | 30.78 | 196.30 | 53.46 | 68.26 | 199.62 | 3.694 |
| S08 | 24.4 | 29.60 | 25.36 | 207.48 | 53.18 | 56.08 | 172.98 | 6.194 |
| S09 | 25.3 | 29.60 | 20.08 | 166.13 | 41.61 | 37.57 | 130.98 | 5.714 |
| S10 | 25.5 | 29.50 | 20.55 | 136.81 | 36.71 | 28.64 | 87.75 | 12.516 |
| S11 | 25.8 | 29.30 | 19.18 | 102.54 | 31.99 | 19.97 | 91.36 | 12.415 |
| S12 | 26.7 | 29.50 | 21.84 | 115.64 | 28.74 | 30.18 | 93.73 | 9.218 |
| S13 | 25.6 | 29.10 | 18.94 | 79.56 | 25.23 | 21.20 | 104.82 | 6.213 |
| S14 | 27 | 29.50 | 17.28 | 86.78 | 17.52 | 39.32 | 135.19 | 25.553 |
| S15 | 25.1 | 29.70 | 11.75 | 38.48 | 12.72 | 43.25 | 49.33 | 4.773 |
| S16 | 24.7 | 29.90 | 18.98 | 65.33 | 19.97 | 54.60 | 59.41 | 8.949 |
| S17 | 25 | 29.60 | 10.57 | 22.71 | 8.37 | 31.02 | 84.94 | 10.391 |
| S18 | 23.9 | 29.80 | 18.58 | 48.23 | 14.70 | 32.18 | 45.38 | 13.894 |
| S19 | 24.3 | 29.70 | 20.13 | 69.69 | 17.68 | 71.13 | 61.54 | 10.408 |
| S20 | 24.1 | 29.20 | 19.57 | 72.29 | 15.21 | 77.40 | 83.16 | 10.558 |
| S21 | 24.2 | 29.10 | 16.03 | 66.20 | 10.92 | 81.68 | 81.89 | 5.072 |
| S22 | 24.5 | 29.50 | 18.15 | 56.12 | 12.44 | 70.39 | 73.84 | 5.909 |
| S23 | 24.6 | 29.70 | 15.12 | 57.75 | 15.60 | 72.04 | 83.06 | 4.482 |
| S24 | 24.7 | 30.00 | 16.43 | 72.03 | 20.10 | 50.09 | 90.05 | 4.021 |
| S25 | 23.1 | 29.90 | 21.19 | 110.97 | 29.35 | 59.85 | 149.12 | 6.869 |
| S26 | 23 | 29.90 | 16.03 | 67.34 | 18.68 | 29.20 | 82.49 | 4.308 |
| S27 | 22.9 | 29.50 | 20.63 | 112.61 | 27.91 | 67.80 | 124.64 | 1.048 |
| S28 | 23 | 29.70 | 17.28 | 90.18 | 24.15 | 30.63 | 95.99 | 0.957 |
| S29 | 23.2 | 29.70 | 17.18 | 90.94 | 25.52 | 21.44 | 92.67 | 1.195 |
| S30 | 24.2 | 29.60 | 11.83 | 25.44 | 7.17 | 16.00 | 30.20 | 4.338 |
| D03 | 12 | NA | NA | NA | NA | NA | NA | NA |
| D08 | 11.9 | 29.30 | 5.05 | 65.40 | 7.47 | 48.49 | 17.37 | 0.954 |
| D11 | 11 | 28.20 | 3.78 | 63.74 | 2.29 | 47.26 | 6.82 | 1.095 |
| D16 | 10.8 | 28.20 | 5.01 | 86.03 | 4.24 | 61.34 | 19.22 | 0.37 |
| D21 | 9.4 | 27.00 | 5.07 | 47.96 | 7.47 | 161.97 | 12.16 | 0.665 |
| D26 | 6.6 | 29.60 | 5.33 | 70.27 | 2.00 | 33.24 | 18.12 | 0.388 |
| D31 | 6.8 | 28.40 | 7.42 | 90.78 | 3.90 | 50.22 | 20.27 | 0.477 |
| 注: NA代表数据缺失。样本列中S代表栈桥样本, D代表西海岸样本 | ||||||||
青岛近海于2021年冬季(12月)突然暴发了一次球形棕囊藻赤潮, 我们对此赤潮事件也进行了时间序列的采样。采样站位位于青岛鲁海丰海洋牧场(图 1), 共完成了7次采样, 包括12月3日、12月8日、12月11日、12月16日、12月21日、12月26日和12月31日采样。赤潮暴发期间, 海水中的球形棕囊藻囊体很多, 肉眼可见(附图 1), 最后一次采集样品时肉眼可见的囊体很少且没有完整的形态。每次采集1.5 L表层海水, 为避免过滤掉囊体, 现场直接采集表层海水, 未经筛娟过滤, 后续的采样流程与青岛栈桥海域时间序列的采样流程相同。
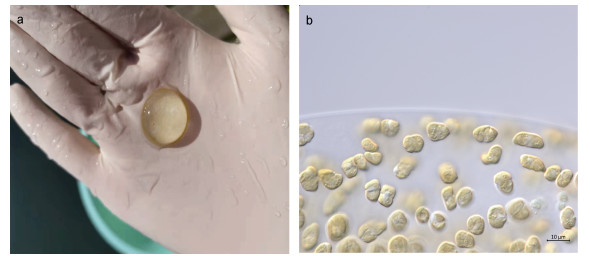 |
| 图 附图 1 西海岸赤潮暴发时球形棕囊藻的形态图(Song et al, 2022) Fig. 附图 1 Morphology of P. globosa during bloom in Xihaian, Qingdao (Song et al, 2022) 注: a: 西海岸赤潮暴发时拍摄到的囊体图片; b: 利用蔡司显微镜拍摄的囊体细胞; 图中右下角标注的比例尺为10 μm |
滤膜细胞的DNA提取方法参照文献(Liu et al, 2020)。为了比较由于引物选择对分子标记18S rDNA V4扩增结果的影响, 分别利用Stoeck引物和Song引物对栈桥海域样本的DNA进行了扩增。
针对西海岸赤潮海域样本, 利用Song引物进行了扩增。
扩增结束后用1%琼脂糖凝胶电泳检测PCR产物的长度, 检测合格后将产物送至北京诺禾致源科技股份有限公司, 使用Illumina公司TruSeq DNA PCR-Free Library Preparation Kit建库试剂盒进行文库的构建, 构建好的文库经过Qubit定量和文库检测, 合格后, 使用NovaSeq 6000 PE250模式进行上机测序。
1.3 生物信息学分析利用R包DADA2对扩增子测序结果展开宏条形码分析(Callahan et al, 2016, 2017), 分析参数设置如下: maxEE = c (2, 2), minLen = 200, truncLen = c (220, 220), minBoot = 80, and Min overlap = 12。运行得到ASV丰度信息以及各个ASV的PR2注释结果。为保证各样本测序深度的可比性, 使用R包Vegan (Dixon, 2003)按照ASV丰度表格中样本的最低数据量抽平, 并采用0.01%的阈值进行丰度筛选。接着对各个ASV进行进一步的blastn注释, 设置PID大于99%, Coverage大于95%, 合并PR2注释结果和blastn注释结果。通过Mega 11.0软件的最大似然法构建了ASV和代表序列之间的遗传进化树(Tamura et al, 2021), Bootstrap值为1 000。各ASV之间的TCS遗传网络图是借助PopART v1.7构建的(Leigh et al, 2015)。利用R包corrplot (Wei et al, 2017)和psych (Revelle, 2021)完成了ASV与环境因子的相关性分析。利用R包Vegan (Dixon, 2003)完成了对测序数据的稀释曲线分析。
1.4 基于18S rDNA V4的遗传多样性分析把从宏条形码分析结果中筛选出注释为球形棕囊藻的18S rDNA V4 ASV序列, 以及从不同海域分离到的代表性球形棕囊藻株系的18S rDNA V4序列一起构建系统发育树。这些代表性球形棕囊藻株系包括: CNS00062(北部湾)、CNS00063(北部湾)、CNS00069(北部湾)、CNS00073(北部湾)、CNS00076 (北部湾)、CNS00082(越南)、CNS00093(越南)、CNS00254(越南)、CNS00079(泰国)、CNS01609(青岛西海岸赤潮暴发海域)和Pg-G(A) (欧洲北海)。
2 结果 2.1 评估18S rDNA V4扩增引物对球形棕囊藻宏条形码分析结果的影响本研究中, 每一个样本的18S rDNA V4扩增子通过二代测序获得约5万条reads (图 2)。稀释曲线分析(附图 2a, 2b)表明测序深度基本达到饱和, 足够用于分析样本中浮游植物的组成。通过对不同扩增引物(Stoeck引物和Song引物)获得的测序结果进行宏条形码分析, 获得了绿藻, 隐藻, 甲藻, 定鞭藻等浮游植物门的组成信息(图 2)。利用Stoeck引物(Stoeck et al, 2010; Liu et al, 2021)的扩增结果开展宏条形码分析获得的甲藻门(Dinoflagellata)、棕鞭藻门(Ochrophyta, 包括硅藻)、定鞭藻门(Haptophyta)、绿藻门(Chlorophyta)和隐藻门(Cryptophyta)的ASV(amplicon sequence variant, 扩增子序列变异)数目分别为479、244、0、43和21个; 利用Song引物(宋伦等, 2016)的扩增结果开展宏条形码分析获得的甲藻门、棕鞭藻门、定鞭藻门、绿藻门和隐藻门分别为581、293、76、49和26个。比较两种引物的分析结果发现差异主要体现在定鞭藻门上, 利用Stoeck引物的宏条形码分析没有发现任何鉴定为定鞭藻门的ASV, 而利用Song引物的宏条形码分析发现了76个鉴定为定鞭藻门的ASVs (图 3a, 3c)。因此, Song引物能够更好地实现对18S rDNA V4的扩增, 从而能够更好地扩增出定鞭藻物种, 更适于针对定鞭藻的宏条形码分析。
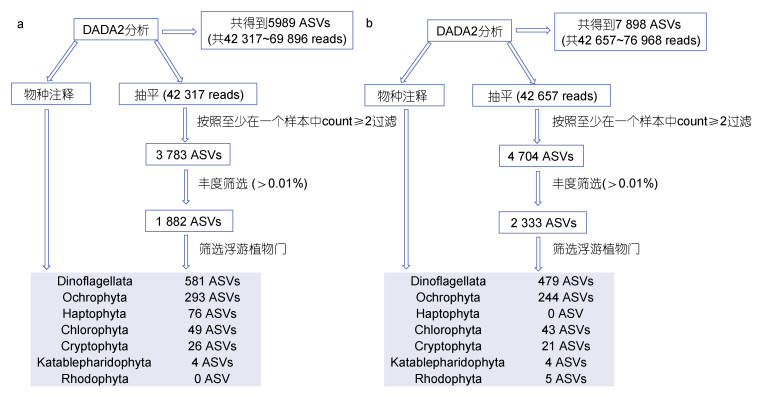 |
| 图 2 栈桥海域样本的宏条形码分析流程 Fig. 2 Metabarcoding analysis of the samples collected in Zhanqiao Pier, Qingdao 注: a图展示的是基于Song引物的分析流程; b图是基于Stoeck引物的分析流程 |
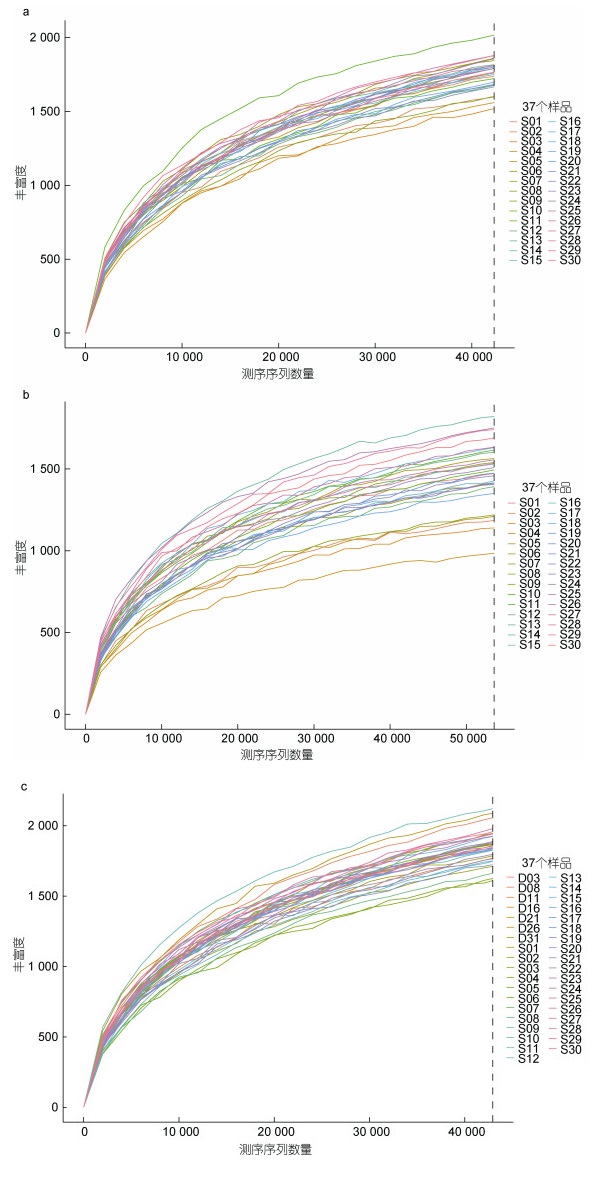 |
| 图 附图 2 稀释曲线 Fig. 附图 2 The rarefaction curves 注: 右侧图例中S代表栈桥样本, D代表西海岸样本。a图是基于宋引物的栈桥海域30个样本的稀释曲线, b图是基于Stoeck引物的栈桥海域30个样本的稀释曲线, c图是基于栈桥和西海岸37个样本的稀释曲线。图例中D代表从青岛西海岸海域采集的30个时间序列的样品; S代表从青岛栈桥海域采集的7个时间序列的样品, 累计37个样品 |
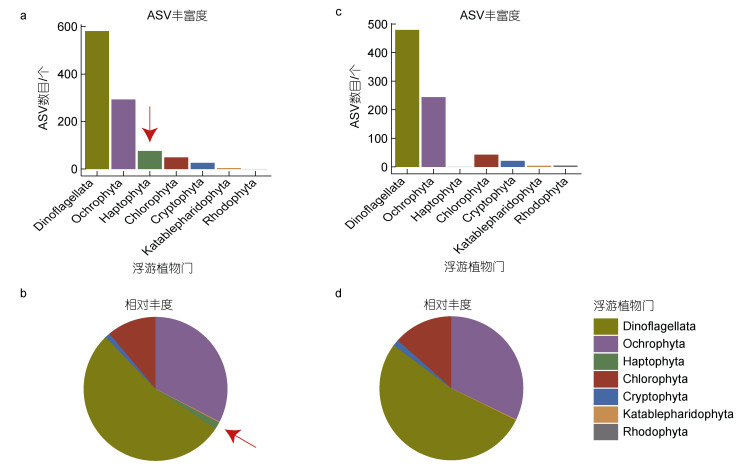 |
| 图 3 青岛栈桥海域样本宏条形码分析结果 Fig. 3 Results of metabarcoding analysis of the samples collected in Zhanqiao Pier, Qingdao 注: a和b图分别展示基于Song引物的ASVs丰富度和相对丰度结果; c和d图是基于Stoeck引物的ASVs丰富度和相对丰度结果。图中的红色箭头标注的是定鞭藻门(Haptophyta) |
通过对青岛栈桥海域的30个逐日样本的宏条形码分析得到的全部ASVs进行物种注释, (图 4a)发现了两个ASVs (ASV_2和ASV_6)注释为球形棕囊藻, 这两个ASVs可能代表两个球形棕囊藻株系。这两个ASVs在所有30个栈桥海域样本中都出现了(图 5d, 5e, 5f), 并且具有相对稳定的水平, 表明青岛海域中存在球形棕囊藻, 并且存在一定的遗传多样性, 是青岛近海的本地株系。本研究表明Song引物不仅可以成功扩增球形棕囊藻的18S rDNA V4, 并且扩增结果可以揭示球形棕囊藻的遗传多样性。
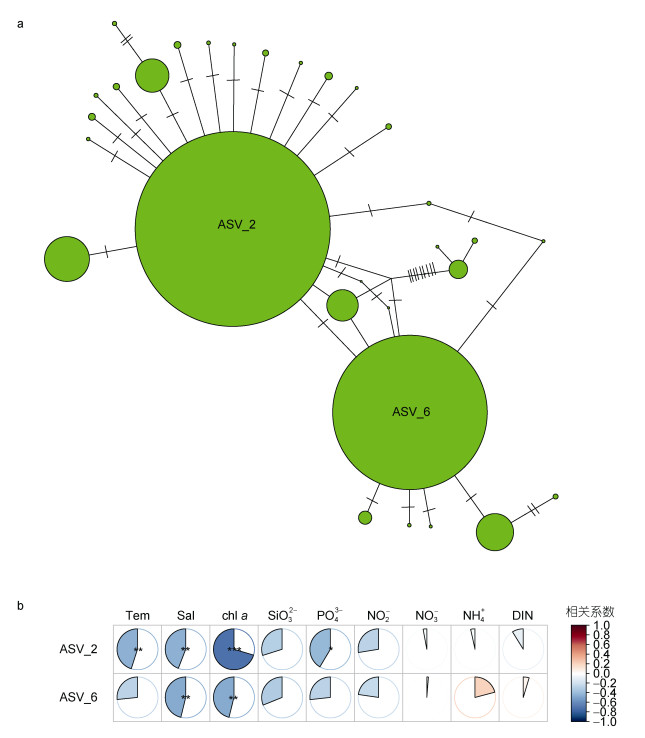 |
| 图 4 球形棕囊藻ASVs之间的遗传多样性及其与环境因子相关性分析 Fig. 4 TCS network display of ASVs annotated as P. globosa and their correlation with environmental factors 注: a图TCS网络图显示了注释为球形棕囊藻的ASVs, 其中ASV_2和ASV_6是主要的ASVs, 每个绿色小球的大小代表ASV丰度的多少, 每个ASV之间连线上的短杠代表两个相邻ASV之间的碱基差异数。b图展示ASV_2和ASV_6与环境因子之间的相关性, *表示P值< 0.05, **表示P值< 0.01, ***表示P值< 0.001。图中Tem代表温度, Sal代表盐度, chl a代表叶绿素a, SiO32-代表硅酸盐, PO43-代表磷酸盐, NO2-代表亚硝酸盐, NO3-代表硝酸盐, NH4+代表铵盐, DIN代表无机氮 |
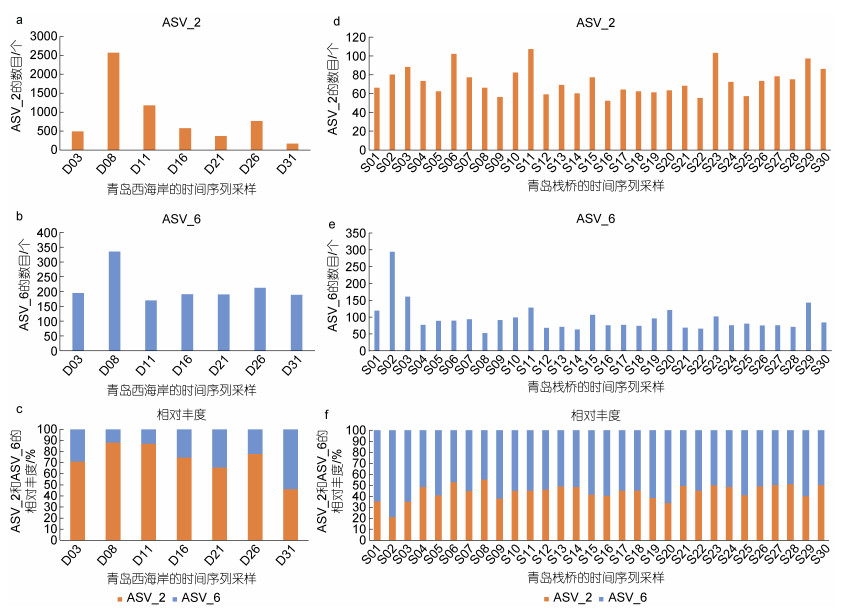 |
| 图 5 ASV_2和ASV_6在青岛西海岸(a, b, c)与青岛栈桥样本(d, e, f)中的时间动态变化 Fig. 5 Dynamic changes of ASV_2 and ASV_6 in Xihaian region, Qingdao (a, b, c) and Zhanqiao Pier region, Qingdao (d, e, f) 注: a、b、c图中的横坐标D代表青岛西海岸海域; d、e、f图中的横坐标S代表青岛栈桥海域。 |
利用Song引物对青岛近海2021年冬季(12月)突发性球形棕囊藻赤潮暴发期间采集的时间序列样本的宏条形码分析也发现了这两个ASVs的信息, 并且比较分析发现两种ASVs的相对丰度显示出不同的时间变化规律(图 5)。在从青岛西海岸球形棕囊藻赤潮暴发过程中采集到的样本中, ASV_2代表的球形棕囊藻株系在赤潮暴发高潮期间的相对丰度较高, 并在赤潮暴发过程中显示出较强的丰度变化, 随着赤潮的消退逐步降低(图 5a)。与ASV_2代表的株系相比, ASV_6代表的球形棕囊藻株系的相对丰度较低, 并在赤潮暴发过程中显示出较弱的丰度变化, 基本维持在接近本底的水平(图 5b)。此外, 在球形棕囊藻赤潮暴发高峰时ASV_2的丰度也高于ASV_ 6 (图 5c)。这说明以ASV_2和ASV_6为代表的两类球形棕囊藻在西海岸赤潮暴发中扮演着不同的角色: 以ASV_2为代表的球形棕囊藻随着西海岸赤潮暴发呈现出先增加后减少的趋势, 且在西海岸赤潮起主要作用, 而以ASV_6为代表的球形棕囊藻变化较小。
ASV_2和ASV_6与青岛海域的环境因子的相关性分析(图 4b)表明, 与ASV_6相比, ASV_2与海水温度呈显著负相关(P < 0.01), 说明ASV_2代表的是一类耐低温的球形棕囊藻株系, 在环境条件适宜时造成此次赤潮暴发。
2.3 基于18S rDNA V4的球形棕囊藻遗传多样性分析前期的研究表明球形棕囊藻具有较高的遗传多样性(Song et al, 2020, 2021, 2022; Wang et al, 2021)。为了探索本研究中发现的ASV_2和ASV_6所代表的球形棕囊藻与前期报道的球形棕囊藻的遗传多样性之间的关系, 我们将ASV_2和ASV_6序列与11株从不同海域分离的球形棕囊藻株系的18S rDNA V4序列进行了遗传进化分析(图 6)。发现这些18S rDNA V4序列可以聚成两个不同的分支, 球形棕囊藻代表性株系的18S rDNA V4序列要么与ASV_2聚在一起, 要么与ASV_6聚在一起(图 6), 表明根据18S rDNA V4可以将球形棕囊藻株系区分为两类。此外, ASV_2序列还与CNS01609株系(在青岛西海岸赤潮暴发海域分离)聚在一起。本研究表明, 宏条形码分析中常用的通用分子标记(即可以用于扩增广谱性物种)18S rDNA V4不仅可以鉴定到球形棕囊藻, 还可以用于初步区分球形棕囊藻的遗传差异。
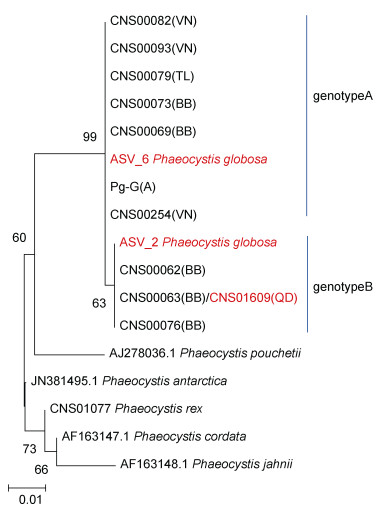 |
| 图 6 基于通用分子标记18S rDNA V4序列的遗传进化分析 Fig. 6 Phylogenetic analysis of the common molecular marker 18S rDNA V4 注: 括号里表示不同地理位置的缩写, BB: 北部湾; TL: 泰国海域; VN: 越南海域; QD: 青岛海域。Pg-G(A)代表欧洲北海株系, 图中的红色字体代表青岛海域的球形棕囊藻株系 |
通过比较针对分子标记18S rDNA V4的两套不同PCR扩增引物(即Stoeck引物和Song引物)发现, 这两套针对18S rDNA V4的扩增引物得到的宏条形码分析结果显示出巨大不同。尽管基于两套引物的宏条形码分析均鉴定出大部分门类的浮游植物组成, 包括甲藻、棕鞭藻、绿藻和隐藻(图 3)。然而只有基于Song引物的宏条形码分析获得了定鞭藻信息(76个ASVs), 基于Stoeck引物的宏条形码分析没有检测到任何定鞭藻信息。本研究结果与宋伦等(2016)的分析结果基本相符。此外, 本研究结果进一步明确了18S rDNA V4扩增引物的选择对研究结果的准确性很重要。
3.2 青岛近岸海域存在当地球形棕囊藻株系本研究发现在青岛近岸海域中可以鉴定到球形棕囊藻信息, 并且该分子生物学鉴定结果与形态学鉴定结果(附图 1)相符, 因球形棕囊藻单细胞尺寸很小, 分子生物学的快速鉴定显示出方法的优势。此外, 针对野外样本的宏条形码分析得到的球形棕囊藻序列ASV_2与2021年冬季青岛西海岸球形棕囊藻赤潮暴发海域分离到的球形棕囊藻株系CNS01609的18S rDNA V4序列完全一致(图 6), 进一步证实青岛近岸海域存在本底球形棕囊藻株系。不仅如此, 经分子生物学鉴定分析发现在青岛栈桥海域和西海岸赤潮暴发海域中均出现了两类不同的球形棕囊藻株系(即由ASV_2和ASV_6代表的两类株系)。ASV_2和ASV_6在2021年9月栈桥海域的整月采样过程中相对比较稳定, 没有受到潮汐的显著影响(图 5)。利用18S rDNA V4 (Liu et al, 2020)针对2019年1月胶州湾海域样本的宏条形码分析以及利用高分辨率分子标记pgcp1 (Song et al, 2020, 2022)和cox1 (Song et al, 2021, 2022)针对2019年1月胶州湾海域样本的分子分析也鉴定到球形棕囊藻的存在, 与本研究结果相符, 表明青岛海域不仅存在本底球形棕囊藻, 还具有一定的遗传多样性。
3.3 不同球形棕囊藻株系对青岛海域突发性赤潮具有不同的贡献本研究基于18S rDNA V4的宏条形码分析发现, 于2021年冬季(12月)在青岛近海突然暴发的球形棕囊藻赤潮样本中可以分辨出两个主要ASVs, 即ASV_2和ASV_6。其中ASV_2的相对丰度较高, 并随赤潮的变化呈现显著的动态变化, 随着赤潮消退呈现下降趋势(图 5)。说明造成此次赤潮的致灾基因型是以ASV_2所代表的这类球形棕囊藻株系。由此可以判断, 不同株系对球形棕囊藻赤潮的形成具有不同的贡献。从该赤潮暴发海域分离到的球形棕囊藻株系CNS01609的18S rDNA V4序列与ASV_2序列在系统发育树中聚在一起(图 6), 表明代表ASV_2的球形棕囊藻株系在赤潮样本中大量存在。
4 结论18S rDNA V4是迄今宏条形码分析中最常用的分子标记(陈楠生, 2020)。本研究比较了两对不同的18S rDNA V4引物在扩增球形棕囊藻时的差别, 包括常用引物(即Stoeck引物)和球形棕囊藻特异性引物(即Song引物)。比较分析表明在展开宏条形码分析时, 选择合适的引物对于分析结果至关重要。宏条形码分析结果表明, 青岛近岸海域存在本底球形棕囊藻, 尽管相对丰度不高, 但是具有一定的遗传多样性, 主要有两种, 分别由ASV_2和ASV_6所代表。其中ASV_2所代表的球形棕囊藻株系更可能是造成此次赤潮暴发的致灾基因型, 表明不同球形棕囊藻株系在球形棕囊藻赤潮暴发过程中的贡献不同。此外, 两种代表ASVs与环境因子的相关性分析表明, ASV_2所代表的球形棕囊藻株系与温度呈显著负相关。本研究表明利用Song引物扩增分子标记18S rDNA V4在鉴定其他大量浮游植物的同时, 不仅可以检测到青岛近岸海域存在本底球形棕囊藻, 还可以鉴定出2种基因型的球形棕囊藻(ASV_2和ASV_6)。因此, 在考虑选择合适的引物开展针对球形棕囊藻以及其他定鞭藻的宏条形码分析时, 建议选择Song引物(宋伦等, 2016)开展基于18S rDNA V4的宏条形码研究。不过, 如果研究目标只是球形棕囊藻的遗传多样性, 可以选择利用高分辨率分子标记pgcp1(Song et al., 2020)或cox1(Song et al., 2021)。
王宁, 陈月琴, 屈良鹄, 等, 2000. 1997粤东海域棕囊藻赤潮原因种18S rDNA基因分析[J]. 中山大学学报(自然科学版), 39(1): 127-128. DOI:10.3321/j.issn:0529-6579.2000.01.032 |
齐雨藻, 沈萍萍, 王艳, 2001. 棕囊藻属(Phaeocystis)的分类与生活史(综述)[J]. 热带亚热带植物学报, 9(2): 174-184. DOI:10.3969/j.issn.1005-3395.2001.02.016 |
齐雨藻, 徐宁, 王艳, 等, 2002. 中国赤潮研究的新进展——球形棕囊藻赤潮及其产硫的研究[J]. 中国基础科学, (4): 25-30. |
何家菀, 施之新, 张银华, 等, 1999. 一种棕囊藻的形态特征与毒素分析[J]. 海洋与湖沼, 30(2): 172-179. DOI:10.3321/j.issn:0029-814X.1999.02.010 |
沈萍萍, 齐雨藻, 欧林坚, 2018. 中国沿海球形棕囊藻(Phaeocystis globosa)的分类、分布及其藻华[J]. 海洋科学, 42(10): 146-162. |
宋伦, 吴景, 刘卫东, 等, 2016. 渤海长兴岛海域微型和微微型浮游植物多样性[J]. 环境科学研究, 29(11): 1635-1642. |
张清春, 向玲, 王锦秀, 等, 2022. 南黄海首次暴发"巨囊"生态型球形棕囊藻藻华[J]. 海洋与湖沼, 53(5): 1098-1107. |
陈菊芳, 徐宁, 江天久, 等, 1999. 中国赤潮新记录种──球形棕囊藻(Phaeocystis globosa)[J]. 暨南大学学报(自然科学版), 20(3): 124-129. |
陈楠生, 2020. 有害藻华的宏条形码分析: 机会与挑战[J]. 海洋科学, 44(7): 116-134. |
CALLAHAN B J, MCMURDIE P J, HOLMES S P, 2017. Exact sequence variants should replace operational taxonomic units in marker-gene data analysis[J]. The ISME Journal, 11(12): 2639-2643. DOI:10.1038/ismej.2017.119 |
CALLAHAN B J, MCMURDIE P J, ROSEN M J, et al, 2016. DADA2: High-resolution sample inference from Illumina amplicon data[J]. Nature Methods, 13(7): 581-583. DOI:10.1038/nmeth.3869 |
DIXON P, 2003. VEGAN, a package of R functions for community ecology[J]. Journal of Vegetation Science, 14(6): 927-930. DOI:10.1111/j.1654-1103.2003.tb02228.x |
GUILLOU L, BACHAR D, AUDIC S, et al, 2013. The Protist Ribosomal Reference database (PR2): a catalog of unicellular eukaryote Small Sub-Unit rRNA sequences with curated taxonomy[J]. Nucleic Acids Research, 41(D1): D597-D604. |
LEIGH J W, BRYANT D, 2015. POPART: full‐feature software for haplotype network construction[J]. Methods in Ecology and Evolution, 6(9): 1110-1116. DOI:10.1111/2041-210X.12410 |
LI D M, XUE Y, SONG Q S, et al, 2022. First report on large-scale Phaeocystis globosa bloom in the southern Yellow Sea, China[J]. Frontiers in Marine Science, 9: 880984. DOI:10.3389/fmars.2022.880984 |
LIU S Y, GIBSON K, CUI Z M, et al, 2020. Metabarcoding analysis of harmful algal species in Jiaozhou Bay[J]. Harmful Algae, 92: 101772. DOI:10.1016/j.hal.2020.101772 |
LIU H, PROBERT I, UITZ J, et al, 2009. Extreme diversity in noncalcifying haptophytes explains a major pigment paradox in open oceans[J]. Proceedings of the National Academy of Sciences of the United States of America, 106(31): 12803-12808. |
LIU S Y, ZHANG M J, ZHAO Y F, et al, 2021. Biodiversity and spatial-temporal dynamics of Margalefidinium species in Jiaozhou Bay, China[J]. International Journal of Environmental Research and Public Health, 18(21): 11637. DOI:10.3390/ijerph182111637 |
REVELLE W, 2021. psych: Procedures for psychological, psychometric, and personality research (Version 2.1. 9). Illinois, USA: Northwestern University, Evanston.
|
ROUSSEAU V, CHRÉTIENNOT-DINET M J, JACOBSEN A, et al, 2007. The life cycle of Phaeocystis: state of knowledge and presumptive role in ecology[J]. Biogeochemistry, 83(1/2/3): 29-47. |
SONG H Y, CHEN Y, GIBSON K, et al, 2021. High genetic diversity of the harmful algal bloom species Phaeocystis globosa revealed using the molecular marker COX1[J]. Harmful Algae, 107: 102065. |
SONG H Y, LIU F, LI Z L, et al, 2020. Development of a high-resolution molecular marker for tracking Phaeocystis globosa genetic diversity through comparative analysis of chloroplast genomes[J]. Harmful Algae, 99: 101911. |
SONG H Y, WANG Y Q, DING X X, et al, 2022. Genetic analysis of a large-scale Phaeocystis globosa bloom offshore Qingdao, China[J]. Microorganisms, 10(9): 1723. |
STOECK T, BASS D, NEBEL M, et al, 2010. Multiple marker parallel tag environmental DNA sequencing reveals a highly complex eukaryotic community in marine anoxic water[J]. Molecular Ecology, 19(S1): 21-31. |
TAMURA K, STECHER G, KUMAR S, 2021. MEGA11: molecular evolutionary genetics analysis version 11[J]. Molecular Biology and Evolution, 38(7): 3022-3027. |
WANG X D, SONG H Y, WANG Y, et al, 2021. Research on the biology and ecology of the harmful algal bloom species Phaeocystis globosa in China: Progresses in the last 20 years[J]. Harmful Algae, 107: 102057. |
WEI T, SIMKO V, 2017. R package "corrplot": Visualization of a correlation matrix(Version 0.84). https://github.com/taiyun/corrplot.
|
 2023, Vol. 54
2023, Vol. 54


