
中国海洋湖沼学会主办。
文章信息
- 谢飞, 于洋, 周海龙, 李富花. 2023.
- XIE Fei, YU Yang, ZHOU Hai-Long, LI Fu-Hua. 2023.
- 一种低密度脂蛋白受体相关蛋白在凡纳滨对虾(Litopenaeus vannamei)抗弧菌感染中的功能研究
- FUNCTION OF A LOW-DENSITY LIPOPROTEIN RECEPTOR-RELATED PROTEIN IN ANTI-VIBRIO INFECTION OF LITOPENAEUS VANNAMEI
- 海洋与湖沼, 54(5): 1454-1462
- Oceanologia et Limnologia Sinica, 54(5): 1454-1462.
- http://dx.doi.org/10.11693/hyhz20230200035
文章历史
-
收稿日期:2023-02-20
收修改稿日期:2023-04-03
2. 中国科学院海洋研究所实验海洋生物学重点实验室 山东青岛 266071
2. Key Laboratory of Experimental Marine Biology, Institute of Oceanology, Chinese Academy of Sciences, Qingdao 266071, China
凡纳滨对虾(Litopenaeus vannamei)是我国重要的水产养殖经济动物, 是对虾养殖的主导品种(Lu et al, 2017; Boyd et al, 2021)。然而, 对虾产业的发展饱受病害问题困扰。近年, 急性肝胰腺坏死病(Acute Hepatopancreatic Necrosis Disease, AHPND)给对虾产业造成严重损失(Wang et al, 2015), 该病致病力强、传播速度快、死亡率高, 以肝胰腺萎缩变白为主要特征, 患病对虾空肠, 空胃, 之后逐渐死亡(Joshi et al, 2014)。该病最初于2009年首次发现, 随后在全球主要对虾养殖国家爆发, 据估计因AHPND造成的对虾养殖业损失已达10亿美元(Lun et al, 2018)。有关AHPND的致病源的研究, Lightner等(2012)首先报道该病的病原是副溶血弧菌(Vibrio parahaemolyticus), 随后研究证实含有PirA、PirB毒素质粒的副溶血弧菌是AHPND的病因(Lee et al, 2015)。虽然AHPND可以通过益生菌、蛭弧菌等控制弧菌的方式进行防控(De Schryver et al, 2014; Gomez-Gil et al, 2014), 但是由于病原菌在养殖水体中已经广泛存在, 生物防控难度较大。
培育抗病对虾良种是防控AHPND暴发的根本方法, 然而抗病性状由于存在测定困难、遗传力低等问题, 采用传统育种技术进行抗病育种难度较大。应用精准、高效的分子育种技术能够显著加快抗AHPND遗传选育, 而筛选抗病基因是开展分子育种的基础。在水产动物中, 随着水产动物基因组的相继破译, 多个抗病相关基因被发掘, 推动了水产动物抗病分子育种研究。在大西洋鲑(Salmo salar)中, 研究鉴定了抗IPN (Infectious pancreatic necrosis)相关QTL和基因, 并筛选了两个与抗IPN性状显著相关的SNP标记, 为抗病性状的改良供了标记来源(Houston et al, 2008, 2012)。此外, 在贝类中分别鉴定了文蛤(Meretrix meretrix)抗副溶血弧菌和栉孔扇贝(Chlamys farreri)抗鳗利斯顿氏菌(Listonella anguillarum)相关分子标记(Li et al, 2009; Nie et al, 2015, 2016)。前期在凡纳滨对虾研究中, 通过关联分析技术, 鉴定了多个抗AHPND相关SNP标记, 并鉴定到LvALF6、LvPI3K等抗弧菌候选基因(Zhang et al, 2019; 李碧瀚等, 2021)。上述抗病分子标记和抗病基因的研究推动了水产动物抗病分子育种工作的开展。
除通过关联分析鉴定抗病标记和基因, 转录组比较分析也是筛选抗病基因的重要方法。前期抗AHPND家系和敏感家系的比较转录组分析鉴定了多个抗弧菌相关基因(Zhang et al, 2021), 其中一种低密度脂蛋白受体相关蛋白1 (Litopenaeus vannamei prolow-density lipoprotein receptor-related protein 1-like, LvLRP1)基因在凡纳滨对虾抗性和敏感家系之间存在显著差异, 提示其可能在对虾抗弧菌中发挥重要作用。LRP1隶属于低密度脂蛋白受体(LDLR)家族, 家族成员基本都是跨膜蛋白, 包括胞外区域和胞内区域。前期研究显示LRP1在内吞和信号转导中发挥重要作用, 同时该基因也是炎症反应的一个重要调节器, 可以影响细胞因子的分泌、吞噬作用和免疫系统细胞的迁移等(May, 2013)。在栉孔扇贝中, 低密度脂蛋白受体相关蛋白可以作为识别和清除病原体的受体, 这为该基因在无脊椎动物免疫中的功能提供了新的线索(Liu et al, 2014)。鉴于前期报道的低密度脂蛋白受体相关蛋白在炎症反应和免疫识别中的作用, 结合抗性和敏感家系转录组数据, 本研究对前期筛选的凡纳滨对虾低密度脂蛋白受体相关蛋白1进行功能研究, 初步解析了其在抗弧菌感染中的功能, 为对虾抗弧菌性状的遗传解析提供了新的线索。
1 材料与方法 1.1 实验动物本实验所用凡纳滨对虾(Litopenaeus vannamei)购自日照星光海洋牧场渔业有限公司(山东日照), 用于弧菌感染实验的对虾平均体重2.33 g, 用于组织表达的对虾平均体重10.66 g。在进行弧菌感染和组织表达取样前, 所有实验材料均在26 ℃的海水中暂养48 h。组织表达分析分别取表皮、肠道、腹神经、肝胰脏、肌肉、脑、淋巴、鳃、胃、心脏、血、眼柄共12个组织, 所有组织经液氮速冻后置于–80 ℃冰箱保存备用。
1.2 总RNA提取和cDNA合成 1.2.1 总RNA提取在液氮中研磨不同组织, 组织粉末使用RNAiso Plus (TaKaRa, 日本)试剂提取总RNA, 具体操作参照说明书。使用1.5%琼脂糖检测总RNA的完整性, 使用Nanodrop1000检测总RNA浓度。
1.2.2 cDNA合成使用PrimeScript RT Reagent Kit (TaKaRa, 日本)合成cDNA, 具体方法参照说明书。首先用gDNA Eraser Buffer在42 ℃下除去基因组DNA, 然后用PrimeScript RT Enzyme Mix在37 ℃下合成cDNA。PCR反应条件为: 37 ℃, 60 min; 85 ℃, 5 s; 4 ℃, 5 min。反应结束后冻存在–20 ℃冰箱。
1.3 凡纳滨对虾低密度脂蛋白受体相关蛋白1的序列分析前期在抗副溶血弧菌家系和敏感家系的比较转录组中筛选到一个差异基因, 注释为低密度脂蛋白受体相关蛋白1 (Litopenaeus vannamei prolow-density lipoprotein receptor-related protein 1-like, LvLRP1) (Zhang et al, 2021)。经与转录组比对发现该基因存在两个转录本, 分别命名为LvLRP1-1和LvLRP1-2。设计引物LvLRP1-F和LvLRP1-R同时扩增两个转录本(表 1), 使用头胸部组织cDNA作为模板进行PCR扩增, 电泳显示扩增出两条带。将两条带分别胶回收后进行连接转化, 之后挑取单克隆送生工生物工程(上海)股份有限公司进行一代测序, 测序结果显示两条带分别与LvLRP1-1和LvLRP1-2序列相同, 证实两个转录本均表达且序列准确。
使用ORFfinder预测LvLRP1-1和LvLRP1-2的CDS区域, 使用SignaIP (http://www.cbs.dtu.dk/services/SignalP-4.1/)进行信号肽预测, 使用SMART (http://smart.embl-heidelberg.de/)和Interproscan (https://www.ebi.ac.uk/interpro/about/interproscan/)进行基因的功能域预测。
1.4 组织表达分析使用荧光定量PCR检测LvLRP1-1和LvLRP1-2在不同组织中的表达水平。用于组织表达的引物如表 1所示, 通过将引物设计在LvLRP1-1和LvLRP1-2的差异区域实现表达量的分别检测, 使用18S作为内参基因, 分别扩增目的基因和内参基因。qRT-PCR退火温度设置为55 ℃, 目的基因相对表达量的计算使用2–ΔΔCt法(Goni et al, 2009)。
| 引物名称 | 引物序列5′~3′ |
| LvLRP1-F | TTTAGAAGTTCGTCTGCTCGTCA |
| LvLRP1-R | ATGTCCGGGTAAAAGCATGTTTG |
| 18S-F | TATACGCTAGTGGAGCTGGAA |
| 18S-R | GGGGAGGTAGTGACGAAAAAT |
| qLvLRP1-1-F | TTGCGAGACAGACCAACCAG |
| qLvLRP1-1-R | CAGGTGCAATCTTCATCGCC |
| qLvLRP1-2-F | TCTTGGTGGTTCTCTTCGCC |
| qLvLRP1-2-R | CACGTGTGTCTGTCTCGCAA |
| dsEGFP-F | TAATACGACTCACTATAGGGCAGTGCTTCAGCCGCTACCC |
| dsEGFP-R | TAATACGACTCACTATAGGGAGTTCACCTTGATGCCGTTCTT |
| dsLRP1-F | TAATACGACTCACTATAGGGTGTTTGAAGAACAATGGCGTG |
| dsLRP1-R | TAATACGACTCACTATAGGGAGCTTCTTAGGCTGGAATGCA |
| PirA-F | GGTGACCAGACCTGCTTTGAG |
| PirA-R | CCAGCTAGGATAACCGTAACATG |
| PirB-F | TCTTACACACATTCTTCCTGGT |
| PirB-R | AGAAGTCGTTTGGGGAGATTGT |
| qPirA-F | TTGGACTGTCGAACCAAACG |
| qPirA-R | GCACCCCATTGGTATTGAATG |
通过浸泡方式进行对虾的副溶血弧菌感染实验, 将冻存于–80 ℃的菌液接种至含有2% NaCl的TSB液体培养基中进行活化, 之后转接到新的培养基中过夜扩培, 培养温度为30 ℃, 摇床转速为220 r/min。在副溶血弧菌生长至对数期后, 使用显微镜和血球计数板进行细菌定量, 并通过PCR扩增检测PirA、PirB质粒的存在(Han et al, 2015), PCR扩增引物如表 1所示, 通过前期预实验确定出半数致死浓度为5×106 CFU/mL。
利用培养的带有PirA、PirB质粒的副溶血弧菌进行浸泡感染实验, 实验水体中副溶血弧菌浓度为5×106 CFU/mL, 根据两个转录本的组织表达情况, 取表皮作为分析的靶组织。分别在浸泡感染前(0 h), 浸泡感染后3、6、12 h取对虾表皮组织, 3尾虾混合作为1个样品, 每个时间点设置3个重复。提取表皮组织RNA并合成cDNA, 使用qPCR检测不同时间点表皮组织中LvLRP1-1和LvLRP1-2的表达变化, qPCR程序和相对表达量计算方法与1.4一致。
1.6 dsRNA合成与最佳干扰剂量的确定由于LvLRP1-1和LvLRP1-2的序列相似性高, 其差异部分无法单独设计dsRNA, 因此使用其共同部分设计dsRNA进行RNA干扰实验。使用Primer3设计dsRNA引物, 并在引物序列前添加T7启动子序列, 引物由生工生物工程(上海)股份有限公司合成, 同时合成EGFP基因的dsRNA作为对照, 引物如表 1所示。使用TranscriptAid T7高产率转录试剂盒(美国Thermo Fisher Science)合成目的基因和EGFP的dsRNA。
为确定最佳干扰剂量, 分别使用1 μg/尾、2 μg/尾和4 μg/尾剂量进行干扰预实验, 同时注射同等剂量的dsEGFP和PBS作为对照, 注射后48 h取表皮组织进行RNA提取和LvLRP1-1和LvLRP1-2的定量检测, 分析不同剂量的干扰效率, 确定最佳干扰剂量。
1.7 RNA干扰与细菌感染使用预实验获得的最佳干扰剂量同时敲降LvLRP1-1和LvLRP1-2, 并在基因干扰后进行弧菌感染。分别设置PBS未感染组、PBS组、dsEGFP组和dsLRP1组, 每组三个平行, 每个平行30尾虾。PBS组每尾虾注射10 μL 1×PBS, dsEGFP组每尾虾注射10 μL的dsEGFP (2 μg dsEGFP), dsLRP1组每尾虾注射10 μL的目的基因双链RNA (2 μg dsLRP1)。
注射双链后48 h, 对PBS组、dsEGFP组和dsLRP1组的样品通过浸泡方式进行弧菌感染, 水体中弧菌浓度设置为5×106 CFU/mL, PBS未感染组不进行弧菌感染。感染后3 h分别从dsEGFP组和dsLRP1组随机挑选9尾个体, 取表皮组织, 3尾个体混合作为一个样品, 提取样品的RNA并通过qPCR检测弧菌PirA基因的相对表达量, qPCR扩增引物如表 1所示。同时记录感染各个时间点对虾的死亡率, 绘制死亡率曲线。
1.8 统计分析使用SPSS软件对获得的基因表达数据和不同组的死亡率数据进行T检验, 计算对照组和实验组间的显著性差异, P < 0.05表示显著性差异(用*标记), P < 0.01表示极显著性差异(用**标记)。
2 结果与分析 2.1 LvLRP1-1和LvLRP1-2的cDNA序列分析LvLRP1-1和LvLRP1-2两个转录本的cDNA序列高度一致, 唯一的差别在于LvLRP1-1的cDNA比LvLRP1-2多129 bp, 多编码43个氨基酸(图 1)。LvLRP1-1的cDNA序列全长916 bp, 开放阅读框681 bp, 编码226个氨基酸, 蛋白质分子量为24 334.69 Da, 等电点pI为5.45。LvLRP1-2的cDNA序列全长787 bp, 开放阅读框552 bp, 编码183个氨基酸, 预测蛋白质分子量为19 646.52 Da, 等电点pI为6.55。两者仅ORF区存在差异, LvLRP1-1比LvLRP1-2多编码43个氨基酸(图 1), 结构域预测显示LvLRP1-1和LvLRP1-2都含有信号肽和低密度脂蛋白受体结构域, 且均含有两个内部重复片段(RPT 1)结构域(图 2)。
 |
| 图 1 凡纳滨对虾低密度脂蛋白受体相关蛋白1基因两种转录本的核苷酸和氨基酸序列 Fig. 1 The nucleotide and amino acid sequences of two low-density lipoprotein receptor-related protein 1 gene in L. vannamei 注: a. LvLRP1-1的核苷酸和氨基酸序列; b. LvLRP1-2的核苷酸和氨基酸序列。方框标注起始密码子和终止密码子, 下划线标注信号肽, 波浪线标注低密度脂蛋白受体结构域, 灰色高亮标注两个转录本翻译的氨基酸相同的部分 |
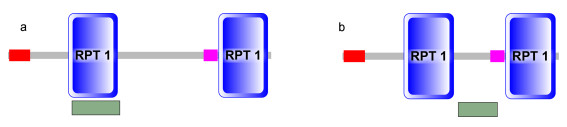 |
| 图 2 凡纳滨对虾低密度脂蛋白受体相关蛋白1基因两种转录本结构域预测 Fig. 2 Prediction of low density lipoprotein receptor-related protein 1 domains in L. vannamei 注: a. LvLRP1-1结构域预测。第1至19个氨基酸为信号肽, 第52至94个氨基酸和第181至223个氨基酸存在内部重复片段(RPT 1), 第168至180个氨基酸存在低复杂度序列, 第55至第96个氨基酸存在低密度脂蛋白受体结构域; b. LvLRP1-2结构域预测。第1至19个氨基酸为信号肽, 第52至94个氨基酸和第138至180个氨基酸存在内部重复片段(RPT 1), 第125到137个氨基酸存在低复杂度序列, 第98到第131个氨基酸存在低密度脂蛋白受体结构域 |
通过荧光定量PCR检测LvLRP1-1和LvLRP1-2在不同组织中的表达量, 结果显示LvLRP1-1在表皮、眼柄、脑和心脏中高表达, LvLRP1-2仅在表皮和眼柄中高表达。表皮和眼柄是LvLRP1-1和LvLRP1-2共同高表达的组织(图 3)。
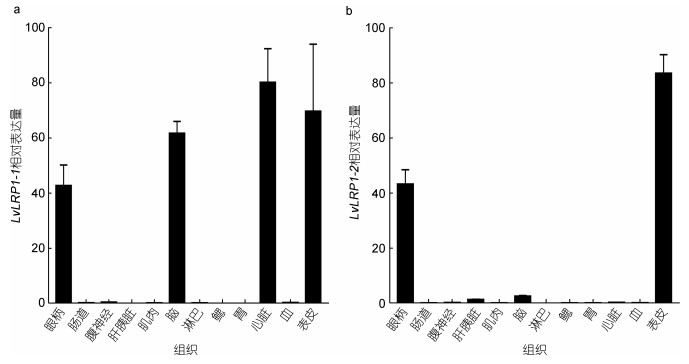 |
| 图 3 LvLRP1-1和LvLRP1-2的组织表达分布 Fig. 3 Tissue expression distribution of LvLRP1-1 and LvLRP1-2 注: a. LvLRP1-1的组织表达分布; b. LvLRP1-2的组织表达分布 |
在副溶血弧菌感染对虾后, LvLRP1-1和LvLRP1-2的转录表达变化趋势一致, 均在感染后3 h其转录水平明显升高, 上调倍数均在10倍以上, 在感染后6 h之后, 其转录表达又恢复到正常水平(图 4)。
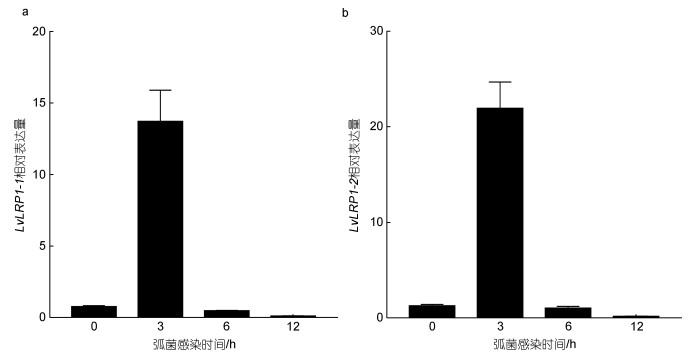 |
| 图 4 副溶血弧菌感染后表皮组织LvLRP1-1和LvLRP1-2表达变化 Fig. 4 Changes of the LvLRP1-1 and LvLRP1-2 expression in epidermal tissue after V. parahaemolyticus infection 注: a. LvLRP1-1的转录表达变化; b. LvLRP1-2的转录表达变化 |
在注射1、2和4 μg双链后LvLRP1-1和LvLRP1-2的表达变化如图 5所示, 在2和4 μg时两个转录本的干扰效率均达98% (图 5), 为了兼顾干扰效率和经济性, 最终确定以2 μg/尾的干扰剂量进行正式实验。
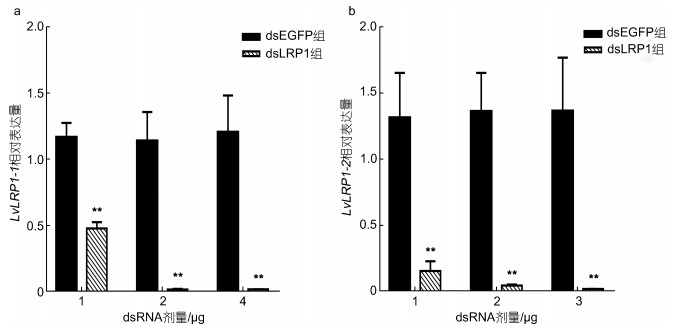 |
| 图 5 注射不同剂量dsRNA后LvLRP1-1和LvLRP1-2的相对表达量 Fig. 5 Relative expression of LvLRP1-1 and LvLRP1-2 after injection with different doses of dsRNA 注: a. LvLRP1-1的相对表达量; b. LvLRP1-2的相对表达量; *表示显著性差异(P < 0.05), **表示极显著性差异(P < 0.01) |
在LvLRP1-1和LvLRP1-2被敲降后进行副溶血弧菌感染, 感染后3 h后检测表皮中PirA的相对表达量来代表弧菌感染和增殖速度, 结果显示目的基因被干扰后表皮中PirA基因的相对表达量显著升高(图 6)。同时, 在基因干扰后, 对虾的死亡速度显著加快。在感染后6 h干扰组死亡率为对照组的3倍, 在感染后12 h干扰组死亡率已达75%, 而对照组的死亡率仅为35%。在感染后24 h, 感染组死亡率达90%, 对照组死亡率为50%。感染后36 h和48 h, 干扰组死亡率为100%, 对照组逐渐趋近平稳, 最终死亡率为60% (图 7)。
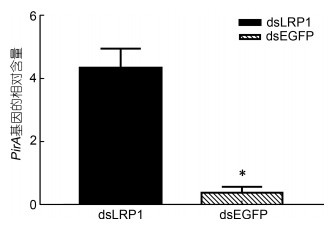 |
| 图 6 LvLRP1-1和LvLRP1-2同时干扰组和对照组在副溶血弧菌感染3 h后表皮组织PirA基因的相对含量 Fig. 6 Relative content of PirA gene in epidermal tissue of LvLRP1-1 and LvLRP1-2 gene interference group and control group after 3 h of V. parahaemolyticus infection 注: *表示显著性差异(P < 0.05) |
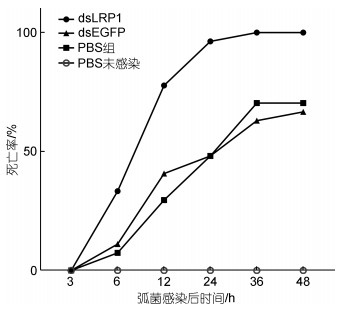 |
| 图 7 LvLRP1-1和LvLRP1-2基因同时干扰后凡纳滨对虾弧菌感染后死亡率 Fig. 7 Mortality following Vibrio infection in L. vannamei after interference of LvLRP1-1 and LvLRP1-2 gene |
抗弧菌相关基因的筛选是开展对虾抗病分子育种的基础。本研究针对前期筛选的抗弧菌相关基因LvLRP1的两个转录本进行了基因序列、组织表达和功能研究, 证实了凡纳滨对虾低密度脂蛋白受体1基因在对虾抵抗弧菌感染的过程中发挥着重要作用。
低密度脂蛋白受体相关蛋白(LRP)是低密度脂蛋白受体家族的一员, 是一种细胞表面蛋白(Auderset et al, 2020)。本研究中发现的LvLRP1-1和LvLRP1-2结构预测是位于胞外区的膜结合蛋白, 符合低密度脂蛋白受体的结构特征, 推测可能发挥细胞表面受体的作用。前期研究表明, LRP1可能是以模式识别受体形式发挥免疫作用, 在扇贝中的研究显示低密度脂蛋白受体可以作为识别和清除病原的受体, 并证实其对弧菌有较强的抑菌活性(Liu et al, 2014)。除了作为模式识别受体, LRP1也是重要的免疫和炎症调节因子。在凡纳滨对虾中鉴定了一种含有低密度脂蛋白受体结构域的凝集素, 免疫刺激后该基因表达上调, 沉默该基因显著提高了对虾在感染副溶血弧菌后的死亡率, 且鳃中细菌载量显著升高, 推测该基因具有细菌凝集活性, 并能增强血细胞的吞噬作用, 进一步研究显示该基因低密度脂蛋白受体结构域的缺失突变体对血细胞的吞噬能力降低, 说明低密度脂蛋白结构域与该基因的免疫活性有关(Liang et al, 2019)。在日本沼虾(Macrobrachium nipponense)的研究中, 氨氮胁迫后LRP1基因显著上调, 提示LRP1基因可能作为重要的免疫及炎症反应因子, 在日本沼虾抗氨氮胁迫中发挥作用(Sun et al, 2020)。
本研究鉴定的LvLRP1-1和LvLRP1-2序列高度相似, 眼柄和表皮是两个转录本共同高表达的组织。表皮是机体免疫的第一道防线, 在浸泡感染中, 表皮组织首先接触弧菌, 并启动弧菌的识别和免疫防御机制。LvLRP1-1和LvLRP1-2均在弧菌感染后快速上调表达, 而在6 h后降至正常水平, 说明该基因在弧菌的早期识别中发挥作用。值得说明的是, 该基因除了含有低密度脂蛋白受体的结构域外, Interproscan的预测结果显示两个转录本编码的109~147氨基酸与WAP结构域具有相似性, WAP结构域是对虾抗菌肽的主要功能域, 其发挥重要的抗菌作用(Lv et al, 2020), 因此LvLRP1在表皮中可能发挥识别和抑菌的双重作用。同时, 该基因在眼柄、心脏和脑中的高表达可能与发挥胆固醇或脂蛋白受体的作用有关, 进一步证实其功能的多样性。
LvLRP1-1和LvLRP1-2序列相似性高, 难以设计双链分别敲降, 鉴于两个转录本在弧菌感染过程中的表达变化一致, 我们推测其在抵抗弧菌感染中的功能相似, 所以本研究采取了对LvLRP1-1和LvLRP1-2同时干扰的方案, 以研究LvLRP1在抗弧菌感染过程中的功能。结果显示, 注射LvLRP1的dsRNA可以显著降低LvLRP1-1和LvLRP1-2的表达量。弧菌感染实验结果显示, LvLRP1基因被沉默后, 对虾死亡率显著上升, 一种原因是该基因的沉默影响了机体对弧菌的识别, 进而影响了机体免疫防御的启动, 另外一种原因是该基因的敲降影响了该基因其对表皮组织中弧菌的清除, 从而使弧菌快速通过表皮进入体内, 该基因的沉默导致其无法发挥免疫效应分子作用, 机体清除弧菌能力减弱, 从而使弧菌快速通过表皮进入体内, 使得死亡率升高。研究结果进一步证实了LvLRP1-1和LvLRP1-2在对虾抗弧菌中发挥重要作用。
4 结论本研究详细分析了LvLRP1-1和LvLRP1-2两个转录本的序列、结构域、组织表达分布和在对虾抗弧菌感染中的功能, 证实LvLRP1基因在弧菌感染过程中发挥重要的免疫和抗病作用, 为对虾抗弧菌性状的遗传解析提供了新的线索, 也为对虾抗弧菌性状的遗传育种提供了理论指导。
李碧瀚, 于洋, 刘桂嘉, 等, 2021. 基于三代测序技术的凡纳滨对虾(Litopenaeus vannamei)高通量候选基因关联分析方法的建立[J]. 海洋与湖沼, 52(5): 1255-1264. |
AUDERSET L, PITMAN K A, CULLEN C L, et al, 2020. Low-density lipoprotein receptor-related protein 1 (LRP1) is a negative regulator of oligodendrocyte progenitor cell differentiation in the adult mouse brain[J]. Frontiers in Cell and Developmental Biology, 8: 564351. DOI:10.3389/fcell.2020.564351 |
BOYD C E, DAVIS R P, WILSON A G, et al, 2021. Resource use in whiteleg shrimp Litopenaeus vannamei farming in Ecuador[J]. Journal of the World Aquaculture Society, 52(4): 772-788. DOI:10.1111/jwas.12818 |
DE SCHRYVER P, DEFOIRDT T, SORGELOOS P, 2014. Early mortality syndrome outbreaks: a microbial management issue in shrimp farming[J]. PLoS Pathogens, 10(4): e1003919. DOI:10.1371/journal.ppat.1003919 |
GOMEZ-GIL B, SOTO-RODRÍGUEZ S, LOZANO R, et al, 2014. Draft genome sequence of Vibrio parahaemolyticus strain M0605, which causes severe mortalities of shrimps in Mexico[J]. Genome Announcements, 2(2): e00055-14. |
GONI R, GARCÍA P, FOISSAC S, 2009. The qPCR Data Statistical Analysis[M]. Integromics, 1-9.
|
HAN J E, TANG K F J, TRAN L H, et al, 2015. Photorhabdus insect-related (Pir) toxin-like genes in a plasmid of Vibrio parahaemolyticus, the causative agent of acute hepatopancreatic necrosis disease (AHPND) of shrimp[J]. Diseases of Aquatic Organisms, 113(1): 33-40. DOI:10.3354/dao02830 |
HOUSTON R D, HALEY C S, HAMILTON A, et al, 2008. Major quantitative trait loci affect resistance to infectious pancreatic necrosis in Atlantic Salmon (Salmo salar)[J]. Genetics, 178(2): 1109-1115. DOI:10.1534/genetics.107.082974 |
HOUSTON R D, DAVEY J W, BISHOP S C, et al, 2012. Characterisation of QTL-linked and genome-wide restriction site-associated DNA (RAD) markers in farmed Atlantic salmon[J]. BMC Genomics, 13: 244. DOI:10.1186/1471-2164-13-244 |
JOSHI J, SRISALA J, TRUONG V H, et al, 2014. Variation in Vibrio parahaemolyticus isolates from a single Thai shrimp farm experiencing an outbreak of acute hepatopancreatic necrosis disease (AHPND)[J]. Aquaculture, 428/429: 297-302. DOI:10.1016/j.aquaculture.2014.03.030 |
LEE C T, CHEN I T, YANG Y T, et al, 2015. The opportunistic marine pathogen Vibrio parahaemolyticus becomes virulent by acquiring a plasmid that expresses a deadly toxin[J]. Proceedings of the National Academy of Sciences of the United States of America, 112(34): 10798-10803. |
LI L, ZHAO J M, WANG L L, et al, 2009. The polymorphism of lysozyme gene in Zhikong scallop (Chlamys farreri) and its association with susceptibility/resistance to Listonella anguillarum[J]. Fish & Shellfish Immunology, 27(2): 136-142. |
LIANG Z W, YANG L W, ZHENG J F, et al, 2019. A low-density lipoprotein receptor (LDLR) class A domain-containing C-type lectin from Litopenaeus vannamei plays opposite roles in antibacterial and antiviral responses[J]. Developmental & Comparative Immunology, 92: 29-34. |
LIGHTNER D V, REDMAN R M, PANTOJA C R, et al, 2012. Early mortality syndrome affects shrimp in Asia[J]. Global Aquaculture Advocate, 15(1): 40. |
LIU R, WANG L L, SUN Y, et al, 2014. A low-density lipoprotein receptor-related protein (LRP)-like molecule identified from Chlamys farreri participated in immune response against bacterial infection[J]. Fish & Shellfish Immunology, 36(2): 336-343. |
LU X, LUAN S, CAO B X, et al, 2017. Estimation of genetic parameters and genotype-by-environment interactions related to acute ammonia stress in Pacific white shrimp (Litopenaeus vannamei) juveniles at two different salinity levels[J]. PLoS One, 12(3): e0173835. DOI:10.1371/journal.pone.0173835 |
LUN J, LIU D, LIU T K, et al, 2018. Evaluation of outer membrane protein U (OmpU) as a novel capture target of Vibrio parahaemolyticus and rapid detection of acute hepatopancreatic necrosis disease (AHPND) using PCR combined with immunomagnetic separation[J]. Aquaculture, 485: 225-232. DOI:10.1016/j.aquaculture.2017.11.046 |
LV X J, LI S H, YU Y, et al, 2020. The immune function of a novel crustin with an atypical WAP domain in regulating intestinal microbiota homeostasis in Litopenaeus vannamei[J]. Developmental & Comparative Immunology, 111: 103756. |
MAY P, 2013. The low-density lipoprotein receptor-related protein 1 in inflammation[J]. Current Opinion in Lipidology, 24(2): 134-137. DOI:10.1097/MOL.0b013e32835e809c |
NIE Q, YUE X, LIU B Z, 2015. Development of Vibrio spp. infection resistance related SNP markers using multiplex SNaPshot genotyping method in the clam Meretrix meretrix[J]. Fish & Shellfish Immunology, 43(2): 469-476. |
NIE Q, YUE X, LIU B Z, 2016. Identification of the MmeHairy gene and expression analysis affected by two SNPs in the 3′-untranslated region in the clam Meretrix meretrix[J]. Fish & Shellfish Immunology, 51: 46-52. |
SUN B, LUO H, ZHAO S, et al, 2020. Characterization and the role of α2-macroglobulin from Macrobrachium nipponense in response to ammonia-N stress[J]. Aquaculture, 522: 735128. DOI:10.1016/j.aquaculture.2020.735128 |
WANG L, WANG X R, LIU J, et al, 2015. Rab from the white shrimp Litopenaeus vannamei: characterization and its regulation upon environmental stress[J]. Ecotoxicology, 24(7): 1765-1774. |
ZHANG Q, YU Y, WANG Q C, et al, 2019. Identification of single nucleotide polymorphisms related to the resistance against acute hepatopancreatic necrosis disease in the pacific white shrimp Litopenaeus vannamei by target sequencing approach[J]. Frontiers in Genetics, 10: 700. |
ZHANG Q, YU Y, LUO Z, et al, 2021. Comparison of gene expression between resistant and susceptible families against VPAHPND and identification of biomarkers used for resistance evaluation in Litopenaeus vannamei[J]. Frontiers in Genetics, 12: 772442. |
 2023, Vol. 54
2023, Vol. 54


