中国海洋湖沼学会主办。
文章信息
- 邓雪, 胡玉斌, 刘春颖, 杨桂朋, 陆小兰, 张洪海. 2016.
- DENG Xue, HU Yu-Bin, LIU Chun-Ying, YANG Gui-Peng, LU Xiao-Lan, ZHANG Hong-Hai. 2016.
- 胶州湾表层海水碳酸盐体系的季节变化
- DISTRIBUTIONS AND SEASONAL VARIATIONS OF CARBONATE SYSTEM IN THE JIAOZHOU BAY, CHINA
- 海洋与湖沼, 47(1): 234-244
- Oceanologia et Limnologia Sinica, 47(1): 234-244.
- http://dx.doi.org/10.11693/hyhz20150800221
-
文章历史
- 收稿日期: 2015-08-18
- 收修改稿日期: 2015-12-25
随着全球人口增长速度和工业化进程的加剧,温室效应对地球气候的影响越来越明显,这引起了人们对大气中CO2的浓度及释放速度的关注。而海洋碳酸盐体系作为调节大气CO2浓度的重要因子之一,调控着海水pH以及碳在生物圈、岩石圈、大气圈和海洋圈的流动,因此海洋在全球CO2的储存和调节中的作用成为近几十年来关注的焦点。虽然陆架边缘海在全球海洋中只占总面积的7%左右,但其初级生产力在全球海洋总初级生产力的比重高达15%— 30%(Walsh,1988; Longhurst et al,1995)。因此近海在全球碳循环中起着重要作用,成为全球碳循环研究的热点之一。
胶州湾位于山东省山东半岛南部,其三面被青岛市环绕,只通过南部湾口与黄海保持着一定强度的水交换,是典型的半封闭型海湾(刘启珍等,2010)。近几十年来,随着青岛市人口和城市化与工业化进程的加快,注入胶州湾的大部分河流,特别是李村河、海泊河、墨水河,已基本成为了市区排放工业废水和生活污水的主要河流通道,也是造成胶州湾海水污染的重要原因(Gao et al,2008)。针 对城市化和人为污染较为严重的胶州湾,开展表层海水碳酸盐体系的研究,分析海水中碳酸盐体系各参量及分布,对于探究CO2在海水中的转移和归宿,海水吸收和转移大气中的CO2的能力以及CO2在海水中的循环过程等,具有重要的意义,而研究河口区海水中的CO2体系对于海洋科学的各个分支也具有重要意义(宋金明,2011)。
关于胶州湾碳酸盐体系的研究,早期有刘辉等(1998)讨论了1995—1996年水体中的溶解无机碳(DIC)和pCO2及HCO3-、CO32-的含量及分布; 沈志良等(1997)通过pH和总碱度(Alk)计算了海水CO2体系中各组分在不同季节的含量和分布; Zhang等(2012)通过实时走航观测得到pCO2数据,并重点分析了pCO2的秋冬季节分布及其影响因素。上述研究对认识胶州湾海水CO2体系及其机制奠定了一定的基础,但缺乏对其CO2体系所有参数的全面分析和探讨。本文依据四个航次对胶州湾的观测数据,给出了CO2体系各参数在不同季节的含量及其分布,并探讨了温度、陆地径流、生物活动及人类活动对各参数的影响。
1 实验部分 1.1 研究海域本研究观测海域在胶州湾内(35°57′—36°18′N,120°04′—120°23′E),调查海区和站位的分布如图 1所示。水样采集时间分别为: 2007年8月5日,2007年10月17日,2008年1月16日和2010年4月13日。
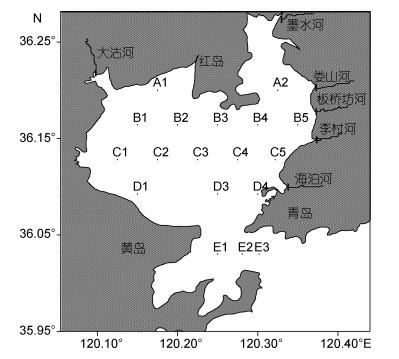 |
| 图 1 调查海区与取样站位 Fig. 1 Study area and locations of sampling stations |
用5L直立式有机玻璃采水器采集水样,现场对pH进行测定,DIC和Alk样品按照溶解氧的采样方法,将水样装于125mL聚丙烯瓶中至溢满,迅速滴加1—2滴饱和HgCl2溶液,然后密闭放置于室温条件下保存,带回陆地实验室后在一个月内测定完毕。
1.3 分析方法利用Fisher pH计(AR15)和Ross-8102 pH电极测定海水pH值(NBS标度),仪器精度为: ±0.002,将实验室测得的数据校正为现场的pH值。DIC采用美国Apollo科技公司AS-C2型溶解无机碳分析仪进行测定,分析精度为0.2%; Alk采用美国Apollo科技公司AS-Alk1+总碱度分析仪利用Gran滴定法测定,精度为0.1%; DIC和Alk均用美国Scripps海洋研究所生产的国际通用的CRMs标准海水校正。pCO2数据则利用Alk和DIC的测定数值,根据Mehrbach等(1973),并由Dickson等(1987)所改进的计算方法,利用CO2计算软件进行计算得到(Lewis et al,1998)。
叶绿素a(Chl-a)浓度的测定: 现场取300mL水样在低压下(<0.05 MPa)经GF/F玻璃纤维滤膜过滤后,滤膜用锡纸包裹,放于冰箱内于-20℃条件下冷冻保存,返回陆地实验室后,用10mL体积分数为90%的丙酮水溶液将滤膜在暗处萃取24h后,离心10min,用分子荧光仪(F-4500,日本Hitach公司)测定其上清液。
溶解有机碳(DOC)浓度的测定: 现场水样立即用已处理好的Whatman GF/F滤膜在全玻璃过滤器上抽滤,然后将滤液转移至已灼烧过的玻璃瓶中,冷冻保存,待返回陆地实验室后,采用总有机碳分析仪(TOC-VCPH,岛津)测定,其相对标准偏差<2%。
2 结果 2.1 胶州湾表层海水二氧化碳体系相关参数的分布特征 2.1.1 温度与盐度胶州湾水温的季节变化呈现典型的温带特征,即夏季最高(平均为26.6℃),冬季最低(平均为4.6℃),春秋为转换季节,但秋季(10月平均为18.5℃)高于初春(4月平均为11.2℃)(图 2)。关于水温的水平分布,水深差异是造成水温分布差异的主要原因,胶州湾平均水深为7m,最大水深约70m位于湾口和中央海域(Yang et al,2010),而湾顶及近岸海域水较浅,这就造成了湾顶和近岸海域因水浅而升温较快,湾口和中央海域因水深而升温较慢,因此升温季节(春、夏季)水温呈现出从湾口向湾顶递增的趋势; 同理,降温季节(秋、冬季)湾顶及近岸海域因水浅而降温较快,湾口和中央海域因水深而降温较慢,水温呈现出从湾口向湾顶递减的趋势。
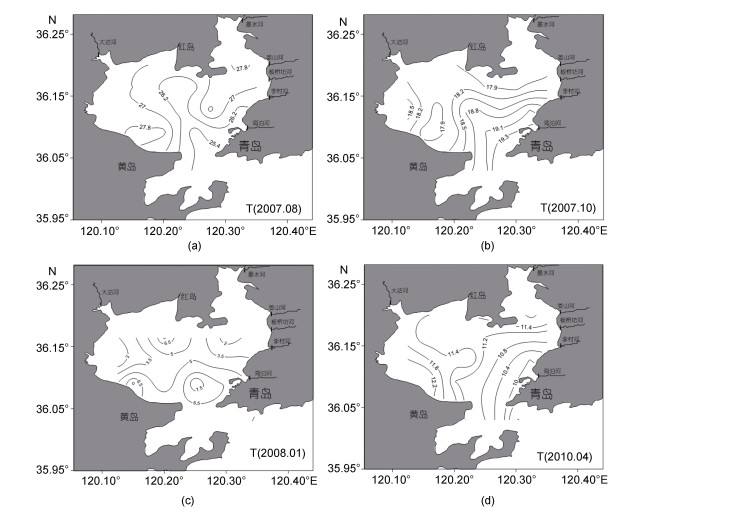 |
| 图 2 夏季(a),秋季(b),冬季(c)和春季(d)表层海水温度(℃)分布图 Fig. 2 Distributions of sea surface temperature(℃)in summer(a),autumn(b),winter(c)and spring(d) |
胶州湾的盐度表现为: 春季最高(平均值为32.1),秋季最低(平均值为28.0),冬季(平均值为30.7)略高于夏季(平均值为30.4)(图 3); 由于注入胶州湾的主要河流皆为季节性河流,汛期一般在7—9月,而陆地径流较汛期稍有滞后性,故秋季盐度因大量淡水的注入而存在最小值; 冬春季为枯水期,因春季的温度高于冬季,因此海水蒸发量较大,故春季的盐度高于冬季。在水平分布上,均表现为从湾口向湾顶及近岸海域呈递减的趋势,这主要是因为湾口与黄海有着较大的水交换,因此盐度较高,而湾顶及近岸海域受陆地径流的影响较大而导致盐度稍有降低。
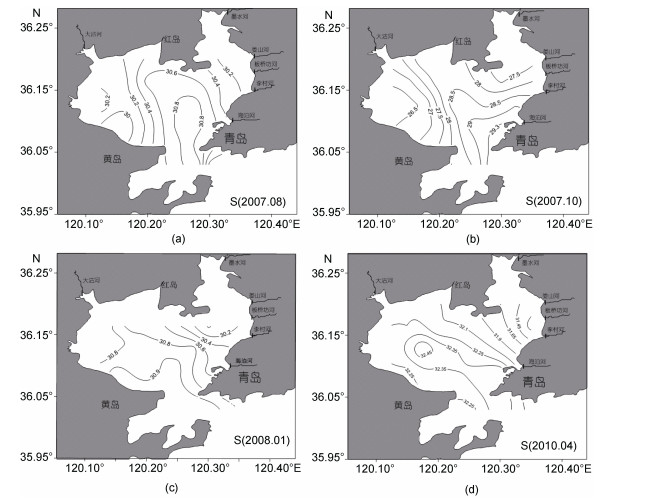 |
| 图 3 夏季(a),秋季(b),冬季(c)和春季(d)表层海水的盐度分布图 Fig. 3 Distributions of sea surface salinity in summer(a),autumn(b),winter(c)and spring(d) |
胶州湾Chl-a含量的季节变化呈现明显的双峰特征,即: 夏季(平均为3.88 μg/L)和冬季(平均为8.59 μg/L)含量较高,秋季(平均为1.77 μg/L)和春季(平均为0.73 μg/L)含量较低,且冬季含量高于夏季(图 4),这与吴玉霖等(2004)和李超伦等(2005)对胶州湾Chl-a的研究结果一致。冬季,湾东北部浮游植物数量剧增,形成了冬季浮游植物水华,因此形成了冬季Chl-a含量达到最高值的格局; 夏季,由于陆地径流带来大量的营养盐,加上水温较高、光照充足,浮游植物生长旺盛,故形成了一年中第二个Chl-a高值期。在水平分布上的明显特征是: 胶州湾的西北部和东北部近岸海区的含量较高,湾中部和南部地区的含量较低。
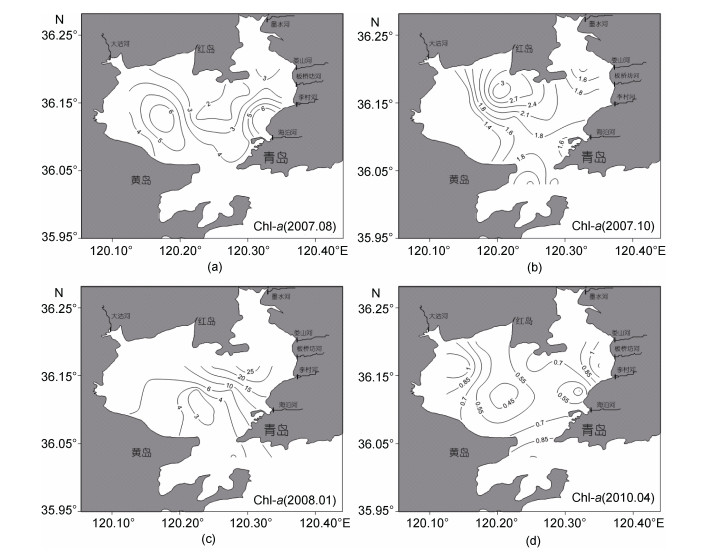 |
| 图 4 胶州湾夏季(a),秋季(b),冬季(c)和春季(d)表层海水Chl-a(μg/L)分布图 Fig. 4 Distributions of Chl-a(μg/L)in the sea surface in summer(a),autumn(b),winter(c)and spring(d) |
胶州湾DOC的季节变化为冬季最高(平均为7.432 mg/L),夏季最低(平均为1.746 mg/L),秋季(平均为5.512 mg/L)高于春季(平均为2.398 mg/L)(图 5)。冬季,正是硅藻大量繁殖的时期,胶州湾内迅速增长繁殖的硅藻生成并释放大量糖类等有机物质(姚云等,2007),这可能是导致冬季海水中具有最高DOC含量的原因之一; 夏季,虽然陆地径流会带来大量的有机碳,但是降水和河流输入也会起到稀释作用,同时生物呼吸作用和生物分解也会消耗大量的有机碳,从而使夏季含量较低。在水平分布上,夏季呈现出由湾东北部和西部及中部地区向湾口递减的趋势,秋季呈现出从湾西北部和湾东部近岸向湾中部递减的趋势,冬季呈现出由湾北部地区向湾中部地区递减的趋势,DOC浓度的最高值出现在李村河河口附近B5站位,最低值出现在C4站位,春季呈现出由湾东北部和湾北部向湾口方向递减的趋势; 这与薛明(2014)在2007—2012年对胶州湾的研究中得出的结论基本一致。
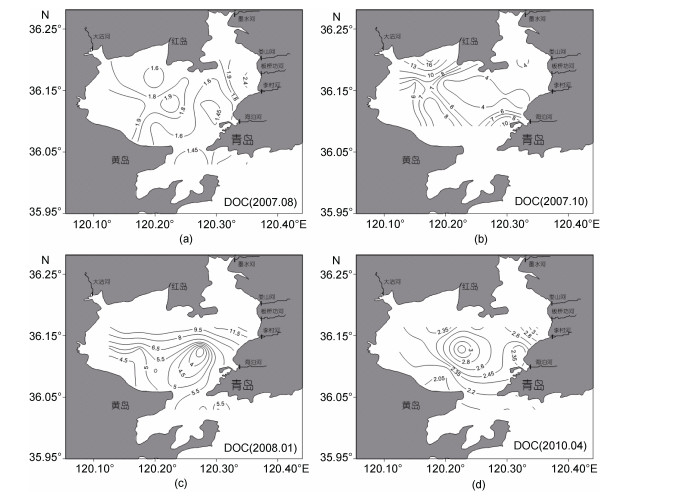 |
| 图 5 胶州湾夏季(a),秋季(b),冬季(c)和春季(d)表层海水DOC(mg/L)分布图 Fig. 5 Distributions of DOC(mg/L)in the sea surface in summer(a),autumn(b),winter(c)and spring(d) |
胶州湾夏、秋、冬和春季DIC范围分别为1949.2—2142.8、2075.9—2201.8、2060.7—2117.7和2128.0—2194.6 μmol/kg,平均分别为2067.1、2131.6、2091.9和2160.1 μmol/kg(图 6)。胶州湾表层海水DIC浓度的分布趋势为: 夏季由湾西部向湾东北部呈递增趋势,秋季由湾口向湾西部呈递增趋势,冬季由湾东部向湾西部呈递增趋势,春季由湾口向湾东北部呈递增趋势。
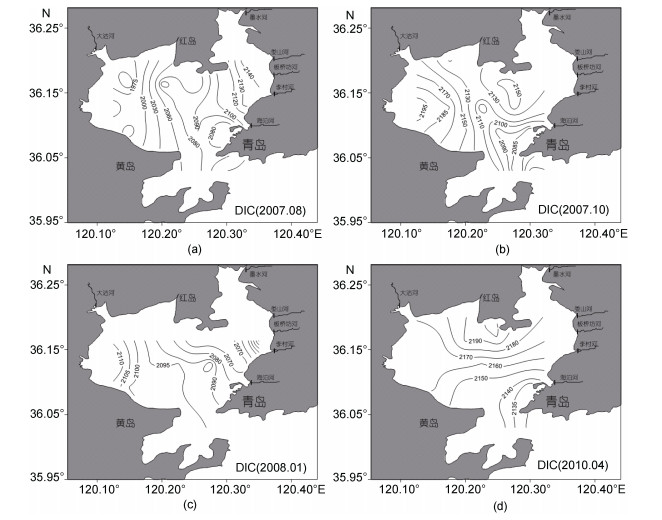 |
| 图 6 夏季(a),秋季(b),冬季(c)和春季(d)表层海水DIC(μmol/kg)分布图 Fig. 6 Distributions of DIC(μmol/kg)in the sea surface in summer(a),autumn(b),winter(c)and spring(d) |
胶州湾夏、秋、冬和春季Alk范围分别为2033.9— 2312.6、2209.0—2310.9、2248.1—2331.9和2312.9— 2382.5 μmol/kg,平均分别为2163.1、2254.3、2265.3和2354.5 μmol/kg(图 7)。胶州湾表层海水Alk浓度的分布趋势为: 夏季由湾西向湾东北部呈递增趋势,秋季由湾口向湾西部呈递增趋势,冬季由湾口向湾北部呈递增趋势,春季由湾口及湾西部向湾北部呈递增趋势。
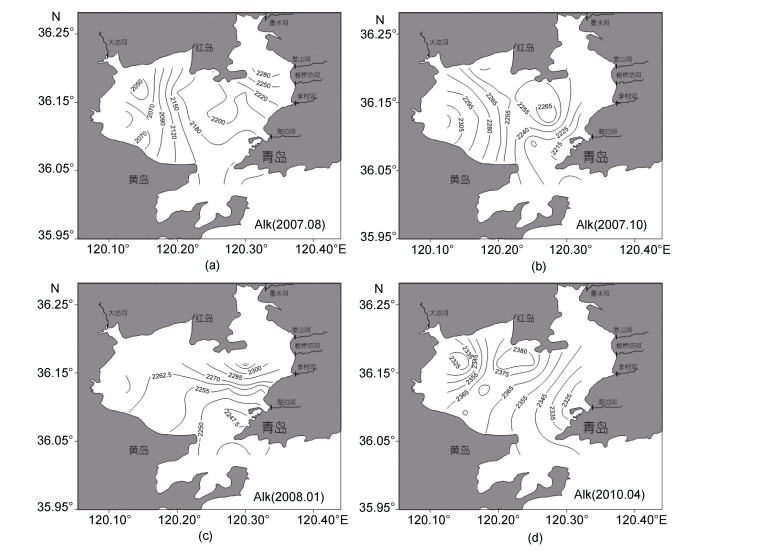 |
| 图 7 胶州湾夏季(a),秋季(b),冬季(c)和春季(d)表层海水Alk(μmol/kg)分布图 Fig. 7 Distributions of Alk(μmol/kg)in the sea surface in summer(a),autumn(b),winter(c)and spring(d) |
胶州湾夏、秋、冬和春季pH范围分别为7.89—7.98,8.00—8.06,7.92—8.30和7.77—8.02,平均分别为7.94,8.03,8.09和7.90(图 8)。胶州湾表层海水pH的分布趋势为: 夏季由湾口及东部近岸向湾西部方向呈递减趋势,秋季由湾西南地区向东北方向呈递减趋势,冬季由湾口向内陆方向呈递增趋势,春季由湾口向内陆地区呈递减趋势。
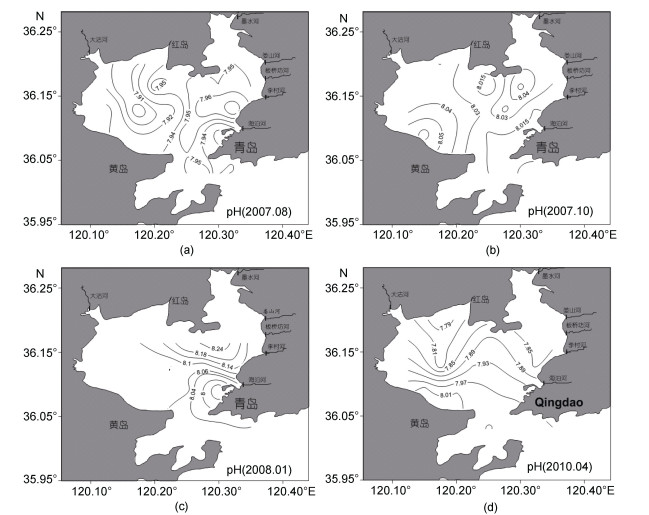 |
| 图 8 夏季(a),秋季(b),冬季(c)和春季(d)表层海水pH分布图 Fig. 8 Distributions of pH in the sea surface in summer(a),autumn(b),winter(c)and spring(d) |
胶州湾夏、秋、冬和春季pCO2范围为604.6— 745.3、413.0—474.5、89.9—283.4和316.3—587.7 μatm,平均分别为673.6、440.5、186.9和436.9 μatm(图 9)。胶州湾表层海水pCO2的分布趋势为: 夏季由湾口向内陆近岸呈递增趋势,秋季由湾西部向湾东北部呈递增趋势,冬季由湾西部和东北部向湾口呈递增趋势,春季由湾口向湾北部呈递增趋势。根据IPCC第五次报告(IPCC,2013)中公布的全球大气中pCO2值为390 μatm的标准,总体上而言胶州湾夏季为大气CO2的强源区,冬季为大气CO2的汇区,秋季和春季为大气CO2的弱源区。
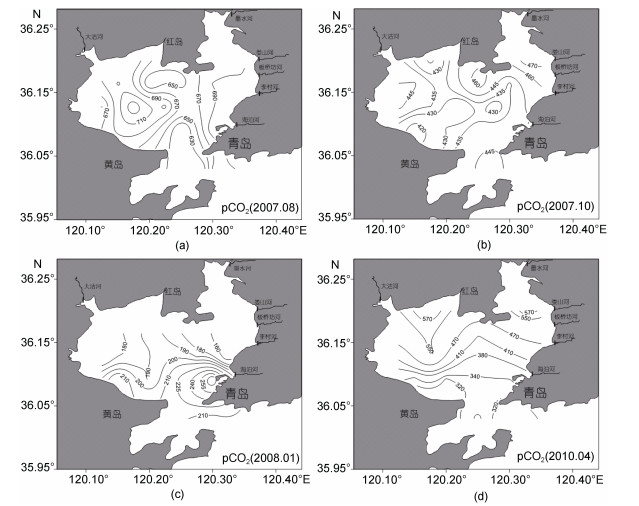 |
| 图 9 胶州湾夏季(a),秋季(b),冬季(c)和春季(d)表层海水pCO2(μatm)分布 Fig. 9 Distributions of pCO2(μatm)in the sea surface in summer(a),autumn(b),winter(c)and spring(d) |
胶州湾表层海水的DIC和Alk均呈现出明显的季节变化,且分布特征基本一致: 春季最高,夏季最低,秋冬季相差不大。这与刘辉等(1998)于1995— 1996年胶州湾总二氧化碳的季节变化规律是基本一致的。从图 6中DIC分布趋势来看,DIC浓度的最高值主要位于李村河口附近和湾西部地区,这可能是由于李村河口以及湾东北部沿岸地区工业较为发达、 人口较为密集,有大量的生活污水和工业废水通过河流输入胶州湾内所造成的,并且沿岸海域的海水的交换和流动能力较弱(赵亮等,2002; Liu et al,2004),污染物在水体中的扩散速度较慢,从而导致该海域的DIC浓度较大; 而湾西部海域人工养殖区众多,养殖区排放的大量废水导致了较多的有机物质进入胶州湾内,进而分解和再矿化成无机碳酸盐等物质,最后使得该海域附近的DIC浓度比其它海域高(白洁等,2004; Yates et al,2007); 由图 7也可看出,Alk的变化规律与DIC基本一致。
DIC/S(归一化DIC)以及Alk/S(归一化Alk)与盐度均呈现出较强的负相关性(图 10),表明了受陆地径流输入影响的水体在盐度降低的同时碳酸盐的比例升高(高彩霞等,2014); 图中不同季节有不同的斜率,表明陆地径流在不同季节的影响程度不同; 同时少雨季节表层水的大量蒸发,会导致表层水的DIC和Alk略微升高,而降水和陆地径流往往使海水DIC和Alk降低(隋永年,1986a)。这与张正斌等(2008)根据2006年4月对黄海的研究中得出的DIC与盐度呈负相关的结论一致。
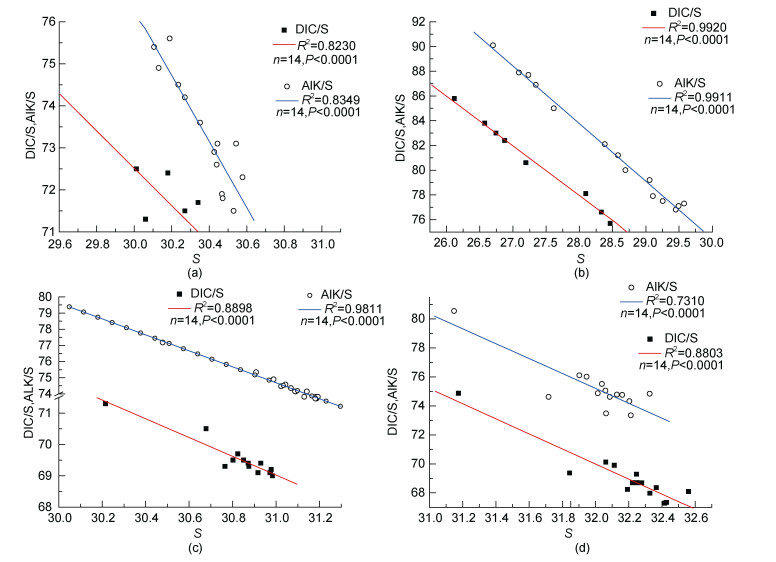 |
| 图 10 夏季(a),秋季(b),冬季(c)和春季(d)DIC/S和S以及Alk/S和S的关系图 Fig. 10 DIC/S vs. salinity and Alk/S vs. salinity in summer(a),autumn(b),winter(c)and spring(d) |
从温度对碳酸盐体系平衡的影响来看,温度的增加会引起pCO2值升高(Takahashi et al,1993),然而CO2的溶解度会随温度的升高而降低。因此,温度对海水中的pCO2的分布有着正负两方面的影响。图 9也显示了pCO2的季节变化特征,即夏季最高,冬季最低,春秋季相差不大。这说明在季节分布上,温度是影响pCO2分布的主要因素之一。然而对于每个季节而言,海水温度变化范围均较小(夏季<3℃,秋季<3℃,冬季<7℃,春季<3℃),因此对pCO2的影响并不大,本文利用Takahashi等(1993)温度对pCO2的校正公式将春、夏、秋、冬四个季节的pCO2分别校正到相应的平均温度后得到npCO2,然而发现校正之后的npCO2的分布趋势并没有发生较大的变化。为了剔除每个季节中的温度对pCO2所产生的影响,在探究和分析其它过程对pCO2的影响时均使用npCO2(Zhang et al,2012)。在近岸海域,由于陆源输入和人类活动等影响,有机物污染比较严重,有机物的降解对于pCO2分布的影响不可忽略,如图 11所示,npCO2与DOC有较为明显的正相关性,这说明有机物的降解造成了胶州湾pCO2的升高(刘启珍等,2010),特别是在湾东部及东北部地区的工业化较为发达的地区影响更为显著,DOC分布的高值区正好与pCO2的分布高值区相对应。
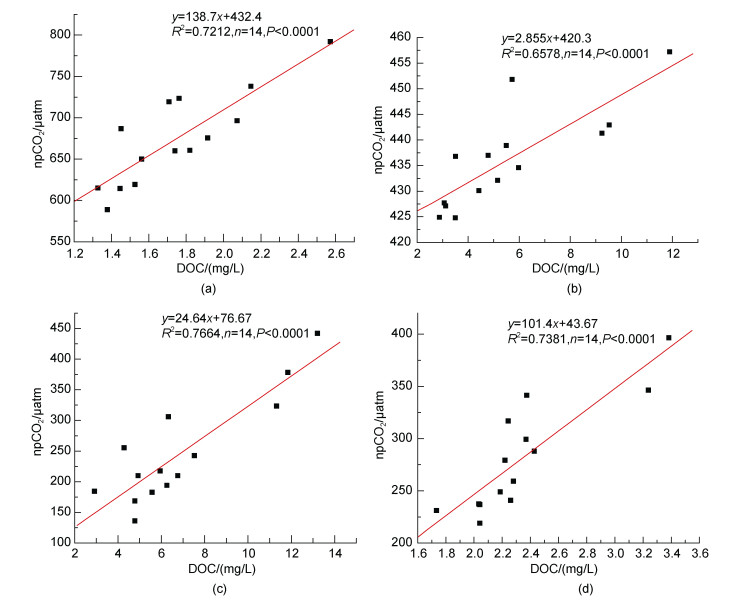 |
| 图 11 夏季(a),秋季(b),冬季(c)和春季(d)npCO2与DOC的关系图 Fig. 11 Correlation of npCO2 with DOC in summer(a),autumn(b),winter(c)and spring(d) |
4月份胶州湾西北部和东北部近岸海域呈现高pCO2高Chl-a的分布特征,而湾中部至湾口海域呈现出低pCO2低Chl-a的分布特征。这与龚信宝(2014)在胶州湾的研究结论是一致的,类似的情况在南黄海也有,Zhang等(2010)在南黄海春末的研究中发现pCO2与Chl-a呈现正相关,且中部海域具有低pCO2低Chl-a的特征。产生这种分布的原因可能是陆源输入带来了大量的营养盐,从而促进了近岸海域中浮游植物的生长和繁殖,而且污水输入、海水养殖等均会带来大量的易降解有机物,加剧了湾内浮游植物及底层沉积物的好氧呼吸,并且通过海水的垂直混合过程使得表层海水拥有较高的pCO2值(龚信宝等,2015)。而湾口及湾中部海域由于受陆源污染程度较小,水质较好,好氧呼吸作用对CO2的贡献不明显,并且与黄海水交换作用明显,从而呈现出湾中部和湾口海域pCO2值最低的分布特征,而此处海域Chl-a值偏低,大多是因为浮游动物摄食对浮游植物的种类和数量产生了较为明显的影响(于庆云等,2009)。
3.3 pH的季节变化及其影响因素pH在季节上的变化规律为: 冬季最高,春季最低,秋季高于夏季。胶州湾全年平均温度为15.23℃,平均pH为7.99,各季节的平均pH与平均温度有一定的负相关性(图 12); 胶州湾海水平均pH值略低于大洋水的主要原因是: 胶州湾三面被青岛市所包围,受人类活动、陆源输入的影响较为显著,特别是东部沿岸B5、D4等站位,大量的排污水经李村河、海泊河进入湾内,从而降低了pH值(刘启珍等,2010)。影响海水pH的主要因素是海水无机碳体系与生物活动,而海水无机碳体系主要是通过温度的变化来改变电离常数的,温度升高使电离常数变大,导致海水pH值降低(隋永年,1986b)。冬季,由于Chl-a含量为全年最高值,因此浮游植物的光合作用吸收海水中溶解的CO2使pH值升高(杨斌等,2012),冬季水温最低也使pH值升高,因此生物活动和温度的协同作用使冬季pH具有最高值; 春季,Chl-a值为全年最低值,光合作用最弱,而生物活动和温度的拮抗作用使春季pH具有最低值,说明该季节生物活动为主导因素; 夏季水温高于全年平均值,Chl-a含量为全年的次高峰值,光合作用较强,降水和陆源输入较为明显,使得夏季pH略低于全年pH平均值,说明该季节温度和淡水输入为主导因素; 秋季水温略高于全年平均值,Chl-a值高于春季,而秋季pH略高于全年pH平均值,说明该季节生物活动为主导因素。
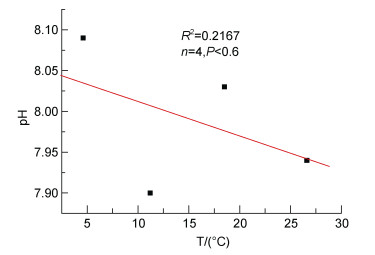 |
| 图 12 各季节平均pH和温度的关系图 Fig. 12 Relationships between average pH and temperature in all seasons |
本研究主要分析了胶州湾无机碳体系pH、DIC、Alk和pCO2四个参数的分布特征、季节变化以及Chl-a、DOC、温度、盐度等相关参数的影响。研究表明,以上参数在时空分布上有明显的季节变化。pH在温度、生物活动和淡水输入的影响下,最终表现为冬季高,春季低; DIC和Alk在陆源输入、人类活动和有机物再矿化作用下,均表现为春季高,夏季低; pCO2在有机物降解和生物活动的作用下,表现为夏季高、冬季低,胶州湾总体上表现为夏季为CO2的强源区,春秋季为CO2的弱源区,冬季为CO2的汇区。在水平方向上,由于沿岸的养殖区、工业区及生活区 的废水、污水的排放,加上胶州湾的半封闭性和湾内较弱的水动力条件使得湾东部、东北部和西部地区存在着多个参数的高值区,这对于胶州湾碳酸盐体系有着很大的影响。同时,从季节尺度上来看,陆地径流和温度以及浮游植物等生物的呼吸、光合作用也对胶州湾碳酸盐体系产生了一定的影响。
| 于庆云,唐学玺,杜恩在等,2009.胶州湾Chl a周年时空分布特征及与环境因子变化的相关性.中国海洋大学学报, 39(S1):120-126 |
| 白洁,张昊飞,李岿然等,2004.胶州湾冬季异养细菌与营养盐分布特征及关系研究.海洋科学, 28(12):31-34 |
| 刘辉,姬泓巍,辛梅,1998.胶州湾水体中的二氧化碳体系.海洋科学, (6):44-47 |
| 刘启珍,张龙军,薛明,2010.胶州湾秋季表层海水pCO2分布及水-气界面通量.中国海洋大学学报, 40(10):127-132 |
| 李超伦,张芳,申欣等,2005.胶州湾叶绿素的浓度、分布特征及其周年变化.海洋与湖沼, 36(6):499-506 |
| 杨斌,张晨晓,钟秋平等,2012.钦州湾表层海水温度盐度及pH值时空变化.钦州学院学报, 27(3):1-5 |
| 吴玉霖,张松,张永山,2004.胶州湾浮游植物数量长期动态变化的研究.海洋与湖沼, 35(6):518-523 |
| 沈志良,刘明星,1997.胶州湾海水中二氧化碳的研究.海洋学报, 19(2):115-120 |
| 宋金明,2011.中国近海生态系统碳循环与生物固碳.中国水产科学, 18(3):703-711 |
| 张正斌,张闯,刘莲生等,2008.黄海春季表面海水溶解无机碳的分层研究.海洋科学, 32(11):36-43 |
| 赵亮,魏皓,赵建中,2002.胶州湾水交换的数值研究.海洋与湖沼, 33(1):23-29 |
| 姚云,郑世清,沈志良,2007.胶州湾营养盐及富营养化特征.海洋通报, 26(4):91-98 |
| 高彩霞,刘春颖,李铁等,2014.青岛近海碱度的研究及其测定方法的比较.中国海洋大学学报, 44(3):64-70 |
| 龚信宝,2014.春季胶州湾和桑沟湾表层海水pCO2分布及影响因素分析.青岛:中国海洋大学硕士学位论文, 23-28 |
| 龚信宝,韩萍,张龙军等,2015.胶州湾春季4月份表层海水pCO2分布及控制因素分析.中国海洋大学学报, 45(4):95-102 |
| 隋永年,1986a.第三节:海水总碱度及其示性特征.山东海洋学院学报, (1):160-172 |
| 隋永年,1986b.第二节:海水pH及其影响因素.山东海洋学院学报, (1):146-159 |
| 薛明,2014.胶州湾海-气CO2通量及其控制.青岛:中国海洋大学博士学位论文, 51-56 |
| Dickson A G, Millero F J,1987. A comparison of the equilibrium constants for the dissociation of carbonic acid in seawater media. Deep Sea Res Part A, 34(10):1733-1743 |
| Gao Z H, Yang D F, Qin J et al,2008. The land-sourced pollution in the Jiaozhou Bay. Chin J Oceanol Limnol, 26(2):229-232 |
| IPCC,2013. http://www.ipcc.ch/pdf/assessment-report/ar5/syr/AR5_SYR_FINAL_SPM.pdf |
| Lewis E, Wallace D W R,1998. Program developed for CO2 system calculations. ORNL/CDIAC-105. Tennessee:Oak Ridge National Laboratory |
| Liu Z, Wei H, Liu G S et al,2004. Simulation of water exchange in Jiaozhou Bay by average residence time approach. Estuarine, Coastal Shelf Sci, 61(1):25-35 |
| Longhurst A, Sathyendranath S, Platt T et al,1995. An estimate of global primary production in the Ocean from satellite radiometer data. J Plankton Res, 17(6):1245-1271 |
| Mehrbach C, Culberson C H, Hawley J E et al,1973. Measurement of the apparent dissociation constants of carbonic acid in seawater at atmospheric pressure. Limnol Oceanogr, 18(6):897-907 |
| Takahashi T, Olafsson J, Goddard J G et al,1993. Seasonal variation of CO2 and nutrients in the high-latitude surface oceans:a comparative study. Global Biogeochem Cycles, 7(4):843-878 |
| Walsh J J,1988. On the Nature of Continental Shelves. New York:Academic Press, 520 |
| Yang G P, Zhang Y P, Lu X L et al,2010. Distributions and seasonal variations of dissolved carbohydrates in the Jiaozhou Bay, China. Estuarine, Coastal Shelf Sci, 88(1):12-20 |
| Yates K K, Dufore C, Smiley N et al,2007. Diurnal variation of oxygen and carbonate system parameters in Tampa Bay and Florida Bay. Mar Chem, 104(1-2):110-124 |
| Zhang L J, Xue L, Song M Q et al,2010. Distribution of the surface partial pressure of CO2 in the southern Yellow Sea and its controls. Continental Shelf Research, 30(3-4):293-304 |
| Zhang L J, Xue M, Liu Q Z,2012. Distribution and seasonal variation in the partial pressure of CO2 during autumn and winter in Jiaozhou Bay, a region of high urbanization. Mar Poll Bull, 64(1):56-65 |
 2016, Vol. 47
2016, Vol. 47


