文章信息
- 刘西汉, 石雅君, 姜会超, 田海兰, 程林, 王红, 王艳霞. 2021.
- LIU Xi-han, SHI Ya-jun, JIANG Hui-chao, TIAN Hai-lan, CHENG Lin, WANG Hong, WANG Yan-xia. 2021.
- 曹妃甸邻近海域浮游动物群落时空变化及其影响因素
- Spatial and temporal variations of zooplankton community and their influential factors in Caofeidian coastal waters
- 海洋科学, 45(4): 114-125
- Marine Sciences, 45(4): 114-125.
- http://dx.doi.org/10.11759/hykx20200601004
-
文章历史
- 收稿日期:2020-06-01
- 修回日期:2020-10-26
2. 中国科学院 烟台海岸带研究所, 山东 烟台 264003;
3. 山东省海洋资源与环境研究院, 山东 烟台 264006;
4. 邯郸市恒达地理信息工程有限责任公司, 河北 邯郸 056011
2. Yantai Institute of Coastal Zone Research, Chinese Academy of Sciences, Yantai 264003, China;
3. Shandong Marine Resource and Environment Research Institute, Yantai 264006, China;
4. Handan Hengda Geographic Information Engineering Co., Ltd., Handan 056011, China
曹妃甸邻近海域位于渤海湾北部, 受到陆源因素和渤海中部冷流的共同影响, 环境因子、初级生产力等特征具有明显的空间差异[1-2]。东侧龙岛附近分布着中国面积最大的鳗草(Zostera marina)海草床, 总面积高达29.17 km2[3], 是鱼类、贝类等多种海洋经济生物的栖息地[4]。近年来, 曹妃甸地区工业、港口和航运等产业发展迅速, 尤其在2004~2011年间实施了大规模围填海工程, 累计填海面积达到274.7 km2[5]。强烈的人类活动干扰使得附近海域的水动力环境、水质、浮游生物和底栖生物等均受到了负面影响[6], 海草床出现明显退化[4], 生态系统健康和渔业资源的可持续发展受到了严重威胁[7]。
浮游动物作为食物链的关键环节, 一方面通过摄食浮游植物进行生长和繁殖, 另一方面是鱼虾蟹类的重要饵料, 与渔业资源的盛衰密切相关, 对海洋生态系统功能和稳定具有重要意义[8]。目前, 曹妃甸邻近海域开展的浮游动物群落研究仅限于间隔较久的几次海洋综合调查以及近年来开展的部分针对性研究[9-11]。王红等[9]利用20世纪50年代~21世纪初期的4次调查资料, 分析了浮游动物群落的长期变化特征。李志伟等[10]在曹妃甸及其附近的乐亭和三岛海域开展航次, 分析了环境因子对浮游动物群落的驱动作用。梁淼等[11]对浮游动物优势种的生态位宽度和重叠程度进行了研究。然而, 曹妃甸邻近海域浮游动物群落的时空变化特征还缺乏深入研究, 尤其缺乏结合围填海前调查资料对浮游动物群落变化的分析。本研究利用2013年8月和2014年5月围绕曹妃甸邻近海域的两次调查资料, 主要研究浮游动物群落的时空变化特征, 分析其与环境因子之间的关系, 并根据围填海前调查资料, 对比分析浮游动物群落在围填海前后的变化。研究结果可进一步阐明曹妃甸邻近海域在围填海后的浮游动物群落特征, 加深认识围填海工程对生态环境的影响, 为生态系统综合管理和补偿性环境整治提供科学依据。
1 材料与方法 1.1 研究区域与站位布设本研究先后于2013年8月22至24日(夏季)和2014年5月19至21日(春季)在曹妃甸邻近海域(118.32°E~118.94°E, 38.74°N~39.12°N)开展2个调查航次, 布设A、B、C和D共4个调查断面, 分别代表曹妃甸西侧、南侧、东侧和东北侧内湾海域, 其中每个断面布设2~3个站位(图 1)。
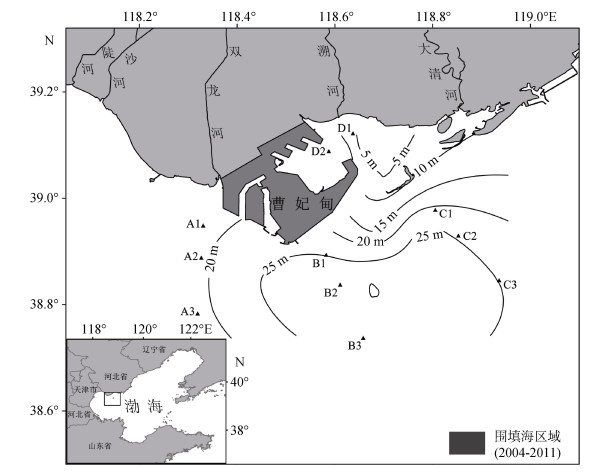 |
| 图 1 曹妃甸邻近海域水深及调查站位 Fig. 1 Bathymetry and sampling sites in Caofeidian coastal waters |
海水和浮游动物样品的采集和分析过程均按照《海洋调查规范》[12, 13]进行。海水温度、盐度、悬浮颗粒物(Suspended Particulate Matter, SPM)、溶解无机氮(Dissolved Inorganic Nitrogen, DIN)、溶解磷酸盐(Dissolved Inorganic Phosphorus, DIP)、溶解硅酸盐(Dissolved Silicate, DSi)和叶绿素a(Chlorophyll a, Chl-a)的测定过程见文献[14]。浮游动物样品采用浅水Ⅱ型浮游生物网(网目孔径0.160 mm, 网口内径31.6 cm, 网口面积0.08 m2, 网长140 cm)自海底至海表垂直拖取, 加入甲醛溶液进行固定(终浓度为5%), 滤水体积由网口流量计进行记录。浮游动物样品经稀释后在显微镜下进行物种鉴定, 浮游幼体鉴定到类, 其他种类鉴定到种。根据滤水体积计算浮游动物丰度(个/m3), 经滤纸吸干水分后采用电子天平称量湿质量生物量(mg/m3)。
1.3 数据处理及统计分析浮游动物多样性采用Shannon-Wiener多样性指数(H′)[15]和Pielou均匀度指数(J)[16]进行计算, 其计算公式分别为:
| $H' = - \sum\limits_{i = 1}^S {{P_i} \times {{\log }_2}} {P_i},$ | (1) |
| $J = \frac{{H'}}{{{{\log }_2}S}}.$ | (2) |
通过计算优势度指数(Y)判断浮游动物优势种(Y > 0.02), 其计算公式为:
| $Y = \frac{{{n_i} \times {f_i}}}{N},$ | (3) |
式中: N为调查海域浮游动物总丰度, S为该站位的种类数, ni为第i种的丰度, fi为该物种在站位中的出现频率, Pi为第i种的丰度与浮游动物总丰度的比值。
浮游动物丰度、生物量、优势种和多样性的空间分布图采用Surfer 12.0进行绘制。筛选出现频率大于20%的物种, 在R软件(The R Package, 3.3.3)中采用vegan包[17]进行冗余分析(Redundancy Analysis, RDA), 用于研究浮游动物群落与环境因子之间的关系, 物种名缩写如后文所示。围填海前调查资料采用2004年实施的河北省第二次海岸带资源调查[18]。受数据可用性限制, 本研究主要对浮游动物丰度和优势种进行对比。
2 结果 2.1 种类组成如表 1所示, 本次调查共鉴定得到浮游动物31种(类), 分别属于水螅水母类、栉水母类、枝角类、桡足类、糠虾类、毛颚类、被囊类和浮游幼体共8个类群, 其中桡足类物种数量最多, 鉴定得到13种, 占总种类数的45.2%, 其次为浮游幼体, 鉴定得到8类, 占总种类数的25.8%, 其他种类的数量相对较少。春季为25种(类), 以桡足类为主, 夏季为23种(类), 以桡足类和浮游幼体为主。
| 门类 | 类群 | 春季 | 夏季 | 总计 | |||||||
| 种类数(类) | 比例(%) | 种类数(类) | 比例(%) | 种类数(类) | 比例(%) | ||||||
| 刺胞动物门 | 水螅水母类 | 3 | 12.0 | 3 | 13.0 | 4 | 12.9 | ||||
| 栉水母动物门 | 栉水母类 | 1 | 4.0 | - | - | 1 | 3.2 | ||||
| 节肢动物门 | 枝角类 | - | - | 1 | 4.3 | 1 | 3.2 | ||||
| 桡足类 | 13 | 52.0 | 8 | 34.8 | 14 | 45.2 | |||||
| 糠虾类 | 1 | 4.0 | 1 | 4.3 | 1 | 3.2 | |||||
| 毛颚动物门 | 毛颚类 | 1 | 4.0 | 1 | 4.3 | 1 | 3.2 | ||||
| 脊索动物门 | 被囊类 | 1 | 4.0 | 1 | 4.3 | 1 | 3.2 | ||||
| 浮游幼体 | 5 | 20.0 | 8 | 34.8 | 8 | 25.8 | |||||
| 合计 | 25 | 100.0 | 23 | 100.0 | 31 | 100.0 | |||||
| 注: “-”表示该类群未出现 | |||||||||||
春季, 研究海域浮游动物平均丰度为(1 1801.5± 5 017.9)个/m3, 主要呈现为近岸高、远岸低的空间分布特征, 曹妃甸东西两侧近岸海域的浮游动物丰度基本均在10 000.0个/m3以上, 远岸海域则呈现西侧高、东侧低的空间分布特征, 曹妃甸甸头及东南侧海域的浮游动物丰度普遍在10 000.0个/m3以下(图 2a)。夏季, 浮游动物平均丰度较春季略低, 为(8 726.7±8 032.0)个/m3, 主要呈现为近岸低、远岸高的分布特征, 近岸海域的浮游动物丰度通常不超过4 000.0个/m3, 远岸海域的浮游动物丰度则可达20 000.0个/m3(图 2b)。
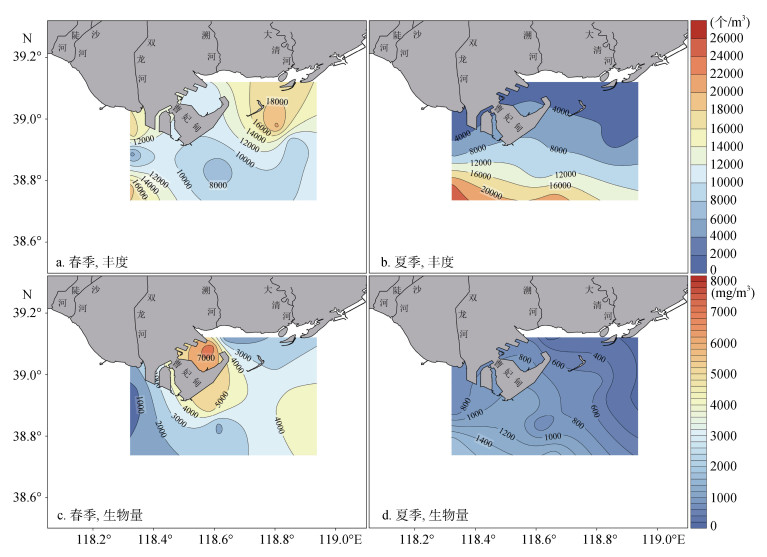 |
| 图 2 浮游动物丰度和生物量的空间分布 Fig. 2 Spatial distribution of zooplankton abundance and biomass |
春季, 浮游动物平均生物量为(3 057.9±2 341.0)个/m3, 空间分布与丰度存在明显差异, 高值区主要出现在D2、B1以及C断面, 生物量普遍超过3 000.0 mg/m3(图 2c)。夏季, 浮游动物生物量显著低于春季, 平均值为(772.2±514.8)mg/m3, 空间分布与丰度较为相似, 基本为近岸低、远岸高的分布特征, 近岸海域生物量在(200.0~800.0)mg/m3范围内, 远岸海域生物量可达1 400.0 mg/m3(图 2d)。
2.3 优势种春季, 浮游动物优势种包括双刺纺锤水蚤(Acartia bifilosa)、小拟哲水蚤(Paracalanus parvus)、桡足类幼体(Copepodid larva)和拟长腹剑水蚤(Oithona similis), 其中双刺纺锤水蚤的优势度最高, 达到0.633, 其次为小拟哲水蚤, 优势度为0.147 (表 2), 均主要分布在近岸海域(图 3a, 3b)。夏季, 浮游动物优势种除包括上述4个种类外, 还包括强壮箭虫(Sagitta crassa)、近缘大眼剑水蚤(Corycaeus affinis)、海蛇尾长腕幼体(Ophiuroidea larva), 其中小拟哲水蚤是最主要的优势种, 优势度达到0.499, 主要分布在远岸海域(图 3d), 其次为双刺纺锤水蚤和桡足类幼体, 优势度均为0.027, 其他优势种优势度相对较低(表 2)。
| 种类名 | 缩略词 | 春季 | 夏季 | ||||||
| fi(%) | Y | fi(%) | Y | ||||||
| 强壮箭虫(Sagitta crassa) | SCRA | 100.0 | 0.004 | 100.0 | 0.031 | ||||
| 异体住囊虫(Oikopleura dioica) | ODIO | 36.4 | 0.001 | 45.5 | 0.012 | ||||
| 小拟哲水蚤(Paracalanus parvus) | PPAR | 100.0 | 0.147 | 100.0 | 0.499 | ||||
| 双刺纺锤水蚤(Acartia bifilosa) | ABIF | 100.0 | 0.633 | 100.0 | 0.127 | ||||
| 真刺唇角水蚤(Labidocera euchaeta) | LEUC | 63.6 | 0.000 | ||||||
| 圆唇角水蚤(Labidocera rotunda) | LROT | 72.7 | 0.000 | ||||||
| 近缘大眼剑水蚤(Corycaeus affinis) | CAFF | 72.7 | 0.006 | 81.8 | 0.029 | ||||
| 强额拟哲水蚤(Parvocalanus crassirostris) | PCRA | 90.9 | 0.009 | 81.8 | 0.007 | ||||
| 拟长腹剑水蚤(Oithona similis) | OSIM | 100.0 | 0.070 | 90.9 | 0.027 | ||||
| 中华哲水蚤(Calanus sinicus) | CSIN | 100.0 | 0.009 | 63.6 | 0.005 | ||||
| 太平洋纺锤水蚤(Acartia pacifica) | APAC | 27.3 | 0.000 | ||||||
| 鸟喙尖头溞(Penilia avirostris) | PAVI | 36.4 | 0.001 | ||||||
| 汤氏长足水蚤(Calanopia thompsoni) | CTHO | 27.3 | 0.000 | ||||||
| 猛水蚤(Microsetella sp.) | MISP | 36.4 | 0.002 | ||||||
| 短角长腹剑水蚤(Oithona brevicornis) | OBRE | 90.9 | 0.019 | 27.3 | 0.001 | ||||
| 糠虾(Mysidacea) | MYSI | 45.5 | 0.000 | 36.4 | 0.000 | ||||
| 桡足类幼体(Copepodid) | COPL | 72.7 | 0.044 | 100.0 | 0.127 | ||||
| 双壳类幼体(Bivalvia) | BIVL | 36.4 | 0.004 | 100.0 | 0.014 | ||||
| 海蛇尾长腕幼体(Ophiuroidea) | OPHL | 72.7 | 0.053 | ||||||
| 多毛类幼体(Polychaeta) | POLL | 27.3 | 0.001 | 100.0 | 0.004 | ||||
| 幼螺(Nail) | NAIL | 81.8 | 0.004 | ||||||
| 阿丽玛幼体(Squillidae alima) | SQUL | 45.5 | 0.000 | ||||||
| 短尾类幼体(Brachyura) | BRAL | 54.5 | 0.000 | ||||||
| 长尾类幼体(Maeruran) | MAEL | 27.3 | 0.001 | 90.9 | 0.003 | ||||
| 真拟杯水母(Phialucium mbengha) | PMBE | 45.5 | 0.000 | 45.5 | 0.001 | ||||
| 八斑芮氏水母(Rothkea octopunctata) | ROCT | 27.3 | 0.000 | ||||||
| 注: 仅显示出现频率高于 20%的种类; 优势种类用粗体显示 | |||||||||
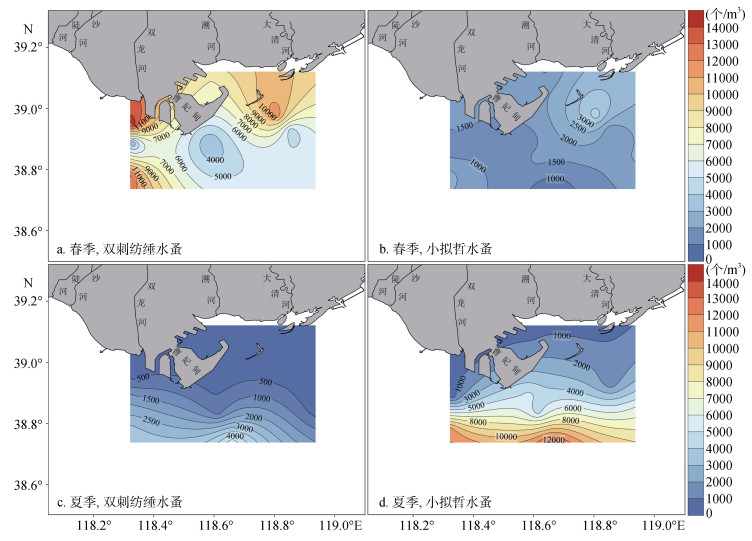 |
| 图 3 浮游动物优势种丰度的空间分布 Fig. 3 Spatial distribution of abundance of dominant zooplankton species |
春季, 多样性指数平均值为1.74±0.45, 从西北向东南海域逐渐升高, 甸头附近的B1站位出现多样性高值, 达到2.50(图 4a)。夏季的多样性指数高于春季, 平均值为2.32±0.46, 其空间分布与春季相反, 基本为从西北向东南海域逐渐降低(图 4b)。
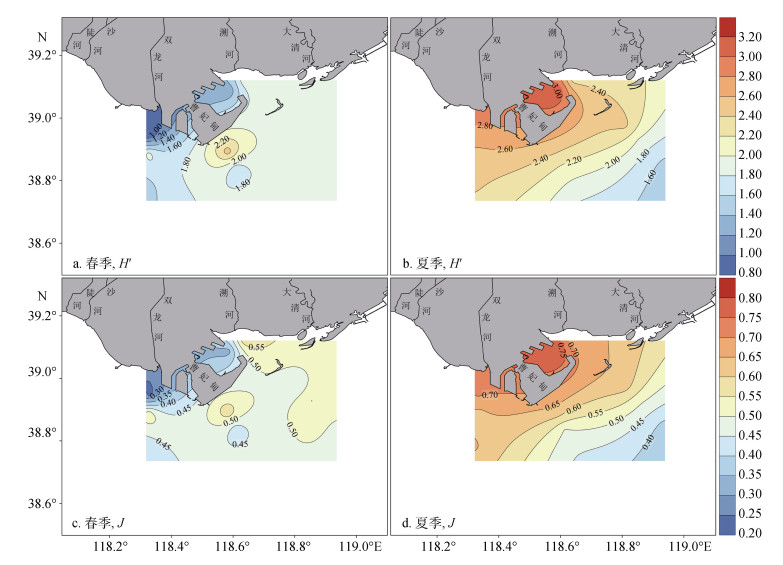 |
| 图 4 浮游动物群落多样性和均匀度指数的空间分布 Fig. 4 Spatial distribution of diversity and evenness index of the zooplankton community |
春季, 均匀度指数平均值为0.46±0.11, 空间分布与多样性指数较为相似, 西北侧海域是均匀度指数的低值区, 位于0.25~0.45范围内, 东侧海域的均匀度指数相对较高, 通常在0.50以上(图 4c)。夏季, 均匀度指数平均值为0.60±0.12, 空间分布与多样性指数基本相同, 从西北向东南海域逐渐降低(图 4d)。
2.5 RDA分析温度、盐度和Chl-a等环境因子对浮游动物群落的时空变化具有重要影响。春季, 桡足类通常与温度、盐度和Chl-a具有正相关关系, 其中双刺纺锤水蚤、小拟哲水蚤和拟长腹剑水蚤等优势种主要与Chl-a正相关, 中华哲水蚤、近缘大眼剑水蚤和强额拟哲水蚤等种类与温度正相关, 桡足类幼体、双壳类幼体与Chl-a负相关, 水母类则与SPM为负相关(图 5a)。夏季, 小拟哲水蚤、双刺纺锤水蚤和近缘大眼剑水蚤等主要的桡足类优势种均与温度具有明显的负相关关系, 同时与盐度正相关, 短角长腹剑水蚤等少数种类与Chl-a正相关, 浮游幼体多与营养盐具有正相关关系(图 5b)。
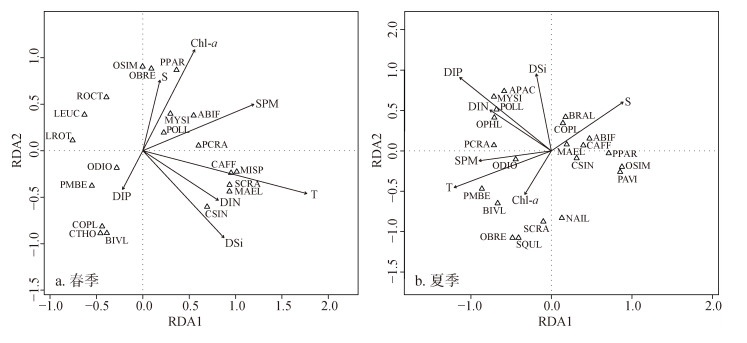 |
| 图 5 浮游动物群落与环境因子的冗余分析 Fig. 5 Redundancy analysis (RDA) ordination between the zooplankton community and its environmental factors |
本次调查两个季节的浮游动物种类数量基本一致, 但丰度、生物量和优势种等存在明显的季节差异。对于渤海而言, 浮游动物丰度的年度高峰主要出现在春季, 春季可超过夏季的数倍甚至数十倍, 与春季水华期间浮游植物的大量增殖为浮游动物提供了充足饵料有关, 另一个高峰则可能出现在夏季或秋季[19-22]。本研究中, 浮游动物丰度的季节变化也表现为春季高于夏季, 春季丰度为夏季的1.35倍(图 2)。然而, 同期浮游植物调查资料表明春季浮游植物丰度为4.8×104个/m3, 远低于夏季的704.3×104个/m3[23], 表明春季浮游植物可能已经度过春华高峰期, 其丰度在浮游动物摄食作用的强烈影响下出现明显下降, 并且使得浮游动物丰度也有所降低, 而夏季浮游植物增殖较快, 有利于浮游动物的摄食和生长, 尤其夏季浮游幼体较多(表 2), 表明夏季可能即将产生一个浮游动物丰度高峰。从浮游动物生物量来看, 春季生物量显著高于夏季(图 2), 主要是与春季出现了较多八斑芮氏水母有关(表 2)。八斑芮氏水母偏向于低温水体, 通常在冬、春季出现数量高峰[24]。从优势种的季节变化来看, 春季优势度最高的物种为双刺纺锤水蚤, 其次为小拟哲水蚤, 而夏季浮游动物优势种则相反, 小拟哲水蚤优势度最高, 其次为双刺纺锤水蚤和桡足类幼体。胶州湾、渤海的多项研究表明双刺纺锤水蚤通常在春季成为优势种, 水温高于20 ℃则不利于该物种的繁殖和发育[22, 24-26]。本次调查期间, 春季水温(14.32±1.50 ℃)[14]较低, 适宜双刺纺锤水蚤生长, 夏季水温(21.60±3.51 ℃)[14]高于20 ℃, 使得其优势度明显降低。小拟哲水蚤通常与水温正相关, 在7~10月的丰度较高[27], 在本次调查中即表现为夏季优势度进一步升高, 成为夏季最主要的优势种。
3.2 浮游动物群落的空间分布与环境因子的关系浮游动物群落的空间分布与环境因子之间存在紧密联系, 并且具有一定的季节差异。春季, 温度和Chl-a是影响浮游动物群落的主要环境因子。桡足类主要通过摄食浮游植物进行生长和繁殖[28], 在本研究中双刺纺锤水蚤、小拟哲水蚤和拟长腹剑水蚤等表现出与Chl-a浓度的正相关关系(图 5a)。异体住囊虫与桡足类之间存在较为强烈的竞争关系, 同时其卵和幼体可被桡足类摄食[29-30], 因此与Chl-a及大部分桡足类呈现负相关关系(图 5a)。水母类与SPM具有较为明显的负相关关系, 可能与较强光照可促进水母生殖[31]有关。中华哲水蚤偏向低温水体, 最适温度范围为13~18 ℃[32], 强壮箭虫的适温范围大致为10~20 ℃[33-34], 与本次春季调查期间的水温范围(12.95~17.30 ℃)[14]较为相似, 因此与水温呈正相关关系(图 5a)。
夏季, 温度是影响浮游动物群落空间分布的主要环境因子。夏季调查期间的水温范围为17.72~ 27.08 ℃[14], 近岸海域水温已接近甚至超过部分种类的适温上限[26-27, 35-36], 使得小拟哲水蚤、双刺纺锤水蚤、拟长腹剑水蚤和近缘大眼剑水蚤等优势度较高的桡足类主要分布在远岸海域, 表现为与温度负相关, 同时由于远岸海域受淡水输入的影响较弱, 这些种类通常与盐度正相关(图 5b)。异体住囊虫、水母类以及部分浮游动物幼体通常在夏季出现较高丰度[22, 37], 在本研究中也与水温呈现正相关关系。Chl-a对浮游动物空间分布的影响并不明显, 仅与短角长腹剑水蚤等少数种类具有正相关关系, 这与夏季浮游植物丰度较高[23]有关, 饵料不再是影响浮游动物生长的主要因素。营养盐的影响相对较弱, 与太平洋纺锤水蚤及部分幼体具有正相关关系, 可能与营养盐通过影响浮游植物生长对浮游动物产生间接影响有关[20]。
3.3 与历史调查资料的比较基于长期观测资料分析浮游生物群落的长期变化是海洋生态研究重点关注的科学问题之一[38]。自20世纪50年代以来, 曹妃甸邻近海域先后于1959、1984、1990和2004年开展了海洋综合调查, 采用浅水Ⅰ型网得到的浮游动物丰度和生物量呈波动增加趋势[9]。本次调查采用浅水Ⅱ型网进行采样, 由于历史调查中仅2004年调查采用了该种网具, 因此本研究主要与2004年调查资料进行对比, 结果表明浮游动物丰度明显减少, 春季和夏季的减少幅度分别为34.1%和61.4%(表 3), 这与1950年~2000年期间Ⅰ型网浮游动物丰度的增加趋势[9]是不同的。李志伟[10]等同样采用Ⅱ型网对曹妃甸海域做了调查, 2015年春季和夏季的浮游动物丰度分别为2 907.2和19 608.2个/m3, 也明显低于2004年资料(表 3), 这与本研究的结果相似。曹妃甸海域浮游动物丰度的上述变化可能与浮游植物、营养盐等因素有关。本次调查期间, 春季的浮游植物丰度明显低于2004年[23], 不利于浮游动物摄食, 使得春季浮游动物丰度显著降低, 而夏季浮游植物受到河流输入淡水和营养盐的较强影响, 细胞丰度显著高于2004年[23], 但可能还未通过摄食作用对浮游动物产生影响, 表明浮游动物可能即将出现丰度高峰。另外, 海水中DIP浓度及其与其他营养元素的比例可直接影响浮游植物细胞的元素组成, 然后通过摄食作用对浮游动物的生长产生影响[39]。石琛[40]等的室内培养实验即表明海洋桡足类在低磷条件下会出现生长发育减缓, 死亡率提高, 摄食率降低等现象。相对于2004年, 本次调查春季和夏季的DIP浓度均显著降低[14], 不利于浮游动物生长繁殖。大西洋[41]、象山港[42]等海域的研究也证明了浮游动物丰度、生物量的减少与DIP浓度降低以及N/P失衡有关。两次调查中, 浮游动物优势种没有发生明显变化, 春季以双刺纺锤水蚤为主, 夏季以小拟哲水蚤为主(表 3)。值得注意的是, 由于调查资料的连续性较为不足, 所采用的浮游生物网也存在差异, 上述浮游动物群落呈现的变化特征可能受到年际变化等因素的干扰, 尚需更多连续调查资料进行验证。
| 季节 | 年份 | 丰度/(个/m3) | 主要优势种 | |||
| 西侧 | 南侧 | 东侧 | 平均 | |||
| 春季 | 2004 | 21 754.7 | 20 187.0 | 8 119.0 | 17 757.9 | 双刺纺锤水蚤 |
| 2013 | 13 499.3 | 8 297.3 | 13 292.5 | 11 696.4 | 双刺纺锤水蚤, 小拟哲水蚤 | |
| 变化率(%) | –38.0 | –58.9 | 63.7 | –34.1 | ||
| 夏季 | 2004 | 20 269.3 | 30 454.3 | 28 769.0 | 26 213.6 | 小拟哲水蚤, 拟长腹剑水蚤 |
| 2013 | 11 500.0 | 13 795.3 | 5 101.2 | 10 132.1 | 小拟哲水蚤, 双刺纺锤水蚤 | |
| 变化率(%) | –43.3 | –54.7 | –82.3 | –61.4 | ||
| 平均 | 2004 | 21 012.0 | 25 320.7 | 18 444.0 | 21 985.8 | |
| 2013 | 12 499.7 | 11 046.3 | 9 196.9 | 10 914.3 | ||
| 变化率(%) | –40.5 | –56.4 | –50.1 | –50.4 | ||
围填海工程对曹妃甸邻近海域的生态环境具有不可忽视的影响[6]。部分研究认为围填海工程的影响具有空间差异, 主要体现在春季: 西侧海域营养状态减弱, Chl-a浓度降低, 浮游植物多样性升高; 东侧海域营养状态加重, Chl-a浓度升高, 浮游植物多样性降低[14, 23]。本研究中, 春季浮游动物丰度在围填海前后的变化也体现出一定的空间差异: 西侧海域浮游动物丰度降低了38.0%, 而东侧海域丰度升高了63.7%(表 3)。这与围填海前后营养状态和Chl-a浓度变化的空间差异是一致的, 表明围填海后水动力环境的变化造成营养盐的重新分布, 西侧海域营养状态的减弱, 限制了浮游植物生长, 通过摄食作用也对浮游动物的生长产生不利影响, 东侧海域营养状态加重, 有利于浮游植物增殖, 为浮游动物提供了充足饵料, 因此浮游动物丰度明显增加。相对而言, 研究海域在本次夏季调查期间受到河流输入的显著影响, 盐度普遍较低[14], 营养状态[14]、浮游植物[23]和浮游动物(表 3)在围填海前后的变化均没有体现出空间差异。
4 结论本次调查共鉴定出浮游动物31种(类), 主要为桡足类和浮游幼体, 毛颚类、被囊类和枝角类等其他类群的种类数量相对较少。春季, 浮游动物丰度和生物量较高, 基本为近岸高、远岸低的空间分布规律, 优势种主要包括双刺纺锤水蚤、小拟哲水蚤和拟长腹剑水蚤等; 夏季, 浮游动物丰度和生物量较低, 基本为近岸低、远岸高的空间分布规律, 小拟哲水蚤、双刺纺锤水蚤和桡足类幼体等是主要的优势种。温度和Chl-a是影响浮游动物时空变化的主要环境因子。
与2004年调查资料相比, 春季和夏季的浮游动物丰度明显下降, 可能与浮游植物丰度、DIP浓度降低有关, 优势种未出现明显变化。春季, 浮游动物丰度的变化还具有空间差异, 西侧海域丰度明显降低, 东侧海域丰度明显升高, 与围填海后营养盐重新分布促进东侧海域浮游植物增殖有关。夏季, 研究海域主要受河流输入影响, 浮游动物丰度的变化没有体现出明显的空间差异。
| [1] |
张海波, 裴绍峰, 祝雅轩, 等. 初夏渤海湾初级生产力分布特征及影响因素[J]. 生态学报, 2019, 39(17): 6416-6424. ZHANG Haibo, PEI Shaofeng, ZHU Yaxuan, et al. Study on the distribution characteristic of primary productivity and its controlling factors in Bohai Bay in the early summer[J]. Acta Ecologica Sinica, 2019, 39(17): 6416-6424. |
| [2] |
LIU X H, WANG Y J, LIU D Y, et al. Temporal and spatial variations and impact factors of nutrients in Bohai Bay, China[J]. Marine Pollution Bulletin, 2019, 140: 549-562. DOI:10.1016/j.marpolbul.2019.02.011 |
| [3] |
周毅, 许帅, 徐少春, 等. 中国温带海域新发现较大面积(大于0.5 km2)海草床: Ⅱ声呐探测技术在渤海唐山沿海海域发现中国面积最大的鳗草海草[J]. 海洋科学, 2019, 43(8): 50-55. ZHOU Yi, XU Shai, XU Shaochun, et al. New discovery of larger seagrass beds with areas >0.50 km2 in temperate waters of China: Ⅱ The largest Zostera marina bed in China discovered in the coastal waters of Tangshan in the Bohai Sea by sonar detection technology[J]. Marine Sciences, 2019, 43(8): 50-55. |
| [4] |
刘慧, 黄小平, 王元磊, 等. 渤海曹妃甸新发现的海草床及其生态特征[J]. 生态学杂志, 2016, 35(7): 1677-1683. LIU Hui, HUANG Xiaoping, WANG Yuanlei, et al. Newly discovered seagrass bed and its ecological characteristics in the coastal area of Caofeidian, Bohai[J]. Chinese Journal of Ecology, 2016, 35(7): 1677-1683. |
| [5] |
吴越, 杨文波, 王琳, 等. 曹妃甸填海造地时空分布遥感监测及其影响初步研究[J]. 海洋湖沼通报, 2013, 1: 153-158. WU Yue, YANG Wenbo, WANG Lin, et al. Primary study on the spatial-temporal changes and the effect of sea reclamation in Caofeidian based on remote sensing[J]. Transactions of Oceanology and Limnology, 2013, 1: 153-158. |
| [6] |
李东, 侯西勇, 张华. 曹妃甸围填海工程对近海环境的影响综述[J]. 海洋科学, 2019, 43(2): 82-90. LI Dong, HOU Xiyong, ZHANG Hua. A review of the impacts of the Caofeidian reclamation project on the offshore environment[J]. Marine Sciences, 2019, 43(2): 82-90. |
| [7] |
程林, 王欣平, 王艳霞, 等. 河北省曹妃甸近岸海域春季生态系统健康现状评价[J]. 海洋通报, 2017, 36(1): 107-113. CHENG Lin, WANG Xinping, WANG Yanxia, et al. Nearshore ecosystem health assessment for the coastal area of Caofeidian of Hebei Province in spring[J]. Marine Science Bulletin, 2017, 36(1): 107-113. |
| [8] |
LALLI C M, PARSONS T R. Biological oceanography: an introduction (2nd ed)[M]. Burlington, USA: Elsevier Butterworth-Heinemann, 1997.
|
| [9] |
王红, 石雅君, 刘西汉, 等. 河北省曹妃甸海域浮游动物群落长期变化特征[J]. 海洋通报, 2015, 34(1): 95-101. WANG Hong, SHI Yajun, LIU Xihan, et al. Research on the long-term variation of zooplankton community in the coastal area of Caofeidian, Hebei Province[J]. Marine Science Bulletin, 2015, 34(1): 95-101. |
| [10] |
李志伟, 崔力拓. 环境因子对唐山湾海域浮游动物群落结构的驱动作用[J]. 应用海洋学报, 2017, 28(11): 3797-3804. LI Zhiwei, CUI Lituo. Environmental control of zooplankton structure in Tangshan Bay, China[J]. Chinese Journal of Applied Ecology, 2017, 28(11): 3797-3804. |
| [11] |
梁淼, 姜倩, 孙丽艳, 等. 曹妃甸近岸海域大、中型浮游动物优势种空间生态位[J]. 生态环境学报, 2018, 27(7): 1241-1250. LIANG Miao, JIANG Qian, SUN Liyan, et al. Spatial niches of dominant macro-zooplankton and meso-zooplankton species in the coastal area of Caofeidian[J]. Ecology and Environmental Sciences, 2018, 27(7): 1241-1250. |
| [12] |
中华人民共和国国家质量监督检验检疫局总局. GB/T12763.4-2007海洋调查规范第4部分: 海水化学要素调查[S]. 北京: 中国标准出版社, 2008, 3-7. General Administration of Quality Supervision, Inspection and Quarantine of the People's Republic of China. GB/T12763.4-2007 Specifications for Oceanographic Survey-Part 4: Survey of Chemical parameters in sea water[S]. Beijing: Standards Press of China, 2008, 3-7. |
| [13] |
中华人民共和国国家质量监督检验检疫局总局. GB/T12763.6-2007海洋调查规范第6部分: 海洋生物调查[S]. 北京: 中国标准出版社, 2008, 34-37. General Administration of Quality Supervision, Inspection and Quarantine of the People's Republic of China. GB/T12763.6-2007 Specifications for Oceanographic Survey-Part 6: Marine biological Survey[S]. Beijing: Standards Press of China, 2008, 34-37. |
| [14] |
刘西汉, 王玉珏, 石雅君, 等. 曹妃甸近海营养盐和叶绿素a的时空分布及其影响因素研究[J]. 海洋环境科学, 2020, 39(1): 89-98. LIU Xihan, WANG Yujue, SHI Yajun, et al. Spatial and temporal distribution of nutrients and chlorophyll a, and their influential factors in Caofeidian coastal waters[J]. Marine Environmental Science, 2020, 39(1): 89-98. |
| [15] |
SHANNON C E, WEAVER W. The mathematical theory of communication[M]. Urbana IL: University of Illinois Press, 1949.
|
| [16] |
PIELOU E C. An introduction to mathematical ecology[M]. New York: Wiley-Interscience, 1969.
|
| [17] |
OKSANEN J, BLANCHET F G, FRIENDLY M, et al. Vegan: Community Ecology Package[EB/OL]. https://cran.r-project.org/web/packages/vegan,2017.
|
| [18] |
河北省国土资源利用规划院. 河北省海洋资源调查与评价专题报告[M]. 北京: 海洋出版社, 2007. Hebei Utilization and Planning Institute of Land Resources. Special report on investigation and evaluation of marine resources in Hebei province[M]. Beijing: China Ocean Press, 2007. |
| [19] |
高文胜, 刘宪斌, 张秋丰, 等. 渤海湾近岸海域浮游动物多样性[J]. 海洋科学, 2014, 38(4): 55-60. GAO Wensheng, LIU Xianbin, ZHANG Qiufeng, et al. Species diversity of zooplankton in the coastal area of Bohai Bay[J]. Marine Sciences, 2014, 38(4): 55-60. |
| [20] |
姜会超, 陈海刚, 宋秀凯, 等. 莱州湾金城海域浮游动物群落结构及与环境因子的关系[J]. 生态学报, 2015, 35(22): 7308-7319. JIANG Huichao, CHEN Haigang, SONG Xiukai, et al. Zooplankton community structure in Jincheng area of Laizhou Bay and its relationship with environmental factors[J]. Acta Ecologica Sinica, 2015, 35(22): 7308-7319. |
| [21] |
韦章良, 柴召阳, 石洪华, 等. 渤海长岛海域浮游动物的种类组成与时空分布[J]. 上海海洋大学学报, 2015, 24(4): 550-559. WEI Zhangliang, CHAI Zhaoyang, SHI Honghua, et al. Species composition, abundance and distribution of zooplankton along the coast of Chang Island in the Bohai Sea, China[J]. Journal of Shanghai Ocean University, 2015, 24(4): 550-559. |
| [22] |
徐东会, 孙雪梅, 陈碧鹃, 等. 渤海中部浮游动物的生态特征[J]. 渔业科学进展, 2016, 37(4): 7-18. XU Donghui, SUN Xuemei, CHEN Bijuan, et al. The ecological characteristics of zooplankton in the central Bohai Sea[J]. Progress in Fishery Sciences, 2016, 37(4): 7-18. |
| [23] |
刘西汉, 王玉珏, 石雅君, 等. 曹妃甸海域浮游植物群落及其在围填海前后的变化分析[J]. 海洋环境科学, 2020, 39(3): 379-386. LIU Xihan, WANG Yujue, SHI Yajun, et al. Phytoplankton community and changes after reclamation in Caofeidian coastal waters[J]. Marine Environmental Science, 2020, 39(3): 379-386. |
| [24] |
毕洪生, 孙松, 高尚武, 等. 渤海浮游动物群落生态特点Ⅲ. 部分浮游动物数量分布和季节变动[J]. 生态学报, 2001, 21(4): 513-521. BI Hongsheng, SUN Song, GAO Shangwu, et al. The characteristics of zooplankton community in the Bohai Sea Ⅲ. The distribution of abundance and seasonal dynamics of major taxa except copepoda[J]. Acta Ecologica Sinica, 2001, 21(4): 513-521. |
| [25] |
仲学锋, 肖贻昌. 胶州湾3种哲水蚤种群动态的研究[J]. 海洋科学, 1992, 16(1): 44-48. ZHONG Xuefeng, XIAO Yichang. Seasonal cycles of abundance of three copepod species population in Jiaozhou Bay[J]. Marine Sciences, 1992, 16(1): 44-48. |
| [26] |
SUN X H, SUN S, LI C L, et al. Seasonal and spatial variability in egg production, abundance and production of small copepods in and near Jiaozhou Bay, China[J]. Journal of Plankton Research, 2011, 33(5): 741-750. |
| [27] |
王秀霞, 左涛, 吴强, 等. 莱州湾小拟哲水蚤(Paracalanus parvus)丰度分布周年变动[J]. 渔业科学进展, 2015, 36(1): 1-9. WANG Xiuxia, ZUO Tao, WU Qiang, et al. Annual dynamic distributions of Paracalanus parvus (Copepoda Calanoida) in Laizhou Bay, China[J]. Progress in Fishery Sciences, 2015, 36(1): 1-9. |
| [28] |
李超伦, 王克. 植食性浮游桡足类摄食生态学研究进展[J]. 生态学报, 2002, 22(4): 593-596. LI Chaolun, WANG Ke. Feeding ecology progress of the herbivorous copepod[J]. Acta Ecologica Sinica, 2002, 22(4): 593-596. |
| [29] |
王永杰. 胶州湾异体住囊虫的生态适应性研究[D]. 青岛: 中国科学院大学, 2014. WANG Yongjie. Ecological adaption of Oikopleura dioica in Jiaozhou Bay[D]. Qingdao: University of Chinese Academy of Sciences, 2014. |
| [30] |
徐翠莲, 李涛, 胡思敏, 等. 大亚湾核电站邻近水域桡足幼体现场摄食研究[J]. 热带海洋学报, 2018, 37(2): 17-25. XU Cuilian, LI Tao, HU Simin, et al. In situ feeding of copepodites in the water near Daya Bay nuclear power plant[J]. Journal of Tropical Oceanography, 2018, 37(2): 17-25. |
| [31] |
LIU W, LO W, PURCELL J, CHANG H. Effects of temperature and light intensity on asexual reproduction of the scyphozoan, Aurelia aurita (L.) in Taiwan[J]. Hydrobiologia, 2009, 616: 247-258. |
| [32] |
WANG R, ZUO T, WANG K. The Yellow Sea cold bottom water-an oversummering site for Calanus sinicus (Copepoda, Crustacea)[J]. Journal of Plankton Research, 2003, 25(2): 169-183. |
| [33] |
刘青, 曲晗, 张硕. 强壮箭虫对温度、盐度的耐受性研究[J]. 海洋湖沼通报, 2007, 1: 111-116. LIU Qing, QU Han, ZHANG Shuo. Preliminary studies on the tolerance to temperature and salinity in Sagitta crassa[J]. Transactions of Oceanology and Limnology, 2007, 1: 111-116. |
| [34] |
刘晓慧, 薛莹, 张崇良, 等. 黄河口及其邻近水域强壮箭虫密度的时空分布及其与环境因子的关系[J]. 海洋学报, 2017, 39(6): 74-83. LIU Xiaohui, XUE Ying, ZHANG Chongliang, et al. Spatio-temporal distribution of density of Sagitta crassa and its relationship with environmental factors in the Yellow River Estuary and its adjacent waters[J]. Haiyang Xuebao, 2017, 39(6): 74-83. |
| [35] |
WANG R, ZHANG H Y, WANG K, et al. Distribution and population dynamics of Paracalanus parvus, Paracalanus crassirostris, and Acartia bifilosa (Copepoda, Calanoida) in the Bohai Sea[J]. Chinese Journal of Oceanology and Limnology, 2002, 20(4): 348-357. |
| [36] |
薛泽, 朱丽岩, 王博渊, 等. 温度和盐度对两种海洋桡足类动物摄食和代谢的影响[J]. 海洋与湖沼, 2020, 51(1): 95-102. XUE Ze, ZHU Liyan, WANG Boyuan, et al. Effects of temperature and salinity on feeding and metabolism of two marine copepods[J]. Oceanologia et Limnologia Sinica, 2020, 51(1): 95-102. |
| [37] |
王永杰. 胶州湾异体住囊虫的生态适应性研究[D]. 青岛: 中国科学院大学, 2014. WANG Yongjie. Ecological adaption of Oikopleura dioica in Jiaozhou Bay[D]. Qingdao: University of Chinese Academy of Sciences, 2014. |
| [38] |
CLOERN J E, ABREU P C, Carstensen J, et al. Human activities and climate variability drive fast-paced change across the world's estuarine-coastal ecosystems[J]. Global Change Biology, 2016, 22: 513-529. |
| [39] |
陈蕾, 李超伦. 海洋浮游生物的生态化学计量学研究进展[J]. 应用海洋学报, 2014, 25(10): 3047-3055. CHEN Lei, LI Chaolun. Research advances in ecological stoichiometry of marine plankton[J]. Chinese Journal of Applied Ecology, 2014, 25(10): 3047-3055. |
| [40] |
石琛, 吕颂辉, 何学佳. 不同磷条件对安氏镖水蚤的生长及摄食的影响[J]. 水生生物学报, 2011, 35(3): 460-466. SHI Chen, LYV Songhui, HE Xuejia. Effect of phosphorus condition on growth and ingestion in Pseudodiaptomus annandalei[J]. Acta Hydrobiologica Sinica, 2011, 35(3): 460-466. |
| [41] |
PIONTKOVSHI S A, CASTELLANI C. Long-term declining trend of zooplankton biomass in the tropical Atlantic[J]. Hydrobiologia, 2009, 632: 365-370. |
| [42] |
骆鑫, 曾江宁, 徐晓群, 等. 象山港浮游动物的分布特征及其中长期变化[J]. 海洋通报, 2018, 37(1): 74-87. LUO Xin, ZENG Jiangning, XU Xiaoqun, et al. Distribution of zooplankton in the Xiangshan Bay and its changes during longer period[J]. Marine Science Bulletin, 2018, 37(1): 74-87. |
 2021, Vol. 45
2021, Vol. 45


